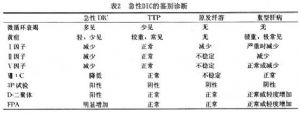
3 概述
播散性血管內凝血(disseminated intravascular coagulation,DIC)不是一個獨立的疾病,而是許多疾病發展過程中的一個重要的中間過程,其特徵爲血管內凝血被激活,微循環血栓形成,大量消耗凝血因子和血小板,導致繼發性纖溶酶大量生成,臨牀出現出血、臟器功能障礙、微血管病性溶血及休克等症狀。
6 別名
senile diffuse intravascular coagulation;老年播散性血管內凝血;老年人彌散性血管內凝血
9 流行病學
感染性疾病是播散性血管內凝血(DIC)最主要最常見的病因,佔播散性血管內凝血(DIC)發病數30%;其次是惡性腫瘤,佔播散性血管內凝血(DIC)患者的24%~34%;產科居第3位,佔播散性血管內凝血(DIC)的4%~17%;手術和外傷佔播散性血管內凝血(DIC)的1%~5%。富含組織因子的器官如:腦、胰腺、子宮等。可用手術及創傷等促進組織因子釋放,誘發播散性血管內凝血(DIC)。
11 發病機制
許多疾病發生發展過程中破壞了正常凝血、抗凝、纖溶系統的平衡,體內即可出現止血、凝血和纖溶的異常。由於病理性凝血酶及纖溶酶的過度生成導致了播散性血管內凝血(DIC)。其機制有以下幾個方面。
11.1 活化內外凝血途徑
嚴重的細菌感染(產生內毒素)、病毒感染、抗原-抗體複合物、手術創傷等引起血管內皮細胞廣泛受損,血管基底膜及膠原纖維暴露,激活因子ⅩⅢ,從而激活內源性凝血途徑;與此同時,手術、嚴重創傷時釋放的組織因子(TF)、病理性促凝物進入血液循環後,在鈣離子的參與下,TF與Ⅶ形成TF/Ⅶ複合物,繼而激活外源性凝血途徑。內、外凝血途徑均可使Ⅹ活化爲Ⅹa,後者與Va、Ca2+、磷脂共同形成凝血酶原複合物,使凝血酶原轉變爲凝血酶;繼之使纖維蛋白原轉變爲纖維蛋白,在微血管內形成血栓。
11.2 單核-吞噬系統功能受損
在內毒素、炎性細胞因子和補體活化的刺激下,單核巨噬細胞表面可表達活化TF,並可分泌TNF、IL-1及血小板活化因子(PAF)。TNF、IL-1可增加纖溶酶原激活物(tPA)和纖溶酶原激活物抑制物-1(PAI-1)的表達,並通過抑制內皮細胞凝血調節蛋白(TM)的生成,減少蛋白C(PC)的活化;另外,由於凝血酶的生成,抑制了單核-吞噬系統對活化凝血因子的清除,也促進了血液的凝固。
11.3 抗凝機制減弱
正常凝血時機體有複雜的抗凝系統拮抗,通過體液和細胞兩方面起作用,保證血液在血管內流通:內皮細胞分泌TM與凝血酶結合,消除了凝血酶對Ⅻ因子、纖維蛋白原和血小板的促凝作用。內皮細胞還分泌一種組織因子途徑抑制物(TFPI),可滅活TF/Ⅶa複合物並抑制Ⅹa活化,對維持微循環灌注起一定作用。病理狀態下,內皮細胞受損,TM作用減弱,從而使凝血酶的促凝活性增強,加速凝血;同時TM減少也降低了蛋白C的活化,Ⅷa和Ⅴa的滅活受抑;促凝物質進入血液循環,過度消耗TFPI,也是播散性血管內凝血(DIC)發生的機制之一。
11.4 纖維蛋白溶解的啓動與增強
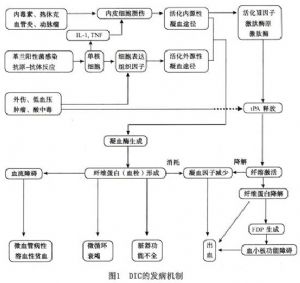
隨着體內微血栓的廣泛形成,大量凝血因子和血小板被消耗。凝血酶在使纖維蛋白原變爲纖維蛋白的同時活化ⅩⅢ因子,並激活纖溶酶;凝血過程中形成Ⅹa和Ⅻa時脫下的碎片也可激活纖溶酶;血管內皮受損時釋放tPA,也可激活纖溶酶並加強纖溶過程。纖溶酶原活化後可消化纖維蛋白原及纖維蛋白,形成相應的降解產物,即FDP,具有抗凝和抗血小板聚集作用,從而加重了因消耗性凝血因子和血小板缺乏導致的出血(圖1)。
12 老年人播散性血管內凝血的臨牀表現
播散性血管內凝血(DIC)發生後其主要症狀、體徵與原發病有關。應強調播散性血管內凝血(DIC)爲一動態發展過程,在疾病發展的不同階段,臨牀表現有很大差異。根據機體凝血和纖溶系統的不同狀態可分爲3期。
12.1 高凝期
往往僅在實驗室檢查時發現血液凝固性增高,急性型很難發現,慢性型較明顯。
12.2 消耗性低凝期
12.2.1 (1)出血
由於血漿凝血因子和血小板大量消耗,臨牀上可見出血症狀明顯。其特徵是出血的廣泛程度和嚴重程度不能用原發病解釋。出血常見的部位是皮膚、腎、胃腸道,穿刺、手術部位和術後廣泛滲血等。早期有出血點、瘀斑,晚期可見大量瘀斑等。
12.2.2 (2)微血管栓塞
因受累血管不同而症狀各異,皮膚可見出血性壞死或手指足趾壞疽;腎受累可引起血尿、少尿、尿閉、腎小管壞死、急性腎衰竭;肺內微血管受累可出現呼吸功能不全,急性Ⅰ型呼衰多見;腦部受累可引起腦缺氧、水腫,臨牀上可出現嗜睡、驚厥甚至昏迷等表現。
12.2.3 (3)休克
是播散性血管內凝血(DIC)較早出現的症狀,用原發病不易解釋,抗休克治療效果較差。其原因主要爲:①微血栓形成使回心血量減少,心排血量下降;②播散性血管內凝血(DIC)時,Ⅻ因子被活化,生成激肽釋放酶,緩激肽使小動脈擴張、血漿滲出,循環血容量下降;③低凝狀態引起出血使血容量進一步減少;④血液濃縮,血漿黏稠度增加;⑤纖溶時裂解出的纖維蛋白肽A(FPA)和B(FPB)可使小血管痙攣,加重休克。
12.2.4 (4)微血管病性溶血
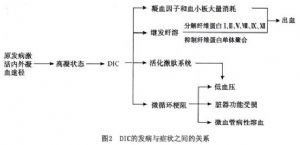
播散性血管內凝血(DIC)時微血管內出現纖維蛋白絲,導致紅細胞機械性損傷,出現紅細胞變形、碎片,嚴重時出現微血管病性溶血性貧血。(圖2)
12.3 繼發纖溶期
臨牀出血廣泛且嚴重,主因消耗大量凝血因子,血液處於低凝狀態,且繼發纖溶亢進。FDP抑制血小板聚集並有抗凝作用,加重出血,而休克、酸中毒也使疾病繼續惡化。
12.4 臨牀分型
根據病程長短分爲:
12.4.1 (1)急性型
12.4.2 (2)慢性型
14 實驗室檢查
分爲篩查試驗和確證試驗。篩查試驗主要是血小板、凝血因子消耗以及纖溶異常的證據,如血小板計數、PT、APTT、3P試驗、Fbg和FDP測定等;確證試驗是爲了找出關鍵的凝血酶和纖溶酶形成的證據。
16 老年人播散性血管內凝血的診斷
應具有引起播散性血管內凝血(DIC)的基礎疾病;符合播散性血管內凝血(DIC)的臨牀表現;有實驗室診斷依據。1994年第五屆中華血液學會全國血栓與止血學術會議制定的播散性血管內凝血(DIC)診斷標準可供參考。
16.1 臨牀表現
(1)存在易引起播散性血管內凝血(DIC)的基礎疾病。
(2)有下列兩項以上臨牀表現:
①多發性出血傾向。
③多發性微血管栓塞的症狀和體徵,如:皮膚、皮下、黏膜栓塞、壞死及早期出現的腎、肺、腦等臟器功能不全。
16.2 實驗室檢查
16.2.1 (1)下列3項以上異常
①血小板計數<100×109/L或呈進行性下降(肝病、白血病患者血小板數可<50×109/L);或有下述2項以上血漿血小板活化產物升高:β血小板球蛋白(β-TG)、血小板第Ⅳ因子(PF4)、血栓素B2(TXB2)或顆粒膜蛋白-140(GMP-140)。
②血漿纖維蛋白原含量<1.5g/L或進行性下降或超過4g/L(白血病或其他惡性腫瘤患者<1.8g/L,肝病<1.0g/L)。
③3P試驗陽性或血漿FDP>20mg/L(肝病>60mg/L)或D-二聚體水平升高(陽性)。
④凝血酶原時原時間縮短或延長3s以上或呈動態變化(肝病患者PT延長5s以上)。
⑤纖溶酶原含量及活性降低。
16.2.2 (2)疑難病例應有以下1項以上異常
①Ⅷ:C活性降低,vWF:Ag升高,Ⅷ:C與vWF:Ag比值降低。
②血漿凝血酶-抗凝血酶複合物(TAT)濃度升高或凝血酶原碎片1+2(F1+2)水平升高。
④血(尿)FPA水平升高。
18 老年人播散性血管內凝血的治療
18.1 原發病的處理
原發病的處理是終止播散性血管內凝血(DIC)的主要措施。有些原發病,如產科的胎死宮內、子癇等,終止妊娠並清除子宮,病情即可顯著好轉。
18.2 改善微循環
18.3 抗凝治療
適時應用抗凝劑可阻斷播散性血管內凝血(DIC)的病理過程,減輕器官損傷並改善其功能,特別是在病因持續存在的情況下。
18.3.1 (1)肝素
臨牀多應用肝素鈉,其作用機制是增強AT-Ⅲ的抗凝活性,故給藥的前提條件是體內有足夠的AT-Ⅲ。用藥時應結合補充凝血因子。
劑量:按每公斤體重5~10U/h靜脈滴注,如治療後APTT縮短,FDP和D-二聚體水平下降,纖維蛋白原上升,說明抗凝有效;如上述指標無改善,需加大肝素用量,直至出現滿意效果;如應用後APTT反而延長,應減少肝素用量。肝素治療應持續至原發病清除或得到控制。
肝素鈣(低分子肝素):本藥抑制凝血酶的作用弱而抑制Ⅹa的作用較強。注入體內後不與內皮細胞膜結合,皮下注射後生物利用度較高。LMWH能促使內皮細胞釋放TFPI,對AT-Ⅲ的依賴性較小,出血的副作用較少,半衰期長,一般不需檢測。但本藥排泄主要通過腎,腎功能不全患者藥物清除半衰期延長,故需謹慎應用,腎衰患者應用劑量可酌減至正常的1/3。LMWH(速必凝)正常劑量0.3~0.5ml,皮下注射,2次/d。
禁忌證:①播散性血管內凝血(DIC)晚期,明顯纖溶亢進;②活動性出血,如潰瘍病出血,肺結核空洞咯血;③有出血傾向的嚴重肝病或高血壓腦病;④手術後或創面未經良好止血者。
肝素應用時的檢測:普通肝素應用時凝血時間(CT,試管法)不應超過30min;控制APTT不超過60~100s。肝素過量可用硫酸魚精蛋白(魚精蛋白)拮抗,一般可按1∶1用藥,每次不宜超過50mg。1mg硫酸魚精蛋白(魚精蛋白)中和肝素100U。
18.3.2 (2)低分子右旋糖酐
低分子右旋糖酐500~1000ml/d,可解除紅細胞和血小板聚集,並可疏通微循環,擴充血容量,用於早期播散性血管內凝血(DIC)及輕症患者。
18.3.3 (3)AT-Ⅲ
AT-Ⅲ可加強肝素的抗凝效果,文獻報道可按AT-Ⅲ30U/(kg·d), 1~2次/d用藥,連用數天。
18.4 補充凝血因子及血小板
由於凝血因子和血小板消耗性減少導致機體廣泛出血,故輸注凝血因子和血小板,同時應用肝素是安全的。目前多用成分輸血,常用的有:
18.4.1 (1)新鮮冰凍血漿(FFP)
含有豐富的凝血因子。
18.4.2 (2)血小板濃縮液
血小板計數低於20×109/L,或有顱內出血傾向時應及時補充血小板。
18.4.3 (3) 凍幹人纖維蛋白原(纖維蛋白原)
可每次2~4g,因半衰期長,可每2~3天輸1次,達到正常水平即可停用。但有人主張不用,因爲播散性血管內凝血(DIC)時是多個凝血因子缺乏,只給凍幹人纖維蛋白原(纖維蛋白原)不但不能止血,反而影響病理觀察。
18.5 纖溶抑制劑
只可用於纖溶亢進期,如氨甲環酸(止血環酸)100~200mg,2~3次/d,靜脈輸注。
18.6 抗血小板藥物
播散性血管內凝血(DIC)時均有血小板凝集活化,使用肝素時聯合應用抗血小板藥有利於阻斷播散性血管內凝血(DIC)的進展。常用的藥物有噻氯匹定250mg,2次/d。
18.7 腎上腺皮質激素
播散性血管內凝血(DIC)時無常規應用指徵,應視原發病情況而定。對各種變態反應性疾病或合併有腎上腺皮質功能不全者可應用。
19 預後
播散性血管內凝血(DIC)的病死率爲50%~80%,可因不同基疾病而異。