2 附錄Ⅸ A 抗生素殘留量檢查法(培養法)
本法系依據在瓊脂培養基內抗生素對微生物的抑制作用,比較對照品與供試品對接種的試驗菌產生的抑菌圈的大小,檢查供試品中氨苄西林或四環素殘留量。
2.1 磷酸鹽緩衝液(pH 6.0)的製備
稱取磷酸二氫鉀8.0g、磷酸氫二鉀2.0g,加水溶解並稀釋至1000ml,經121℃滅菌30分鐘。
2.2 抗生素Ⅱ號培養基的製備
稱取腖6g、牛肉提取粉1.5g、酵母浸出粉6g,加入適量水溶解後,加入瓊脂13~14g,加熱使之溶脹,濾過除去不溶物,加入葡萄糖1g,溶解後加水至1000ml,調pH值使滅菌後爲6.5~6.6;分裝於玻璃管或錐形瓶中,經115℃滅菌30分鐘,4℃保存。
2.3 對照品溶液的製備
取氨苄西林對照品適量,用0.01mol/L鹽酸溶解並稀釋成每1ml中含氨苄西林10mg的溶液,精密量取適量,用磷酸鹽緩衝液稀釋成每1ml中含1.0μg的溶液。
取四環素對照品適量,用生理氯化鈉溶液溶解並稀釋成每1ml中含0.125μg的溶液。
2.4 菌懸液的製備
(1)金黃色葡萄球菌(Staphylococcus aureus)懸液 用於檢測氨苄西林。取金黃色葡萄球菌(CMCC 26003)營養瓊脂斜面培養物,接種於營養瓊脂斜面上,35~37℃培養20~22小時。臨用時,用滅菌水或0.9%無菌氯化鈉溶液將菌苔洗下,備用。
(2)藤黃微球菌(Micrococcus luteus)懸液 用於檢測四環素。取藤黃微球菌[CMCC (B) 28001]營養瓊脂斜面培養物,接種於營養瓊脂斜面上,置26~27℃培養24小時。臨用時,用0.9%無菌氯化鈉溶液將菌苔洗下,備用。
2.5 檢查法
取直徑8cm或10cm的培養皿,注入融化的抗生素Ⅱ號培養基15~20ml,使在碟底內均勻攤布,放置水平臺上使凝固,作爲底層。取抗生素Ⅱ號培養基10~15ml置於1支50℃水浴預熱的試管中,加入0.5%~1.5% (ml/ml)的菌懸液300μl混勻,取適量注入已鋪制底層的培養皿中,放置水平臺上,冷卻後,在每個培養皿上等距離均勻放置鋼管(內徑6~8mm、壁厚1~2mm、管高10~15mm的不鏽鋼管,表面應光滑平整),於鋼管中依次滴加供試品溶液、陰性對照溶液(磷酸鹽緩衝液)及對照品溶液。培養皿置37℃培養18~22小時。
2.6 結果判定
對照品溶液有抑菌圈,陰性對照溶液無抑菌圈。供試品溶液抑菌圈的直徑小於對照品溶液抑菌圈的直徑時判爲陰性;否則判爲陽性。
2.7 【附註】
3 附錄Ⅸ B 外源性DNA殘留量測定法
在進行外源性DNA殘留量測定時,可根據供試品具體情況選擇下列任何一種方法進行測定。
3.1 第一法 DNA探針雜交法
供試品中的外源性DNA經變性爲單鏈後吸附於固相膜上,在一定溫度下可與相匹配的單鏈DNA復性而重新結合成爲雙鏈DNA,稱爲雜交。將特異性單鏈DNA探針標記後,與吸附在固相膜上的供試品單鏈DNA雜交,並使用與標記物相應的顯示系統顯示雜交結果,與已知含量的陽性DNA對照比對後,可測定供試品中外源性DNA殘留量。
3.1.1 試劑
(1) DNA標記和檢測試劑盒。
(3)2%蛋白酶K溶液 稱取蛋白酶K 0.20g,溶於滅菌水(電阻率大於18.2MΩ·cm) 10ml中,分裝後儲藏於-20℃備用。
(4)3%牛血清白蛋白溶液 稱取牛血清白蛋白0.30g,溶於滅菌水(電阻率大於18.2 MΩ·cm) 10ml中。
(5)1mol/L三羥甲基氨基甲烷(Tris)溶液(pH8.0) 用鹽酸調pH值至8.0。
(7)0.5mol/L乙二胺四乙酸二鈉溶液(pH8.0)用10mol/L氫氧化鈉溶液調pH值至8.0。
(8)20%十二烷基硫酸鈉(SDS)溶液 用鹽酸調pH值至7.2。
(9)蛋白酶緩衝液(pH8.0) 量取1mol/L Tris溶液1.0ml(pH8.0)、5mol/L氯化鈉溶液2.0ml、0.5mol/L乙二胺四乙酸二鈉溶液(pH8.0)2.0ml、20% SDS溶液2.5ml,加滅菌水(電阻率大於18.2 MΩ·cm)至10ml。
(10) TE緩衝液(pH8.0) 量取1mol/L Tris溶液(pH8.0) 10ml、0.5mol/L乙二胺四乙酸二鈉溶液(pH8.0)2ml,加滅菌水(電阻率大於18.2 MΩ·cm)至1000ml。
(11)1%魚精DNA溶液 精密稱取魚精DNA 0.10g,置10ml量瓶中,用TE緩衝液溶解並稀釋至刻度,搖勻,用7號針頭反覆抽打以剪切DNA成爲小分子,分裝後貯藏於-20℃備用。
(12) DNA稀釋液 取1%魚精DNA溶液50μl,加TE緩衝液至10ml。
3.1.2 用於探針標記和陽性對照的DNA製備
用於探針標記和陽性對照的DNA,由生產供試品用的傳代細胞、工程菌或雜交瘤細胞提取純化獲得,其提純和鑑定可參考下述推薦方案進行,具體方法可參考《分子克隆實驗指南》([美]J.薩姆布魯克等著,黃培堂等譯,科學出版社,2002)或《精編分子生物學實驗指南》([美]F.奧斯伯等著,顏子穎、王海林譯,科學出版社,1998)。
將待提取的細胞基質懸液的細胞濃度調整爲每1ml約含107個細胞,如果爲細菌,則將其濃度調整爲每1ml約含108個細菌。量取懸液1ml,離心,在沉澱中加裂解液400μl混勻,37℃作用12~24小時後,加入飽和苯酚溶液450μl,劇烈混勻,以每分鐘10000轉離心10分鐘,轉移上層液體,以飽和苯酚溶液450μl重複抽提1次;轉移上層液體,加入三氯甲烷450μl,劇烈混勻,以每分鐘10000轉離心10分鐘;轉移上層液體,加入pH 5.2的3mol/L醋酸鈉溶液40μl,充分混合,再加入-20℃以下的無水乙醇1ml,充分混合,-20℃以下作用2小時,以每分鐘15000轉離心15分鐘;用適量-20℃70%乙醇溶液洗滌沉澱1次,以每分鐘15000轉離心15分鐘,棄上清液,保留沉澱,吹至乾燥後,加適量滅菌TE緩衝液溶解,RNase酶切,酚-三氯甲烷抽提,分子篩純化DNA,即得。
用1%瓊脂糖凝膠電泳法和分光光度法鑑定陽性對照品的DNA純度:應無RNA和寡核苷酸存在;A260/A280比值應在1.8~2.0之間(測定時將供試品稀釋至A260爲0.2~1.0)。
用於陽性對照和標記探針的DNA在使用前應進行酶切或超聲處理,使其片段大小適合於DNA雜交和探針標記。
陽性對照品的DNA、濃度按下式計算:
DNA濃度(μg/ml)=50×A260
陽性對照品可分裝於適宜的小管中,-20℃以下保存,長期使用。
3.1.3 探針的標記
按試劑盒使用說明書進行。
3.1.4 測定法
(1)蛋白酶K預處理 按下表對供試品、陽性對照和陰性對照進行加樣,混合後於37℃保溫4小時以上,以保證酶切反應完全。
加樣量 | 加水至終體積 | ||||
供試品 | 100μl | 1μl | 20μl | 200μl | |
D1 | 100μl | 1μl | 20μl | 適量 | 200μl |
D2 | 100μl | 1μl | 20μl | 適量 | 200μl |
D3 | 100μl | 1μl | 20μl | 適量 | 200μl |
陰性對照 | 100μl | 1μl | 20μl | 適量 | 200μl |
注意事項:供試品的稀釋
根據成品最大使用劑量,用DNA稀釋液將供試品(原液)稀釋至每100μl含1人份劑量;如成品最大使用劑量較大,而供試品的蛋白質含量較低,可用DNA稀釋液將供試品稀釋至每100μl含1/10人份劑量或每100μl含1/100人份劑量。
D1、D2、D3爲稀釋的陽性DNA對照。用DNA稀釋液稀釋至每1ml中含DNA 1000ng,然後依次10倍稀釋成10ng/100μl (D1)、1ng/100μl (D2)、100pg/100μl(D3)3個稀釋度;如成品使用劑量較大,而且DNA限量要求(100pg/劑量)較嚴格時,則需要提高DNA檢測靈敏度,相應的陽性DNA對照應稀釋成100pg/100μl(D1)、10pg/100μl (D2)、1pg/100μl(D3)3個稀釋度。陰性對照爲DNA稀釋液,空白對照爲未進行蛋白酶K預處理的TE緩衝液。
當供試品1/100人份劑量大於100μl時,終體積也隨之增大,一般終體積爲供試品體積的1倍左右,供試品體積和終體積相差過小,可能會影響蛋白酶K的活性。
2%蛋白酶K溶液和蛋白酶緩衝液的比例爲1: 20,蛋白酶緩衝液和終體積的比例爲1:16。
加入3%牛血清白蛋白溶液適量,是爲了使陽性對照和陰性對照中含有一定的蛋白質,與供試品(通常爲蛋白質)的酶切條件保持一致;如供試品爲其他物質,則應改用其他相應物質。
若預處理後的供試品溶液中的蛋白質干擾本試驗,可用上述飽和苯酚溶液抽提法或其他適宜方法提取供試品DNA(陽性對照、陰性對照也應再次提取DNA,與供試品溶液平行)。
(2)點膜 用TE緩衝液浸潤雜交膜後,將預處理的供試品、陽性對照、陰性對照與空白對照置100℃水浴加熱10分鐘,迅速冰浴冷卻,以每分鐘8000轉離心5秒。用抽溶加樣器點樣子雜交膜(因有蛋白質沉澱,故要視沉澱多少確定加樣量,以避免加入蛋白質沉澱。所有供試品與陽性對照、陰性對照、空白對照加樣體積應一致,或按同樣比例加樣)。晾乾後置80℃真空幹烤1小時以上。
(3)雜交及顯色 按試劑盒使用說明書進行。
結果判定 陽性對照應顯色,其顏色深度與DNA含量相對應,呈一定的顏色梯度;陰性對照、空白對照應不顯色,或顯色深度小於陽性DNA對照D3,試驗成立。將供試品與陽性對照進行比較,根據顯色的深淺判定供試品中外源性DNA的含量。
3.2 第二法 熒光染色法
應用雙鏈DNA熒光染料與雙鏈DNA特異結合形成複合物,在波長480nm激發下產生超強熒光信號,可用熒光酶標儀在波長520nm處進行檢測,在一定的DNA濃度範圍內以及在該熒光染料過量的情況下,熒光強度與DNA濃度成正比,根據供試品的熒光強度,計算供試品中的DNA殘留量。
3.2.1 試劑
(1) 1mol/L三羥甲基氨基甲烷(Tris)溶液(pH7.5) 用鹽酸調pH值至7.5。
(2)0.5mol/L乙二胺四乙酸二鈉溶液(pH7.5)用10mol/L氫氧化鈉溶液調pH值至7.5。
(3) TE緩衝液(pH7.5) 量取1mol/L Tris溶液(pH7.5) 1.0ml、0.5mol/L乙二胺四乙酸二鈉溶液(pH7.5)0.2ml,加滅菌注射用水至100ml。
(5) DNA標準品 取DNA標準品適量溶於TE緩衝液中,製成100μg/ml DNA標準品,於-20℃保存。
DNA標準品濃度根據下式計算;
DNA濃度(μg/ml)=50×A260
3.2.2 DNA標準品溶液的製備
用TE緩衝液將DNA標準品配成0ng/ml、1.25ng/ml、2.5ng/ml、5.0ng/ml、10ng/ml、20ng/ml、40ng/ml、80ng/ml的標準品溶液。
3.2.3 測定法
精密量取DNA標準品溶液和供試品溶液各400μl於1.5ml離心管中,分別加入新配製的雙鏈DNA熒光染料400μl,混勻後,避光室溫放置5分鐘。取250μl上述反應液於96孔黑色酶標板中,並做3個復孔。用熒光酶標儀在激發波長480nm、發射擻長520nm處測定熒光強度。以TE緩衝液測得的熒光強度爲本底,測定和記錄各測定孔的熒光值。以標準品溶液的濃度對其相應的熒光強度作直線迴歸,求得直線迴歸方程(相關係數應不低於0.99),將供試品溶液的熒光強度代入直線迴歸方程,求出供試品中DNA殘留量。
3.2.4 注意事項
(1) DNA殘留量在1.25~80ng/ml範圍內,本法線性較好,因此供試品DNA殘留量在該範圍內可定量測定;當DNA殘留量低於1.25ng/ml時應爲限量測定,表示爲小於1.25ng/ml。
(2)供試品首次應用本法測定時需要進行方法學驗證,驗證內容至少包括精密度試驗和回收率試驗。若供試品干擾回收率和精密度,應採用適宜方法稀釋或純化DNA(可參見本項目第一法)以排除干擾,直至精密度試驗和回收率試驗均符合要求。需要純化DNA後再進行測定的供試品,每次測定均應從純化步驟起增加回收率試驗,並用回收率對測定結果進行校正。
4 附錄Ⅸ C 大腸桿菌菌體蛋白質殘留量測定法
本法系採用酶聯免疫法測定大腸桿菌表達系統生產的重組製品中菌體蛋白質殘留量。
4.1 試劑
(1)包被液(pH9.6碳酸鹽緩衝液) 稱取碳酸鈉0.32g、碳酸氫鈉0.586g,置200ml量瓶中,加水溶解並稀釋至刻度。
(2)磷酸鹽緩衝液(pH7.4) 稱取氯化鈉8g、氯化鉀0.2g、磷酸氫二鈉1.44g、磷酸二氫鉀0.24g,加水溶解並稀釋至500ml,121℃滅菌15分鐘。
(3)洗滌液(pH7.4) 量取聚山梨酯20 0.5ml,加磷酸鹽緩衝液至500ml。
(4)稀釋液(pH7.4) 稱取牛血清白蛋白0.5g,加洗滌液溶解並稀釋至100ml。
(5)濃稀釋液 稱取牛血清白蛋白1.0g,加洗滌液溶解並稀釋至100ml。
(6)底物緩衝液(pH5.0,枸櫞酸-磷酸鹽緩衝液)稱取磷酸氫二鈉(Na2HPO4·12H2O) 1.84g、枸櫞酸0.51g,加水溶解並稀釋至100ml。
(7)底物液 取鄰苯二胺8mg、30%過氧化氨30μl,溶於底物緩衝液20ml中。臨用時現配。
(8)終止液 1mol/L硫酸溶液。標準品溶液的製備 按菌體蛋白質標準品介紹加
水復溶,精密量取適量,用稀釋液稀釋成每1ml中含菌體蛋白質500ng、250ng、125ng、62.5ng、31.25ng、15.625ng、7.8125ng的溶液。
4.2 供試品溶液的製備
取供試品適量,用稀釋液稀釋成每1ml中約含250μg的溶液。如供試品每1ml中含量小於500μg時,用濃稀釋液稀釋1倍。
4.3 測定法
取兔抗大腸桿菌菌體蛋白質抗體適量,用包被液溶解並稀釋成每1ml中含10μg的溶液,以100μl/孔加至96孔酶標板內,4℃放置過夜(16~18小時)。用洗滌液洗板3次;用洗滌液製備1%牛血清白蛋白溶液,以200μl/孔加至酶標板內,37℃放置2小時;將封閉好的酶標板用洗滌液洗板3次;以100μl/孔加入標準品溶液和供試品溶液,每個稀釋度做雙孔,同時加入2孔空白對照(稀釋液),37℃放置2小時;用稀釋液稀釋辣根過氧化物酶(HRP)標記的兔抗大腸桿菌菌體蛋白質抗體1000倍,以100μl/孔加至酶標板內,37℃放置1小時,用洗滌液洗板10次,以100μl/孔加入底物液,37℃避光放置40分鐘,以50μl/孔加入終止液終止反應。用酶標儀在波長492nm處測定吸光度,應用計算機分析軟件進行讀數和數據分析,也可使用手工作圖法計算。
以標準品溶液吸光度對其相應的濃度作標準曲線,並以供試品溶液吸光度在標準曲線上得到相應菌體蛋白質含量,按以下公式計算:

n爲供試品稀釋倍數;
T爲供試品蛋白質含量,mg/ml。
5 附錄Ⅸ D 假單胞菌菌體蛋白質殘留量測定法
本法系採用酶聯免疫法測定假單胞菌表達系統生產的重組製品菌體蛋白質殘留量。
5.1 試劑
(1)包被液(pH9.6碳酸鹽緩衝液) 精密稱取碳酸鈉0.32g、碳酸氫鈉0.586g,置200ml量瓶中,加水溶解並稀釋至刻度。
(2)磷酸鹽緩衝液 稱取氯化鈉8.0g、氯化鉀0.20g、磷酸氫二鈉1.44g、磷酸二氫鉀0.24g,置500ml量瓶中,加水溶解並稀釋至刻度,121℃滅菌15分鐘。
(3)洗滌液 量取聚山梨酯20 0.5ml,加磷酸鹽緩衝液稀釋至500ml。
(4)濃稀釋液 稱取牛血清白蛋白1.0g,加洗滌液溶解並稀釋至100ml。
(5)稀釋液 濃稀釋液與水等體積混合。
(6)底物緩衝液(0.005mol/L醋酸鈉-枸櫞酸緩衝液) 稱取醋酸鈉0.68g、枸櫞酸(C6H8O7·H2O)1.05g,加水溶解並稀釋至1000ml,調pH值至3.6。
(7)底物液A 稱取3,3',5,5'-四甲基聯苯胺(TMB) 0.08g,加二甲基亞碸40ml溶解,加甲醇60ml,混勻,加底物緩衝液100ml,避光攪拌2小時至完全溶解,室溫靜置4小時。
(8)底物液B 量取1.5%過氧化氫溶液3.2ml,加底物緩衝液至1000ml。
(9)底物液 臨用前取底物液A、B等體積混合。
5.2 標準品溶液的製備
按試劑盒使用說明書用稀釋液溶解菌體蛋白質標準品,精密量取適量,用稀釋液稀釋成每1ml中含菌體蛋白質20ng、10ng、5ng、2.5ng、1.2ng、0.6ng、0.3ng的溶液。
5.3 供試品溶液的製備
取供試品適量,用稀釋液稀釋成每1ml中約含蛋白質100μg的溶液。如供試品每1ml中含蛋白質量小於200μg時,用濃稀釋液將供試品稀釋1倍。
5.4 測定法
取包被抗體,用包被液稀釋至適宜的濃度(稀釋倍數參見試劑盒介紹),以100μl/孔加至96孔酶標板內,在2~8℃放置16~20小時;用洗滌液洗板3次;用洗滌液製備1%牛血清白蛋白溶液,以200μl/孔加至酶標板內,置室溫振盪(每分鐘200~300轉)1小時,用洗滌液洗板3次;以100μl/孔加入標準品溶液和供試品溶液,每個稀釋度做雙孔,同時加入2孔空白對照(稀釋液),置室溫振盪(每分鐘200~300轉)1小時;用洗滌液洗板3次;按試劑盒介紹用稀釋液稀釋一抗至適宜的濃度,以100μl/孔加至酶標板內,置室溫振盪(每分鐘200~300轉)1小時;用洗滌液洗板3次;然後按試劑盒介紹用稀釋液稀釋辣根過氧化物酶(HRP)標記的二抗至適宜的濃度,以100μl/孔加至酶標板內,置室溫振盪(每分鐘200~300轉)30分鐘,用洗滌液洗板8次;以100μl/孔加入底物液,置室溫避光反應10~15分鐘,以100μl/孔加入終止液終止反應。用酶標儀在波長450nm處測定吸光度,應用計算機分析軟件進行讀數和數據分析,也可使用手工作圖法計算。
以標準品溶液吸光度對其相應的濃度作標準曲線,並以供試品溶液吸光度在標準曲線上得到相應菌體蛋白質含量,按以下公式計算:

n爲供試品稀釋倍數;
T爲供試品蛋白質含量,mg/ml。
6 附錄Ⅸ E 酵母工程菌菌體蛋白質殘留量測定法
本法系採用酶聯免疫法測定酵母表達系統生產的重組製品菌體蛋白質殘留量。
6.1 試劑
(1)包被液(pH9.6碳酸鹽緩衝液) 稱取碳酸鈉0.32g、碳酸氫鈉0.586g,加水溶解並稀釋至200ml。
(2) PBS 稱取氯化鈉8.0g、氯化鉀0.20g、磷酸氫二鈉1.44g、磷酸二氫鉀0.24g,加水溶解並稀釋至1000ml,調pH值至7.4,121℃滅菌15分鐘。
(3)洗滌液(PBS-Tween20) 量取聚山梨酯200.5ml,加PBS至1000ml。
(4)稀釋液 稱取牛血清白蛋白0.5g,加洗滌液溶解並稀釋至100ml。
(5)底物緩衝液(0.005mal/L醋酸鈉-枸櫞酸緩衝液) 稱取醋酸鈉0.68g、枸櫞酸(C6H8O7·H2O)1.05g,加水溶解並稀釋至1000ml,調pH值至3.6。
(6)底物液A 稱取3,3',5,5'-四甲基聯苯胺(TMB) 0.08g,加二甲基亞碸40ml溶解,加甲醇60ml,混勻,加底物緩衝液100ml,避光攪拌2小時至完全溶解,室溫靜置4小時。
(7)底物液B 量取1.5%過氧化氫溶液3.2ml,加底物緩衝液至1000ml。
(8)底物液 臨用前取底物液A、底物液B等體積混勻。
6.2 標準品溶液的製備
按試劑盒使用說明書加水復溶,精密量取適量,用稀釋液稀釋成每1ml中含菌體蛋白質1000ng、500pg、250ng、125ng、62.5ng的溶液。
6.3 供試品溶液的製備
取供試品適量,用稀釋液稀釋成適當濃度。
6.4 測定法
取豚鼠抗酵母工程菌蛋白質抗體適量,用包被液稀釋成適當濃度,以100μl/孔加至酶標板內,用保鮮膜封好,於4℃放置過夜;用洗滌液洗板3次,用洗滌液製備1%牛血清白蛋白溶液,以200μl/孔加至酶標板內,37℃放置2小時;將封閉好的酶標板用洗滌液洗板3次;以100μl/孔加入標準品溶液及供試品溶液,每個稀釋度做雙孔,同時加入2孔空白對照(稀釋液),封板,37℃放置1小時;用洗滌液洗板6次;按試劑盒使用說明書取兔抗酵母工程菌蛋白質抗體適量,用稀釋液稀釋成適當濃度,以100μl/孔加至酶標板內,封板,37℃放置1小時;用洗滌液洗板6次;用稀釋液稀釋辣根過氧化物酶標記的羊抗兔抗體溶液(IgG-HRP)至適當濃度,以100μl/孔加至酶標板內,用保鮮膜封好,37℃放置1小時;用洗滌液洗板6次,以100μl/孔加入底物液,室溫避光放置5~10分鐘;以100μl/孔加入終止液終止反應。用酶標儀以630nm波長爲參比波長,在波長450nm處測定吸光度,應用計算機分析軟件進行讀數和數據分析,也可使用手工作圖法計算。
以標準品溶液吸光度對其相應的濃度作標準曲線,並以供試品溶液吸光度在標準曲線上得到相應菌體蛋白質含量,按以下公式計算:

n爲供試品稀釋倍數;
T爲供試品蛋白質含量,mg/ml。
7 附錄Ⅸ F 激肽釋放酶原激活劑測定法
本法系採用顯色底物法(或顯色基質法)測定供試品中激肽釋放酶原激活劑(PKA)含量。
7.1 試劑
(1)0.05mol/L三羥甲基氨基甲烷-鹽酸(Tris-HCl)緩衝液(含0.15mol/L氯化鈉溶液,簡稱TNB) 稱取6.06g三羥甲基氨基甲烷(Tris,分子量爲121.14)及8.77g氯化鈉,加適量水溶解後,用1mol/L鹽酸調pH值至8.0,補加水至1000ml。
(2) 2mmol/L激肽釋放酶顯色底物(S-2302)溶液稱取S-2302 12.5mg,加10ml水溶解。
(3)前激肽釋放酶(PK) 採用適宜方法提純PK,小體積分裝,-30℃以下保存備用。
7.2 PKA標準品溶液的製備
取PKA標準品適量,用0.85%氯化鈉溶液分別稀釋成每1ml中含10.0IU、20.0IU、30.0IU、40.0IU、50.0IU的溶液。按每次用量,小體積分裝,-30℃保存備用。用前融化(僅允許凍融1次),並用TNB稀釋10倍。
7.3 供試品溶液的製備
取供試品適量,用TNB稀釋10倍。
7.4 測定法
取供試品溶液20μl,加至96孔微量滴定板孔內,加PK 20~50μl,同時開動秒錶計時,向每孔加PK的時間間隔應相同,將微孔滴定板振盪1分鐘;加蓋,於25~30℃放置30分鐘後,按加PK的順序和時間間隔向各反應孔加2mmol/L S-2302溶液20μl,振盪1分鐘;加蓋,於25~30℃放置15分鐘後,再以同樣的加液順序和時間間隔加50%醋酸溶液20μl,振盪1分鐘後,照紫外-可見分光光度法(2010年版藥典三部附錄Ⅱ A),在波長405nm處測定吸光度;同時以TNB 20~50μl代替PK 20~50μl,同法操作,作爲空白對照。用PKA標準品溶液的20μl替代供試品溶液,同法操作。以PKA標準品溶液的PKA活性的對數對其相應的吸光度對數作直線迴歸,求得直線迴歸方程,計算出供試品PKA活性。
7.5 【附註】
(1)每個PKA標準品溶液和供試品溶液做3孔,其中2個爲測定孔、1個爲對照孔,2個測定孔吸光度差值應小於0.020。
(2)每次測定可根據供試品PKA含量,適當調整PKA標準品溶液的範圍。
(4)加PK、S-2302及50%醋酸溶液時,各孔的間隔時間應相同,加液的順序要一致,儘可能使各孔處於同一反應條件下。
(5)加PK和加S-2302溶液後的放置時間系從第一孔加液時算起。
(6)如放置溫度低於25℃,應分別在兩次反應過程的限定時間內於37℃放置10分鐘。
8 附錄Ⅸ G 質粒丟失率檢查法
大腸桿菌表達系統的工程菌含有表達目的蛋白的表達質粒,質粒上一般帶有抗生素抗性基因便於篩選,在菌體傳代過程中,在一定濃度的抗生素環境下(如種子培養液),質粒丟失後菌體便不能存活,而在不含抗生素的發酵培養液中,隨着傳代代次的提高,可能有部分大腸桿菌丟失了質粒,失去了抗生素抗性基因,也同時失去表達目的蛋白的能力。通過比較在含有或不含抗生素培養基的菌體存活數,可以檢測質粒的丟失率,考查質粒穩定性。
實際操作中一般用模擬發酵或發酵過程實時收集的發酵液,包括最後階段(傳代最多代次)的收集液,經過適當稀釋後塗布於不含抗生素的培養基上,置37℃培養過夜;挑取不少於100個單菌落,分別接種到含抗生素和不含抗生素的培養皿中,置37℃培養過夜。比較兩者差異,一般應重複2次以上,計算質粒丟失率。工藝驗證中
9 附錄Ⅸ H SV40核酸序列檢查法
本法系通過設計2對特異引物擴增SV40 VP1 100bp(2220~2319)和大T抗原C端451bp (2619~3070)2個片段,採用PCR檢查供試品中是否存在SV40核酸序列。
供試品溶液及對照溶液的製備 取供試品400μl,加2%蛋白酶K溶液25μl、10% SDS溶液50μl、0.05mol/LEDTA溶液(pH8.0) 10μl,置56℃培養1小時,用等體積的酚-三氯甲烷(1:1)混合液抽提後,再用等體積的三氯甲烷抽提,加2倍體積的乙醇,-20℃放置16小時,以每分鐘10000轉離心15分鐘,沉澱用75%乙醇溶液洗滌乾燥,加無DNA酶和RNA酶的水10μl,使溶解。陽性對照及陰性對照按上述方法與供試品同時處理。
9.1 引物
VP1上游引物:2220 5'-ACA CAG CAA CCA CAG TGG TTC-3' 2240
VP1 下游引物:2319 5'-GTA AAC AGC CCA CAA ATG TCA AC-3' 2297
T抗原C端上游引物:3070 5'-GAC CTG TGG CTG AGT TTG CTC A-3' 3049
T抗原C端下游引物:2619 5'-GCT TTA TTT GTA ACC ATT ATA AG3' 2641
9.2 檢查法
(1)每個待擴增的供試品引物加量爲30×10-12mol,DNA模板加量爲1μl.總體積50μl。在PCR儀上以94℃先變性3分鐘,然後94℃變性20秒、50℃退火20秒、72℃延伸40秒,共進行40個循環;72℃延伸3分鐘。
(2)擴增產物電泳檢查 2%瓊脂糖凝膠(每1ml含1μg溴化乙錠),緩衝液爲1×TAE.在100V條件下電泳40分鐘,檢查擴增片段。VP1擴增片段爲100bp,大T抗原C端片段爲451bp。
(3)以同樣模板重複擴增VP1片段,排除污染因素導致的非特異擴增;或將擴增產物及對照從膠上移至Hybond N尼龍膜上,與VP1探針進行免疫印跡試驗,以證明所擴增片段確爲VP1片段。
(4)以自動測序儀對供試品及陽性對照的大T抗原C端擴增產物進行序列測定。
9.3 結果判定
若未能擴增出VP1片段,則結果判定爲未檢出SV40核酸序列。
若擴增出VP1片段,可重複試驗1次,仍未擴增出VP1片段者,判定爲未檢出SV40核酸序列。
若重試仍能擴增出VP1片段,則應擴增大T抗原C端片段,如擴增出大T抗原C端片段,應將其擴增產物和陽性對照擴增產物進行測序並比較,核酸序列一致判定爲檢出SV40核酸序列;如未擴增出大T抗原C端片段,則可按上述步驟(1)~(3)重複試驗1次,如仍未擴增出大T抗原C端片段,則可判定爲未檢出SV40核酸序列。
10 附錄Ⅸ I 類A血型物質測定法(血凝抑制法)
本法系用標準類A血型物質和供試品分別與抗A血型血清反應.通過比較血凝反應終點,測定供試品中類A血型物質含量。
10.1 1%A型人紅細胞懸液
將6人份A型血等量混合,加適量生理氯化鈉溶液混勻,以每分鐘2000轉離心10分鐘,傾去上清液,用生理氯化鈉溶液洗3次,吸取沉積紅細胞1ml.加生理氯化鈉溶液99ml,混勻,製成1%A型人紅細胞懸液。
10.2 標準類A血型物質溶液的製備
由國家藥品檢定機構分發或經其認可。將標準品製成每1ml中含1mg的標準溶液。取1組10支直徑9mm的試管,將標準溶液用生理氯化鈉溶液做2倍系列稀釋,體積爲0.1ml,由1/100稀釋度(每1mt含0.01mg)開始。
10.3 供試品溶液的製備
取1組10支直徑9mm的試管,將供試品用生理氯化鈉溶液做2倍系列稀釋,體積爲0.1ml,由供試品開始。
10.4 抗A血型血清試驗劑量的測定
取1組10支直徑9mm的試管,將抗A血型血清用生理氯化鈉溶液做2倍系列稀釋,體積爲0.1ml,由1/2稀釋度開始,加1%A型人紅細胞懸液0.1ml;同時取生理氯化鈉溶液0.1ml與1%A型人紅細胞0.1ml作爲陰性對照。搖勻,室溫放置15分鐘,以每分鐘1500轉離心1分鐘,根據細胞沉降壓縮情況觀察凝集程度。以呈現完全凝集(++++)的抗A血型血清的最高稀釋度爲1個抗體試驗劑量。
10.5 測定法
在每稀釋度供試品及標準類A血型物質溶液中分別加含2個抗體試驗劑量的抗A血型血清0.1ml。搖勻,36.5~37.5℃放置10分鐘,再於上述各管中分別加入1%A型人紅細胞懸液0.1ml,搖勻,36.5~37.5℃放置15分鐘.以每分鐘1500轉離心1分鐘,根據紅細胞沉降壓縮情況觀察凝集程度。
10.6 結果判定
供試品呈現完全血凝抑制(終點)的最高稀釋倍數乘以對照組呈現相似瓶凝抑制的最高倍稀釋管的血型物質含量,即爲每1ml供試品所含類A血型物質的質量( mg)。
11 附錄Ⅸ J 抗A、抗B血凝素測定法(間接抗人球蛋白法)
本法系採用間接抗人球蛋白法(Coombs試驗),測定供試品中抗A、抗B血凝素。
11.1 試劑
(1)紅細胞懸液 取A型、B型及RhD陽性的O型紅細胞各3例,分別混合,用適量生理氯化鈉溶液洗滌3次,最後以每分鐘2000轉離心5分鐘,吸取沉澱紅細胞適量,用生理氯化鈉溶液分別製成5% (ml/ml)紅細胞懸液。自紅細胞採集之日起1周內使用。
(2)抗人球蛋白血清 爲多價抗人球蛋白血清,使用前需標定,選擇適宜的稀釋度用於試驗,如生產廠商有說明,按介紹稀釋後使用,也可按附註方法確定。
11.2 測定法
取供試品適量,用生理氯化鈉溶液做2倍系列稀釋,每個稀釋度的供試品使用2排管( 75mm×12mm小試管),每管分別加入供試品溶液0.2ml,向第1排各管加A型5%紅細胞懸液0.2ml,第2排各管加B型5%紅細胞懸液0.2ml,混勻,置37℃水浴30分鐘,用適量的生理氯化鈉溶液洗滌3次,每次以每分鐘1000轉離心1分鐘,每管加入抗人球蛋白血清0.2ml,混勻,以每分鐘1000轉離心1分鐘,肉眼觀察結果。本試驗同時設陰性對照、陽性對照及紅細胞對照。
(1)陰性對照 取AB型人血清0.2ml(雙份),分別加入5%A型及B型紅細胞懸液0.2ml,混勻,自“置37℃水浴30分鐘”起,同法操作。
(2)陽性對照 取抗RhD血清(IgG型)0.2ml,加入5% RhD陽性O型紅細胞0.2ml,混勻,自“置37℃水浴30分鐘”起,同法操作。
(3)紅細胞對照 取生理氯化鈉溶液0.2ml(雙份),分別加入5%A型及B型紅細胞懸液0.2ml,混勻,自“置37℃水浴30分鐘”起,同法操作。
11.3 結果判定
陰性對照及紅細胞對照結果均呈陰性,陽性對照結果不低於“+++”,試驗成立。
抗A、抗B血凝素滴度以產生“+”凝集的供試品最高稀釋倍數計算,不計紅細胞懸液及抗人球蛋白血清的體積。
11.4 【附註】
(1)供試品爲凝血因子Ⅷ製劑時,需先用生理氯化鈉溶液預稀釋成每1ml中含4IU後,再進行測定。
(2)抗人球蛋白血清的標定 將抗人球蛋白血清和抗RhD血清分別用生理氯化鈉溶液做2倍系列稀釋,每管0.2ml,於稀釋的抗RhD血清管中加入5% RhD陽性的O型壓積紅細胞懸液0.1ml,混勻後置37℃水浴中30分鐘,用生理氯化鈉溶液洗3次並配成2%紅細胞懸液,取每個稀釋度致敏紅細胞懸液0.2ml,分別加入1排稀釋的抗人球蛋白血清中,混勻,以每分鐘1000轉離心1分鐘,判定結果。用等量未致敏人RhD陽性O型紅細胞替代致敏紅細胞,同法操作,作爲陰性對照。陰性對照成立,以出現“+”血凝反應的抗RhD血清的最高稀釋倍數所對應的抗人球蛋白血清的最高稀釋倍數爲最適稀釋度。
++++ 一個結實的凝集塊;
+++ 幾個大的凝集塊;
++ 中等大的凝集塊,背景清晰;
+ 小凝集塊,背景渾濁;
12 附錄Ⅸ K 抗補體活性測定法
本法系採用免疫溶血反應作指示系統,根據供試品消耗補體所反映出的溶血率變化,測定供試品的抗補體試劑
(1)鎂-鈣貯備液 稱取氯化鈣1.103g、氯化鎂(MgCl2·6H2O) 5.083g,加水溶解並稀釋至25ml。
(2)巴比妥緩衝液貯備液 稱取氯化鈉41.5g、巴比妥鈉5.1g,加水800ml溶解。用1mol/L鹽酸溶液調pH值至7.3,加鎂-鈣貯備液2.5ml。加水稀釋至1000ml,用0.22μm膜濾過,4℃保存備用。
(3)明膠巴比妥緩衝液(GVB) 稱取明膠0.625g,加水30ml煮沸使溶解,加巴比妥緩衝液貯備液100ml,再加水稀釋至500ml,新鮮製備,當天使用。
(4)阿氏液(Alsever's 液) 稱取枸櫞酸0.5g、枸櫞酸鈉8.0g、葡萄糖20.5g、氯化鈉4.2g,加水溶解並稀釋至1000ml(pH6.2左右)。根據一次採羊血需要量將該溶液分裝於採血瓶中,116℃蒸汽滅菌10分鐘(滅菌後,儘快釋放蒸汽)。放冷後置4℃冰箱保存備用。
(5)綿羊紅細胞 由綿羊頸靜脈無菌採集全血適量,與等體積的阿氏液混合,無菌分裝,4℃保存1周後方可使用。
(7)豚鼠血清(補體) 取10只以上豚鼠血清,混合,4℃離心除去血細胞,分裝,-70℃保存,也可凍幹保存。豚鼠血清每1ml中的補體總活性應不低於100 CH50。
12.1 5%羊紅細胞懸液製備
取綿羊紅細胞適量,用加明膠巴比妥緩衝液至少洗3次後,懸浮於適量明膠巴比妥緩衝液中。取0.2ml紅細胞懸液,加至2.8ml水中,待紅細胞完全溶解後照紫外-可見分光光度法(2010年版藥典三部附錄Ⅱ A)在波長541nm處測定吸光度,根據下列公式,將該溶液的吸光度調節至0.62±0.01(每1ml紅細胞懸液含紅細胞1×109個)。
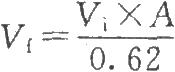
式中Vi爲稀釋前紅細胞懸液體積,ml;
Vf爲稀釋後紅細胞懸液體積,ml。
12.2 溶血素滴定
按表1稀釋溶血素。從1: 75稀釋的溶血素開始,1.0ml不同稀釋度的溶血素分別與5%羊紅細胞懸液1.0ml混合,37℃放置30分鐘後,取0.2ml,加明膠巴比妥緩衝液1.10ml,稀釋的豚鼠補體溶液(如150倍稀釋補體)0.2ml,37℃放置60分鐘後,以每分鐘2000轉離心5分鐘,吸取上清液,照紫外-可見分光光度法(2010年版藥典三部附錄Ⅱ A)在波長541nm處測定各管吸光度。每個稀釋度做2管,同時再做3管未溶血對照管(明膠巴比妥緩衝液1.4ml,加5%羊紅細胞懸液0.1ml),3管全溶血管(水1.4ml加5%羊紅細胞懸液0.1ml),同法操作。按下式計算各管溶血率(Y),以Y值爲縱座標,以不同溶血素稀釋度爲橫座標作圖,從而確定敏化羊紅細胞所用的溶血素的稀釋度。選擇增加溶血素的量也不影響Y值的溶血素的稀釋度,爲每1ml含1個最小溶血單位(即每1ml含1MHU)。最小溶血率應在50%~70%範圍,否則試驗不成立。

表1 溶血素稀釋
製備 | 製備 | ||||||
溶血素 稀釋度 | 明膠巴比妥 緩衝液/ml | 溶血素 | 溶血素 稀釋度 | 明膠巴比妥 緩衝液/ml | 溶血素 | ||
稀釋度 | ml | 稀釋度 | ml | ||||
7.5 10 75 100 150 200 300 400 | 0.60 0.90 1.80 1.80 1.00 1.00 1.00 1.00 | 未稀釋的 未稀釋的 7.5 10 75 100 150 200 | 0.1 0.1 0.2 0.2 1.0 1.0 1.0 1.0 | 600 800 1200 1600 2400 3200 4800 | 1.00 1.00 1.00 1.00 1.00 1.00 1.00 | 300 400 600 800 1200 1600 2400 | 1.0 1.0 1.0 1.0 1.0 1.0 1.0 |
最適敏化的羊紅細胞(EA)的製備 量取每1ml含2MHU的溶血素(A)適量,緩慢注入等體積的5%羊紅細胞(E)懸液中,37℃放置15分鐘後,2~8℃保存,6小時內使用。
12.3 滴定豚鼠血清中補體活性
用明膠巴比妥緩衝液適當稀釋豚鼠血清,然後按表2滴定補體。以補體用量的對數對Y/(1-Y)的對數作直線迴歸,求出直線迴歸方程的截距(a)、斜率(b)和相關係數(r)。補體活性按下式計算:
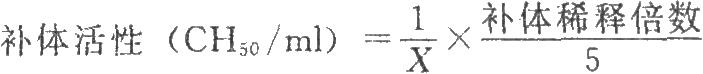
式中1/X爲a值反對數的倒數。
1 | 2 | 3 | 4 | 5 | 6 | 7 | |
GVB/ml | 1.2 | 1.1 | 1.0 | 0.9 | 0.8 | 0.7 | 0.6 |
適當稀釋的補體/ml | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 |
EA/ml | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
8 | 9 | 10 | 11 | 12 | 13 | 14 | |
GVB/ml | 0.5 | 0.4 | 0.3 | 0.2 | 0.1 | 1.3 | 1.3(水) |
適當稀釋的補體/ml | 0.8 | 0.9 | 1.0 | 1.1 | 1.2 | - | - |
EA/ml | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
37℃培養60分鐘→冰浴中冷卻→每分鐘2000轉離心5分鐘→取上清液測吸光度
12.4 抗補體活性測定
根據測得的豚鼠血清補體活性,用加明膠巴比妥緩衝液稀釋成每1ml含100CH50溶液,按表3製備培養混合物。表3中靜注人免疫球蛋白(IVIG)是按每1ml含50mg濃度計算的。如果IVIG的濃度不是每1ml含50mg時,則按下式計算IVIG的加量(V),然後再根據IVIG的實際取量計算明膠巴比妥緩衝液的加入量;但要保持供試品加緩衝液的總量爲0.8ml。將此混合物於37℃放置60分鐘後,取0.2ml加9.8ml明膠色比妥緩衝液(50倍稀釋),測定剩餘補體活性。

表3 供試品及補體對照管制備
按下式計算供試品抗補體活性。D爲每1ml含80~120 CH50時,試驗成立。
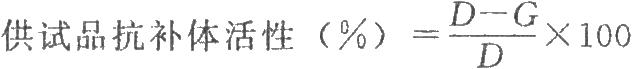
G爲供試品管剩餘補體活性,CH50/ml。
12.5 【附註】
13 附錄Ⅸ L 鼠IgG殘留量測定法
本法系用酶聯免疫法測定經單克隆抗體親和色譜方法純化的重組製品中鼠IgG殘留量。
13.1 試劑
(1)包被液(pH9.6碳酸鹽緩衝液) 稱取碳酸鈉0.32g、碳酸氫鈉0.586g,加水溶解並稀釋至200ml。
(2) PBS (pH7.4) 稱取氯化鈉8.0g、氯化鉀0.20g、磷酸氫二鈉1.44g、磷酸二氫鉀0.24g,加水溶解並稀釋至1000ml,121℃滅菌15分鐘。
(3)洗滌液(PBS-Tween20) 量取聚山梨酯200.5ml,加PBS稀釋至1000ml。
(4)稀釋液 稱取牛血清白蛋白0.5g,加洗滌液溶解並稀釋至100ml。
(5)底物緩衝液(枸櫞酸-PBS) 稱取磷酸氫二鈉(Na2HPO4·12H2O)1.84g、枸櫞酸0.51g,加水溶解並稀釋至100ml。
(6)底物液 取鄰苯二胺8mg、30%過氧化氫溶液30μl,溶於底物緩衝液20ml中。臨用前配製。
13.2 標準品溶液的製備
按使用說明書用適量水復溶鼠IgG標準品。精密量取適量,用稀釋液稀釋成每1ml中含100ng、50ng、25ng、12.5ng、6.25ng、3.13ng的溶液。
13.3 供試品溶液的製備
取供試品適量,用稀釋液稀釋成每1ml中含1個成品劑量(如未能確定製劑的規格,則按成品的最大劑量計算)的溶液。
13.4 測定法
取山羊抗鼠IgG抗體適量,用包被液稀釋成每1ml含10μg的溶液;以100μl/孔加至96孔酶標板內,4℃放置過夜(16~18小時),用洗滌液洗板3次;用洗滌液製備1%牛血清白蛋白溶液,以200μl孔加至酶標板內,37℃封閉2小時,將封閉好的酶標板用洗滌液洗3次,以100μl/孔加標準品溶液和供試品溶液,37℃放置1小時,將封閉好的酶標板用洗滌液洗3次;按使用說明書用稀釋液稀釋辣根過氧化物酶標記的綿羊抗鼠IgG抗體,以100μl/孔加至酶標板內,37℃放置30分鐘,用洗滌液洗板3次;以50μl/孔加入底物液,37℃避光放置20分鐘,以50μl/孔加入終止液(1mol/L,硫酸溶液)終止反應。用酶標儀在波長492nm處測定吸光度,應用計算機分析軟件進行讀數和數據分析,也可使用手工作圖法計算。以標準品溶液吸光度對其相應的濃度作標準曲線,線性迴歸的相關係數應大於0.995。以供試品溶液吸光度在標準曲線上讀出相應的鼠IgG殘留量。
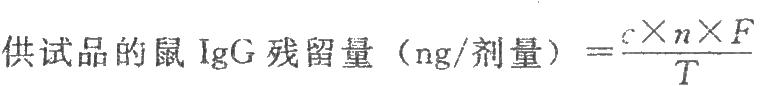
式中 c爲供試品溶液鼠IgG殘留量,ng/ml;
n爲供試品溶液的稀釋倍數;
14 附錄Ⅸ N 人凝血酶活性檢查法
本法系依據凝.血酶能使人纖維蛋白原凝固的原理,將供試品和人纖維蛋白原混合,觀察是否產生凝塊,以此判定供試品是否具有凝血酶活性。
14.1 試劑
(1)0.5%纖維蛋白原溶液 用生理氯化鈉溶液將復溶的凍幹人纖維蛋白原溶液稀釋成每1ml含5ng的溶液。
(2)人凝血酶溶液 用生理氯化鈉溶液將復溶的凍幹人凝血酶稀釋成每1ml中含0.5IU的溶液。
14.2 測定法
取供試品0.2ml,加0.5%纖維蛋白原溶液0.2ml,37℃放置24小時,觀察有無凝塊或纖維蛋白析出。放置期聞至少觀察2次,同時做陰性對照及陽性對照。
(1)陰性對照 用0.2ml生理氯化鈉溶液替代供試品,同法操作。
(2)陽性對照 用0.2ml凝血酶溶液(每1ml含0.5 IU)替代供試品,同法操作。
14.3 結果判定
陰性對照無任何凝塊或纖維蛋白析出,陽性對照有凝塊或纖維蛋白析出,則試驗成立。肉眼觀察供試品應無凝塊或纖維蛋白析出。
【附註】 含肝素的供試品應根據肝素含量,用適量的硫酸魚精蛋白中和供試品內的肝素(按10μg硫酸魚精蛋白中和1IU肝素進行),再取供試品照上述方法檢查。
15 附錄Ⅸ O 活化的凝血因子活性檢查法
本法系依據活化的凝血因子在腦磷脂存在下,使缺血小板人血漿發生凝固的原理,將供試品和缺血小板人血漿及腦磷脂混合,測定凝固時間,根據凝固時間判定供試品是否含有活化的凝血因子。
15.1 試劑
(1)缺血小板人血漿 無菌採集人全血於3.8%枸櫞酸鈉抗凝劑(體積比9:1)中,混勻,以每分鐘1500轉4℃離心30分鐘,用塑料注射器取上層2/3的血漿,以每分鐘3500轉4℃離心30分鐘,取上層2/3血漿,分裝於塑料管中,每支3ml,保存於-40℃備用。
(2)三羥甲基氨基甲烷(Tris)緩衝液(pH7.5)稱取三羥甲基氨基甲烷7.27g、氯化鈉5.27g,加水溶解並稀釋至1000ml(用鹽酸調pH值至7.5)。
(3)腦磷脂混懸液 凍幹腦磷脂加水復溶,量取適量用生理氯化鈉溶液稀釋,稀釋後的腦磷脂混懸液應使空白凝固時間在200~300秒。
(4) 0.025mol/L氯化鈣溶液 稱取氯化鈣(CaCl2·2H2O) 147g溶予1000ml水中,製成1mol/L氯化鈣貯備液。臨用時,用水將1mol/L氯化鈣貯備液稀釋40倍。(5)硫酸魚精蛋白溶液 稱取硫酸魚精蛋白適量,用pH7.5的Tris緩衝液溶解並稀釋成適宜濃度的溶液。
15.2 供試品溶液的製備
取復溶後的供試品,根據測得的肝素含量(2010年版藥典三部附錄Ⅸ P)加硫酸魚精蛋白溶液適量,中和供試品中的肝素(10μg硫酸魚精蛋白中和1IU肝素),再用Tris緩衝液(pH7.5)稀釋10倍和100倍。
15.3 測定法
取缺血小板人血漿0.1ml,加腦磷脂混懸液0.1ml,混勻,37℃放置1分鐘,加供試品溶液(10倍或100倍稀釋液)0.1ml、已預熱至37℃的0.025mol/L氯化鈣溶液0.1ml,記錄凝固時間。用Tris緩衝液(pH7.5) 0.1ml替代供試品溶液,同法操作,作空白對照。
15.4 結果判定
空白對照凝固時間不低於200秒,試驗成立。1: 10和1: 100供試品稀釋液凝固時間均應不低於150秒。
15.5 【附註】
(1)直接與血和血漿接觸的器具應爲塑料製品或硅化的玻璃製品。從供試品稀釋到測定完畢應在30分鐘內完成。
(2)供試品每個稀釋度做2管。
16 附錄Ⅸ P 肝素含量測定法(凝固法)
本法系依據硫酸魚精蛋白能中和抗凝劑肝素,從而影響血漿凝固時間的原理,測定供試品中肝素含量。
16.1 試劑
(1)缺血小板人血漿 無菌採集人全血於3.8%枸櫞酸鈉抗凝劑(體積比9:1)中,混勻,以每分鐘1500轉4℃離心30分鐘,用塑料注射器取上層2/3的血漿,以每分鐘3500轉4℃離心30分鐘,取上層2/3血漿,分裝於塑料管中,每支3ml,-40℃保存備用。
(2)三羥甲基氨基甲烷(Tris)緩衝液(pH7.5) 稱取三羥甲基氨基甲烷7.27g、氯化鈉5.27g,加水溶解並稀釋至1000ml(用鹽酸調pH值至7.5)。
(3)腦磷脂混懸液 凍幹腦磷脂加水復溶,取適量,用生理氯化鈉溶液稀釋,稀釋後的腦磷脂混懸液應使空白凝固時間在200~300秒。
(4) 0.025mol/L氯化鈣溶液 稱取氯化鈣(CaCl2·2H2O) 147g溶於1000ml水中,製成1mol/L氯化鈣貯備液。臨用時,用水將1mol/L氯化鈣貯備液稀釋40倍。
(5)硫酸魚精蛋白溶液 取硫酸魚精蛋白適量,用pH7.5 Tris緩衝液溶解並稀釋成每1ml含1~20mg的溶液。
16.2 供試品溶液的製備
於每支含不同濃度的硫酸魚精蛋白溶液10μl的塑料管中,分別加入按標示量復溶後的供試品0.5ml,混勻。
16.3 測定法
在已含有缺血小板人血漿0.1ml的塑料管中,加入腦磷脂混懸液0.1ml,混勻,37℃放置1分鐘,加供試品溶液0.1ml、已預熱至37℃的0.025mol/L氯化鈣溶液0.1ml,記錄凝固時間。用Tris緩衝液(pH7.5)0.1ml替代供試品溶液,同法操作,作空白對照。空白對照凝固時間不低於200秒,試驗成立。取凝固時間最短的供試品管,作爲硫酸魚精蛋白中和0.5ml供試品中的肝素量。硫酸魚精蛋白10μg中和1IU肝素。例如凝固時間最短的供試品管中含硫酸魚精蛋白30μg,則中和供試品0.5ml中的肝素量爲3IU,即供試品每1ml含6IU肝素。
16.4 【附註】
17 附錄Ⅸ Q 人紅細胞抗體測定法(微量板法)
本法系依據紅細胞與紅細胞抗體結合後發生凝集的原理,通過比較血凝反應終點,測定供試品中人紅細胞抗體效價。
17.1 試劑
1% O型紅細胞懸液 取3例或3例以上O型抗凝血混合,採血後7天內使用。用前以生理氯化鈉溶液洗滌3次,末次以每分鐘2000轉離心10分鐘,取壓積紅細胞適量,用生理氯化鈉溶液製成1%濃度備用。
17.2 測定法
在“V"形、底角呈90°的96孔微量板上,用生理氯化鈉溶液將供試品做2倍系列稀釋,每個供試品做2排,每孔加入50μl。再向每孔加入1% O型紅細胞懸液50μl,輕拍微量板30秒混勻。室溫靜置3小時觀察結果,同時用生理氯化鈉溶液替代供試品,同法操作,作陰性對照。
17.3 結果判定
將微量板置於白色背景之上,將供試品孔與陰性對照孔比較,紅細胞沉於底部成一規則的圓點而孔壁未粘有紅細胞判爲陰性;孔壁上均勻附着1層紅細胞,或紅細胞未全部沉於底部,部分附着於孔壁上均判爲陽性。以供試品出現陽性的最高稀釋倍數爲其紅細胞抗體的效價。如同批供試品前後排結果相差在1個以上稀釋度時應重試。相差1個稀釋度時,則以2排結果中出現陽性的最高稀釋度爲該供試品的紅細胞抗體效價。
18 附錄Ⅸ R 人血小板抗體測定法
本法系採用血小板與血小板抗體結合後,使血小板發生凝集的原理,通過比較凝集反應終點測定供試品中人血小板抗體效價。
18.1 試劑
(1)5%乙二胺四乙酸二鈉(EDTA)抗凝劑稱取磷酸氫二鈉(Na2HPO4·12H2O)0.365g、磷酸二氫鉀0.875g、氯化鈉2.125g、乙二胺四乙酸二鈉(EDTA-Na2·2H2O) 12.5g,加水溶解並稀釋至250ml。
(2)0.33% EDTA溶液 稱取磷酸氫二鈉(Na2HPO4·12H2O)0.73g、磷酸二氫鉀1.75g、氯化鈉4.25g、乙二胺四乙酸二鈉(EDTA-Na2·2H2O)1.65g、加水溶解並稀釋至500ml。
(3)血小板稀釋液 取3人份以上AB型血清混合,56℃滅能30分鐘,按AB型血清每100ml加硫酸鋇50g的比例加入硫酸鋇,置37℃吸附1小時,隨時攪動,然後以每分鐘3000轉離心30分鐘,棄去沉澱,吸上清液備用。試驗當天按1份血清加3份生理氯化鈉溶液配成血小板稀釋液(注意AB型血清中不得混有紅細胞及溶血)。(4)血小板懸液的製備 採集人靜脈血 20ml,按5%EDTA溶液與全血以1:9(體積比)的比例混合,於20℃以每分鐘800轉離心15分鐘,取上層血漿加0.33%EDTA溶液至原全血體積,於20℃以每分鐘1500轉離心10分鐘,棄去上清液,如此再重複用0.33% EDTA洗滌2次,棄上清液,向沉澱中加血小板稀釋液0.5ml,混勻,計數並將血小板濃度調至2.5×105~3.5×105/mm3即可(注意:計數時血小板懸液應在計數板上靜置2~3分鐘,並在10分鐘內計數完)。
18.2 供試品溶液的製備
用生理氯化鈉溶液將供試品做2倍系列稀釋至1: 16。
18.3 陽性對照溶液的製備
取經人血小板免疫的豬血漿(或兔血清)0.5ml,60℃滅能10分鐘,用硫酸鋇0.05g於37℃吸附15分鐘後,以每分鐘3000轉離心20分鐘,取上清液備用。
18.4 陰性對照溶液的製備
18.5 測定法
量取不同稀釋度供試品溶液各0.1ml,分別加血小板懸液0.1ml,於37℃保溫30分鐘後,滴到計數板上,靜置2~3分鐘,在20~40倍顯微鏡下觀察結果。本試驗同時設陰性對照、陽性對照組。
(1)陽性對照 取陽性對照溶液0.1ml,自“加血小板懸液0.1ml”起,同法操作。
(2)陰性對照 取陰性對照溶液0.1ml,自“加血小板懸液0.1ml”起,同法操作。
18.6 結果判定
陽性對照爲“++”;陰性對照爲“-”;試驗成立。以“+”爲判定終點,即以供試品出現“+”的最高稀釋度爲該供試品的血小板抗體效價。
18.7 【附註】
(1)“-”無凝塊或偶見2~3個血小板成串。
19 附錄Ⅸ S 無細胞百日咳疫苗鑑別試驗(酶聯免疫法)
本法系採用酶聯免疫法測定無細胞百日咳疫苗有效組分百日咳毒素(PT)和絲狀血凝素(FHA)。
19.1 試劑
(1)包被液(pH9.6碳酸鹽緩衝液) 稱取碳酸鈉1.59g,碳酸氫鈉2.93g,加水溶解,定容至1000ml。
(2)磷酸鹽緩衝液(pH7.4) 稱取氯化鈉8.0g、氯化鉀0.20g、磷酸氫二鈉1.44g、磷酸二氫鉀0.24g,加水溶解並稀釋至1000ml,121℃滅菌15分鐘。
(3)洗滌液(PBS-Tween20) 量取聚山梨酯20(Tween20)0.5ml,加磷酸鹽緩衝液稀釋至1000ml。
(4)封閉液 稱取牛血清白蛋白1.0g,加洗滌液溶解並稀釋至100ml。
(5)稀釋液 稱取牛血清白蛋白0.5g,加洗滌液溶解並稀釋至100ml。
(6)底物緩衝液(0.005mol/L醋酸鈉-枸櫞酸緩衝液) 稱取醋酸鈉0.68g、枸櫞酸(C6H8O7·H2O)1.05g.加水溶解並稀釋至1000ml,調pH值至3.6。
(7)底物液A 稱取3,3',5,5'-四甲基聯苯胺(TMB) 0.08g,加二甲基亞碸40ml溶解,加甲醇60ml,混勻,加底物緩衝液100ml,避光攪拌2小時至完全溶解.室溫靜置4小時後使用。
(8)底物液B 量取1.5%過氧化氫溶液3.2ml,加底物緩衝液稀釋至1000ml。
(9)底物液 取底物液A和底物液B等體積混勻,臨用前配製。
19.2 陽性對照的製備
用純化的PT或FHA參考品作陽性對照(2~8μg/ml)。
19.3 陰性對照的製備
用PBS或其他適宜的對照品作陰性對照。
19.4 供試品溶液的製備
取疫苗供試品適量,加枸櫞酸鈉或其他適宜的試劑進行疫苗解吸附處理。
19.5 測定法
分別取PT抗體或FHA抗體(2~5μg/ml)適量,以100μl/孔加至酶標板內,用封口膜封好,2~8℃放置16~20小時;用洗滌液洗板3次,以200μl/孔加封閉液至酶標板內,用封口膜封好,37℃放置1小時;將封閉好的酶標板用洗滌液洗板3次,以100μl/孔加入,PT或FHA陽性對照和供試品溶液,37℃放置1小時;用洗滌液洗板6次,稀釋辣根過氧化物酶標記的PT抗體或FHA抗體至適當濃度,以100μl/孔加至酶標板內,用封口膜封好,37℃放置1小時;用洗滌液洗板6次,以100μl/孔加入底物液,室溫避光放置5~l5分鐘;以50μl/孔加入終止液終止反應。用酶標儀在適宜波長處測定吸光度。
19.6 結果判定
20 附錄Ⅸ T 抗毒素、抗血清製品鑑別試驗(酶聯免疫法)
20.1 試劑
(1)包被液(pH9.6碳酸鹽緩衝液) 稱取碳酸鈉0.32g、碳酸氫鈉0.586g,加水溶解並稀釋至200ml。
(2)磷酸鹽緩衝液(pH7.4) 稱取氯化鈉8.0g、氯化鉀0.20g、磷酸氫二鈉(Na2HPO4)1.44g、磷酸二氫鉀0.24g,加水溶解並稀釋至1000ml,121℃滅菌15分鐘。
(3)洗滌液(PBS-Tween20) 量取聚山梨酯200.5ml,加磷酸鹽緩衝液至1000ml。
(4)封閉液 稱取牛血清白蛋白2.0g,加洗滌液溶解並稀釋至100ml。
(5)稀釋液 稱取牛血清白蛋白0.5g,加洗滌液溶解並稀釋至100ml。
(6)底物緩衝液(0.005mol/L醋酸鈉-枸櫞酸緩衝液) 稱取醋酸鈉0.68g、枸櫞酸(C6H8O7·H2O)1.05g,加水溶解並稀釋至1000ml,調pH值至3.6。
(7)底物液A 稱取3,3',5,5'-四甲基聯苯胺0.08g.加二甲基亞碸40ml溶解,加甲醇60ml,混勻,加底物緩衝液100ml,避光攪拌2小時至完全溶解,避光室溫靜置4小時。
(8)底物液B 量取1.5%過氧化氫溶液3.2ml,加底物緩衝液稀釋至1000ml。
(9)底物液 取底物液A、底物液B等體積混勻。臨用前配製。
20.2 陰性對照、陽性對照的製備
用馬IgG作陽性對照,用人IgG、牛IgG、羊IgG、豬IgG作陰性對照,取陰性對照、陽性對照,用包被液稀釋至適宜濃度。
20.3 供試品溶液的製備
取供試品適量,用包被液稀釋成5~10μg/ml。
20.4 測定法
取供試品溶液及對照溶液,分別以100μl/孔加至酶標板內,供試品溶液及對照溶液均做雙孔,用封口膜封好,2~8℃放置16~20小時;用洗滌液洗板3次,用封閉液以200μl/孔加至酶標板內,用封口膜封好,37℃放置1小時;將封閉好的酶標板用洗滌液洗板3次,用稀釋液按1: 2000稀釋辣根過氧化物酶標記的兔抗馬IgG抗體,以100μl/孔加至酶標板內,用封口膜封好,37℃放置1小時;用洗滌液洗板6次,以100μl/孔加入底物液,室溫避光放置5~15分鐘;以100μl/孔加入終止液終止反應。用酶標儀在波長450nm處測定吸光度。
20.5 結果判定
取4種陰性對照中吸光度最高的計算Cutoff值,Cutoff值爲陰性對照吸光度(2孔平均值)的2.1倍。陽性對照的吸光度大於Cutoff值則試驗成立,供試品吸光度大於Cutoff值時爲陽性,表示供試品與馬IgG同源。