3 標準基本信息
ICS 11.020
C 50
中華人民共和國衛生行業標準 WS/T 489—2016《尿路感染臨牀微生物實驗室診斷》(laboratory diagnosis of urinary tract infections)由中華人民共和國國家衛生和計劃生育委員會於2016年07月07日發佈,自2016年12月15日起實施。
4 前言
本標準按照GB/T 1.1—2009給出的規則起草。
本標準起草單位:中國醫學科學院北京協和醫院、中國人民解放軍總醫院第一附屬醫院、北京醫院、上海交通大學附屬瑞金醫院、天津市公安醫院、復旦大學附屬中山醫院、華中科技大學同濟醫學院附屬同濟醫院、北京電力醫院、香港瑪麗醫院。
本標準主要起草人:徐英春、竇紅濤、張麗、陳雨、範欣、蔣偉、胡云建、倪語星、王金良、胡必傑、孫自鏞、趙銳、梁浩鈞。
5 標準正文
5.1 1 範圍
本標準適用於開展尿液標本細菌培養、鑑定和藥物敏感性試驗的微生物實驗室。
5.2 2 術語和定義
下列術語和定義適用於本文件。
2.1
尿路感染 urinary tract infection
由各種病原體入侵泌尿系統引起的疾病。根據感染部位可分爲上尿路感染(腎盂腎炎、輸尿管炎)和下尿路感染(膀胱炎、尿道炎);根據有無尿路異常(如梗阻、結石、畸形、膀胱輸尿管反流等)分爲複雜性和非複雜性尿路感染。
2.2
白細胞尿 leukocyturia
膿尿 pyuria
5.3 3 標本採集
5.3.1 3.1 總則
宜採集晨尿,囑患者睡前少喝水或不喝水,尿液在膀胱內瀦留至少4h以上,可降低假陰性率。無症狀的患者應連續採集3天晨尿送檢。尿液標本質量的影響因素較多,即使採用侵入性的尿液採集法仍可能被皮膚、會陰或尿道等處正常菌羣污染,因此減少污染是保證尿液標本質量的關鍵。
5.3.2 3.2 清潔中段尿採集
清晨起牀後用肥皂水清洗會陰部,女性應分開大陰脣,男性應上翻包皮,仔細清洗,再用清水沖洗尿道口周圍。將前段的尿液丟棄,留取中段尿液約10 mL直接排入無菌容器中,立即送檢,採集後於0.5 h內進行接種。尿流不暢、包皮過長或衛生條件不好的患者易造成尿液標本污染。清潔中段尿是臨牀最易獲得的尿液標本。
5.3.3 3.3 恥骨上膀胱穿刺採集
評估膀胱內細菌感染的“金標準”。消毒臍部至尿道皮膚,對穿刺部位皮膚進行局麻;在恥骨聯合和臍部中線部位將針頭插入充盈的膀胱,從膀胱吸取約20 mL尿液;無菌操作將尿液注入無菌螺口杯,送至實驗室。這一方法可用於診斷尿道厭氧菌感染,也是兒科患者、脊柱損傷患者和沒有獲得明確培養結果的患者最常用的方法。
5.3.4 3.4 留置導尿管採集
採用無菌技術用注射器經導尿管抽取尿液。先消毒導尿管採樣口,按無菌操作方法用注射器穿刺導尿管吸取尿液;如果需要,將導管夾閉在管中採集尿標本,但夾閉時間不能超過0.5 h。尿液標本不能通過收集袋引流管口流出的方式採集。長期留置導管的患者進行常規尿培養意義不大,這些患者通常會培養出大量定植菌。
5.3.5 3.5 膀胱導尿採集
局部消毒後,採用導尿管經尿道插入膀胱收集尿液,嚴格採用無菌技術插入導管,避免帶入細菌,棄去最開始導出的15 mL~30 mL尿液後再收集培養的尿液。注意避免將下尿道細菌經導管引入膀胱,導致繼發性感染。
5.3.6 3.6 嬰幼兒尿液採集袋採集
由於嬰幼兒不能自主控制膀胱收縮,需要用採集袋。此法很難避免會陰部正常菌羣的污染,易出現假陽性,因此該方法尿液培養結果陰性更有意義。如培養結果陽性,必要時可用膀胱導尿或恥骨上膀胱穿刺法採集尿液標本進一步確證有無尿道感染。
5.3.7 3.7 其他採集方法
其他不常用的尿液採集方法還包括迴腸導管導尿採集、間歇性導尿管採集、腎盂造瘻術、輸尿管造口術、膀胱鏡檢查術採集等。
5.4 4 標本標識
應註明患者的基本信息、採集方法、採集時間、臨牀初步診斷(需註明有無尿路感染的臨牀表現)、患者是否攝入過量的水以及抗菌藥物使用情況等。
5.5 5 標本運送
尿液標本應儘快送到實驗室,若不能及時送達,應4℃冷藏或添加防腐劑(含0.5 mL的硼酸甘油或硼酸甲酸鈉),但均不能超過24 h。加人防腐劑的尿液標本,至少採集3 mL尿液量,以避免高濃度的防腐劑對致病微生物產生抑制或稀釋作用。
5.6 6 標本接收
收集尿液容器爲廣口的無菌防漏容器,收到尿液標本後應立即接種。冷藏的標本不能用於淋病奈瑟菌培養。
5.7 7 標本拒收
5.7.1 7.1 不合格標本處理
收到不合格標本,應與臨牀醫師聯繫,註明拒收的原因並退回,可要求重新留取標本,並做記錄。若不合格不能重新留取尿液而需培養時,應在報告中注明,並強調此培養結果僅供參考。
5.7.2 7.2 標本拒收的情況
標本拒收的情況包括:
a) 標本標識與申請單不符,標識錯誤或沒有標識;
b) 未提供採集時間及採集方法;
f) 導尿管尖端培養;
h) 標本送檢時容器有滲漏;
i) 除恥骨上膀胱穿刺法外,採用其他方法採集標本申請做厭氧菌培養。
5.8 8 實驗室檢查
5.8.1 8.1 尿常規(與尿路感染相關指標)
8.1.1 白細胞酯酶
8.1.2 亞硝酸鹽
正常值爲陰性。陽性常見於大腸埃希菌等革蘭陰性桿菌引起的尿路感染,陽性反應程度與尿液中細菌的數量成正比。
8.1.3 尿蛋白
正常定性爲陰性,定量<100 mg/24 h。尿路感染可有蛋白尿。
5.8.2 8.2 尿沉渣檢查(與尿路感染相關指標)
8.2.1 人工檢查
取10 mL尿液RCF 400×g離心5 min,棄上清,留0.2 mL混勻後,計數1μL中的有形成分。白細胞計數大於正常參考區間,同時伴有上皮細胞增多提示尿路感染。吞噬細胞出現提示泌尿系統急性炎症,其數量常與嚴重程度密切相關。
8.2.2 儀器檢查
尿液分析儀主要有2大類:影像式尿液有形成分分析儀,流式細胞術和電阻抗檢測相結合的全自動尿有形成分分析儀。白細胞計數大於儀器正常參考區間,同時伴有上皮細胞增多提示尿路感染。但應人工檢查排除干擾因素。
5.8.3 8.3 革蘭染色鏡檢
觀察有無細菌、多形核白細胞和扁平上皮細胞。女性尿液標本中如果存在許多扁平上皮細胞,提示標本很可能受到陰道分泌物污染,應重新送檢。該方法適用於篩查有較高的菌落計數患者、大部分無症狀患者以及患有腎盂腎炎的患者。爲了提高在104CFU/mL水平的敏感度,推薦細胞離心塗片後再革蘭染色鏡檢。當革蘭染色陽性時,與菌尿症相關,並且可以根據細菌形態和染色特性,幫助臨牀經驗治療選擇抗菌藥物。
5.8.4 8.4 尿培養
8.4.1 培養類型選擇:如何接種培養尿液標本,取決於標本的採集方法、患者的症狀和臨牀指徵。尿液標本接種要求實驗室收集必要的信息,包括尿液採集方法、患者的類型(例如:泌尿科或老年病科)、臨牀症狀、尿液常規鏡檢分析結果以及既往培養結果,以選擇相應的培養類型,見表1。
表1 尿液培養類型與結果的解釋
培養 類型 | 適用人羣 | 採集方法 | 培養方法 | 生長情況CFU/mL | 後續試驗 |
常規 | a)門診患者 | 清潔中段尿 | 1μL或10μL接種至血瓊脂平板,麥康凱或中國藍瓊脂平板。5%CO2培養18 h~24 h。若無菌生長,應延長培養至48 h | 鑑定+藥敏 | |
其他任何種類的細菌≥104 | 初步鑑定 | ||||
b)留置導尿管患者 c)老年患者 | 清潔中段尿 | 1μL或10μL接種至血瓊脂平板,麥康 | 菌≥104 | 鑑定+藥敏 | |
其他任何種類的細菌≥104 | 初步鑑定 | ||||
特殊 | b)膀胱導尿採集 | 10μL,接種至血瓊脂平板、巧克力瓊脂、麥康凱瓊脂或中國藍瓊脂。懷疑特殊病原菌感染,如厭氧菌、淋病奈瑟菌、結核分枝桿菌,應當分別選擇厭氧培養、GC瓊脂及羅氏培養基。5%CO2培養48 h | 鑑定+藥敏 | ||
2種菌≥102 |
5.8.5 8.5 接種方法
8.5.1 輕搖混勻尿液,將定量接種環垂直浸入尿液標本表面下3 mm~5 mm,將標本吸至環中。
8.5.2 在血瓊脂平板上劃十字,再進行密集均勻塗布。
8.5.3 除接種至血平板進行定量外,還需分區劃線接種至麥康凱或中國藍瓊脂平板進行菌株篩查。
5.8.6 8.6 病原菌同源性檢測
病原菌同源性檢測可協助診斷多次尿道感染的患者爲複發性感染還是再發性感染(如患有反覆尿道感染的女性),也可用於檢測不同患者感染同一細菌克隆的情況(如可疑醫院感染或社區內暴發流行)。常用的基因分型方法包括脈衝場凝膠電泳、核酸分型、多位點酶電泳、普通PCR或多重PCR分型方法。
5.9 9 抗菌藥物敏感試驗
5.9.1 9.1 抗菌藥物敏感試驗
對菌落計數結果有意義的臨牀分離菌株,鑑定到種水平並進行標準抗菌藥物敏感試驗,可採用微量肉湯稀釋法、紙片擴散法、Etest法或自動化藥敏分析儀等。
5.9.2 9.2 直接抗菌藥物敏感試驗
直接抗菌藥物敏感試驗僅適用於細菌計數≥105CFU/mL的純培養菌,其目的是縮短報告時間,減少患者醫療花費。但需注意,該方法缺乏標準化程序,不建議作爲常規藥敏試驗方法;不能用於混合細菌生長的標本;不適用於細菌計數<105CFU/mL的標本;由微生物實驗室自行解釋藥敏試驗結果。
5.10 10 結果解釋
5.10.1 10.1 總述
採用1μL接種量,計數結果爲平板菌落數×103CFU/mL;採用10μL接種量,計數結果爲平板菌落數×102CFU/mL。建議臨牀醫師結合尿常規結果分析尿培養結果的臨牀意義。
5.10.2 10.2 一般解釋
清潔中段尿定量培養後,單種細菌菌落數>105CFU/mL可能爲感染;<104CFU/mL可能爲污染,104CFU/mL~105CFU/mL需要根據患者的臨牀表現進行評估,大部分腎盂腎炎和膀胱炎可以根據這些參數正確地予以判斷。對於複雜性尿道感染可多次送檢。連續3次清潔中段晨尿培養>105CFU/mL高度懷疑尿路感染。
5.10.3 10.3 不同類型尿培養的解釋
不同感染類型的清潔中段尿定量培養結果相應的解釋,分別見表2和表3;侵入性採集標本培養結果解釋見表4。
5.10.4 10.4 特殊細菌感染的解釋
10.4.1 採用特殊培養基並延長培養時間後分離出大量的尿道或陰道的正常菌羣時,包括棒桿菌屬、陰道加德納菌、流感嗜血桿菌和副流感嗜血桿菌等,可能與尿道感染相關。
10.4.2 解脲棒桿菌(Corynebacterium urealyticum):較少引起尿道感染的革蘭陽性桿菌。通常發生在嚴重免疫缺陷、泌尿道侵入性操作或長期住院的老年患者,並與腎盂腎炎有關,且在無抗菌藥物治療情況下可自動消失。
10.4.3 解葡糖苷棒桿菌(Corynebacterium glucuronolyticum):也稱爲生殖棒桿菌(Corynebacterium seminale),可引起前列腺炎和尿道炎,並能產生大量尿素酶。
臨牀表現 | 細菌計數CFU/mL | 病原菌種數 | 結果解釋 | 是否做藥敏試驗 | |
有 | ≥104/mL | 其他菌種≥105 | ≤2 | 是 | |
有 | ≥104/mL | <103 | b) 正在使用抗生素 | 不確定 | |
有 | <104/mL | ≥105 | ≤2 | 否 | |
是 | |||||
無 | 不確定 | 103~104 | ≥1 | 否 | |
無 | 不確定 | >105 | ≥2 | 定植 | 否 |
不確定 | <104/mL | <103 | — | 無尿路感染或定植 | 不確定 |
背景 | 臨牀表現 | ≤2種病原菌菌尿CFU/mL | 結果解釋 | 是否做藥敏試驗 | |
無導尿管患者 | 有 | ≥104/mL | ≥103 | 是 | |
<103 | b) 正在使用抗生素 | 不確定 | |||
無 | 不確定 | ≥103 | 定植 | 否 | |
<103 | 不確定 | ||||
有 | <104/mL | ≥105 | 否 | ||
植患者) | 是 |
表3(續)
背景 | 臨牀表現 | ≤2種病原菌菌尿CFU/mL | 結果解釋 | 是否做藥敏試驗 | |
插導尿管患者 | 有 | 有導尿管存在時白細胞尿沒有意義 | ≥105 | 是 | |
<105 | b) 正在使用抗牛素 | 否 | |||
無 | 有導尿管存在時白細胞尿沒有意義 | ≥103 | 定植 | 否 | |
<103 | 不確定 |
10.4.4 流感嗜血桿菌(Haemophilus influenzae)和副流感嗜血桿菌(Haemophilus parainfluenzae):尿道感染的發生率很低。建議在兒童的尿培養中加用巧克力平板。
10.4.5 很少引起尿路感染的細菌:厭氧菌、放線桿菌屬、乳桿菌屬、α-溶血鏈球菌、凝固酶陰性葡萄球菌(年輕女性尿標本分離腐生葡萄球菌除外)、棒桿菌屬和一些不常見革蘭陰性桿菌。
5.11 11 報告結果
5.11.1 11.1 陰性結果
培養48 h無菌生長,應報告“接種1μL尿液,培養48 h無菌生長(<103CFU/mL,無臨牀意義)”,或“接種10 μL尿液,培養48 h無菌生長(<102CFU/mL,無臨牀意義)”。嚴格無菌操作如恥骨上膀胱穿刺採集的尿液,可直接報告“培養48 h無菌生長”。
5.11.2 11.2 陽性結果
11.2.1 有明確臨牀意義:報告菌落計數、細菌種名及抗菌藥物敏感試驗結果。
11.2.2 無明確臨牀意義:報告菌落計數、革蘭染色形態特徵並註明純菌或混合菌生長。
5.12 12 操作流程
操作流程見圖1。
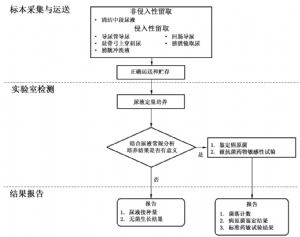
圖1 尿路感染實驗室診斷操作流程
6 參考文獻
[1] 徐英春,倪語星,王金良,等.尿道感染實驗診斷規範.上海:上海科學技術出版社,2009.
[2] Eileen M.Burd and K.Sue Kehl.A Critical Appraisal of the Role of the Clinical MicrobiologyLaboratory in the Diagnosis of Urinary Tract Infections.J Clin Microbiol.2011.49(9):S34-S38.
[3] Cornaglia G,Courcol R,Herrmann JL,et al.European Mannual of Clinical Microbiology,1stEdition: 133-143.ESCMID.
[4] Clarridge JE,Johnson JR,Pezzlo MT,et al.Laboratory Dianosis of Urinary Tract Infections.cumitech 2B.American Society for Microbiology.1998: 1-2.