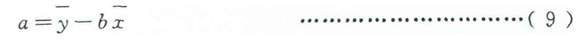2 英文參考
Guide to interference testing in clinical chemistry
ICS 11.020
C50
中華人民共和國衛生行業標準 WS/T 416—2013《干擾實驗指南》(Guide to interference testing in clinical chemistry)由中華人民共和國國家衛生和計劃生育委員會於2013年07月16日發佈,自2013年12月01日起實施。
3 前言
本標準按照GB/T 1.1—2009給出的規則起草。
本標準主要起草單位:衛生部臨牀檢驗中心、北京大學第一醫院、北京協和醫院、首都醫科大學附屬北京同仁醫院。
本標準主要起草人:汪靜、陳文祥、趙海艦、謝潔紅、王冬環、申子瑜、王學晶、邱玲、劉向褘。
干擾實驗指南
5 2 術語和定義
下列術語和定義適用於本文件。
2.1
干擾 interference
在臨牀化學中,被測物濃度因樣品特性或其他成分的影響而出現的臨牀顯著性偏差。這種影響可見於檢測系統的非特異性、指示反應響應不佳、被測物活性抑制等情況。
2.2
干擾物 interfering substance
[JJF 1001—1998,定義4.8]
2.2.1
內源性干擾物 endogenous interferent
因病理原因在樣品中出現的物質(如膽紅素或血紅蛋白),可干擾對其他物質的檢測。
2.2.2
外源性干擾物 exogenous interferent
樣品中來自於體外的可干擾其他物質檢測的物質(如藥物及其代謝物、樣品防腐劑等)。
2.3
干擾標準 interference criteria
被測物濃度與真值間可產生的最大允許干擾偏差,此偏差可能影響醫生的醫療決定。
2.4
被測量 measurand
作爲測量對象的特定量。
[JJF 1001—1998,定義4.7]
2.5
特異性specificity
2.6
總分析誤差 total analytical error
[JCGM 200:2008,定義2.16]
6 3 干擾實驗方案
6.1 3.1 干擾物對檢測結果的影響
6.1.1 3.1.1 干擾物的干擾效果
3.1.1.1 檢測方法的總分析誤差有3個主要來源:不精密度、方法特異性偏差、樣品特異性偏差。方法學評價時通常只考慮前兩者,樣品特異性偏差常被認爲與特定樣品有關,不屬於方法學的計量特徵。但如果一種檢測方法本身易受某種干擾物質的影響,則干擾物既可引起系統誤差也可引起偶然誤差。
3.1.1.2 當採用特異性更好的方法做爲比對方法時,特定病人羣體樣品中某種干擾物的平均濃度可引起系統偏差,而偏離平均偏差的個體差異則成爲總偶然誤差的成分。某些方法中隨機干擾效果超過不精密度成爲偶然誤差的主要來源。
3.1.1.3 對於個體患者,干擾物的干擾效果可隨樣品中干擾物濃度的不同發生變化,這可被誤認爲是患者病情的改變。
3.1.1.4 干擾物對檢測結果的影響可通過一些方法進行補償或修正,使干擾效果在特定患者羣體中減小。對於常見的內源性干擾物(如膽紅素、血紅蛋白、脂類等),可通過樣品前處理、樣品空白、血清基質校準或數學修正等方法減少干擾效果。
6.1.2 3.1.2 干擾效果機制
——化學效應:干擾物通過與試劑競爭或抑制指示反應改變反應結果,也可通過絡合或沉澱作用改變分析物的形式。
——物理效應:干擾物可具有與被測量相近的性質,如熒光、顏色、光散射、洗脫位置或檢測時的電極反應等。
——基質效應:干擾物可改變樣品基質的物理特性,如黏度、表面張力、濁度或離子強度等,從而改變被測量濃度。
——酶抑制作用:干擾物可與金屬激活因子形成螯合物、與催化位點結合、氧化必需巰基基團而改變被測量或試劑中酶的活性。
——檢測方法的非特異性:干擾物以與被測量同樣的方式參與反應。儘管非特異性與干擾有所不同,但對實驗結果的效果是相同的。如酮酸在鹼性苦味酸法測肌酐時發生反應,吲哚硫酸鹽在重氮法測膽紅素時發生反應,免疫化學中的交叉反應等。
——水的取代效應:非水溶性物質(蛋白、脂類等)可通過取代液體血漿量影響活性測量。但如測定的是血漿水中被測量的濃度,則不存在水的取代效應。
6.2 3.2 干擾標準及被測量與干擾物實驗濃度的確定
6.2.1 3.2.1 建立被評價方法的干擾標準
因干擾所致的允許誤差標準與實驗結果的臨牀應用有關,可通過總允許誤差進行推斷。總允許誤差(TEa)包含方法學偏差、不精密度及干擾成分,是對檢測方法的準確性要求。對於已明確提出準確性要求的分析物,可從總允許誤差中減去方法學偏差、不精密度及相應生物學變異,剩餘殘差即爲干擾成分。對於無明確準確性要求的分析物,可採用下述方法確定總允許誤差:
a) 根據生物學變異確定總允許誤差:不同被測量均有其固有的個體內生物學變異(CvI)及個體間生物學變異(CvG).現被廣泛接受的觀點是檢測方法的理想質量指標爲結果偏倚BA<
b)通過臨牀實踐得出總允許誤差:基於大量臨牀和實驗室經驗,經過廣泛討論,由專業學會、組織或個人在專業建議中提出的準確性指標。
c) 據分析變異確定總允許誤差:干擾標準也可從總的長期分析不精密度中得出。如果干擾物所引起的誤差小於一個標準差,則可認爲被評價干擾物的作用不大可能影響臨牀決定,因此不認爲這種物質是干擾物。但考慮到現有的檢測系統常具有極佳的精密度,用這種方法決定干擾標準可能使很多物質的干擾效果放大。
d)基於法規和室間質量評價的質量規範:總允許誤差也可以從有關實驗室質量管理的法規中得到。如《臨牀實驗室改進修正案1988》(CLIA'88)中提供的常見檢測項目的質量規範。常見生化檢驗項目的CLIA'88質量規範參見附錄A。
6.2.2 3.2.2 被測量實驗濃度的確定
宜選取被測量的2個醫學決定水平作爲干擾實驗時的被測量濃度,也可根據臨牀需要選用參考範圍的高限或低限或病理濃度。附錄B中列出了常見被測量的建議實驗濃度。
6.2.3 3.2.3 可能引起干擾作用的物質清單
干擾實驗開始前應根據被評價方法的檢測原理和預期用途列出可能引起干擾效果的物質清單。常見的可能產生干擾作用的物質有:
——樣本中的異常物質:高濃度的血紅蛋白、膽紅素、甘油三酯等。
——藥物:常見處方與非處方藥,接受某項目檢測的特定病人羣體中常用的藥物。
——代謝物:在特定病人羣體中可能出現的異常生化代謝物與藥物代謝物。
——樣品添加劑及在樣品採集與處理過程中可與之接觸的物質:抗凝劑(肝素、EDTA、檸檬酸鹽、草酸鹽等)與防腐劑(NaF、HCl、碘醋酸鹽等).血清分離膠,樣品採集容器及膠塞、導管、導管衝冼液、皮膚消毒劑、手部清潔劑、玻璃清洗液、手套粉末等。
——文獻中提及的對與被評價方法類似的其他方法有干擾作用的物質。
6.2.4 3.2.4 干擾物的實驗濃度
進行干擾實驗時干擾物的濃度可根據表1確定,常見可能內源性干擾物的建議實驗濃度參見附錄C,藥物干擾物的建議實驗濃度請參見有關文獻。
表1 干擾物的實驗濃度確定原則
表1(續)
可能干擾物 | 樣品類型 | 干擾物實驗濃度 |
樣品採集與處理設備 | 樣品與設備接觸24 h,樣品體積應與實際使用相同,需注意防止樣品蒸發與不穩定分析物的丟失,同時應準備一份與實驗樣品相同的對比樣品,此樣品除了不與實驗設備接觸外其餘處理過程均與實驗樣品相同 |
6.3 3.3 對實驗操作人員的要求
實驗操作人員應熟悉被評價檢測系統的性能,熟練掌握操作流程,明確樣品的正確處理方法,在確保儀器狀態正常的情況下采用適當的校準品對儀器進行校準。
6.4 3.4 對檢測系統的要求
6.4.1 3.4.1 儀器
儀器性能應滿足干擾實驗的要求。精密度應與廠家參數相一致,也可根據相應衛生行業標準進行精密度評估。方法學偏差應通過回收實驗或方法學比較實驗(參見相應衛生行業標準)確定,恆定偏差不會影響干擾實驗結果,但比例性偏差卻可能造成對干擾實驗結果的錯誤判斷。儀器檢測時不應存在明顯的攜帶污染。在實驗開始前,分析系統應表現出穩定的運行狀態。實驗期內應據統計學質控程序對運行狀態進行監測。
6.4.2 3.4.2 試劑
進行干擾實驗時應採用有效期內的相同批號試劑。試劑的貯存與配製應嚴格按照產品說明進行。
6.4.3 3.4.3 校準品
應採用與被評價試劑配套的校準品或經實驗驗證可用於被評價檢測系統的產品。校準品的使用應嚴格按照產品說明,儀器校準步驟與間隔應按照實驗室內標準操作程序進行。
6.5 3.5 實驗室安全
干擾評價實驗中使用的所有樣品均應按感染性物質處理。實驗室廢棄物的處理、實驗人員防護及實驗室環境應符合生物安全2級防護要求。
6.6 3.6 干擾物篩查實驗
6.6.1 3.6.1 概述
3.2.3中列出的干擾物清單中可能包括多種物質,需要通過干擾物篩查實驗對這些物質進行初步鑑別。實驗方法爲首先在基礎樣品中添加較高濃度的可能干擾物質,使之成爲實驗樣品,然後分別檢測實驗樣品與對照樣品中的被測量濃度,通過配對£檢驗判斷兩樣品的測定結果間差異是否具有統計學意義。如沒有統計學意義,則由此物質引起的偏差不會影響臨牀決定,不認爲此物質是干擾物。如具有統計學意義,則考慮此物質可能具有干擾作用,需進一步實驗以確定干擾物濃度與其產生的干擾效應間的關係。
6.6.2 3.6.2 樣品製備
6.6.2.1 3.6.2.1 基礎樣品
從未服用過藥物的健康人羣中採集新鮮標本(血清、尿液等),將標本混勻後即成爲基礎樣品。
如新鮮標本難以取得,也可採用冰凍或凍幹樣品。但應注意這類樣品中含有防腐劑與穩定劑或其他可能會對檢測結果造成影響的成分。因此在應用此類樣品之前應對其基質效應進行評價。
確定基礎樣品中的被測量濃度,可通過添加純分析物使樣品中被測量濃度達到醫學決定水平。
6.6.2.2 3.6.2.2 干擾物原液
干擾物質的純品多爲固體,需要用適當的溶劑將其溶解,製成干擾物原液。如所用的是藥品級製品,應注意所含賦形劑、防腐劑、殺菌劑、抗氧化劑、着色劑、調味劑、金屬氧化物、填充物等對檢測結果造成的影響。
溶劑應使干擾物充分溶解且不會影響檢測結果。常用溶劑有純水、鹽酸溶液或氫氧化鈉溶液、乙醇或甲醇、丙酮、二甲基亞碸等。
原液濃度應至少20倍於實驗濃度,以減少對基礎樣品基質的稀釋。應注意防止有機溶劑的揮發並考慮其在水中的溶解度。
6.6.2.3 3.6.2.3 實驗樣品與對照樣品
以20倍於實驗濃度的干擾物原液爲例,實驗樣品與對照樣品的製備方法見表2。注意樣品製備時取樣體積必須準確,必要時可採用容量瓶。
6.6.3 3.6.3 測定重複次數
爲排除被評價方法的精密度對干擾效果的影響,每份樣品的測定次數需根據統計學檢驗的置信水平與檢驗效能及被評價方法的批內精密度與干擾標準計算得出。設統計假設1類錯誤的概率爲α,2類錯誤的概率爲β,干擾方向不明確時使用雙側檢驗,計算公式見式(1).干擾方向已確定時則使用單側檢驗,計算公式見式(2)。
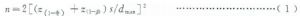
式中:
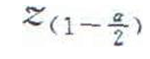
z(1-β)——檢驗效能100(1-β)%時正態分佈所對應的百分位數,常見檢驗效能下的Z值參見表3;
式中:
Z(1-α)——單邊檢驗100(1-α)%置信水平時正態分佈所對應的百分位數。
其餘符號所示內容見式(1)。
爲便於使用,表4中列出了95%置信水平與檢驗效能下不同干擾標準所需要的樣品重複測定數。
6.6.4 3.6.4 測定步驟
3.6.4.1 將實驗樣品(T)與對照樣品(C)按3.6.3中計算出的重複數n各分裝n份。
3.6.4.2 用被評價方法檢測樣品中被測量濃度,樣品測定順序爲C1、T1、C2、T2、C3、T3---Cn、Tn。
3.6.4.3 如檢測系統存在攜帶污染,可在檢測過程中加測對照樣品以減少實驗樣品的可能污染,測定順序爲C1、T1、Cx、Cx、C2、T2、Cx、Cx、C3、T3…Cx、Cx、Cn、Tn。此處Cx爲加測的對照樣品,其測定結果不參加實驗數據分析。
3.6.4.4 記錄檢測結果,格式可參照附錄D。
6.6.5 3.6.5 數據處理與分析
3.6.5.1 計算干擾效果
用實驗樣品與對照樣品測定均值間的偏差(dobs)表示干擾效果,計算公式見式(3)。

式中:
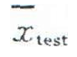

3.6.5.2 計算界值dc
雙側檢驗時界值計算公式見式(4),單側檢驗時界值計算公式見式(5)。

式中:
dnull——無效假設的值,通常爲0;
z(1-α/2)——相對於雙邊檢驗100(1-α)%置信水平時正態分佈的百分數;
z(1-α)——相對於單邊檢驗100(1-α)%置信水平時正態分佈的百分數;
n——樣品重複次數。
3.6.5.3 計算干擾效果的95%置信區間
計算干擾效果的95%置信區間η見式(6)。
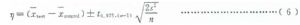
式中:
t0.97s,(n-1)——自由度爲n-1,t分佈的第97.5%概率密度值。當n>30時t0.975,(n-1)近似等於2.0;
η——每個樣品的重複次數。其餘符號所示內容見式(3)。
3.6.5.4 結果分析
如果dobs≤dc,則可判斷由被評價干擾物所致偏差未超過允許標準,不認爲此物質爲干擾物。反之則認爲被評價干擾物對被評價方法有明顯干擾作用。
6.7 3.7 干擾物劑量效應評價實驗
6.7.1 3.7.1 概述
對於經干擾篩查證明對被評價方法有明顯干擾作用的可能干擾物,需對其在不同濃度下對測定結果的干擾效應進行評價。
6.7.2 3.7.2 樣品製備
6.7.2.1 3.7.2.1 基礎樣品
參見3.6.2.1製備方法。
6.7.2.2 3.7.2.2 干擾物原液
參見3.6.2.2製備方法。
6.7.2.3 3.7.2.3 干擾物高實驗濃度樣品與低實驗濃度樣品
干擾物高實驗濃度樣品製備方法參見3.6.2.3中實驗樣品的製備,其干擾物終濃度可參見附錄C。干擾物低濃度樣品的製備參見3.6.2.3中對照樣品的製備,其干擾物終濃度爲臨牀標本中此干擾物的平均濃度,常可忽略爲零。
6.7.2.4 3.7.2.4 實驗樣品系列的製備
將3.7.2.3中干擾物高實驗濃度樣品與低實驗濃度樣品定量混合,可得到干擾物濃度介於兩樣品之間的一系列實驗樣品。確定線性劑量相關關係時需要5個濃度水平。具體制備方法見表5。
6.7.3 3.7.3 測定重複次數
與干擾篩查實驗一樣,評價干擾物劑量效應時也需排除方法精密度對結果的影響,通常每個水平重複測定3次即可滿足要求。
6.7.4 3.7.4 測定步驟
3.7.4.1 將實驗系列樣品每份分裝3支。
3.7.4.2 所有樣品一次檢測完成。將樣品按干擾物濃度從低到高的順序命名爲樣品1、2、3、4、5,則檢測順序爲第一組測定按升序(12345).第二組測定按降序(54321),第三組爲升序。
3.7.4.3 也可按隨機數表爲樣品進行分組,決定檢測順序。
3.7.4.4 記錄檢測結果,格式可參照附錄E。
6.7.5 3.7.5 數據處理與分析
6.7.5.1 3.7.5.1 概述
計算最低干擾物濃度樣品的測定均值,用5個水平樣品的每個測定值減去此均值得出不同濃度干擾物的干擾效果。以干擾效果爲Y值,干擾物濃度爲X值,繪出干擾物劑量相關曲線。根據曲線趨勢進行數據分析。
6.7.5.2 3.7.5.2 線性相關
3.7.5.2.1 如曲線爲近似直線,可用最小二乘法分析,數學模型見式(7)。
Yij= a+bXij+Eij ……(7)
式中:
α——截距;
b——斜率;
Eij——第i個樣品第j次重複測定時實測值與預測值的差。
3.7.5.2.2 計算線性迴歸方程的相關參數,通過迴歸分析,可得到Yi與Xi間的數學關係式及相關參數。斜率b的計算公式見式(8)。
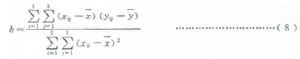
式中:
截距a的計算公式見式(9)。
式中符號所示內容見式(8)。
迴歸方程的估計標準誤syx計算公式見式(10)。
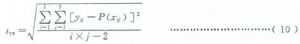
式中:
P(xij)——樣品中干擾物濃度爲xij時由迴歸方程得出的y預測值;
i——樣品數,此處爲5;
j——每份樣品的重複測定次數,此處爲3;
其餘符號所示內容見式(7)。
迴歸方程斜率b的標準誤sb計算公式見式(11)。

式中符號所示內容見式(7)、式(8)、式(10)。
3.7.5.2.3 對斜率b進行統計學檢驗:對迴歸方程的斜率b進行t檢驗。設總體迴歸係數爲β,假設檢驗爲H0:β=0,H1:β≠0。
據式(12)計算統計量t。

式中:
β——總體迴歸係數,此處爲0;
b——迴歸方程的斜率;
sb——迴歸方程斜率b的標準誤。
由t值表查出t(0.05,i·j-2),如t>t(0.05,i·j-2),表明p<0.05,否定H0,接受H1,斜率b有統計學意義,直線迴歸方程成立。如t
3.7.5.2.4 計算干擾物濃度對測定結果干擾效應的90%置信區間:某一確定干擾物濃度對測定結果干擾效應的雙側95%置信區間的計算公式見式(13)。
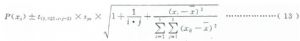
式中:
P(xi)——樣品中干擾物濃度爲xi時由迴歸方程得出的y預測值;
t(0.025,i·j-2)——自由度爲i·j-2,此處爲13,t分佈的第2.5%概率密度值;
其餘符號所示內容見式(7)、式(8)、式(10)。
3.7.5.2.5 結果分析:迴歸方程的斜率b表示干擾物每個濃度單位所造成的干擾效果,斜率爲正表明干擾物引起正向干擾,反之爲負向干擾。截距a表示對內源性干擾物濃度的修正。干擾物任意濃度下對測定結果的影響程度可由迴歸方程得出。
6.7.5.3 3.7.5.3 非線性相關
如干擾劑量效應曲線爲非線性,可採用非線性迴歸分析得出相應的最佳擬合曲線與數學模型,置信區間可用適當的非線性迴歸分析程序計算。具體計算方法較爲複雜,建議採用統計學軟件,如SPSS、SAS等進行計算。根據得出的最佳數學模型可推斷出在評價範圍內任意干擾物濃度所引起的干擾效應值。
7 4 干擾實驗報告
干擾實驗報告中應包括以下主要內容:
a) 被評價檢測系統的名稱、品牌、型號、所用試劑、校準品、質控品的生產廠家、批號;
b) 被測量的名稱;
c) 被評價干擾物化學名稱或通用名稱;
d) 干擾評價方案依據;
g) 在描述干擾效果時,可用以下方式:
1) 列出干擾物質的特定濃度.高於此濃度可引起超過干擾標準的偏差;
2) 列出干擾物質的特定濃度.低於此濃度未觀察到具臨牀意義的干擾。
h) 當定量信息無法得到或引用參考文獻中的相關內容時,須將可能干擾物質及其對被評價方法不具干擾性的信息以方法特異性說明的方式進行總結說明。
8 附錄A(資料性附錄)常見生化項目質量指標
項目 | CLIA'88中的質量規範 | ||||||
允許cv% | 允許的偏倚% | 允許總誤差(Tea)% | 允許變異 | 允許的偏倚 | 允許總誤差 | ||
期望 | 最低 | ||||||
12.2 | 12 | 32.1 | 48.1 | 6.67% | 10.0% | 20% | |
6 | 5.4 | 15.2 | 22.8 | 6.67% | 10.0% | 20% | |
AMY | 4.8 | 7.8 | 15.7 | 23.5 | 10.0% | 15.0% | 30% |
LDH | 4.3 | 4.3 | 9.5 | 14.2 | 6.67% | 10.0% | 20% |
11.4 | 11.5 | 30.3 | 45.5 | 10.0% | 15.0% | 30% | |
GGT | 6.9 | 10.8 | 22.2 | 33.3 | - | - | - |
ALP | 3.2 | 6.4 | 11.7 | 17.5 | 10.0% | 15.0% | 30% |
1.4 | 1.2 | 3.4 | 5.2 | 3.33% | 5.0% | 10% | |
ALB | 1.6 | 1.3 | 3.9 | 5.8 | 3.33% | 5.0% | 10% |
T-BIL | 12.8 | 10 | 31.1 | 46.6 | - | - | - |
D-BIL | 18.4 | 14.2 | 44.5 | 66.8 | - | - | -- |
UA | 4.3 | 4.8 | 11.9 | 17.9 | 5.67% | 8.5% | 17% |
UREA | 6.2 | 5.5 | 15.7 | 23.5 | 0.33 mg/dL或4.5% | 1 mg/dL或4.5% | 2 mg/dL或9% |
CREA | 2.2 | 3.4 | 6.9 | 10.4 | 0.1 mg/dL或5% | 0.15 mg/dL或7.5% | 0.3 mg/dL或15% |
GLU | 3.3 | 2.3 | 7.9 | 11.8 | 2 mg/dL或3.3% | 3 mg/dL或5% | 6 mg/dL或10% |
T-C | 3 | 4.1 | 9 | 13.6 | 3.33% | 5.0% | 10% |
10.5 | 10.7 | 28 | 42 | 8.33% | 12.5% | 25% | |
LDL-C | 4.2 | 6.8 | 13.6 | 20.4 | - | - | - |
HDL-C | 3.6 | 5.2 | 11.1 | 16.6 | 10.0% | 10.0% | 30% |
Apo A1 | 3.3 | 3.7 | 9.1 | 13.6 | - | - | - |
Apo B | 3.5 | 6 | 11.6 | 17.5 | - | - | - |
K | 2.4 | 1.8 | 5.8 | 8.7 | 0.17 mol/L | 0.2 mmol/L | 0.5 mmol/L |
0.4 | 0.3 | 0.9 | 1.3 | 0.13 mmol/L | 2 mmol/L | 4 mmol/L | |
C1 | 0.6 | 0.5 | 1.5 | 2.2 | 1.67% | 2.0% | 5% |
1 | 0.8 | 2.4 | 3.6 | 0.33 mg/dL | 0.5 mmol/L | 1.0 mg/dL | |
1.8 | 1.8 | 4.8 | 7.2 | 8.33% | 12.5% | 25% | |
P | 4.3 | 3.2 | 10.2 | 15.3 | - | - | - |
9 附錄B(資料性附錄)常見被測量的建議實驗濃度
常見被測量的建議實驗濃度見表B.1。
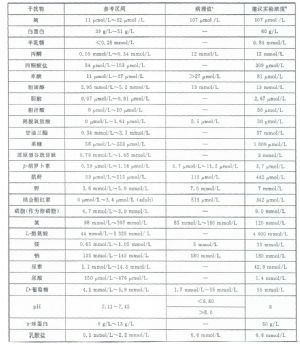
表B.1 常見被測量的建議實驗濃度
分析物 | 實驗濃度低值 | 實驗濃度高值 | ||
氨 | 10μmol/L | 14μg/dL | 80μmol/L | 112μg/dL |
35 g/L | 3.5 g/dL | 50 g/L | 5 g/dL | |
苯巴比妥 | 215 mol/L | 5μg/mL | 1722 mol/L | 40}上g/mL |
61μmol/L | 1 mg/dL | 1211μmol/L | 20 mg/dL | |
12μmol/L | 3μg/mL | 79μmol/L | 20μg/mL | |
0.34 mmol/L | 2 mg/dL | 3.4 mmol/L | 20 mg/dL | |
35 mol/L | 5μg/mL | 693 mol/L | 100μg/mL | |
0.01 g/L | 1 mg/dL | 0.04 g/L | 4 mg/dL | |
33.3μmol/L | 6μg/mL | 111μmol/L | 20μg/mL | |
促甲狀腺素(TSH) | 0.3 mIU/L | 0.3 uIU/mL | 8 mIU/L | 8μU/mL |
139 nmol/L | 40 ng/mL | 1040 nmol/L | 300 ng/mL | |
0.5 nmol/L | 0.4 ng/mL | 2.6 nmol/L | 2 ng/mL | |
33μmol/L | 5μg/mL | 199μmol/L | 30μg/mL | |
HDL膽固醇 | 0.9 mmol/L | 35 mg/dL | 1.8 mmol/L | 70 mg/dL |
皋酮 | 1.7 nmol/L | 50 ng/dL | 10.4 nmol/L | 300 ng/dL |
黃體生成素(LH) | 5 IU/L | 5 mIU/mL | 110 IU/L | 110 mIU/mL |
肌酐 | 133μmoL/L | 1.5 mg/dL | 442μmol/L | 5 mg/dL |
300 ng/L | 30 ng/dL | 150μg/L | 150 ng/mL | |
鉀 | 3 mmol/L | 3 mEq/L | 5 mmol/L | 5 mEq/L |
結合膽紅素 | 3.4μmol/L | 0.2 mg/dL | 86μmol/L | 5 mg/dL |
12.7μmol/L | 3μg/mL | 50.8μmol/L | 12μg/mL | |
6.2μmol/L | 2 μg/mL | 15μmol/L | 5μg/mL | |
221μmol/L | 4 mg/dL | 1104μmol/L | 20 mg/dL | |
1 mmol/L | 4 mg/dL | 2 mmol/L | 8 mg/dL | |
鋰 | 0.2 mmol/L | 0.14 mg/dL | 1.5 mmol/L | 1 mg/dL |
氯 | 90 mmol/L | 90 mEq/L | 110 mmol/L | 110 mEq/L |
卵泡刺激素(FSH) | 5 IU/L | 5 rnIU/mL | 40 IU/L | 40 mIU/mL |
鎂 | 1.6 mmol/L | 3.9 mg/dL | 2.6 mmol/L | 6.3 mg/dL |
N-乙酰普魯卡胺(NAPA) | 18 mol/L | 5μg/mL | 108 mol/L | 30μg/mL |
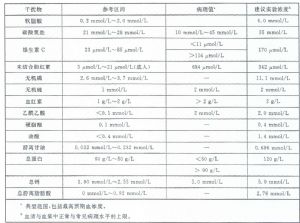
表B.1(續)
分析物 | 實驗濃度低值 | 實驗濃度高值 | ||
鈉 | 130 mmol/L | 130 mEq/L | 150 mmol/L | 150 mEq/L |
3 mmol/L | 9 mg/dL | 7 mmol/L | 40 mg/dL | |
0.2 mmol/L | 3 mg/dL | 0.5 mmol/L | 9 mg/dL | |
138 nmol/L | 5μg/dL | 828 nmol/L | 30μg/dL | |
4.4 mmol/L | 80 mg/dL | 6.7 mmol/L | 120 mg/dL | |
普里米酮 | 14 mol/L | 3μg/mL | 55 mol/L | 12μg/mL |
17 mol/L | 4μg/mL | 42 mol/L | 10μg/mL | |
鉛 | 1.21μmol/L | 2Sμg/dL | 4.83μmol/L | 100μg/dL |
前白蛋白 | 100 g/L | 10 mg/dL | 400 g/L | 40 mg/dL |
0.65 nmol/L | 110 pg/mL | 4.14 nmol/L | 700 pg/mL | |
0.2 nmol/L | 8 ng/dL | 1.1 nmol/L | 40 ng/dL | |
人絨毛膜促性腺激素(hCG) | 5 IU/L | 5 mIU/mL | 50 IU/L | 50 mIU/mL |
0.7 mmol/L | 6.3 mg/dL | 2.6 mmol/L | 23.4 mg/dL | |
218 pmol/L | 40 pg/mL | 546 pmol/L | 100 pg/mL | |
水楊酸鹽 | 0.14 mmol/L | 2 mg/dL | 1.45 mmol/L | 20 mg/dL |
鐵 | 7.2μmol/L | 40μg/dL | 26.9μmol/L | 150μg/dL |
45 pmol/L | 20 ng/mL | 449 pmol/L | 200 ng/mL | |
鐵結合力 | 44.8μmol/L | 250μg/dL | 80.6μmol/L | 450μg/dL |
維生素B12 | 148 pmol/L | 200 pg/mL | 740 pmol/L | 1000 pg/mL |
未結合膽紅素 | 17μmol/L | 1 mg/dL | 257μmol/L | 15 mg/dL |
無機磷 | 0.8 mmol/L | 2.5 mg/dL | 2.1 mmol/L | 6.5 mg/dL |
100 g/L | 10 g/dL | 200 g/L | 20 g/dL | |
11 nmol/L | 5 ng/mL | 34 nmol/L | 15 ng/mL | |
2.17 mmol/L | 10 mg/dL | 21.7 mol/L | 100 mg/dL | |
遊離甲狀腺素(FT4) | 13 pmol/L | 1 ng/dL | 32.5 pmol/L | 2.5 ng/dL |
遊離三碘甲腺原氨酸(FT3) | 3.9 pmol/L | 250 pg/dL | 10.8 pmol/L | 700 pg/dL |
3.2 nmol/L | 1 ng/mL | 64 nmol/L | 20 ng/mL | |
0.8 g/L | 80 mg/dL | 1.8 g/L | 180 mg/dL | |
0.6 g/L | 60 mg/dL | 1.3 g/L | 130 mg/dL | |
2 g/L | 200 mg/dL | 4 g/L | 400 mg/dL | |
總CO2 | 20 mmol/L | 20 mEq/L | 35 mmol/L | 35 mEq/L |
3.88 mmol/L | 150 mg/dL | 6.47 mmoI/L | 250 mg/dL | |
總鈣 | 2 mmol/L | 8 mg/dL | 3 mmol/L | 12 mg/dL |
表B.1(續)
13 參考文獻
[1] CLSI EP7-A2:Interference Testing in Clinical Chemistry; Approved Guideline-Second Edition
[2] 金丕煥.醫學統計學.2版.上海:復旦大學出版社,2006
[3] 周尊英,實用統計技術標準,北京:中國標準出版社,2003
[4] 王治國.臨牀檢驗方法確認與性能驗證,北京:人民衛生出版社,2009
[5] CLSI EP5-A. Precision performance of clinical chemistry devices—Approved Guideline
[6] CLSl EP6-P2. Evaluation of the linearity of quantitarive analytical methods. Proposed GuideLine-Second Edition
[7] CLSI EP9-A2. Method comparison and bias estimation using patient samples. Approved Guideline-Second Edition
[8] CLSI EP21-A. Estimation analytical error for clinical laboratory methods. Approved Guideline
[9] Burtis CA, Ashwood ER, eds. Tietz Textbook of Clinical Chemistry.3rd ed. Philadelphia: W.B.Saunders,1999

 ——全部
——全部 ——全部
——全部