3 新食品原料·透明質酸鈉
透明質酸鈉是以葡萄糖、酵母粉、蛋白腖等爲培養基,由馬鏈球菌獸疫亞種(Streptococcus equisubsp.zooepidemicus)經發酵生產而成,是由D-葡糖醛酸和N-乙酰基-D-氨基葡萄糖雙糖單元構成的糖胺聚糖的鈉鹽,是一種直鏈大分子多糖。
我國於2008年批准透明質酸鈉爲新資源食品,使用範圍爲保健食品原料。目前透明質酸鈉及以其爲主要成分的產品在日本、韓國、美國、歐盟、澳大利亞、新西蘭和巴西被允許添加在食品或膳食補充劑中。基於在其他國家和國際組織的批准使用情況,本產品申請擴大使用範圍爲乳及乳製品,飲料類,酒類,可可製品、巧克力和巧克力製品(包括代可可脂巧克力及製品)以及糖果,冷凍飲品。透明質酸鈉在嬰幼兒、孕婦和哺乳期婦女人羣中的食用安全性資料不足,從風險預防原則考慮,上述人羣不宜食用,標籤及介紹中應當標註不適宜人羣,並標註推薦食用量≤200毫克/天。
2020年12月28日國家衛生健康委發佈《關於蟬花子實體(人工培植)等15種“三新食品”的公告》,宣佈對透明質酸鈉的安全性評估材料審查通過。新食品原料生產和使用應當符合公告內容以及食品安全相關法規要求。食品安全指標按照公告規定執行。
3.1 中文名稱
3.2 英文名稱
Sodium Hyaluronate[1]
3.3 基本信息
3.3.1 來源
馬鏈球菌獸疫亞種(Streptococcus equi subsp. zooepidemicus)
3.3.2 結構式
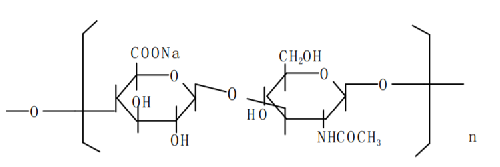
3.3.3 分子式
(C14H20NNaO11)n,n爲200–10000
3.3.4 分子量
8.02×104–4.01×106
3.4 生產工藝簡述
以葡萄糖、酵母粉、蛋白腖等爲培養基,由馬鏈球菌獸疫亞種經發酵生產而成[1]。
3.5 推薦食用量
≤200 毫克/天[1]
3.6 質量要求
3.6.1 性狀
白色顆粒或粉末
3.6.2 透明質酸鈉含量
≥87.0g/100g
3.6.3 水分
≤10.0g/100g
3.6.4 pH
6.0–8.0
3.6.5 灰分
≤13.0g/100g
3.7 其他需要說明的情況
1.使用範圍和推薦最大使用量:乳及乳製品(0.2g/kg),飲料類(液體飲料≤50 mL 包裝 2.0 g/kg,51–500 mL 包裝 0.20 g/kg,固體飲料按照衝調後液體體積折算),酒類(1.0 g/kg),可可製品、巧克力和巧克力製品(包括代可可脂巧克力及製品)以及糖果(3.0 g/kg),冷凍飲品(2.0 g/kg)。
2.嬰幼兒、孕婦及哺乳期婦女不宜食用,標籤及介紹應當標註不適宜人羣,並標註推薦食用量≤200 毫克/天。
3.食品安全指標須符合以下規定:
鉛(Pb) ≤0.5mg/kg
砷(As) ≤0.3mg/kg
4 透明質酸鈉藥品介紹
4.1 適應症
透明質酸可在包括眼房水及玻璃體液在內的組織和細胞內液中廣泛分佈。透明質酸鈉粘液應用於眼部外科手術中,通過一根細管或針將本品引入前房或後房部位,使組織得到分離,免受手術損傷。透明質酸和透明質酸鈉也可關節內注射,並已試用於關節炎的治療。
4.2 用量用法
遵醫囑。
4.3 注意事項
4.4 規格
注射劑:1.5ml, 2ml.
滴眼劑:0.1%.
5 參考資料
- ^ [1] 國家衛生健康委.關於蟬花子實體(人工培植)等15種“三新食品”的公告[Z].2020-12-28.