7 概述
病變不論爲腫瘤或增殖所引起,其主要表現皆爲以皮質醇爲主的激素產生過盛而致的全身性改變。如爲腫瘤,病程短而發展快,症狀與體徵表現典型;如爲雙側增生所引起,則病程較長而發展慢。而由垂體瘤或異位促皮素瘤(ectopic ACTH tumor)所致的腎上腺皮質增生,其臨牀特徵則與上述兩類在某些方面又有所差異。自1932年Cushing第1次報道本病後,在最初的20年間共診治10例,認爲罕見。但實際上本症並非少見,隨着認識的提高及檢診手段的完善與精確,在我國的病例數急劇增加。按病因分析,以垂體依賴性皮質醇症及病因未能肯定的雙側增生約佔65%,腎上腺皮質腺瘤或癌約佔20%,異位促皮素瘤約佔15%。第1類多需腎上腺手術治療;第2類只能施行腎上腺手術;而第3類則屬於各自發病靶器官的手術範圍,如縱隔、盆腔各器官,對繼發性的皮質增生待原發病切除後即自行消退,勿需腎上腺手術處理。
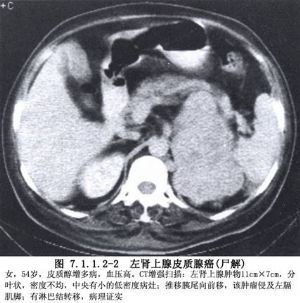
腎上腺皮質癌少見。原發性皮質癌可發生於任何年齡,在小兒的Cushing綜合徵中,癌爲常見的病因,且多發生於女孩。腫瘤生長快,病程短,臨牀發現時瘤體多較大,常在上腹部可觸到腫物。腫瘤所產生的大量皮質激素類物質,由於C11或C21羥基化酶的作用不全或受到阻滯,使體內的各類皮質素前驅物,皮質醇、皮質酮、醛固酮、腎上腺雄性激素、孕酮等都有不同比例的增加,因而既可出現Cushing綜合徵,又可表現出腎上腺生殖性徵異常症,如女性男性化,性早熟,男性女性化等。電解質異常、高血壓等各類症狀也表現得很明顯。但由於真正的皮質醇的分泌量不足,早期常不表現典型的Cushing綜合徵,直到腫瘤長至很大,轉移,以至晚期時始被發現而確診。約50%在2年內死亡,約1/4可經手術切除腫瘤後獲得3年以上的臨牀治癒。切除部分腫瘤,可以緩解症狀,延長存活期。殘存癌組織或轉移癌的內分泌功能可借藥物控制,常用的化學制劑爲鄰、對二氯苯二氯乙烷(Mitotane,o,p′DDD,又稱密妥坦),氨魯米特,又稱氨基導眠能或胺麩精(aminoglutethi-mide)等。O,p′DDD可減少皮質癌內分泌功能的50%以上。由於合成真正皮質醇量明顯減少,不足生理需求量,經病理反饋機制過程中ACTH的作用,常致癌腫以外的皮質增殖。藥物的全身性反應尤其消化道症狀較重,迫使中途停止用藥。藥物早期抑制癌的內分泌作用較好,有效抑制期平均爲4.8個月,有效率約爲50%(Luton,1990),也見有使腫瘤完全消失的個案報道,故皮質癌仍以手術治療爲主,藥物治療可作爲輔助療法,或用於不能手術切除的腫瘤,並須與氫化可的松聯合應用。由於腫瘤浸潤快,轉移早,很難根除,術後複發率較高(圖7.1.1.2-1,7.1.1.2-2)。

8 適應症
腎上腺皮質癌切除術適用於:
經檢診發現的腎上腺腫瘤而屬於功能性者,不論其爲良性或惡性,手術治療爲首選方法。即使有浸潤和轉移的癌,也不應放棄手術切除的機會,儘管不能完全清除腫瘤,切除部分瘤體,也將有利於減輕症狀和控制病情的迅速發展,提高輔助藥物的療效。
10 術前準備
1.術前需應用阻滯皮質素合成的藥物,以減輕症狀,有利於手術,常用的有效藥物爲:
鄰、對二氯苯二氯乙烷(o,p′DDD):此藥物能選擇性地阻滯束狀帶及網狀帶細胞功能,可降低皮質素分泌量的50%以上。每日劑量爲3~6g,最大劑量可加至8~10g,並可使原發癌及轉移癌的瘤體縮小,提高手術切除率。對手術未能切除或切除未淨的殘餘瘤組織亦有療效。術後症狀消失緩慢或未完全消失者,也應給予此藥,但遠期並無防止癌腫復發的作用。消化道反應症狀重而多見,只能於術前3d內短期用。
氨魯米特(aminoglutethimide):亦有抑制皮質激素合成的作用。每日劑量爲0.75~2g。術前應用可減輕症狀,亦可作爲對殘餘癌組織及轉移癌的保守療法。
甲雙吡丙酮(metopirone,SU4885):具有抑制氫化酶的功能,使皮質激素的合成受到影響,可減輕手術前的症狀。劑量爲250~500mg/6h。
若癌瘤所分泌的皮質激素以雄性素及皮質素的前驅物爲主,而真正的皮質醇含量不足者,可配合上述阻滯劑加用氫化可的松,以減輕對垂體的反饋性刺激,降低ACTH的分泌量。劑量爲50mg,每日1~3次。術後須常規應用氫化可的松行補替治療。根據腫瘤切除的完全與否,對側腎上腺皮質代償性萎縮的程度,對術後用藥的時間及劑量加以調整,逐漸遞減劑量直到完全停用。術後一般不應用ACTH治療,等待皮質功能自然恢復。爲減輕對電解質的影響,可用地塞米松代替氫化可的松。
12 手術步驟
較小的腫瘤,可選用背部或腰部切口,經腹膜外途徑切除。瘤體較大,能在腹部觸到者宜經腹部切口,由腫瘤側腹部行縱長切口進入腹腔,經結腸旁溝廣泛切開後腹膜,使後腹膜間隙完全顯露並顯露腹主動脈及下腔靜脈,便於清掃主動脈旁淋巴組織,以便整塊切除腫瘤及腎上腺。對一側腎臟已受侵犯而對側腎臟正常者,可連同患側腎臟一併切除(圖7.1.1.2-4,7.1.1.2-5)。


對腫瘤巨大且局部已有浸潤的腎上腺皮質癌,則常採用患側胸腹聯合切口。採用胸膜外胸腹聯合手術途徑切除巨型腎上腺皮質癌亦可得到較滿意的顯露,並避免了切開肋骨弓的弊端,不污染胸腔。無疑將較其他途徑的手術切除率高,腎上腺癌及浸潤組織被整塊切除的機會也多一些。如腹部切口仍不夠大時,可向下延長,因此是值得推薦的手術徑路。此處介紹此徑路行左側腎上腺皮質癌切除術。
12.1 1.切開胸壁及腹壁
沿切口方向依次切開皮膚、皮下組織、背闊肌及部分後下鋸肌,向前切開腹外斜肌、腹內斜肌及腹橫肌,並切開同側腹直肌前鞘和切斷腹直肌(圖7.1.1.2-6)。

12.2 2.切開肋間肌
沿第10肋間隙仔細切開肋間肌,注意勿切破其下的胸膜,在切口的下方即可見到膈肌(圖7.1.1.2-7)。

12.3 3.切開膈肌
給氧充起肺,使肺下緣充滿胸腔,以手指鈍性分離胸膜反折部並將胸膜向上推起,沿第11肋上緣在胸膜外切開膈肌(圖7.1.1.2-8),並將膈肌的兩切緣分別縫合固定於腰背各肌和兩側切緣上,以保護上推的胸膜反折部,使手術野與胸腔隔離,避免胸腔污染(圖7.1.1.2-9)。


12.4 4.顯露腹膜後間隙
向下向內切開腹直肌後鞘及腹膜,進入腹腔。將腹膜內臟推向內側下方,切開結腸旁溝腹膜,在左側切開降結腸外側的後腹膜及脾結腸韌帶,將結腸脾曲及降結腸遊離推移至內下方,使左側的腹膜後間隙廣泛地顯露出來(圖7.1.1.2-10)。

12.5 5.顯露腎上腺
切開腎周筋膜,分離腎周脂肪,腎、腎上腺及其巨大的腫瘤即被暴露在視野中(圖7.1.1.2-11)。

12.6 6.切除腎上腺及腫瘤
顯露腫瘤後,沿其周邊進行遊離。結紮血管,但此類巨大腎上腺皮質癌多浸潤至腎臟,不易與腎臟分離,爲徹底切除腫瘤,如對側腎正常,需將腎上腺及其腫瘤連同腎臟、腎周脂肪組織、淋巴整塊切除(圖7.1.1.2-12)。此手術技術及步驟與根治性腎切除術基本相同。

