3 基本信息
ICS 11.020
C 05
中華人民共和國衛生行業標準 WS/T 550—2017《全血及成分血質量監測指南》(Guidelines on quality monitoring of whole blood and blood components)由中華人民共和國國家衛生和計劃生育委員會於2017年05月12日《關於發佈〈全血及成分血質量監測指南〉等2項推薦性衛生行業標準的通告》(國衛通〔2017〕3號)發佈,自2017年11月01日起實施。
4 發佈通知
關於發佈《全血及成分血質量監測指南》等2項推薦性衛生行業標準的通告
國衛通〔2017〕3號
現發佈《全血及成分血質量監測指南》等2項推薦性衛生行業標準,其編號和名稱如下:
WS/T 550-2017 全血及成分血質量監測指南
上述標準自2017年11月1日起施行。
特此通告。
國家衛生計生委
2017年5月12日
5 前言
本標準按照GB/T 1.1—2009給出的規則起草。
本標準起草單位:上海市血液中心、北京市紅十字血液中心、天津市血液中心。
本標準主要起草人:鄒崢嶸、邱豔、邱穎婕、龔裕春、張錫敏、郭瑾、李浩瀧、林俊杰、章懌、徐忠、徐蓓。
6 標準正文
6.1 1 範圍
本標準規定了全血及成分血質量的監測方法、檢查結果分析與利用原則。
6.2 2 規範性引用文件
下列文件對於本文件的應用是必不可少的。凡是注日期的引用文件,僅注日期的版本適用於本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
全國臨牀檢驗操作規程
6.3 3 術語和定義
下列術語和定義適用於本文件。
3.1
全血及成分血質量監測 quality monitoring of whole blood and blood components
6.4 4 監測方法
6.4.1 4.1 抽樣方法
4.1.1 全血每月抽取月供應量的1%或至少4袋,如全血每月供應量少於4袋,由血站根據統計過程抽樣原則自行制定抽樣頻次。
4.1.2 成分血每月抽取月製備量的1%或至少4袋,如該成分血每月製備量少於4袋,由血站根據統計過程抽樣原則自行制定抽樣頻次。
6.4.2 4.2 符合率的計算
4.2.1 樣本中單位全血及成分血相應質量檢查項目是否達標,按GB 18469的規定進行判斷。
4.2.2 樣本符合率按式1計算:

式中:
P——符合率
n——樣本中判定爲達標的單位數
N——樣本總單位數
6.4.3 4.3 檢查方法
6.4.3.1 4.3.1 標籤檢查
標籤上應包括但不限於以下項目:血站名稱及其許可證號、獻血編號或條形碼、血型、血液品種、採血日期及時間(製備日期及時間)、有效日期及時間、儲存條件、容量、注意事項。
6.4.3.2 4.3.2 其他質量特性檢查
全血及各類成分血的質量特性宜按表1-表19所述的方法進行檢查。
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率100% |
血紅蛋白含量 | 見附錄C | 符合率≥75% |
儲存期末溶血率 | 見附錄D | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
血紅蛋白含量 | 見附錄C | 符合率≥75% |
白細胞殘留量 | 見附錄E | 符合率≥75% |
儲存期末溶血率 | 見附錄D | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
見附錄H | 符合率≥75% | |
血紅蛋白含量 | 見附錄H | 符合率≥75% |
白細胞殘留量 | 見附錄D | 符合率≥75% |
儲存期末溶血率 | 見附錄C | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
見附錄C | 符合率≥75% | |
血紅蛋白含量 | 見附錄C | 符合率≥75% |
儲存期末溶血率 | 見附錄D | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
見附錄C | 符合率≥75% | |
血紅蛋白含量 | 見附錄C | 符合率≥75% |
白細胞殘留量 | 見附錄E | 符合率≥75% |
儲存期末溶血率 | 見附錄D | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查 | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
血紅蛋白含量 | 見附錄C | 符合率≥75% |
遊離血紅蛋白含量 | 見附錄D | 符合率≥75% |
白細胞殘留量 | 見附錄E | 符合率≥75% |
甘油殘留量 | 見附錄G | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
儲存期末pH | 見附錄C | 符合率≥75% |
血小板含量 | 見附錄C | 符合率≥75% |
紅細胞混入量 | 見附錄H | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
儲存期末pH | 見附錄C | 符合率≥75% |
血小板含量 | 見附錄C | 符合率≥75% |
紅細胞混入量 | 見附錄C | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
儲存期末pH | 見附錄C | 符合率≥75% |
血小板含量 | 見附錄C | 符合率≥75% |
白細胞混入量 | 見附錄C | 符合率≥75% |
紅細胞混入量 | 見附錄C | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
儲存期末pH | 見附錄C | 符合率≥75% |
血小板含量 | 見附錄C | 符合率≥75% |
白細胞殘留量 | 見附錄E | 符合率≥75% |
紅細胞混入量 | 見附錄C | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
血漿蛋白含量 | 見附錄C | 符合率≥75% |
Ⅷ因子含量 | 見附錄C | 符合率≥75% |
亞甲藍殘留量 | 見附錄H | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
血漿蛋白含量 | 見附錄C | 符合率≥75% |
亞甲藍殘留量 | 見附錄H | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
檢查項目 | 符合性目標 | |
目視覈查 | 符合率100% | |
外觀 | 目視檢查,見附錄A | 符合率100% |
容量 | 見附錄B | 符合率≥75% |
纖維蛋白原含量 | 見附錄C | 符合率≥75% |
Ⅷ因子含量 | 見附錄C | 符合率≥75% |
無菌試驗 | 見附錄C | 符合率100% |
6.4.3.3 4.3.3 輻照血液
4.3.3.1 經輻照後的血液製劑,其質量檢查要求與原血液製劑的要求相同。
4.3.3.2 每次血液輻照過程宜採用指示劑的方法來驗證血液己受到適當劑量的射線輻照。
6.5 5 檢查結果分析與利用
5.1 全血及成分血的抽檢結果分析時,對由於獻血者個體差異引起的,且不影響血液安全性的指標,如果檢查符合率≥75%,可認爲血液採集、製備和儲存等過程受控。
5.2 抽檢符合率結果不達標時,應增加抽檢頻率和數量,對涉及的全血或成分血質量進行評估,對不達標原因進行系統分析,並採取糾正和預防措施。
5.3 趨勢分析:血站應定期對血液質量監測結果進行趨勢分析,出現異常趨勢時,應對過程涉及的各要素進行評估,分析原因,必要時採取糾正和預防措施。
7 附錄
7.1 附錄A(規範性附錄)血液乳糜程度檢測方法
7.1.1 A.1 材料
外觀爲淡黃色透明的正常血漿2份以上,潔淨的玻璃器皿一個,生理鹽水,5mL質地均勻的一次性硬塑料試管若干,1mL加樣器一隻,比濁用圖片。
7.1.2 A.2 檢測方法
A.2.1 將2份以上正常血漿等量混合於潔淨的玻璃器皿中製成標準血漿,取至少2mL於試管中作爲正常標準管。
A.2.2 將乳糜血離心分離出的血漿或上清液取至少2mL置於管中。
A.2.3 取待測乳糜血樣品定量加入試管內,然後取等量生理鹽水稀釋樣品,分別取不同稀釋比例的樣品管與標準管並列緊貼於比濁用圖片上,置於光線亮處,操作人背向光源,使兩管所受光線的亮度一致,並將兩管左右換位,反覆對比,通過兩管目測圖片上圖形清晰程度,判定樣品管是否與標準管清晰度一致,若某一稀釋度待測樣品管較標準管混,則取更高倍稀釋樣品管與標準管比較,直至兩管後圖片上的圖形清晰程度相同爲止。
A.2.4 將稀釋倍數作爲乳糜指數來評價血液乳糜程度,乳糜指數越大血液乳糜程度越重。將乳糜指數≤2的乳糜血定爲輕度乳糜,2<乳糜指數≤5定爲中度乳糜,乳糜指數>5定爲重度乳糜。
7.1.3 A.3 其他
7.2 附錄B(規範性附錄)容量檢測方法
7.2.1 B.1 方法
使用最小分度值爲0.1g的稱量器具,稱取全血或成分血質量,按式B.1計算容量:

式中:
V——全血或成分血的體積,單位爲毫升(mL),全血容量檢測還應減去保養液容量;
m2——空袋質量,單位爲克(g);
7.2.2 B.2 全血及成分血比重
參照《中華人民共和國藥典》四部通則“相對密度測定法”,測定全血及成分血比重。或按以下比重進行全血及成分血容量計算:
a)全血比重:1.050;
b)血漿比重:1.027;
7.3 附錄C(規範性附錄)其他質量檢查項目檢測方法
7.3.1 C.1 無菌試驗
參照《中華人民共和國藥典》三部通則“無菌檢查法”。如使用細菌培養儀進行無菌試驗,應參照廠家介紹。
7.3.2 C.2 儲存期末pH
在血小板儲存期的最後24h取樣。檢測方法參照《中華人民共和國藥典》三部附錄“pH值測定法”。如使用酸度計進行測定,應參照廠家使用說明。
7.3.3 C.3 血紅蛋白含量
參照《全國臨牀檢驗操作規程》“血紅蛋白測定”。如使用血細胞分析儀進行測定,應參照廠家使用說明進行操作。血紅蛋白含量的計算方法見式C.1。
Hb=CHb×V……(C.1)
式中:
Hb——血紅蛋白含量,單位爲克(g);
7.3.4 C.4 血細胞比容
參照《全國臨牀檢驗操作規程》“紅細胞比容測定”。如使用血細胞分析儀進行測定,應參照廠家使用說明進行操作。
此檢測項目可用於單採粒細胞質量檢查方法中“紅細胞混入量”的檢測。
7.3.5 C.5 血小板含量
參照《全國臨牀檢驗操作規程》“血小板計數”。如使用血細胞分析儀進行測定,應參照廠家使用說明進行操作。血小板含量的計算見式C.2。
PLT=PLTC×V……(C.2)
式中:
PLT——血小板含量,單位爲1011每升(1011/L);
PLTC——血小板計數,單位爲109每升(109/L);
V——血小板體積,單位爲升(L)。
7.3.6 C.6 紅細胞混入量
參照《全國臨牀檢驗操作規程》“紅細胞計數”。紅細胞混入量的計算方法見式C.3。
RBC=RBCC×V……(C.3)
式中:
RBC——紅細胞混入量,單位爲109每升(109/L);
RBCC——細胞計數,單位爲1012每升(1012/L);
V——血小板體積,單位爲升(L)。
7.3.7 C.7 白細胞混入量
參照《全國臨牀檢驗操作規程》“白細胞計數”。如使用血細胞分析儀進行測定(白細胞數量需在該血細胞分析儀的檢測線性範圍內),應參照廠家使用說明。白細胞混入量的計算方法見式C.4。
WBC=LC×V……(C.4)
式中:
WBC——白細胞混入量,單位爲108每升(108/L);
LC——白細胞計數,單位爲109每升(109/L);
V——血小板體積,單位爲升(L)。
7.3.8 C.8 Ⅷ因子含量
參照《全國臨牀檢驗操作規程》“凝血因子Ⅷ(FⅧ:C)、Ⅸ (FⅨ:C)、Ⅺ (FⅪ:C)、Ⅻ (FⅫ:C)的活性測定(一期法)”。如使用血凝儀測定,應參照廠家使用說明。
7.3.9 C.9 血漿蛋白含量
7.3.10 C.10 纖維蛋白原含量
參照《全國臨牀檢驗操作規程》“血漿纖維蛋白原含量測定”。如使用血凝儀測定,應參照廠家使用說明。
7.3.11 C.11 中性粒細胞含量
參照《全國臨牀檢驗操作規程》“白細胞計數”和“白細胞分類計數”。如使用血細胞分析儀測定,應參照廠家使用說明。
7.4 附錄D(規範性附錄)溶血率檢測方法
7.4.1 D.1 檢測時間
保存期爲24h的洗滌紅細胞,在儲存期內取樣,全血及其他成分血在儲存期的最後一週取樣。
7.4.2 D.2 檢測方法
7.4.2.1 D.2.1 計算公式
按式D.1計算溶血率

式中:
P——溶血率;
Hct——血細胞比容;
CFHb——血漿或上清液遊離血紅蛋白濃度,單位爲克每升(g/L);
7.4.2.2 D.2.2 血紅蛋白檢測
參照《全國臨牀檢驗操作規程》“血紅蛋白測定”。如使用血細胞分析儀進行測定,應參照廠家使用說明。
7.4.2.3 D.2.3 遊離血紅蛋白含量檢測
參照《全國臨牀檢驗操作規程》“遊離血紅蛋白測定”。或使用其他經驗證可使用的方法。
7.4.2.4 D.2.4 血細胞比容檢測
參照《全國臨牀檢驗操作規程》“紅細胞比容測定”。如使用血細胞分析儀進行測定,應參照廠家使用說明。
7.5 附錄E(規範性附錄)白細胞殘留量檢測方法
7.5.1 E.1 材料
大容量Nageotte血細胞計數板、顯微鏡、結晶紫染色液。其中結晶紫染色液配製方法是:
a) 儲存液配製:250mg結晶紫溶於250mL的50%醋酸溶液中。室溫放置可保存6個月。
b) 使用液配製:1份儲存液加9份3%的醋酸溶液,最終濃度爲:結晶紫0.01%(按質量濃度表述換算),醋酸7.7%(V/V,按體積分數表述換算)。然後使用0.22μm孔徑的過濾器過濾。
7.5.2 E.2 計數方法
50μL血液標本加入450μL使用液中,充分混勻。在Nageotte計數池中加入上述混合液,將計數池置於帶蓋潮溼容器中,於室溫放置10min~15min。在顯微鏡下對計數池中兩個計數區(每區有20個長方形格)的白細胞計數,40行相當於50μL。應在血液採集後48h內完成白細胞殘留量的檢測。
7.5.3 E.3 結果計算
按式E.1計算白細胞殘留量
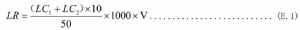
式中:
LR一一白細胞殘留量,單位爲個每袋;
10——稀釋倍數;
50——計數池2個區的體積,單位爲微升(μL);
1000——體積換算係數,1mL=1000μL;
E.4 其他
7.6 附錄F(規範性附錄)上清蛋白質含量檢測方法
7.6.1 F.1 檢測方法
7.6.2 F.2 計算公式
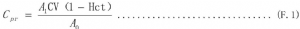
式中:
Cpr一一上清蛋白質含量,單位爲克(g);
A1一一樣品吸光度;
A0一一標準品吸光度;
C一一標準品濃度,單位爲克每升( g/L);
V一一洗滌紅細胞容量,單位爲升(L);
Hct一一血細胞比容。
7.6.3 F.3 其他
7.7 附錄G(規範性附錄)甘油殘留量檢測方法
7.7.1 G.1 過碘酸鈉法
7.7.1.1 G.1.1 原理
根據過碘酸鈉能氧化有機化合物中的羥基、胺基,使甘油氧化成酸和醛,以溴甲酚紫作指示劑,並用氫氧化鈉進行滴定。從消耗氫氧化鈉的毫升數,即可算出樣品中所含甘油的量。
7.7.1.2 G.1.2 試劑
G.1.2.1 16.5%鎢酸鈉溶液:稱取16.5克鎢酸鈉,用適量蒸餾水溶解,再加蒸餾水稀釋至100mL。
G.1.2.2 0.5mol/L H2SO4:吸取30mL濃硫酸緩緩注入適量蒸餾水中,冷卻至室溫,加蒸餾水稀釋至1000mL。
G.1.2.3 0.1mol/L NaOH:配製方法參見《中華人民共和國藥典》二部附錄“滴定液”。
G.1.2.4 0.1%溴甲酚紫溶液:稱取0.1g溴甲酚紫,溶入20mL NaOH溶液(濃度爲0.02mol/L)中,再加入蒸餾水稀釋至100mL。
G.1.2.5 14%過碘酸鈉:稱取14g過碘酸鈉,先加入適量蒸餾水中溶解,再加入2mL濃硫酸使其完全溶解,最後用蒸餾水稀釋至100mL。
7.7.1.3 G.1.3 血濾液製備
精密量取15mL血樣放入三角燒瓶中,依次加入蒸餾水75mL、16.5%鎢酸鈉溶液6mL、0.5mol/L H2SO47.5mL,用力振搖。待紅細胞完全破壞後,使用定量濾紙進行過濾。取過濾後的上清液按表G.1測定。
7.7.1.4 G.1.4 甘油殘留量測定
按表G.1進行測定
表G.1 甘油殘留量測定
試劑 | 備註 | ||
15 | 精密量取 | ||
100.0mL | 100.0mL | ||
2滴 | 2滴 | ||
0.1mol/L NaOH溶液 | 滴定至藍色 | ||
14%過碘酸鈉 | 10.0mL | 10.0OmL | 精密量取 |
38℃±1℃恆溫 | 15min | ||
2滴 | 2滴 | ||
0.1mol/L NaOH溶液 | 滴定至藍色 |
G.1.5 計算
按G.1式計算甘油含量。
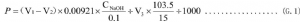
式中:
P——甘油含量,單位爲克每升(g/L):
V1——試驗全程樣品消耗NaOH的體積,單位爲毫升(mL);
V2——試驗全程空白消耗NaOH的體積,單位爲毫升(mL);
0.00921——換算係數,0.1mol/L NaOH溶液相當於0.00921g甘油;
CNaOH——滴定NaOH濃度,單位爲摩爾每升(mol/L);
0.1——NaOH溶液濃度校正因子;
V3——血濾液的體積,單位爲毫升(mL);
103.5——製備血濾液的所有血樣和試劑的體積總量,單位爲毫升(mL);
15——精密量取的血樣體積,單位爲毫升(mL);
1000——體積換算係數。
7.7.2 G.2 滲透壓測定法
正常血清滲克分子濃度爲289mmol (289mOsm),甘油含量爲1% (10g/L)質量濃度時,其滲克分子濃度爲420mmol(420mOsm),因此滲透壓測定法可作爲一種檢測去甘油紅細胞甘油殘存量的參考方法,操作方法應參照滲透壓儀器生產廠家使用說明書。
7.7.3 G.3 折射儀測定法
使用折射儀是測定滲克分子濃度的一種篩選方法。折射儀讀數到28(如折射儀型號爲10401,折射指數或比重<1.3384T.S.)與甘油水平不高於1%(10g/L)相關。折射儀測定法可作爲一種檢測甘油含量的參考方法。方法參見生產廠家使用說明書。
7.7.4 G.4 GPO-PAP法
7.7.4.1 G.4.1 試劑
20%三氯醋酸溶液:稱取20克三氯醋酸,用適量蒸餾水溶解,再加蒸餾水稀釋至100mL。
7.7.4.2 G.4.2 樣品處理
吸取血液1mL於試管中,加20%三氯醋酸溶液1mL,沉澱10分鐘(破壞紅細胞並使血紅蛋白沉澱)。於3500r/min離心5min,取上清液。按GPO-PAP法試劑盒介紹操作。
7.7.4.3 G.4.3 計算
按G.2式計算甘油含量

式中:
P——甘油含量,單位爲克每升(g/L);
A1——樣品吸光度;
A0——標準品吸光度;
2——樣品稀釋倍數;
1000——體積換算係數。
7.7.5 G.5 其他
7.8 附錄H(規範性附錄)亞甲藍殘留量檢測方法
7.8.1 H.1 試驗儀器、試劑
7.8.1.1 H.1.1 試驗儀器
固相提取柱”、配套固相提取裝置、分光光度計、離心機。
7.8.1.2 H.1.2 試劑
7.8.2 H.2 操作步驟
7.8.2.1 H.2.1 標準品配製與製備
7.8.2.1.1 H.2.1.1 亞甲藍標準濃縮儲備液配製
精密稱取亞甲藍對照品粉末38.0mg,用蒸餾水溶解並稀釋至100mL,配製成1.0mmol/L的亞甲藍標準濃縮儲備液,避光保存。
7.8.2.1.2 H.2.1.2 標準品製備
精密量取1.0mmol/L亞甲藍標準濃縮儲備液50μL,置50mL容量瓶中,用血漿稀釋至刻度,配成亞甲藍濃度爲1.0μmol/L的亞甲藍標準品。取3mL Waters Oasis小柱,置於固相提取裝置上,取6mL甲醇活化,加入6mL標準品,提取亞甲藍;用30%甲醇6mL清洗,隨後用含1%乙酸的甲醇溶液6mL洗脫,於3500rpm離心洗脫液10min,取上清液作爲標準品溶液。
7.8.2.2 H.2.2 樣品製備
取3mL Waters Oasis小柱,置於固相提取裝置上,取6mL甲醇活化,加入6mL供試血漿,提取亞甲藍;用30%甲醇6mL清洗,隨後用含1%乙酸的甲醇溶液2mL洗脫(樣品濃縮3倍),於3500rpm離心洗脫液10min,取上清液作爲樣品溶液。
7.8.2.3 H.2.3 測定
用含1%乙酸的甲醇溶液做試劑空白,在654nm±2nm處測定吸光度。亞甲藍殘留量的計算參見式H.1。

式中:
X——血漿中亞甲藍殘留量,單位爲微摩爾/升(μmol/L):
1) 本標準起草者使用Waters Oasis小柱。本標準中提及的具體的公司或製造商的產品,不代表本標準起草者認爲其優於其他同類未提及的產品而對其進行支持和推薦。
A1一一樣品吸光度;
3一一樣品濃縮倍數;
A0一一標準品吸光度;
0.1一一體積換算係數。