6 概述
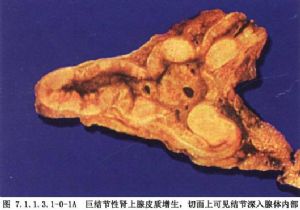
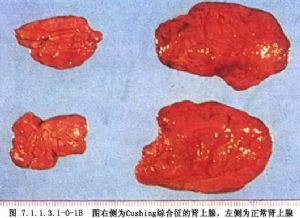
腎上腺皮質增生所致的庫欣綜合徵的手術治療意見仍未完全一致,這與病因學未能做出確切定論直接相關。根據垂體病因學說,認爲雙側腎上腺皮質增殖是垂體依賴性的,是繼發性者,應施行垂體放射治療,包括60Co,深部X線照射等。但療效頗令人失望,總有效率在20%~50%之間(Richard,1979)。在以往施行過腎上腺全切術或次全切除術的皮質增生中,經5~10年的長期隨診,只有少數病人的垂體顯示出腫瘤影。在1組屍檢病人中,垂體瘤的發現率高達10%,但無任何皮質增殖的內分泌症狀。因此,僅根據垂體有無腫瘤影並不是針對垂體治療的指徵,也不是施行腎上腺切除的絕對禁忌證。在Dennis及Styne所收集的1組小兒庫欣綜合徵中,垂體瘤的發現率高達93%~95%(1984)。因此,近年來對腎上腺增生症又主張針對垂體治療,並開展了經蝶竇顯微外科技術切除垂體瘤(transsphenoidal microadenomectomy),並收到了較好的效果(Tyrrell,Styne),但此類病人在庫欣綜合徵中畢竟是少數,而大部分成人仍屬垂體無腫瘤的腎上腺皮質增生,因此腎上腺切除術仍然是目前治療皮質增生採用的方法。自從20世紀60年代Liddle將庫欣綜合徵按病因作了劃分以後,對外科治療方法的選擇開始有了較明確的概念:凡屬垂體依賴性及異位促皮素瘤所致的繼發性皮質增生,稱爲庫欣病(Cushing disease),應首先對垂體瘤施行治療,切除異位促皮素瘤,增生的腎上腺不做處理,等待自行恢復常態。凡非垂體依賴性及無異位促皮素瘤的皮質增生,稱爲庫欣綜合徵(Cushing syndrome),施行腎上腺切除術。國內外文獻報道的大組病例中,均以後者爲主,各家所報道的腎上腺切除術的療效也很受鼓舞。國內所收集到的資料及經驗發現,因增生而施行腎上腺切除術者,大部臨牀治癒。國外早年的療效也大體相似,其中包含部分未被發現原發瘤的庫欣病在內。因爲不論皮質增生的病因在視丘下、垂體,還是其他異位臟器或腎上腺本身,皆由於分泌過量的皮質素、皮質醇等激素而產生症狀。腎上腺切除後,其周圍效應即被阻斷,病原被清除,各種症狀及體徵逐漸消失。由於各種維持生命所必需的皮質類激素已化學合成,並已廣泛用於臨牀各種疾病的治療,手術切除腎上腺後,可以行充分的補替治療,以補充其生理功能不足的缺陷。因此,對腎上腺皮質增生而言,腎上腺切除術已是一種療效好,安全性大,併發症少,死亡率極低的治療手段,被認爲是首選術式。(圖7.1.1.3.1-0-1A,7.1.1.3.1-0-1B)。
7 適應症
腎上腺次全切除術適用於:
1.臨牀症狀、體徵典型,病程長,內分泌激素檢測及藥物試驗均表現爲Cushing綜合徵者。
2.各項影像檢診皆顯示爲雙側腎上腺體積增大、變形、垂體無腫瘤者。
3.身體其他部位及有關的臟器無可疑的異位促皮素瘤者。
9 術前準備
爲增強手術的耐受性及防止手術切除腺體後所發生的急劇性體內皮質醇不足,必須給予較充分的術前準備。
1.術前1~2d給予醋酸可的可的可的松50mg,每日4次。術中在次全切除腎上腺前,由靜脈滴注氫化可的松100~200mg,以維持其基礎所需量,並以此靜注量延續至手術全過程。
11 手術步驟
手術可一期完成,也可兩側分期施行。一期完成雙側手術時,可採用上腹部橫切口或雙側背部切口。國內採用經腹切口者居多,術中可同時探查腹腔或盆腔存在腎上腺外腫瘤的可能性。若分期進行,可採用上腹部斜直切口。至於先做何側,則根據腎上腺形態變化而定。凡增生體積較大、可疑有小腺瘤或結節性增殖側,則先行該側手術,病理診斷爲增生後,延期再行另一側手術。
2.次全切除腎上腺 腎上腺次全切除的腺體量應包括一側全切,另一側切除3/4~1/3的腺體,即切除兩側腺體總量的85%~90%,最低不能少於80%。何側全切何側部分切除,如無特殊指徵,一期手術時,先施行左側,切除中、上部3/4腺體,只保留近腎門部帶有腎上腺靜脈的下1/4部的腺體,腎上腺下動脈也同時被得以保留(圖7.1.1.3.1-1)。因這一部分腎上腺解剖位置低,血運易保留,症狀復發時再次手術易於探查而切除之。
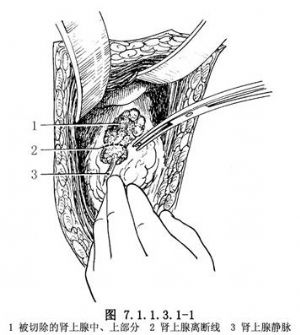
腎上腺中、上部分切除後,觀察保留部分的色澤,如呈鮮紅色,則判定血循環良好,術後能保持良好功能。創面可有少量出血,可壓迫止血,不必縫合結紮,使腺體組織遭到破壞。手術部不必置引流。縫合後腹膜,復位內臟。
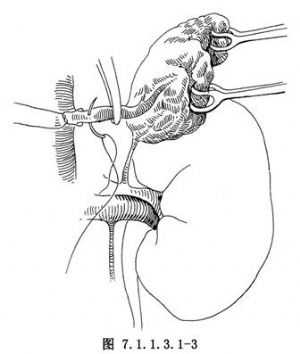
切除並保留左腎上腺,再探查、切除右側腎上腺。右側腎上腺靜脈短而直接匯入下腔靜脈,須將肝、膽囊牽向外、上,打開後腹膜將十二指腸拉向內、下,將腎上極遊離、下拉,部分腺體上部居於腔靜脈後方,將腔靜脈外緣翻起,始能暴露出整個腎上腺及其靜脈與腔靜脈的匯合部(圖7.1.1.3.1-2)。以無損傷性組織鉗抓起腺體上部並向上牽拉翻起。分離顯露清楚腎上腺靜脈,絲線貫穿縫扎1次後,切斷腎上腺靜脈,完整地切除右側腎上腺(圖7.1.1.3.1-3)。