2 英文參考
graft-rejection
transplant rejection
在同種異體組織、器官移植時,受者的免疫系統常對移植物產生排異反應(transplant rejection),這是一個十分複雜的免疫學現象,涉及細胞和抗體介導的多種免疫損傷機制,都是針對移植物中的人類主要組織兼容抗原HLA(human leucocyte antigen) 的反應,供者與受者HLA的差異程度決定了排異反應的輕或重。除單卵雙生外,二個個體具有完全相同的HLA系統的組織配型幾乎是不存在的,但選擇供者與受者配型儘可能地接近,是異體組織器官移植成功的關鍵。
HLA系統是目前人類已知的最複雜的基因羣—HLA複合體,或稱MHC基因的編碼產物。HLA複合體位於第六對染色體的短臂,是免疫遺傳的調控中心。每個基因位點存在多種等位基因,導致HLA系統的高度多態性。HLA複合體的基因位點,從功能角度可分爲三類。第一類:包含基因位點HLA-A·B·C,所有真核細胞均具有Ⅰ類基因位點。第二類即HLA-D(DR)位點,主要見於抗原遞呈細胞、B細胞及T輔助細胞,此外,血管內皮細胞、纖維母細胞及腎小管上皮細胞等如果受到淋巴因子IFN-γ的誘導,亦可表達Ⅱ類抗原。第三類則屬於編碼補體C2、C4和B因子的基因位點。HLA分子的主要生理作用是將抗原遞呈給T細胞,因而無論對誘導體液及細胞免疫反應均起重要作用。已知調控免疫反應的Ir(immune response)基因亦位於HLA-D區,所以Ⅱ類抗原的基因亦具有Ir基因的功能,調控免疫反應的幅度。因而可以認爲與HLA直接相關的免疫病理現象是:移植排斥反應、對疾病的反應過度或反應不足。
3 排斥反應的機制
移植排斥反應過程很複雜,既有細胞介導的又有的抗體介導的免疫反應參與作用。
3.1 T細胞介導的排斥反應
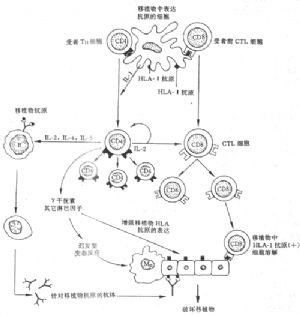
在人體和實驗性組織、器官移植中證實,T細胞介導的遲發性超敏反應與細胞毒作用對移植物的排斥起着重要的作用。移植物中供體的淋巴細胞(過路淋巴細胞)、樹突細胞等具有豐富的HLA-Ⅰ、Ⅱ抗原,是主要的致敏原,它們一旦被受體的淋巴細胞識別,即可引起以下系列變化(圖4-3)。
(1)CD8+細胞毒性T細胞(CTL)前細胞:前細胞具有HLA-I受體,與HLA-i 抗原結合後可引起分化,成爲成熟的CTL,溶解移植組織。
(2)CD4+T輔助細胞(TH):TH細胞能識別HLA-Ⅱ抗原並與之發生作用引起移植物中抗原遞呈細胞釋放白細胞介素I(IL-I),後者可促進TH細胞增生和釋放IL-2,而IL-2可進而促進TH細胞增生併爲CTL細胞的分化提供輔助信號。除了IL-2之外,TH細胞還能產生IL-4、IL-5、促進B細胞分化併產生抗移植物的抗體,參與移植排斥。此外與遲發變態反應相拌隨的血管損害、組織缺血及巨噬細胞介導的破壞作用,也是移植物毀損的重要機制。
3.2 抗體介導的排斥反應
T細胞在移植排斥反應中無疑起着主要作用,但抗體也能介導排斥反應,其形式有二:①過敏排斥反應,發生在移植前循環中已有HLA抗體存在的受者。該抗體來自過支曾多次妊娠、接受輸血、人工透析或感染過某些其表面抗原與供者HLA有交叉反應的細菌或病毒。在這種情況下,器官移植後立即可發生排斥反應(超急性排斥),此乃由於循環抗體(抗HLA)固定於移植物的血管內皮(表達HLA)發生Ⅱ型變態反應,引起血管內皮受損,導致血管壁的炎症、血栓形成和組織壞死;②在原先並無致敏的個體中,隨着T細胞介導的排斥反應的形成,可同時有抗HLA抗體形成,此抗體在移植後接受免疫抑制治療的患者中對激發晚期急性排斥反應頗爲重要。免疫抑制藥雖能一定程度上抑制T細胞反應,但抗體仍在繼續形成,並能過補體介導的細胞毒(CMC)、依賴抗體介導的細胞毒(ADCC)及抗原抗體免疫複合物形成等方式,引起移植物損害。
4 排斥反應的類型
在同種異體移植中,排斥反應有兩種基本類型:宿主抗移植物反應(hostversusgraftreaction,HVGR)和移植物抗宿主反應(graftversushostreaction,GVHR),臨牀最多見的是前者;根據發生的機制、時間、速度和臨牀表現,HVGR又可分爲3種類型。
1.超急排斥反應發生在移植物與受者血管接通的數分鐘到數小時內,出現壞死性血管炎表現,移植物功能喪失,患者有全身症狀。發生的基本原因是受者循環內存在抗供者的抗體,常見於下列情況:①ABO血型不符;②由於多次妊娠或反覆輸血等使受者體內存在抗HLA抗體;③移植物保存或處理不當等其他原因。超急排斥發生迅速,反應強烈,不可逆轉;需立即切除移植物,否則會導致受者死亡。如果事先認真進行ABO基至Rh血型檢查和交叉配合試驗,多可避免這種現象的發生。
2.急性排斥反應是排斥反應最常見的一種類型,多發生在移植後數週到1年內,發生迅速,臨牀表現多有發熱、移植部位脹痛和移植器官功能減退等;病理特點是移植物實質和小血管壁上有以單個核細胞爲主的細胞浸潤、間質水腫與血管損害,後期在大動脈壁上有急性纖維素樣炎症。急性排斥出現得早晚和反應的輕重與供-受者HLA相容和程度有直接的關係,相容性高則反應發生晚、症狀輕、有些可遲至移植後2年纔出現。急性排斥反應經過及時恰當的免疫抑制治療多可緩解。
3.慢性排斥反應屬於遲髮型變態反應,發生於移植後數月甚至數年之後,表現爲進行性移植器官的功能減退直至喪失;病理特點是血管壁細胞浸潤、間質纖維化和瘢痕形成,有時伴有血管硬化性改變。本型反應雖然進展緩慢,但用免疫抑制治療無明顯的臨牀效果。
4.移植物抗宿主反應多發生於同種骨髓移植者,也可見於脾、胸腺和小腸移植中;此時患者的免疫狀態極度低下,而移植物中豐富的免疫活性細胞則將受者細胞視爲非己抗原,對其發生免疫應答;移植物的T細胞在受者淋巴組織中增殖併產生一系列損傷性效應。GVHR分爲急性與慢性兩型。急性型多見,多發生於移植後3個月以內,患者出現肝脾腫大、高熱、皮疹和腹瀉等症狀;雖是可逆性變化,但死亡率較高;慢性型由急性型轉來,患者呈現嚴重的免疫失調,表現爲全身消瘦,多個器官損害,以皮膚和粘膜變化最突出,病人往往因嚴重感染或惡液質而死亡。
5 排斥反應的病變
移植排斥反應按形態變化及發病機制的不同有超急性排斥反應、急性排斥反應和慢性排斥反應三類。茲以腎移植中各類排斥反應的病理變化爲例加以說明。類似的變化亦可見於其他組織、器官的移植。
5.1 超急性排斥反應
是受體對移植物的一種迅速而劇烈的反應,一般於移植後數分鐘至24小時內出現.本型反應的發生與受體血循環中已先有供體特異性HLA抗體存在,或受體、供體ABO血型不符有關.這主要是由於循環抗體與移植物細胞表面HLA抗原相結合並激活補本系統,釋放出多種生物活性物質,從而引起局部炎症、血管內皮細胞損害、血栓形成和組織損傷。本質上屬Ⅱ型變態反應,但廣泛分佈的急性小動脈炎、血栓形成和因而引起的組織缺血性壞死,在形態上類似於Arthus反應。
移植腎肉眼觀表現爲色澤迅速由粉紅色轉變爲暗紅色,伴出血或梗死,出現花班狀外觀。體積明顯腫大,質地柔軟,無泌尿功能。鏡下表現爲廣泛的急性小動脈炎伴血栓形成及缺血性壞死。受累的動脈壁有纖維素樣壞死和中性粒細胞浸潤,並有IgG、IgM、補體沉積;管腔中有纖維蛋白和細胞碎屑阻塞。腎小球腫大,腎小管上皮細胞發生缺血性壞死,間質水腫並有中性粒細胞浸潤,有時還可有淋巴細胞和巨噬細胞浸潤。
5.2 急性排斥反應
較常見,在未經治療者此反應可發生在移植後數天之內;而經過免疫抑制治療者,可在數月或數年後突然發生。此種排斥反應可以細胞免疫爲主,也可以體液免疫爲主,有時兩者可同時參與作用。
(1)細胞型排斥反應:常發生在移植後幾個月,臨牀上表現爲驟然發生的移植腎功能衰竭。鏡下可見腎間質明顯水腫伴有大量細胞浸潤,以單核細胞和淋巴細胞爲主,並夾雜一些具有嗜酸性胞漿和水泡狀胞核的轉化淋巴細胞和漿細胞。免疫組化染色證實有大量CD4+、CD8+細胞存在。腎小球及腎小管周圍毛細血管中有大量單核細胞,間質中浸潤的淋巴細胞可侵襲腎小管壁,引起局部腎小管壞死(圖2)。
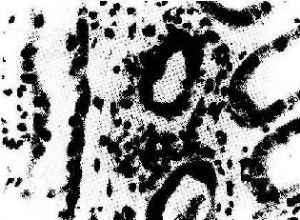
腎間質水腫,腎小管上皮細胞變性,間質及毛細血管內有大量單核細胞
(2)血管型排斥反應:主要爲抗體介導的排斥反應(CMC,ADCC和免疫複合物形成),往往在稍後出現,以突出的血管病變爲特徵。表現爲腎細、小動脈的壞死性血管炎,可呈瀰漫或局竈性分佈。免疫熒光證實有免疫球蛋白、補體及纖維蛋白沉積,腎小球毛細血管袢亦可受累。纖維蛋白樣壞死的血管壁內常有淋巴細胞、泡沫細胞及中性粒細胞浸潤,腔內可有血小板凝集、血栓形成(圖3)。後期的血管內膜纖維化,管腔狹窄。間質內常有不同程度淋巴細胞、巨噬細胞及漿細胞浸潤。肉眼觀,腎常明顯腫大,呈暗紅色並有出血點,有時可出現黃褐色的梗死竈,可伴有腎盂及腎盞出血(圖4).臨牀上,移植腎出現功能減退,大劑量免疫抑制劑療效不佳。
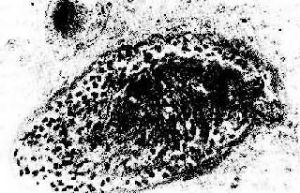
小葉間動脈呈纖維素樣壞死,並有大單核細胞及中性白細胞浸潤和血栓形成
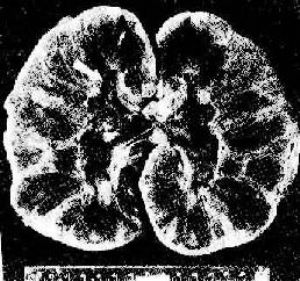
腎腫脹,明顯出血,腎盞及腎盂中充滿血塊
5.3 慢性排斥反應
慢性排斥是反覆急性排斥的積累,其突出的病變是血管內膜纖維化,常累及小葉間弓形動脈。動脈內膜纖維化引起管腔嚴重狹窄(圖5),導致腎缺血,表現爲腎小球毛細管袢萎縮、纖維化、玻璃樣變,腎小球萎縮,間質除纖維化外尚有中等量單核、淋巴細胞浸潤。肉眼觀,腎體積明顯縮小,並有多少不等的瘢痕(“小瘢痕腎”)。包膜明顯增厚並有粘連。患者腎功能呈進行性減退,其程度與間質纖維化和腎小球、腎小管萎縮的程度成正比。
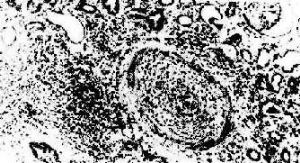
小葉間動脈管壁纖維化,管腔閉塞,內膜有中等量單核細胞浸潤,管周組織內也有類似的細胞浸潤
5.4 移植物抗宿主反應
移植物抗宿主反應(graft versus host reaction,GVH)是免疫缺陷患者接受骨髓移植可發生的一種反應,。在此過程中,移植骨髓的部分幹細胞分化成T細胞或B細胞,當其與宿主組織HLA相接觸時可誘發:①CTL和淋巴因子形成,導致細胞介導免疫反應;②抗宿主HLA抗體形成,導致體液免疫反應,是GVH發生的主要機制。臨牀上,患者表現發熱、體重減輕、剝脫性皮炎、腸吸收不良、肺炎及肝脾腫大等,其中些是由於感染所致。GVH的程度與供體和受體的HLA差別程度有關。本型反應多見於用骨髓移植治療再生障礙性貧血、造血系統惡性腫瘤,特別是經細胞毒性藥物或放射治療後正常造血細胞和白血病細胞均被消滅的病例。
6 排斥反應的免疫學監測
排斥反應的臨牀判斷主要依靠症狀和體徵、移植物功能狀態及實驗室檢測等綜合指標。超急排斥很容易診斷,急性排斥和GVHR的臨牀表現較明顯,慢性排斥多無典型臨牀表現。移植器官的功能測定根據移植物不同而異,多需做大量的生化測定和血液學指標,某些輔助檢查例如B型超聲和彩色多普勒等對了解移植器官的形態、血管通暢性和血流量等也有一定的幫助。免疫學監測是在排斥反應發生之前檢查受者體內參與反應的免疫細胞及某些免疫分子的變化,對判斷患者是否會出現排斥反應有重要的參考意義。
1.外周血T細胞計數用單克隆抗體免疫熒光法或流式細胞儀測定T細胞及其亞羣,在急性排斥的臨牀症狀出現前1~5天,T細胞總數和CD4/CD8比值升高,鉅細胞病毒感染時比值降低;各家報道的比值不同,一般認爲當比值大於1.2時,預示急性排斥即將發生;比值小於1.08則感染的可能性很大。如果能進行動態監測,對急性排斥和感染的鑑別診斷會有重要價值。另外,淋巴細胞轉化試驗對測定T細胞總數和功能狀態也有一定意義。
2.殺傷細胞活性測定移植後因免疫抑制劑的應用,殺傷細胞的活性受抑制,但在急性排斥前會明顯增高。取供者淋巴滅活後作爲刺激細胞,分離患者淋巴細胞作反應細胞,將兩種細胞混合直接做CML,測得的結果是Tc細胞和NK細胞共同作用的結果;進行動態監測的意義更大一些。
3.血清IL-2R測定T細胞激活後可釋出IL-2R,在急性排斥和病毒感染時IL-2R的血清含量升高,以鉅細胞病毒感染時增高最明顯。環孢黴素A腎毒性的腎功能減退時血清肌酐值增高,而IL-2R明顯降低。血清肌酐值和IL-2R同時增高對急性排斥的診斷有意義。但個體間血清IL-2R的含量差別顯著,無公認的診斷標準,限制了它的臨牀的應用,動態測定可克服這一缺點。