6 概述
腹主動脈瘤腔內隔絕術用於腹主動脈瘤的治療。 經典的腹主動脈瘤切除術(準確的名稱是腹主動脈瘤切開人造血管置換術)創傷大,併發症多,病死率較高。許多高齡病人或伴有心、肺、肝、腎等基礎疾病者因無法耐受此種手術而失去了治療的機會。1990年Parodi首先開展腔內隔絕術,其後在全球範圍內得到推廣並不斷完善,爲腹主動脈瘤病人開闢了新的治療途徑。腔內隔絕術是將支架-人造血管複合體(外層爲滌綸人造血管,內層爲可充張的金屬支架)導入腹主動脈,膨脹後將腹主動脈瘤與血管腔隔絕,促使其逐漸機化、縮小,從而消除瘤體破裂、出血的隱患,達到治癒的目的。
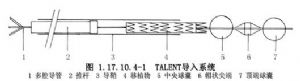
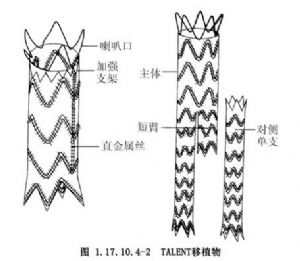
爲施行血管腔內隔絕術,研製開發出了各種各樣的導入(工具)系統和移植物系統,這裏簡要介紹當前在我國廣泛使用的TALENT系統。導入系統由硅塑料鞘(16~17F)、多腔導管(尖端下方可帶有中央球囊,用於擴張移植物,有的在頂端處還有另一球囊,用於阻斷近端血流)和推杆(前方帶有不鏽鋼帽狀尖端)組成(圖1.17.10.4-1)。移植物屬全程支撐彈性自擴張式,有直管型、分叉形和主動脈-髂動脈型3種(圖1.17.10.4-2)。組成部分有:①自擴張支架,由單根鍍鈦的鎳合金絲呈Z形摺疊成環製成;②滌綸編織無螺紋人造血管。使用前,將幾個支架順序塞入人造血管,支架保留5mm間距,以滌綸線連續縫合,再用一根直的金屬絲將所有的支架連接起來。這種全程分級內支架移植物有一定的可彎曲率,又有足夠的強度。在移植物近心和遠心端各加一個直徑稍大的Z形支架,一端縫合於移植物上,另端暴露於人造血管之外呈喇叭口狀(圖1.17.10.4-2),以便提供足夠的周向張力來維持移植物的無縫合固定。要根據術前CT血管造影成像所測得的各種參數選擇適當的移植物。
7 適應症
腹主動脈瘤腔內隔絕術適用於:
1.原則上所有腎動脈開口以下、近端瘤頸≥1.5cm的腹主動脈瘤都是腔內隔絕術的適應證。但在目前,腔內隔絕術大多用於年齡較大、伴發病較嚴重或有多種伴發病、不能耐受傳統腹主動脈瘤人工血管置換術的病人。
2.遠端瘤頸≥1cm者,可採用直管型或分叉形移植物。
8 禁忌症
1.腹主動脈瘤的位置或形態不適於腔內隔絕手術者,如範圍廣泛的胸腹主動脈瘤或近端瘤頸<1.5cm因而無法固定移植物者。但近年已開發出近端帶有裸支架的移植物,近腎腹主動脈瘤已經不是絕對禁忌證。
2.導入通路病變使手術難以完成者,如雙側髂動脈嚴重狹窄扭曲以至導絲、導管不能通過。
9 術前準備
1.全面檢查,重點查清並認真評估病人心、肺、肝、腎及出凝血系統功能。
2.如合併有高血壓症、糖尿病,應加強治療,將其控制在儘量好的狀態。
4.術前3d開始口服腸溶阿司匹林(50mg,4次/d)、雙嘧達莫(25mg,3次/d)。
5.術前留置導尿。
6.預防性應用抗生素。
11 手術步驟
1.選擇髂動脈通暢的一側,在腹股溝韌帶下沿股動脈走行做縱行切口長約5cm,解剖出長3cm的一段股總動脈,遠近兩端分別穿過止血吊帶備用。
2.直視下以Seldinger法穿刺股動脈,導入5F導管鞘。
3.經導鞘送入導絲至腹主動脈,沿導絲送入豬尾巴導管到第12胸椎水平,撤出導絲,行主動脈造影。
4.在監視屏上做相應標記後,準確測量瘤頸和瘤體的長度和直徑、髂總動脈直徑、腎動脈開口至髂內動脈開口的距離,並與術前螺旋CT和磁共振動脈造影結果對照,據此選擇適當口徑和長度的移植物。下面主要介紹最常見的分叉形移植物置入方法。
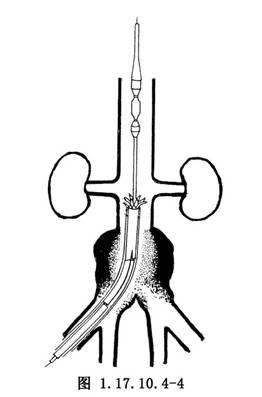
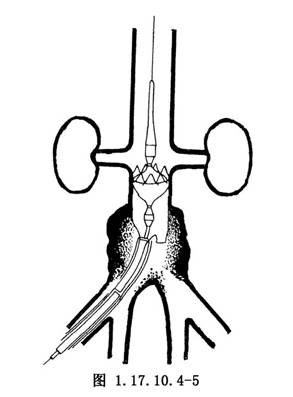
5.插入超強導絲後退出造影導管,靜脈注射肝素125U/kg使全身肝素化。以穿刺點爲中心做股動脈橫行切口約1/2周徑,沿導絲導入TALENT導管至腹主動脈。當移植物上緣到達腎動脈開口後(圖1.17.10.4-3),釋放移植物的前端(2節)(圖1.17.10.4-4),向遠端拉動移植物,使預置的移植物上緣標記與腎動脈開口下緣標記重合,然後充張導管內附有的球囊,使移植物近端擴張並牢靠固定於腹主動脈壁上(圖1.17.10.4-5)。

6.保持球囊充盈以固定移植物,退出外鞘管,使被釋放的記憶合金支架自動張開,移植物下端短臂位於瘤體內,長臂則進入髂動脈。緩慢退出球囊,在此過程中移植物被逐節擴張,固定於血管壁上(圖1.17.10.4-6)。
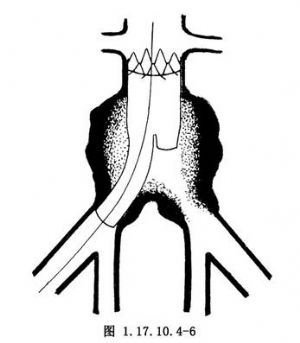
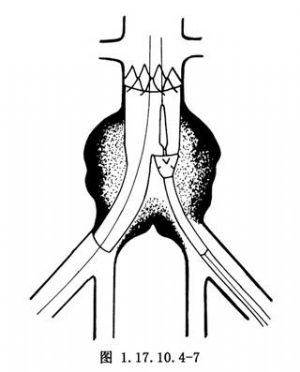
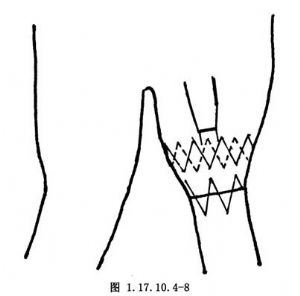
7.暴露對側股總動脈,穿刺後插入超硬導絲經移植物短臂開口送入移植物主體。切開股動脈,沿導絲將長度適宜的人造血管送入移植物短臂內,準確定位後,釋放該單支,使其自動張開,與移植物短臂妥善連接(圖1.17.10.4-7),連接部分至少要重疊一節支架的長度(圖1.17.10.4-8),遠段固定於髂動脈血管壁上。
8.再次做腹主動脈造影,觀察移植物和腎動脈、髂動脈是否通暢,移植物有無扭曲、異位,近端和遠端有無內漏。
9.證實瘤體已被完全隔絕後,退出TALENT導管,以5-0 Prolene線橫向縫合股動脈切口。逐層縫合切口。
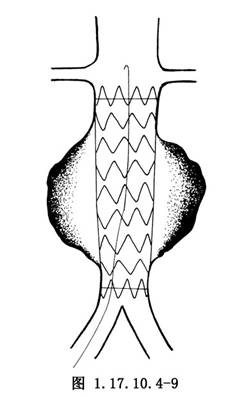
10.直管型移植物只需將其遠端固定於腹主動脈分叉上方,操作更爲容易(圖1.17.10.4-9),但由於腹主動脈瘤自身有向遠端蔓延的傾向,目前已較少應用。
12 術中注意要點
1.近腎(瘤頸長度<1.5cm)腹主動脈瘤不能使用普通移植物,應使用近端帶裸支架、即近端1.5~2.0cm一段支架外沒有人造血管覆蓋的移植物。這種支架可以固定在腎動脈開口部位或開口以上的動脈壁上而不會阻斷腎動脈的血流。
2.導入動脈狹窄者,可先行球囊擴張,再插入導絲和導管。如不能成功擴張,需通過輔助手術經腹膜外途徑顯露髂總動脈,直接插入導絲和導管。
3.在釋放近端移植物過程中,要注意監測腎動脈通暢情況,避免誤閉腎動脈。如誤閉不幸發生,應儘量採取補救措施,例如將充張適當的球囊保留於原位,藉助血流衝擊帶動球囊和移植物一同下移,直到腎動脈開口開放。確實無法補救時,應緊急施行腹主動脈-腎動脈旁路術。
4.放置分叉形移植物時,要掌握好移植物的三維位置,謹防移植物短臂在轉向狀態下被釋放。一旦發生短臂位置錯誤,可試行將導絲導入短臂以幫助其與隨後導入的單支人造血管對接,若原導絲無法導入短臂,或雖然導入短臂但仍無法實現對接,則應放棄此種嘗試,改從一側肱動脈插入導絲,經移植物主體和短臂出口導入髂動脈,以兩頭持引導絲法完成與單支人造血管的對接。
5.兩段移植物的對接,必須重疊一節支架(2cm)的長度,嚴防滑脫造成嚴重內漏。一旦發生滑脫,應另選一段口徑適宜的移植物,經原導絲導入,將滑脫的兩端對接起來。若無法按原導絲導入,可經兩頭持引導絲導入。
6.擴張移植物遠側端時,應掌握好力度,防止造成動脈破裂。一旦發生破裂,可立即用球囊阻斷破裂部位,暫時控制出血,同時準備一段口徑適宜的移植物,導入至適當部位,將破裂處封閉隔絕。
14 併發症
14.1 1.內漏
發生率約7%~20%。持續存在的內瘻可導致腔內隔絕術失敗,瘤體繼續擴大甚至破裂。發生內漏的主要原因包括:①適應證選擇不當(瘤頸血管壁斑塊鈣化,瘤頸嚴重扭曲,動脈瘤壁大量斑塊使移植物變形等);②移植物類型選擇不當;③移植物口徑和長度不適當;④未曾處理仍保持通暢的腰動脈和腸繫膜下動脈。繼發性內漏可以通過手術結束前腹主動脈造影發現;延遲性內漏的診斷則有賴於定期的嚴密隨診。近端內漏後果最爲嚴重,應在手術中即時解決。可用球囊在瘤頸部做適當擴張,或添加一段套管,一般可以奏效。如仍有大量內漏,應果斷施行傳統手術,以免發生破裂。遠端附着點內漏大多由移植物與動脈口徑不匹配造成,延長一段移植物通常有效,但應避免同時隔絕雙側髂內動脈。
14.2 2.腎動脈閉塞
腎動脈閉塞大多在釋放移植物後立刻發生。原因是定位不準確或操作失誤,致使帶膜支架覆蓋了腎動脈開口。少數病人發生手術後延遲性腎動脈閉塞,可能與移植物裸支架超腎動脈固定對腎動脈血流動力學產生干擾有關。腎動脈閉塞會導致腎功能減退和高血壓,但若腎梗死面積不很大,腎功能有逆轉可能,高血壓也可用藥物控制。如果腎動脈完全閉塞,需行腹主動脈-腎動脈旁路手術。
14.3 3.腹主動脈瘤腔內隔絕術後綜合徵
有些病人手術後出現不明原因的發熱,一般不超過38.5℃,紅細胞、白細胞和血小板計數下降,一過性C-反應蛋白升高,但無感染證據,故籠統稱之爲“術後綜合徵”。發生機制尚不清楚,可能與瘤腔內血栓形成後的吸收、移植物的異物反應、移植物對血細胞的機械性破壞等因素有關。對症治療可用非甾體類鎮痛藥(如吲哚美辛)和腎上腺糖皮質激素,一般可以奏效。
14.4 4.缺血性結腸炎
多發生於乙狀結腸,主要原因是腸繫膜下動脈封堵後乙狀結腸側支循環供血不足。因此,兩側髂內動脈不宜同時隔絕或栓塞,至少保留一側通暢。即時發生乙狀結腸缺血病死率甚高(>50%),但很少見。在腔內隔絕術後,多數缺血是由逐漸發生的髂內動脈閉塞引起,病情呈漸進性,從出現症狀到發生腸壞死有一個過程。早期發現、早期治療十分重要。主要症狀是腹痛,結腸鏡檢查發現腸黏膜蒼白、水腫或散在出血點便可確診。使用血管擴張劑和降低血液黏稠度、疏通微循環的藥物,促使側支循環儘快建立是主要治療措施,效果尚好。若發生腸壞死,只能手術切除。