1 拼音
yào wù dài xiè chǎn wù ān quán xìng shì yàn jì shù zhǐ dǎo yuán zé
《藥物代謝產物安全性試驗技術指導原則》由國家食品藥品監督管理局於2012年5月15日國食藥監注[2012]122號印發。
2 一、概述
藥物安全性的非臨牀研究通常由標準的動物毒理學試驗組成,這些試驗通常包含了藥物暴露量的評價,主要是母體藥物血漿濃度的評價。一般情況下,通常將非臨牀試驗中獲得的血漿藥物濃度和系統暴露量與人體的系統暴露量進行比較,對非臨牀試驗結果提示的潛在風險進行評估,並指導臨牀試驗中的風險控制。當人體中的代謝特徵與非臨牀試驗中使用的至少一種動物種屬中的代謝特徵相似時,這種試驗模式通常認爲是可行、充分的。但是,不同動物種屬的代謝特徵在質和量上均可能存在差異,而且還存在臨牀相關的代謝產物在非臨牀安全性試驗中未被確定或未被充分評價的情況。如果某種代謝產物僅在人體中出現而在受試動物種屬中不存在,或者某種代謝產物在人體的暴露比例水平高於採用母體藥物進行標準毒理學試驗的動物種屬中的暴露比例水平時,代謝產物的安全性就值得關注,應考慮進行代謝產物的非臨牀安全性評價。
3 二、背景信息
常規情況下,臨牀前安全性試驗不要求在動物中對代謝產物進行評價。因此,代謝產物在總體藥物毒性中的作用通常不明確。缺乏代謝產物在藥物毒性中作用的評價,其部分原因可能是因爲用於檢測和鑑別母體藥物代謝產物特徵的分析方法的靈敏度不夠。隨着過去10年的技術進步,分析檢測能力有了顯著提高,現在已能夠對代謝產物進行檢測、鑑別和定性,這將有助於更好理解代謝產物在藥物安全性評價中的地位。
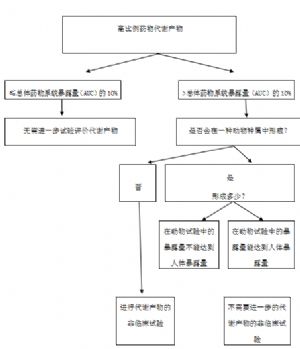
進入機體的藥物通常通過I相和II相代謝途徑進行生物轉化。根據所涉及的化學反應性質,I相反應產生的代謝產物,很可能具有化學反應性或/和藥理學活性,因此可能更需要進行安全性評價。活性代謝產物可能與治療靶點受體或其他受體結合,或與其他靶點(如酶、蛋白)相互作用,引起非預期的效應。尤其是當代謝產物僅在人體中形成時,這個問題更爲重要。但是,僅在人體中存在而不在實驗動物種屬中存在的代謝產物,出現的機率極低。更爲常見的情況是,人體中形成的代謝產物比例水平遠遠高於母體藥物在動物安全性試驗中代謝產物的比例水平,這緣於人體和動物的代謝特徵存在質和/或量的差異。如果在母體藥物的毒理學試驗中確定至少有一種實驗動物種屬中形成特定代謝產物的暴露量水平足夠高(與人體暴露量大致相當或更高),則可認爲該代謝產物對總體毒性的作用已經得到了確定。代謝產物安全性評價的決策流程圖見附錄A。
對於代謝產生的活性中間體,因其半衰期短,常難以檢出和測定。但是,它們能形成可檢測的穩定產物(如谷胱甘肽結合物),因此可能不需要對活性中間體做進一步的安全性評價。II相結合反應通常會使一個化合物的水溶性增加並失去藥理學活性,故也不再需要進一步評價。但是,如果結合反應形成一種毒性化合物如乙酰葡萄糖醛酸(acylglucuronide),則可能需要進一步的安全性評價。
若研究發現代謝產物在靶受體上無藥理學活性,這並不能確保其無毒性,該代謝產物也可能需要在非臨牀毒理學試驗中進行安全性評價。列舉案例見附錄B。
4 三、目的和適用範圍
本指導原則主要針對需要進行非臨牀毒性評價的藥物代謝產物,爲研發者何時以及如何鑑定高比例藥物代謝產物並研究其安全性特徵提供建議。
本指導原則適用於小分子化學新藥。本指導原則不適用於那些需要考慮風險效益評價的抗腫瘤藥物。針對抗腫瘤藥物代謝產物的安全試驗可參考ICH S9指導原則。
5 四、代謝產物安全性試驗的一般考慮
在藥物開發過程中應儘早確認非臨牀安全評價中所用動物種屬和人體間的藥物代謝差異。如在獲得人體藥代數據後,通過比較藥代信息決定是否需要儘早開展代謝產物的安全性評價。在藥物開發晚期發現高比例藥物代謝產物(Disproportionate drug metabolite)時可能會導致藥物開發或上市延遲。
一般情況下,對於僅在人體中出現的代謝產物,或人體中代謝產物水平遠高於已知或已進行評價的實驗動物種屬中的水平時,應考慮進行安全性評價。若人體中的代謝產物水平高於穩態時體內藥物總暴露量的10%時,通常會引起安全性擔憂。代謝產物水平通常採用曲線下面積(AUC)來表示,但有時也會採用達峯濃度(Cmax)來表示。
5.1 (一) 評價代謝產物安全性的一般方法
如果在動物中發現的代謝產物在人體中不存在,意味着在該動物種屬中觀察到的謝產物引起的毒性可能與人體無相關性。相反,如果在臨牀開發過程中發現的代謝產物在實驗動物種屬中不存在,或在動物中水平遠低於人體水平,則建議進行進一步的動物試驗以確定該代謝產物的潛在毒性。
這種情況下,可考慮採用以下兩種方法來評價藥物代謝產物的安全性。第一種方法是,確定一種在常規毒理學試驗中的動物種屬,在該動物種屬上能形成充分暴露水平的該代謝產物(與人體暴露量相當或更高),然後在該動物種屬中研究藥物毒性。第二種方法是,如果不能確定一種形成該代謝產物的相關動物種屬,則可合成該代謝產物,通過摻入法或直接給藥來開展進一步的安全性評價。上述試驗需建立能夠在非臨牀毒理學試驗中鑑別和檢測該代謝產物的分析方法。
衆所周知,特定代謝產物的合成存在困難,代謝產物直接給藥也有其固有的複雜性。直接將代謝產物給予動物,可能還會存在後續代謝,因而可能無法反映臨牀實際情況,這樣使得毒理學評價變得複雜化。以代謝產物給藥可能會出現在母體藥物試驗中未觀察到的新的毒性,但儘管有這樣的複雜問題,檢測和評價藥物代謝產物潛在的毒性,對於保障藥物的臨牀安全性仍具有重要性。確定是否進行直接的代謝產物的安全性試驗,應基於對母體藥物的數據以及代謝產物各方面信息的綜合評價。
5.2 (二) 代謝產物鑑別
在藥物開發過程中需要確定藥物的代謝特徵,可以在不同開發階段,通過體外和體內試驗方法來完成代謝特徵的確定。體外試驗可採用不同動物和人體的肝微粒體、肝臟切片或肝細胞,體外試驗通常應在臨牀試驗開始前進行。非臨牀試驗動物種屬中的體內代謝試驗通常應在藥物開發早期進行,其結果可以證實體外試驗獲得的結果,或者提示動物種屬間代謝存在的質和/或量的差異,而後者可能會帶來安全性擔憂。人體的體內代謝試驗通常是在藥物開發的相對後期進行,但仍建議人體內代謝研究儘早進行。
對於在非臨牀試驗動物中暴露水平遠低於人體的代謝產物,其暴露是否充分應具體問題具體分析。通常情況下,通過測定穩態時血清或血漿中藥物濃度來分析系統暴露量。但如果由於某種原因無法在受試動物的血漿中測定時,則可通過測定代謝產物在其他生物基質的水平以驗證暴露是否充分,如尿液、糞便或膽汁。
5.3 (三)非臨牀試驗設計的一般考慮
對一種高比例藥物代謝產物設計非臨牀試驗時,需要考慮以下因素:代謝產物與母體分子的相似性,藥理學或化學分類,溶解性,胃液環境下的穩定性,I相或II相代謝產物,人體中暴露水平與動物中暴露水平的相對量。
其他需要考慮的因素包括藥物擬定適應症和患者人羣[例如對於嚴重疾病適應症時非臨牀試驗可以簡化,如肌萎縮性側索硬化症(ALS)]。在對代謝產物設計非臨牀試驗時,還需要考慮擬定的用藥療程(短期、中期或長期用藥)以及治療劑量下的暴露水平。
6 五、推薦的代謝產物的安全性試驗
需要進行安全性評價的藥物代謝產物的非臨牀試驗應符合GLP。可能需要進行以下試驗來評價高比例藥物代謝產物的安全性。
6.1 (一)一般毒理試驗
在一般毒理試驗中,應評價高比例藥物代謝產物的潛在毒性,進行代謝產物與其母體藥物間的毒性比較。代謝產物直接給藥的一般毒理試驗的期限,可參考國內相關指導原則和ICH M3(支持藥物進行人體試驗需要的非臨牀安全性試驗)技術指導原則。應在數倍於人體暴露量或者在至少與人體中檢測到的暴露量相當水平下評價代謝產物的毒性。建議採用母體藥物擬定的臨牀給藥途徑給藥。但如果可以使高比例藥物代謝產物達到足夠的暴露量,也可以採用其他給藥途徑。如果臨牀給藥途徑爲口服,確認代謝產物在胃液環境中的穩定性十分重要。爲了保證高比例藥物代謝產物的充分暴露,上述試驗中需包括毒代動力學研究。
6.2 (二) 遺傳毒性試驗
需以一項檢測點突變的體外試驗和另外一項檢測染色體畸變的試驗來評價代謝產物的潛在遺傳毒性。這些試驗可參考SFDA《藥物遺傳毒性研究技術指導原則》。如果其中一項試驗或兩項試驗結果是可疑和/或陽性時,可能需要進行完整的遺傳毒性標準組合試驗。
6.3 (三) 胚胎-胎仔發育毒性試驗
如果藥物擬定的用藥人羣包括有生育可能的婦女時,需進行代謝產物的胚胎-胎仔發育毒性試驗。根據一般毒理試驗和胚胎-胎仔發育毒性試驗的結果,在具體問題具體分析的基礎上,可能會要求進行其他生殖毒性試驗。這些試驗可參考SFDA《生殖毒性研究技術指導原則》。某些情況下,可僅在一種能形成該代謝產物的動物種屬中進行胚胎-胎仔發育毒性試驗。
6.4 (四)致癌性試驗
藥物連續用藥至少6個月,或需間歇用藥用於治療慢性或週期性復發疾病,如果在母體藥物的致癌性試驗中不能對代謝產物的致癌性潛力進行充分評價,則應該進行代謝產物的致癌性試驗。這些試驗可參考SFDA《藥物致癌試驗必要性的技術指導原則》和國外的致癌性試驗技術指導原則。
7 六、安全性研究的時間安排
需儘早確證人體中可能存在的高比例藥物代謝產物,這可以爲非臨牀試驗的合理性提供證明,有助於闡明和制訂臨牀試驗計劃,並避免藥物開發進程的延遲。通常首先採用體外試驗來預測動物和人體的藥物代謝差異,然後根據人體和動物的代謝差異來考慮是否需要開展藥物代謝產物的安全性試驗。如果在體外代謝研究提示有人體的高比例藥物代謝產物,可考慮開展動物和人體的同位素標記法的代謝研究,爲開展高比例藥物代謝產物的臨牀前安全性研究提供依據。
如果需要進行代謝產物的毒理學試驗,應在大規模臨牀試驗開始前完成這些試驗,並向藥品審評部門提交試驗報告。
爲了優化和加快研發用於包括腫瘤疾病在內的其它嚴重或危及生命疾病(如ALS、中風、HIV)的藥物,對於那些具有重大治療利益的藥物,以及用於尚缺乏有效治療手段疾病的藥物,代謝產物的非臨牀試驗的數量和類型可根據具體情況具體分析的原則進行調整。晚期癌症患者治療時,這些代謝產物並不要求必需開展單獨的毒理評價。此種情況下,申辦人應聯繫相關藥品審評部門進行討論。
8 詞彙表
高比例藥物代謝產物(Disproportionate drug metabolite):僅在人體存在的代謝產物,或在人體循環系統的暴露量顯著高於非臨牀試驗所用動物中暴露量的代謝產物。一般情況下,以穩態的曲線下面積(AUC)來計算。血漿水平中高於人體總體藥物系統暴露量10%的代謝產物應給予關注。
代謝產物(Metabolite):母體藥物經過I和/或II相代謝途徑產生的物質。
藥理活性代謝產物(Pharmacologically active metabolite):在靶受體具有藥理學活性的代謝產物,其活性可能高於、等於或低於母體藥物。
10 附錄B 案例
案例1
從初步的物料平衡試驗中發現,1種代謝產物在大鼠血漿中約佔總放射性劑量的1%-2%,犬中爲5%,人體爲20%(尿液和/或糞便中該代謝產物的放射性很低)。根據上述數據,人體中該代謝產物的暴露量比動物高達20倍,因此建議進行代謝產物的非臨牀安全性試驗。但是,大鼠和犬中母體藥物一般毒理試驗的數據提示,測試的最高劑量下產生的代謝產物暴露量至少與最大推薦人用劑量時的治療暴露量相當。同時,以母體藥物進行的體內遺傳毒性試驗、胚胎-胎仔發育毒性試驗及致癌性試驗中,檢測該代謝產物的血漿濃度後發現有足夠的該代謝產物的暴露量,因此不需要對該代謝產物進行其他試驗。
案例2
採用人、猴、大鼠、犬、家兔和小鼠的肝細胞和肝微粒體檢測發現,兩種初級羥基化代謝產物M1和M2進一步氧化形成次級代謝產物M3和M4。後續體內試驗數據也證實了該代謝特徵。藥代研究信息如下:1)M1與M4是人體、猴和犬微粒體中的主要代謝產物,而大鼠、小鼠和家兔微粒體中的是M2和M3。2)在人體中形成的M4水平比母體藥物高4倍,但M4在齧齒類動物中的水平很低,在猴中僅佔母體藥物暴露量的1/3(見下表)。
表:最高劑量下的AUC0-24hr
安全性研究顯示:在猴中母體藥物出現了嚴重的藥物相關的、新的靶器官毒性,而大鼠中未出現。此外,在藥物靶受體中M4無藥理學活性。
爲此,代謝產物M4進行了以下附加試驗:
體外遺傳毒性試驗:M4的點突變和染色體畸變試驗結果爲陽性,母體藥物爲陰性。
案例3
M2是一種I相氧化代謝產物,在人體中高達母體藥物暴露量的50%,在小鼠中約爲母體藥物暴露量的10%,犬中約爲母體藥物暴露量的15%,大鼠中僅爲痕量。這些動物種屬的體外代謝試驗結果支持體內研究結果。根據構效關係分析結果,與母體藥物分子比較,該代謝產物預期不會產生任何不同的毒性或加重毒性。在安全性評價試驗所測試的所有動物種屬中,母體藥物未見明顯毒性,也未見可確定的毒性靶器官。但是,由於人體中出現了高比例藥物代謝產物,故需要進一步的安全性試驗。在犬的短期耐受性試驗中,M2出現了非預期的、顯著的心臟毒性,包括所有劑量和所有受試犬。M2對治療靶受體無藥理學活性。
11 參考文獻
1. FDA Guidance:Safety Testing of Drug Metabolites,2008
2. ICH M3(R2): Nonclinical Safety Studies forthe Conduct of Human Clinical Trials and Marketing Authorization forPharmaceuticals,2010
3. ICH S9: Nonclinical Evaluation forAnticancer Pharmaceuticals,2010
4. ICH S6: 生物技術藥物的臨牀前安全性評價和S7A人用藥物安全藥理學研究指導原則(http://www.ich.orgicache/compo/276-254-1.html)。
5. ICH S3A:毒代動力學指導原則註釋:毒性研究中全身暴露量的評價(http://www.ich.orgicache/compo/276-254-1.html).
6. U.S. Environmental Protection Agency, 1998,Health Effects Test Guidelines, OPPTS 870.7485, Metabolism andPharmacokinetics. (http://www.epa.gov/epahome/research.htm)。
12 起草說明
1.本指導原則主要參考USA FDA的指導原則Safety testing of drug metabolites來起草,同時也考慮了ICHM3 中對代謝物的安全性研究要求。指導原則內容代表了目前國際上對藥物代謝產物安全性研究的基本要求。
2.考慮到該技術要求在國內尚處於起始階段,文中簡介瞭如何識別藥物代謝產物的種屬差異,以及何時關注代謝產物安全性的時間安排,具體見第6部分。關於具體的體外代謝研究方法和體內的放射自顯影方法,需要結合其他相關指導原則要求來一併考慮。
3.關於代謝比例的10%,原文中是指母體藥物暴露量的10%,在專家討論中認爲,國外已經認爲該定義方法存在問題,在後續討論中認爲應該將分母定義爲原型藥物和代謝物的總體藥物暴露量,因此明確10%是指藥物總體暴露量的10%。
4.USA FDA指導原則中的Disproportionatedrug metabolite在翻譯中有不同譯法,最後統一爲高比例藥物代謝產物,並通過定義對其給予具體說明。
5.關於參見的安全性研究指導原則,如果SFDA已經發布,則將USA FDA指導原則原文中的ICH或FDA相關指導原則修改爲SFDA已經發布的指導原則。