3 概述
高脂蛋白血癥(hyperlipoproteinemia)是指血漿中膽固醇(TC)和(或)三酰甘油(TG)水平升高。實際上是血漿中某一類或某幾類脂蛋白水平升高的表現。近年來已逐漸認識到血漿中LDL-C(低密度脂蛋白膽固醇)降低也是一種血脂代謝紊亂。因而有人建議採用脂質異常血癥(dyslipidemia),並認爲這一名稱能更爲全面準確地反映血脂代謝紊亂狀態。高脂蛋白血癥是一類較常見的疾病,除少數是由於全身性疾病所致外(繼發性高脂蛋白血癥),絕大多數是因遺傳基因缺陷(或與環境因素相互作用)引起(原發性高脂蛋白血癥)。高脂蛋白血癥在動脈粥樣硬化的發生和發展及其引起的心血管事件中起非常重要的作用,是冠狀動脈疾病、卒中和外周血管疾病的主要危險因素之一。脂蛋白代謝異常最常見的併發症是動脈粥樣硬化;高三酰甘油及乳糜微粒血癥,常可併發急性胰腺炎等致命性疾病。
高脂血症的臨牀表現主要包括兩大方面:一方面是脂質在真皮內沉積所引起的黃色瘤;另一方面脂質在血管內皮沉積所引起的動脈粥樣硬化,產生冠心病和外周血管病等。通過採用藥物使過高的血脂降至正常,這在臨牀上較爲常用,其降脂效果肯定,病人常易於接受,但也有其侷限性。非藥物性降脂治療包括飲食控制、血漿淨化、外科手術和基因治療等。其中飲食治療因爲是高脂血症治療的基礎,所以已被普遍採用。血漿淨化和外科手術治療則是藥物性降脂治療的補充,應用並不廣泛。基因治療僅適應於極少數嚴重的高脂血症。
8 流行病學
高脂血症與動脈硬化之間有因果關係,其中高膽固醇血癥是動脈硬化的一個獨立的、重要的危險因素。血漿HDL-膽固醇水平與冠心病的發生率呈負相關,是一種具有抗動脈硬化作用的保護因素,此點與LDL-膽固醇正好相反。正常人血清LDL-膽固醇水平高於0.91mmol/L(35mg/dl),低於此值者,不論血清TC水平是否增高,均有易發生冠心病的傾向。LDL-膽固醇水平下降是動脈硬化的一個獨立的危險因素。 LCL-膽固醇/HDL-膽固醇比值是反映冠心病發病風險的最好指標。在合併有其他的一些危險因素(如吸菸、肥胖、高三酰甘油血癥和體力活動少等)時,血漿HDL-膽固醇水平往往降低。
近年來大量的流行病學資料分析表明,血漿三酰甘油(TG)是老年女性冠心病的獨立危險因素。TG水平升高>2.26mmol/L(200mg/dl)還是家族性高三酰甘油血癥患者的一個獨立的危險因素。
脂蛋白LP(a)是冠心病的又一個獨立的危險因素,正常人血漿中LP(a)平均0.076g/L,其濃度不受年齡、性別及飲食等因素的影響。流行病學研究顯示,LP(a)水平增高與冠心病發病率密切相關。如果同時伴有LDL增多,則危險性可升高5倍。LP(a)與冠心病的相關性,在女性和55歲以下的中、青年男性表現似乎更加顯著。一般認爲,LP(a)濃度0.30~0.40g/L可作爲冠心病發病的危險閾值。
9 高脂蛋白血癥的病因
9.1 臨界高膽固醇血癥的病因
人類臨界高膽固醇血癥的原因除了其基礎值偏高外,主要是飲食因素即高膽固醇和高飽和脂肪酸攝入以及熱量過多引起的超重,其次包括年齡效應和女性的更年期影響。
9.1.1 (1)基礎血漿LDL-C(低密度脂蛋白膽固醇)水平高
這種較高的基礎LDL-C是人類臨界高膽固醇血癥的主要原因之一。爲什麼人類的基礎膽固醇會相對較高?可能是由於人體內膽固醇轉化爲膽汁酸延緩,肝內膽固醇含量升高,繼而抑制LDL受體活性。
9.1.2 (2)飲食膽固醇高
一般西方國家的人羣攝入膽固醇量爲400mg/d,而低膽固醇人羣的攝入量爲200mg/d左右。膽固醇攝入量從200mg/d增加爲400mg/d,可升高血膽固醇0.13mmol/L(5mg/dl)。其機制可能與肝臟膽固醇含量增加、LDL受體合成減少有關。
9.1.3 (3)飲食飽和脂肪酸高
臨界膽固醇升高的一個主要原因是較高的飽和脂肪酸飲食攝入。典型的西方人所攝入的飽和脂肪酸大約爲每天總熱量的14%,而理想的量應爲7%。一般認爲飽和脂肪酸攝入量佔總熱量的14%(即多7%),可致血膽固醇增高大約0.52mmol/L(20mg/dl),其中多數爲LDL-C。有資料表明,飽和脂肪酸抑制LDL受體活性。雖然其確切的機制尚不清楚,但可能與下列5個方面有關:①抑制膽固醇酯在肝內合成;②促進無活性的非酯化膽固醇轉入活性池;③促進調節性氧化類固醇形成;④降低細胞表面LDL受體活性;⑤降低LDL與LDL受體的親和性。
9.1.4 (4)體重增加
有研究提示血漿膽固醇升高可因體重增加所致。一般認爲體重增加,大約可使人體血膽固醇升高0.65mmol/L(25mg/dl)。至少有兩種代謝機制可解釋這種膽固醇升高:①肥胖促進肝臟輸出含Apo B的脂蛋白,繼而使LDL生成增加;②肥胖使全身的膽固醇合成增加,引起肝內膽固醇池擴大,因而抑制LDL受體的合成。
有人認爲肥胖是血漿膽固醇升高的一個重要因素,其作用尚被低估了。依照體重指數(BMI)將受試者分爲6組:A組BMI≤21.0;B組BMI 21.1~23.0;C組BMI 23.1~25.0;D組BMI 25.1~27.0;E組BMI 27.1~30.0;F組BMI>30.0。結果發現,E組的平均血漿膽固醇水平較B組高0.46mmol/L(18mg/dl)。這種體重增高伴隨血漿膽固醇水平升高不僅見於男性,也見於女性(包括青年和更年期的女性)。
9.1.5 (5)年齡效應
隨着年齡的增加,體重也會增加。但是,依年齡增加而伴隨的膽固醇升高並非全是體重增加所致。有人發現老年人的LDL受體活性減退,LDL分解代謝率降低,也是年齡效應的原因。老年人LDL受體活性減退的機制尚不清楚,可能是由於隨着年齡的增加,膽汁酸合成減少,使肝內膽固醇含量增加,進一步抑制LDL受體的活性。現有資料表明,除體重因素外,年齡本身可使血漿膽固醇增加0.78mmol/L(30mg/dl)左右。
9.1.6 (6)絕經後婦女
在45~50歲前,女性的血膽固醇低於男性,隨後則會高於男性。這種絕經後膽固醇水平升高很可能是由於體內雌激素減少所致。已知在人類和動物雌激素能增加LDL受體的活性。美國婦女絕經後總膽固醇可增高大約0.52mmol/L(20mg/dl)。
9.1.7 (7)其他因素
除上述引起臨界高膽固醇血癥的因素之外,尚有一些其他的因素也可造成在某些相同的環境下部分個體的血漿膽固醇水平偏高。這些因素包括個體的膽固醇吸收率、合成率、肝臟膽汁分泌率以及體內LDL分解代謝率差異等。這可能與個體間某些遺傳基因變異有關。已知Apo E的基因型和Apo AⅣ多態性等均可影響個體間對食物膽固醇吸收率的不同。
9.2 輕度高膽固醇血癥的病因
輕度高膽固醇血癥是指血漿TC(膽固醇)濃度爲6.21~7.49mmol/L(240~289mg/dl)或LDL 4.15~5.41mmol/L(160~209mg/dl)。大多數輕度高膽固醇血癥的病人,可能是由於上述臨界高膽固醇血癥的原因所致,同時合併有遺傳基因的異常。由於異常基因的存在,使體內LDL分解代謝速率降低,LDL合成增加或LDL結構改變。但是,在大多數情況下,尚未能在分子水平上完全認識這些異常的遺傳基因。基於脂蛋白動力學研究結果,已知有幾種異常能引起輕度高膽固醇血癥。
9.2.1 (1)LDL清除率低下
LDL體內更新代謝研究揭示,某些原發性輕度高膽固醇血癥的病人,與臨界性高膽固醇血癥相比較,有LDL清除異常性低下。其可能的原因有兩種:①LDL受體活性受抑制,即較臨界性高膽固醇血癥患者更低下;②另一部分病人則可能有LDL顆粒與其受體結合能力差。
家族性Apo B100(載脂蛋白B100)缺陷是目前已知引起LDL在體內分解代謝緩慢的原因之一。而在家族性Apo B100缺陷中,現已鑑定的異常有Apo B3500,是該載脂蛋白的第3500位上的谷胺酰胺被精氨酸所替代,引起所謂的“B3500缺陷”。其他Apo B缺陷尚待澄清。
9.2.2 (2)LDL輸出增加
輕度高膽固醇血癥的另一個原因是LDL產生過多,即VLDL(極低密度脂蛋白)轉變成LDL增加。有3種可能的機制與其有關:①LDL受體活性下降。當LDL受體活性下降時,VLDL顆粒經LDL受體分解代謝減少,因而過多的VLDL轉化爲LDL。②肝臟產生過多含Apo B(載脂蛋白B)脂蛋白。在這種情況下,LDL的分解代謝率並無顯著下降,屬基本正常或輕度下降。③VLDL顆粒自身的缺陷。這可使VLDL顆粒(或其殘核)經肝臟直接清除減少。在這種情況下,LDL受體清除LDL是增高的。這是由於LDL受體因VLDL負荷減少所致,LDL分解代謝率相對較高。雖然如此,由於VLDL顆粒的缺陷,仍能引起LDL濃度增加。因爲在正常情況下,VLDL顆粒與LDL顆粒相比較,VLDL與受體的親和力大於LDL。所以,經受體途徑分解代謝LDL顆粒的速度相對較VLDL緩慢。
已有報道,在家族性混合型高脂血症時,LDL-Apo B產生過多,這種情況可稱爲“高載脂蛋白B血癥”(Hypelipo B)。其特徵爲LDL顆粒中膽固醇與Apo B的比例低下(<1.25)。
9.2.3 (3)LDL富含膽固醇酯
LDL-C水平從臨界狀態上升爲輕度升高的最後一個原因是LDL顆粒富含膽固醇酯。這種情況則會伴有LDL膽固醇與Apo B比例增加。多數輕度高膽固醇血癥者,其LDL-C/Apo B比例(1.62)均高於臨界高膽固醇血癥者(1.42)。引起LDL顆粒富含膽固醇酯的機制尚不清楚,很可能與下列影響LDL膽固醇酯含量諸因素有關:①卵磷脂膽固醇酰基轉移酶;②膽固醇酯轉移蛋白的活性;③LDL在血循環中生存時間;④新分泌的脂蛋白膽固醇的含量。在大多數情況下,LDL顆粒雖富含膽固醇酯,但LDL-Apo B水平則正常。所以,LDL顆粒富含膽固醇酯可能是因膽固醇代謝的某一階段有障礙所致。以往對於LDL顆粒富含膽固醇酯所致的輕度高膽固醇血癥尚未引起重視。然而這種情況在西方人羣的輕度高膽固醇血癥者中又是較常見的原因。
9.3 重度高膽固醇血癥的原因
重度高膽固醇血癥是指血漿膽固醇濃度超過7.51mmol/L(290mg/dl)或LDL-C>5.44mmol/L(210mg/dl)。重度高膽固醇血癥的最好例子是雜合子型家族性高膽固醇血癥(FH)。在一般人羣中,雜合子型FH的發病率爲1/500,而重度高膽固醇血癥在成人中則爲5/100。顯然,許多重度高膽固醇血癥是由於其他基因異常所致。
在絕大多數情況下,重度高膽固醇血癥是下列多種因素共同所致:LDL分解代謝減低,LDL產生增加,LDL-Apo B代謝缺陷,LDL顆粒富含膽固醇酯。另外還有上述引起臨界高膽固醇血癥的原因。由此可見,大多數重度高膽固醇血癥很可能是多基因缺陷與環境因素的相互作用所致。
9.4 高三酰甘油血癥的病因
血漿中乳糜微粒(CM)的三酰甘油含量達90%左右,極低密度脂蛋白(VLDL)中三酰甘油含量也達60%~65%,因而這兩類脂蛋白統稱爲富含三酰甘油的脂蛋白。也就是說,血漿三酰甘油濃度升高實際上是反映了CM和(或)VLDL濃度升高。凡引起血漿中CM和(或)VLDL升高的原因均可導致高三酰甘油血癥。
9.4.1 (1)繼發性高三酰甘油血癥
許多代謝性疾病、某些疾病狀態、激素和藥物等都可引起高三酰甘油血癥,這種情況一般稱爲繼發性高三酰甘油血癥。
9.4.2 (2)營養因素
許多營養因素均可引起血漿三酰甘油水平升高。大量攝入單糖亦可引起血漿三酰甘油水平升高,這可能與伴發的胰島素抵抗有關;也可能是由於單糖可改變VLDL的結構,而影響其清除速度。
飲食的結構也對血漿三酰甘油水平升高有影響。我國人羣的膳食是以高糖低脂爲特點。有調查表明,糖佔總熱量的76%~79%,脂肪僅佔8.4%~lO.6%,而高脂血症的發生率達11%。以內源性高三酰甘油血血漿爲最多見。有研究結果提示,進食糖量的比例過高,引起血糖升高,刺激胰島素分泌增加,出現高胰島素血癥。後者可促進肝臟合成三酰甘油和VLDL增加,因而引起血漿三酰甘油濃度升高。此外,高糖膳食還可誘發Apo CⅢ(載脂蛋白CⅢ)基因表達增加,使血漿Apo CⅢ濃度增高。已知Apo CⅢ是脂蛋白脂酶(LPL)的抑制因子,血漿中Apo CⅢ增高可造成LPL活性降低,繼而影響CM和VLDL中三酰甘油的水解,引起高三酰甘油血癥。
飲酒對血漿三酰甘油水平也有明顯影響。在敏感的個體,即使中等量飲酒亦可引起高三酰甘油血癥。酒精可增加體內脂質的合成率,減少氧化脂肪酸的比例,並增加酯化脂肪酸的比例。此外,酒精還可降低LPL的活性,而使三酰甘油分解代謝減慢。
9.4.3 (3)生活方式
習慣於靜坐的人血漿三酰甘油濃度比堅持體育鍛煉者要高。無論是長期或短期體育鍛煉均可降低血漿三酰甘油水平。鍛鍊尚可增高LPL活性,升高HDL-C(高密度脂蛋白膽固醇)水平特別是HDL2-C水平,並降低肝脂酶(HL)活性。長期堅持鍛鍊還可使外源性三酰甘油從血漿中清除增加。
吸菸也可增加血漿三酰甘油水平。流行病學研究證實,與正常人平均值相比較,吸菸可使血漿三酰甘油水平升高9.1%。然而戒菸後多數人有暫時性體重增加,這可能與脂肪組織中LPL活性短暫上升有關,此時應注意控制體重,以防體重增加而成三酰甘油濃度升高。
9.4.4 (4)基因異常所致血漿三酰甘油水平升高
①CM和VLDL裝配的基因異常:人類血漿Apo B包括兩種,即Apo B48和Apo Bl00,這兩種Apo B異構蛋白是通過Apo B mRNA的單一剪接機制合成。Apo B100出現在LDL中,通過肝臟以VLDL形式分泌。而Apo B48則在腸道中合成,並以CM的形式分泌。由於Apo B在剪接過程中有基因缺陷,造成CM和VLDL的裝配異常,由此而引致這兩種脂蛋白A的代謝異常。
②LPL和Apo CⅡ(載脂蛋白CⅡ)基因異常:血漿CM和VLDL中的三酰甘油有效地水解需要LPL和它的複合因子Apo C參與。LPL和Apo CⅡ的基因缺陷將導致三酰甘油水解障礙,因而引起嚴重的高三酰甘油血癥。部分Apo CⅡ缺陷患者可通過分析肝素化後LPL活性來證實。
③Apo E(載脂蛋白E)基因異常使含有Apo E的脂蛋白代謝障礙,這主要是指CM和VLDL。CM(乳糜微粒)的殘粒是通過Apo E與LDL受體相關蛋白結合而進行分解代謝,而VLDL則是通過Apo E與LDL受體結合而進行代謝。Apo E基因有3個常見的等位基因即EⅡ、EⅢ和EⅣ,Apo EⅡ是一種少見的變異,由於EⅡ與上述兩種受體的結合力都差,因而造成CM和VLDL殘粒的分解代謝障礙。所以Apo EⅡ等位基因攜帶者血漿中CM和VLDL殘粒濃度增加,因而常有高三酰甘油血癥。
10 發病機制
血脂是血漿中的中性脂肪(三酰甘油、膽固醇)和類脂(磷脂、糖脂、固醇、類固醇)的總稱,廣泛存在於人體中。它們是生命細胞的基礎代謝必需物質。三酰甘油和膽固醇都是疏水性物質,必須與血液中的特殊蛋白質和極性類脂(如磷脂)一起組成一個親水性的球狀巨分子,才能在血液中被運輸,並進入組織細胞。這種球狀巨分子複合物就是脂蛋白。血脂代謝就是指脂蛋白代謝。要了解高脂蛋白血癥的發生機制,首先需瞭解血漿脂蛋白的組成和來源、血漿脂蛋白的代謝以及血脂異常對動脈粥樣硬化的影響等。
10.1 血漿脂蛋白組成和來源
應用超速離心方法,可將血漿脂蛋白分爲五大類或六大類:乳糜微粒(CM)、極低密度脂蛋白(VLDL)、中間密度脂蛋白(IDL)、低密度脂蛋白(LDL)和高密度脂蛋白(HDL)。HDL又可再進一步分爲兩個亞組分即HDL2和HDL3。這5類脂蛋白的密度是依次增加,而顆粒則依次變小(表1)。此外,還有一種脂蛋白是後來發現的,稱作脂蛋白(a)[Lp(a)],它的密度雖然比LDL大,而其顆粒卻較LDL大。Lp(a)的化學結構與LDL很相似,僅多含1個載脂蛋白(a)。
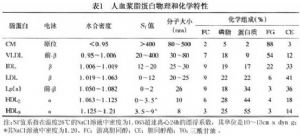
10.1.1 (1)乳糜微粒(CM)
CM來源於食物脂肪,顆粒最大,含外源性三酰甘油近90%,因而其密度最低。正常人空腹12h採血時,血漿中無CM。餐後以及某些病理狀態下血漿中含有大量的CM時,因其顆粒大能使光發生散射,血漿外觀混濁。將含有CM的血漿放在4℃靜置過夜,CM會自動漂浮到血漿表面,形成一層“奶酪”,這是檢查有無CM存在最簡單而又實用的方法。CM中的載脂蛋白(Apo)主要是Apo AI和C,其次是含有少量的Apo AⅡ、AⅣ、B48和E。
10.1.2 (2)極低密度脂蛋白(VLDL)
VLDL中三酰甘油含量仍然很豐富,佔一半以上。由於CM和VLDL中都是以三酰甘油爲主,所以這兩種脂蛋白統稱爲富含三酰甘油的脂蛋白。在無CM的血漿中,其三酰甘油的水平主要反映VLDL的多少。VLDL中的載脂蛋白含量近10%,其中40%~50%爲Apo C,30%~40%爲Apo B100,10%~15%爲Apo E。
10.1.3 (3)中間密度脂蛋白(IDL)
IDL是VLDL向LDL轉化過程中的中間產物,與VLDL相比,其膽固醇的含量已明顯增加,但仍屬於富含三酰甘油的脂蛋白類。正常情況下,血漿中IDL含量很低。目前有關IDL的認識仍不大一致,有人將其歸於VLDL,稱其爲VLDL的殘粒。但也有人認爲IDL是大顆粒的LDL,命名爲LDL1。最新的研究結果表明,IDL是一種有其自身特點的脂蛋白,應將其與VLDL和LDL區別開來。IDL中的載脂蛋白以Apo B100爲主,佔60%~80%,其次是Apo C(10%~20%)和Apo E(10%~15%)。
10.1.4 (4)低密度脂蛋白(LDL)
LDL是血漿中膽固醇含量最多的一種脂蛋白,其膽固醇的含量(包括膽固醇酯和遊離膽固醇)佔一半以上。所以,LDL被稱爲富含膽固醇的脂蛋白。血漿總膽固醇約70%是在LDL內,單純性高膽固醇血癥時,血漿膽固醇濃度的升高與血漿中LDL-膽固醇(LDL-C)水平是一致的。由於LDL顆粒小,即使血漿中LDL-C濃度很高,血漿也不會混濁。LDL中載脂蛋白幾乎全部爲Apo B100(佔95%以上),僅含有微量的ApoC和E。
10.1.5 (5)脂蛋白(a)[Lp(a)]
Lp(a)是1963年由Berg(北歐的一位遺傳學家)利用免疫方法發現的一種新的脂蛋白。Lp(a)的脂質成分類似於LDL,但其所含的載脂蛋白部分除一分子Apo B100外,還含有另一分子載脂蛋白即Apo(a),兩個載脂蛋白以二硫鍵共價結合。目前認爲Lp(a)是直接由肝臟產生的,不能轉化爲其他種類脂蛋白,是一類獨立的脂蛋白。
10.1.6 (6)高密度脂蛋白(HDL)
HDL顆粒最小,其結構特點是脂質和蛋白質部分幾乎各佔一半。HDL中的載脂蛋白以Apo AⅠ爲主,佔65%,其餘載脂蛋白爲Apo AⅡ(10%~23%)、Apo C(5%~15%)和Apo E(1%~3%),此外還有微量的Apo AⅣ。
HDL可進一步再分爲HDL2和HDL3兩個亞組分。HDL2顆粒大於HDL3,而其密度則小於HDL3。兩者的化學結構差別是:HDL2中膽固醇酯的含量較多,而載脂蛋白的含量則相對較少。
10.2 脂蛋白代謝
一般說來,人體內血漿脂蛋白代謝可分爲外源性代謝途徑和內源性代謝途徑。外源性代謝途徑是指飲食攝入的膽固醇和三酰甘油在小腸中合成CM及其代謝過程;而內源性代謝途徑則是指由肝臟合成VLDL,後者轉變爲IDL和LDL,LDL被肝臟或其他器官代謝的過程。此外還有一個膽固醇逆轉運途徑,即HDL的代謝。
10.2.1 (1)外源性代謝途徑
乳糜微粒(CM)是在十二指腸和空腸的黏膜細胞內合成。小腸黏膜吸收部分被水解的食物中所含三酰甘油、磷脂、脂肪酸和膽固醇後,腸壁細胞能將這些脂質再酯化,合成自身的三酰甘油和膽固醇酯;此外,腸壁細胞還能合成Apo B48和Apo AⅠ;在高爾基體內脂質和載脂蛋白組裝成乳糜微粒,然後分泌入腸淋巴液。原始的CM不含有Apo C,由Apo B48、Apo AⅠ和Apo AⅡ與極性遊離膽固醇、磷脂組成單分子層外殼,包住非極性脂質核心。在淋巴液中原始CM接受來自於HDL的Apo E和Apo C後逐漸變爲成熟,然後經由胸導管進入血液循環。
因爲Apo CⅡ是LPL的輔酶,CM獲得Apo CⅡ後,則可使LPL激活。CM的分解代謝是發生在肝外組織的毛細血管牀,在此處脂蛋白脂酶(LPL)水解CM中的三酰甘油,釋放出遊離脂肪酸。從CM中水解所產生的脂肪酸被細胞利用,產生能量或以能量的形式儲存。在脂解的過程中,CM所含Apo AⅠ和Apo C大量地轉移到HDL,其殘餘顆粒即CM殘粒則存留在血液中。這時CM顆粒明顯變小,三酰甘油含量顯著減少,而膽固醇酯則相對豐富。CM殘粒是由肝臟中的LDL受體和Apo E受體分解代謝。CM殘粒被吞飲入細胞後,其核心成分和Apo B在溶酶體內降解,爲肝細胞提供脂質原料,而其他載脂蛋白則可被再利用。CM在血液循環中很快被清除,半衰期<1h。由於Apo B48始終存在於CM中,所以Apo B48可視爲CM及其殘粒的標誌,這可與肝臟來源的VLDL(含Apo B100)相區別。
10.2.2 (2)內源性代謝途徑
①極低密度脂蛋白(VLDL)代謝:VLDL是由肝臟合成,其主要脂類爲肝臟合成的三酰甘油。脂質原料來源於吸收的CM以及糖類物質在肝臟中的轉化和脂肪組織動員出來的遊離脂肪酸、甘油。VLDL中的膽固醇除來自CM殘粒外,肝臟自身亦合成一部分。VLDL的Apo B100全部在肝臟內合成。VLDL的合成大體上可分爲兩個主要的步驟:第1步是VLDL前體合成,第2步是VLDL前體轉化爲成熟的VLDL。現在認爲VLDL前體的合成受微粒體三酰甘油轉運蛋白(MTP)的調節,故有關MTP的基因變異是目前血脂代謝基礎研究的熱點。有研究報告MTP抑制劑具有強效的降脂作用,對膽固醇和三酰甘油的降低作用可能大於他汀類藥物,並很可能還具有降低Lp(a)作用。
VLDL剛分泌進入血液循環時,含有極少量的膽固醇酯,而大量的膽固醇酯則來源於HDL,這是由於血液中存在有膽固醇酯轉移蛋白(CETP),後者的生理功能是將HDL中膽固醇酯轉移到其他類脂蛋白(主要是VLDL)。
源性三酰甘油是在肝臟中合成的,其最重要的底物是遊離脂肪酸。流經肝臟的血液中游離脂肪酸含量增加或肝臟自身合成的遊離脂肪酸增加,都可加速肝臟合成和分解VLDL。
VLDL分解代謝的初始階段類似於CM,即從HDL中獲Apo CⅡ後,大量的三酰甘油被存在於周圍組織毛細血管牀中的LPL水解,釋放出遊離脂肪酸,VLDL顆粒逐漸縮小,Apo C和Apo E又轉移到HDL顆粒中去。Apo B100保留在VLDL顆粒中,殘留在血液中的顆粒稱爲VLDL殘粒(亦有人稱之爲IDL)。
②中間密度脂蛋白(IDL)代謝:IDL是由VLDL轉變而來。IDL在體內的分解代謝迅速,因此正常情況下血漿中IDL濃度很低。大約1/2的IDL被LDL受體直接分解代謝。由於IDL含有豐富的Apo E,而LDL受體對Apo E的親和力遠大於Apo B100,所以IDL是因Apo E與LDL受體相結合而被肝臟攝取,分解代謝釋放出脂質。另1/2的IDL則轉變爲LDL,這一過程需要有肝脂酶(HL)和Apo E的參與,但其確切機制尚不十分清楚。
③低密度脂蛋白(LDL)代謝:LDL是由IDL轉化而來,但新近的研究結果提示,肝臟可直接合成分泌少量LDL。一般認爲,大多數LDL是由肝臟內和肝外的LDL受體進行代謝,佔體內LDL代謝的70%~75%,其餘的LDL則經由非特異性、非受體依賴性的途徑進行代謝。LDL與受體結合後,LDL顆粒被吞飲,然後進入溶酶體。在溶酶體中,LDL被水解並釋放出遊離膽固醇。遊離膽固醇可滲入細胞漿膜中,被細胞膜所利用或轉換成其他物質。而LDL受體則可再循環。在這個過程中,LDL向細胞提供膽固醇,同時又受到多方面的調節,其中最主要的是LDL受體的調節。
LDL受體的活性是決定LDL分解代謝速率的重要因素。細胞內遊離膽固醇的含量可調節LDL受體的合成和表達。細胞內遊離膽固醇含量增加則抑制LDL受體的合成和表達,反之亦然。
有人認爲人體內的LDL至少由兩個亞組分組成。而且這兩個亞組分LDL的分解速度和代謝途徑均不相同。其中一亞組分LDL迅速地被分解代謝,這是由受體途徑進行的;而另一亞組分則在體內清除緩慢,因爲是經由非受體的途徑。
LDL是所有血漿脂蛋白中首要的致動脈粥樣硬化性脂蛋白。已經證明粥樣硬化斑塊中的膽固醇來自血液循環中的LDL。LDL的致動脈粥樣硬化作用與其本身的一些特點有關,即LDL相對較小,能很快穿過動脈內膜層。近來的研究發現,經過氧化或其他化學修飾後的LDL,具有更強的致動脈粥樣硬化作用。由於小而緻密的LDL(sLDL)顆粒易被氧化,所以較大顆粒LDL更具有致動脈粥樣硬化作用。
人體內膽固醇可來源於食物,亦可由肝臟合成。內源性肝臟合成膽固醇是一個複雜的過程。膽固醇合成開始於乙酰輔酶A,三分子乙酰輔酶A合成一分子β-羥基β-甲基戎二酸輔酶A(HMG CoA),然後合成甲羥戊酸,繼而合成鯊烯,最後合成膽固醇。在這個過程中,HMG CoA還原酶是一個關鍵的限速酶。
10.2.3 (3)高密度脂蛋白(HDL)代謝——膽固醇“逆轉運”途徑
HDL主要是由肝臟和小腸合成。新生的HDL呈碟形,由磷脂、遊離膽固醇和載脂蛋白組成,其中的Apo AⅡ含量較Apo AⅠ多。
HDL轉運肝外組織細胞中的膽固醇,第一步是與細胞表面結合,這個過程可能是由HDL受體介導。與LDL不同,HDL與其受體結合後,並不被細胞吞飲入胞內。當HDL與其受體結合時,可產生一種信號,這種信號則誘導細胞內的遊離膽固醇向細胞表面轉移,最後進入HDL。從細胞來的遊離膽固醇,在卵磷脂膽固醇酰基轉移酶(LCAT)的作用下酯化成膽固醇酯。膽固醇酯則向HDL中心核轉移,以使LCAT作用的活性部位能進一步接受遊離膽固醇。新生HDL在接受大量的膽固醇後則變爲成熟的HDL,這時HDL的形狀也由碟形變成球形。由於LCAT酯化膽固醇幾乎發生在瞬間,因此正常人血液中幾乎難以發現新生的碟形HDL。
成熟的球形HDL可分爲HDL2和HDL3。從新生的HDL顆粒形成的球形HDL是HDL3,其密度高,膽固醇含量相對較少。隨着膽固醇酯的進一步滲入,使HDL的密度降低而形成HDL2。HDL在成熟的過程中除了獲得膽固醇酯外,還獲得一些其他成分,包括Apo AⅠ、Apo C、三酰甘油和磷脂等。
HDL除了參與膽固醇的逆轉運外,還爲其他脂蛋白提供多種必需成分。例如,HDL將Apo E和Apo CⅡ提供給CM和VLDL,以促進CM和VLDL的分解代謝。此外,HDL還是Apo AⅠ的儲存庫。
由於HDL參與膽固醇的“逆轉運”,被認爲具有抗動脈粥樣硬化作用。有研究觀察到HDL3以內的Apo AⅠ能刺激磷脂酰膽鹼降解,因而誘導細胞內膽固醇流出。另有動物試驗證實肝細胞膜上有B類Ⅰ型清道夫受體(SR-BⅠ),是一種高親和力的HDL受體,該受體能選擇性清除HDL中的氧化性膽固醇酯,在膽固醇的“逆轉運”中起重要作用。
HDL的抗動脈粥樣硬化作用可能是由於它能將周圍組織包括動脈壁內的膽固醇轉運到肝臟進行代謝有關。最近有人發現,HDL還具有抗LDL氧化的作用,並能促進損傷內皮細胞的修復,還能穩定前列環素的活性。曾認爲在臨牀上測定HDL2亞類濃度對預測冠心病的價值較大,其敏感性約比總HDL-C高1.5倍。但新近的研究表明,測定HDL3亞類濃度對預測冠心病具有同樣的價值,並可能大於HDL2亞組分的測定。也有人提出依HDL顆粒所含載脂蛋白而分亞類:含有Apo AI的爲Lp AⅠ;含有Apo AI和Apo AⅡ的爲Lp AⅠ∶AⅡ。但由於該亞類的檢測方法複雜,難以在臨牀上推廣應用,同時該亞類分類法的臨牀意義也不十分明確。
10.3 載脂蛋白結構與功能
載脂蛋白是一類能與血漿脂質(主要是指膽固醇、三酰甘油和磷脂)結合的蛋白質,爲構成血漿脂蛋白的主要成分。在體內載脂蛋白具有許多重要的生理功能,如作爲配基與脂蛋白受體結合、激活多種脂蛋白代謝酶等。現已認識到載脂蛋白不僅對血漿脂蛋白的代謝起着決定性的作用,而且對動脈粥樣硬化的發生和發展亦有很大的影響。目前已報道的載脂蛋白有20餘種(表2),而臨牀意義較爲重要且認識比較清楚的有Apo AⅠ、Apo AⅡ、ApoⅣ、Apo B、Apo CⅡ、Apo CⅢ、Apo E和Apo(a)。此外還有一種蛋白質稱爲膽固醇酯轉移蛋白(CETP),與血漿脂蛋白代謝的關係非常密切,亦屬於載脂蛋白之列。
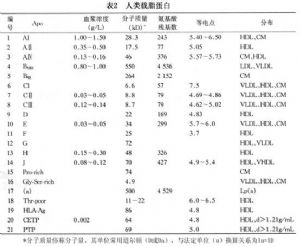
10.3.1 (1)載脂蛋白AⅠ(Apo AⅠ)
ApoAⅠ主要分佈於血漿CM、HDL2和HDL3中,約佔這3類脂蛋白中蛋白含量的33%、65%和62%。正常情況下血漿中Apo AⅠ濃度爲1.00~1.50g/L。成熟的人Apo AⅠ分子質量爲28.3kD,其分子爲單一的多肽鏈。Apo AⅠ主要由小腸和肝髒合成。
Apo AⅠ的生理功能:①是CM、HDL的結構蛋白;②作爲一種輔助因子,參與激活LCAT,使遊離膽固醇酯化;③參與膽固醇的逆轉運過程。
Apo AⅠ的基因缺陷可引起Tangier病,該病的特點是血漿中Apo AⅠ缺乏或明顯減少,常伴有嚴重的低HDL-C血癥。
10.3.2 (2)載脂蛋白AⅡ(Apo AⅡ)
Apo AⅡ是人HDL顆粒中第2種主要的載脂蛋白,約佔HDL中蛋白質總量的20%;在HDL2中佔15%,而在HDL3中佔25%。在乳糜微粒中它的含量可達總載脂蛋白的7%~10%。在VLDL中也有少量Apo AⅡ存在。血漿中Apo AⅡ的濃度爲0.35~0.50g/L。Apo AⅡ是由2條各含77個氨基酸的肽鏈組成,分子質量爲17kD。
Apo AⅡ的生理功能尚不十分清楚,除了作爲HDL的結構成分外,可能還具有抑制LCAT活性的作用。亦有人認爲,Apo AⅡ是肝脂酶(HL)的激活因子。
10.3.3 (3)載脂蛋白AⅣ(Apo AⅣ)
Apo AⅣ是一種酸性糖蛋白,分子質量46kD。Apo AⅣ是CM、VLDL和HDL的組成成分。健康人空腹血漿Apo AⅣ濃度平均值爲0.13~0.16g/L,但也有報道高達0.37g/L。血漿中Apo AⅣ至少以3種方式存在:①與Apo AⅠ和少量的Apo E一起組成HDL;②作爲單一的載脂蛋白構成HDL;③與少量的膽固醇和磷脂結合,以遊離狀態存在於脂蛋白缺乏的血漿中。
Apo AⅣ的功能:①激活卵磷脂膽固醇酰基移換酶(LCAT);②參與膽固醇逆轉運;③輔助激活LPL;④調節食慾。
10.3.4 (4)載脂蛋白B(Apo B)
Apo B是一類在分子質量、免疫性和代謝上具有多態性的蛋白質,依其分子質量及所佔百分比可分爲B100、B48、B74、B26及少量B50。在正常情況下,以Apo Bl00、Apo B48較爲重要。Apo B100主要分佈於血漿VLDL、IDL和LDL中,佔這3類脂蛋白中蛋白含量的25%、60%、95%。而Apo B48則分佈於CM中,佔其蛋白含量的5%。正常情況下Apo B濃度爲0.80~1.00g/L。
Apo B具有如下功能:①參與VLDL的合成、裝配和分泌;②Apo Bl00是肝臟合成和分泌富含三酰甘油的VLDL所必需的載脂蛋白;③與肝素及不同的糖蛋白結合,可能參與LDL與動脈粥樣斑塊結合;④Apo Bl00是VLDL、IDL和LDL的結構蛋白,參與脂質轉運;⑤80%的LDL經受體途徑清除,Apo B100是介導LDL與相應受體結合必不可少的配體;⑥Apo B48爲CM合成和分泌所必需,參與外源性脂質的消化吸收和運輸。
10.3.5 (5)載脂蛋白CⅡ(Apo CⅡ)
Apo CⅡ是CM、VLDL和HDL的結構蛋白之一,分別佔其蛋白成分的14%、7%~10%及1%~3%。Apo CⅡ在血漿中的濃度爲0.03~0.05g/L。人Apo CⅡ爲含79個氨基酸殘基的單鏈多肽,分子質量爲9.1kD。
Apo CⅡ具有下列生理功能:①是脂蛋白脂酶(LPL)不可缺少的激活劑;②Apo CⅡ還具有抑制肝臟對CM和VLDL攝取的作用;③可抑制HL的活性,抑制程度與Apo CⅡ濃度呈線性關係。②Apo CⅡ也能激活LCAT,但其作用遠弱於Apo AⅠ和Apo CⅠ等。
10.3.6 (6)載脂蛋白CⅢ(Apo CⅢ)
Apo CⅢ是一種水溶性低分子蛋白質,主要分佈於血漿HDL、VLDL和CM中。正常人血漿中Apo CⅢ的濃度爲0.12~0.14g/L,分別佔前述三類脂蛋白中的蛋白含量的2%、40%和36%。成熟的Apo CⅢ由79個氨基酸殘基組成,分子質量爲8.7kD。
Apo CⅢ的生理功能:①抑制LPL活性;②使HDL特別是HDL2的部分分解代謝率降低。HDL中Apo CⅢ含量增加,可使肝臟對HDL的清除減慢,反之,HDL中Apo CⅢ含量減少則可造成HDL的清除加快。
10.3.7 (7)載脂蛋白E(Apo E)
Apo E是一個含有299個氨基酸結合有磷脂的糖蛋白,其分子質量爲34kD。Apo E可以在各種組織中合成,但以肝臟爲主。正常人血漿Apo E濃度爲0.03~0.05g/L。Apo E的濃度與血漿三酰甘油含量呈正相關。
Apo E的一級結構是一條單多肽鏈,其全部的氨基酸組成順序已經被Apo E mRNA的cD-NA分析所證實。其氨基酸組成上含有10%~12%的精氨酸(按其氨基酸摩爾計算),故曾稱爲富含精氨酸載脂蛋白。Apo E是一個多態性蛋白,有3個常見的異構體,即EⅡ、EⅢ和EⅣ。各種Apo E異構體的主要區別是氨基酸一級結構的不同,這涉及半胱氨酸(Cys)和精氨酸(Arg)的交換:EⅢ含一個Cys(第112位);EⅣ不含Cys,但比EⅢ多一個Arg(第112位);EⅡ含2個Cys,但比EⅢ少一個Arg(第158位)。Apo E的二級結構中含有較多的a-螺旋,這種結構在去垢劑或脂類環境中僅有極微小的改變,是比較穩定的。Apo E除具有與LDL受體結合的能力外,還可以與Apo E受體結合。Apo E受體只能與ApoE結合,它只存在於肝臟中。
Apo E的生理功能:①組成脂蛋白,是CM、VLDL、IDL和部分HDL的結構蛋白;②作爲配體與LDL受體和Apo E受體結合;③具有某種免疫調節作用;④參與神經細胞的修復。
Apo E基因突變可引起許多Apo E的異構體,目前已報道的有近20種,其中多數可伴隨有高脂蛋白血癥。
10.3.8 (8)載脂蛋白(a)[Apo(a)]
Apo(a)是構成Lp(a)的重要蛋白質。Lp(a)是一獨立存在的脂蛋白系統,其脂質成分和LDL極爲相似,而其蛋白質部分由Apo B100和一富含神經氨酸的糖蛋白即Apo(a)組成,在完整Lp(a)顆粒中二者以雙硫鍵共價相連,其比例因人而異,可爲2∶1,1∶2或1∶1。標準的Lp(a)顆粒中含有一分子質量約645kD的Apo(a)分子。Apo(a)是一高度糖化的蛋白質,其糖的含量較高,約爲Apo B的6倍。Apo(a)約佔Lp(a)蛋白組分的20%左右。1987年CeLean等首先應用分子生物學技術檢測Apo(a)的一級分子結構,發現其分子質量爲503kD,含有27個Kingle結構,約4529個氨基酸。進一步研究證明,Apo(a)與血漿纖溶纖溶酶纖溶酶原約80%左右有同源性,兩者在染色體上的基因位點十分接近,均位於第6號染色體長臂上。基因位點的相近導致了二者的結構十分相似,現已證明,Apo(a)分子由3個結構域組成:疏水性信號肽、KringleⅡ(可以15~37重複製)和KringleⅣ。
Apo(a)的生理功能目前尚不十分清楚,但已有許多研究均提示血漿中Lp(a)水平升高是冠心病的獨立危險因素。
10.3.9 (9)膽固醇酯轉移蛋白
20世紀70年代中期有人發現,血漿無脂蛋白部分含有一種特殊的轉運蛋白,能促進血漿各脂蛋白間膽固醇酯、三酰甘油和磷脂的單向或雙向轉運和交換,這類特殊轉運蛋白稱脂質轉運蛋白(LTP)。LTP包括3種成分:膽固醇酯轉移蛋白(CETP)、磷脂轉運蛋白(PTP)和三酰甘油轉運蛋白(TTP)。也有人根據這類蛋白質對熱穩定性的不同將其分爲兩種:LTP1(熱穩定性)和LTP2(熱不穩定性)。
CETP系一疏水糖蛋白,分子質量約爲74kD。用固相競爭放射免疫法測定,正常人羣中男性血漿CETP水平爲(1.50±0.26)mg/L[(1.50±0.26)µg/ml],女性爲(1.92±0.52)mg/L[(1.92±0.52)µg/ml]。1987年有人從克隆CETP的cDNA測定了CETP的完整一級結構,爲17個氨基酸組成的信號肽和476個氨基酸組成的單條多肽鏈,含有豐富的非極性氨基酸。與其他的載脂蛋白相比,含有更多的疏水氨基酸(44%),另外還散在分佈着4個潛在的天冬酰胺相連的糖基化部位。研究表明,CETP分子中疏水基的相互作用對維持其結構起重要作用,而糖基化對CETP的活性形式的形成是必需的。
CETP的主要生理功能是:①介導HDL中的膽固醇酯與VLDL中的三酰甘油等量交換,亦促進HDL中的膽固醇淨轉運;同時在HDL顆粒之間的膽固醇酯轉運中也起作用;②促進脂固醇酯在細胞與血漿脂蛋白間的轉運,參與膽固醇的逆轉運過程。
有關CETP與動脈粥樣硬化的關係尚不明確。有研究提示,純合子CETP缺乏症者罹患冠心病的危險性降低。
10.4 血脂異常引起動脈粥樣硬化的發生機制
10.4.1 (1)脂質浸潤學說
儘管動脈粥樣硬化的發病機制還不十分清楚,但脂質浸潤學說是比較早得到公認的學說之一。它認爲動脈粥樣硬化病變主要是因血漿脂質水平升高所引起。由於血漿脂質水平升高促使大量脂質尤其是膽固醇進入動脈壁,並在局部沉積聚集,引起局部巨噬細胞和平滑肌細胞集結,這些細胞吞噬脂質後形成泡沫細胞;同時細胞合成間質增多,血管內膜增厚,導致動脈粥樣硬化病變形成。
脂質浸潤學說具有比較堅實的科學依據,得到了大部分學者的認同。後續的許多研究資料也進一步支持此說:①血脂水平與動脈粥樣硬化發病率呈正相關,降低血漿膽固醇濃度可明顯降低冠狀動脈粥樣硬化發病率和嚴重程度。②放射性核素標記實驗證實動脈壁內的脂質來自血液。③動脈粥樣斑塊內存在大量脂質,尤其是膽固醇酯,泡沫細胞中堆積的也主要是膽固醇酯。④高脂、高膽固醇飼料餵養動物均可引發類似人類動脈粥樣硬化的病變。⑤家族性高膽固醇血癥患者僅僅由於細胞表面低密度脂蛋白受體功能缺陷,導致血漿膽固醇水平極度升高,就使患者早年發生動脈粥樣硬化,有力地證明高脂血症在動脈粥樣硬化發生中的重要地位。此外,大量流行病學調查均已證實血漿膽固醇水平的升高與冠心病的發生之間的密切關係。
有關血漿脂質侵入動脈壁的機制,許多學者應用免疫組織化學、定量免疫電泳、核素標記等技術的研究取得了重要結果,對血脂跨越內皮進入內膜的具體途徑有了較深入的認識。目前一般認爲脂蛋白浸潤入動脈內膜主要有兩條途徑。一是血漿脂質隨同血漿其他成分一起非選擇性地浸入動脈壁,這個過程實際上就是通過細胞間隙的超濾作用,多數學者認爲這是血漿脂蛋白進入動脈壁的主要途徑;二是血漿中脂質由內皮細胞血管腔面的胞膜小泡攝取,通過穿胞作用進入內皮下間隙,有學者認爲這種穿胞作用可能是LDL通過動脈內皮細胞的主要途徑。
10.4.2 (2)血漿脂質成分對動脈粥樣硬化的作用特點
與動脈粥樣硬化發生過程相關的血漿脂質成分主要是低密度脂蛋白(LDL)、脂蛋白(a)、三酰甘油(TG)和高密度脂蛋白(HDL)。
10.4.2.1 ①LDL
LDL是最早確定的獨立危險因素,大量證據表明血漿LDL水平升高與動脈粥樣硬化發生之間的因果關係。但由於經LDL受體進入細胞的LDL水解後產生的遊離膽固醇可引起負反饋調節,所以LDL本身並不會導致細胞內的膽固醇積聚;而滯留於內皮下的LDL經過細胞氧化修飾形成氧化低密度脂蛋白(oxLDL),之後oxLDL可通過細胞膜上的清道夫受體介導進入細胞,由於經過清道夫受體途徑攝入胞內的膽固醇缺乏負反饋調節機制,促使oxLDL不斷攝入胞內造成脂質大量積聚,導致泡沫細胞形成。
10.4.2.2 ②Lp(a)
經過長時間的研究探討,已經確定Lp(a)是動脈粥樣硬化的一個獨立危險因素,還是冠心病的重要預報因子。Lp(a)致動脈粥樣硬化的機制比較複雜,可能與下述過程有關:Lp(a)化學修飾之後可通過清道夫受體介導大量進入巨噬細胞,促使泡沫細胞形成;Lp(a)與鈣離子或多聚葡胺結合後很容易在動脈壁和其他組織中沉積;沉積於受損傷的血管內皮細胞下的Lp(a)還可促進血管平滑肌細胞的增殖。
10.4.2.3 ③HDL
HDL具有防止動脈內膜脂質堆積,抑制動脈粥樣硬化病變形成的作用。流行病學研究已經證實血漿HDL水平與動脈粥樣硬化心血管病的發病率呈負相關,血漿HDL減少是動脈粥樣硬化發生的危險因素之一;提高血漿HDL水平可以減少膽固醇在血管壁的沉積,縮小斑塊脂質並且可以阻止脆性斑塊的形成。HDL的抗動脈粥樣硬化作用主要與其促進膽固醇逆轉運以清除動脈壁多餘的膽固醇有關。
10.4.2.4 ④三酰甘油
經過近30年的研究,1999年在希臘雅典召開的第71屆歐洲動脈粥樣硬化年會上總結評價三酰甘油與動脈粥樣硬化的關係,證實了富含三酰甘油的脂蛋白(TRLs)與冠狀動脈狹窄程度呈顯著正相關,確定TRLs在動脈粥樣硬化病變進展中的重要作用。2003年國際動脈粥樣硬化學會(LAs)發佈的《動脈粥樣硬化性心血管病預防綜合指南》也將血漿三酰甘油水平升高列爲冠心病的獨立危險因素。目前除集中研究TRLs在動脈粥樣硬化病變發生過程中的直接作用之外,更引人注目的是對高三酰甘油血癥所伴隨的各種異常狀態在動脈粥樣硬化發病過程影響的研究。
儘管動脈粥樣硬化的脂質浸潤學說得到很多研究結果的支持和多數學者的認同,並且對動脈粥樣硬化性心血管病的預防和診治具有指導意義,但是如果只重視血脂而忽略血管壁那就不是完全的學說。事實上,動脈粥樣硬化病變好發的部位和分佈的特點不是該學說所能圓滿解釋的,並且臨牀研究也顯示冠心病病變的嚴重程度與血脂水平之間也缺乏平行關係等,這些都有待繼續研究完善。
11 高脂蛋白血癥的臨牀表現
高脂血症的臨牀表現主要包括兩大方面:一方面是脂質在真皮內沉積所引起的黃色瘤;另一方面脂質在血管內皮沉積所引起的動脈粥樣硬化,產生冠心病和外周血管病等。由於高脂血症時黃色瘤的發生率並不十分高,動脈粥樣硬化的發生和發展則需要相當長的時間,所以多數高脂血症患者並無任何症狀和異常體徵發現。而患者的高脂血症則常常是在進行血液生化檢驗(測定血膽固醇和三酰甘油)時被發現的。
11.1 血液生化檢驗
臨牀測定血漿(清)總膽固醇(TC)、三酰甘油(TG)和低密度脂蛋白膽固醇(LDL)濃度升高,高密度脂蛋白膽固醇(HCL)低下。
11.2 脂質在全身的沉積表現
11.2.1 (1)黃色瘤(xanthoma)
黃色瘤是一種異常的侷限性皮膚隆凸起,其顏色可爲黃色、橘黃色或棕紅色,多呈結節、斑塊或丘疹形狀,質地一般柔軟。主要是由於真皮內集聚了吞噬脂質的巨噬細胞(泡沫細胞)又名黃色瘤細胞所致。根據黃色瘤的形態、發生部位,一般可分爲下列6種:
①肌腱黃色瘤(tendon xanthoma):是一種特殊類型的結節狀黃色瘤,發生在肌腱部位,常見於跟腱、手或足背伸側肌腱、膝部股直肌和肩三角肌腱等處。爲圓或卵圓形質硬皮下結節,與其上皮膚粘連,邊界清楚。這種黃色瘤常是家族性高膽固醇血癥的較爲特徵性的表現。
②掌皺紋黃色瘤(palmar creases xanthoma):是一種發生在手掌部的線條狀扁平黃色瘤,呈橘黃色輕度凸起,分佈於手掌及手指間皺褶處。此種黃色瘤對診斷家族性異常β-脂蛋白血症有一定的價值。
③結節性黃色瘤(tuberous xanthoma):發展緩慢,好發於身體的伸側,如肘、膝、指節伸處以及髖、踝、臀等部位。爲圓形狀結節,其大小不一,邊界清楚。早期質地較柔軟,後期由於纖維化,質地變硬。此種黃色瘤主要見於家族性異常β-脂蛋白血症或家族性高膽固醇血癥。
④結節疹性黃色瘤(tuberous eruptive xanthoma):好發於肘部四肢伸側和臀部,皮損常在短期內成批出現。呈結節狀有融合趨勢,疹狀黃色瘤常包繞着結節狀黃色瘤。瘤的皮膚呈橘黃色,常伴有炎性基底。這種黃色瘤主要見於家族性異常β-脂蛋白血症。
⑤疹性黃色瘤(eruptive xanthoma):表現爲針頭或火柴頭大小丘疹,橘黃或棕黃色伴有炎性基底。有時口腔黏膜也可受累。主要見於高三酰甘油血癥。
⑥扁平黃色瘤(xanthelasma):見於瞼周,又有瞼黃色瘤之稱,是較爲常見的一種黃色瘤。表現爲眼瞼周圍處發生橘黃色略高出皮面的扁平丘疹狀或片狀瘤,邊界清楚,質地柔軟。泛發可波及面、頸、軀幹和肢體,爲扁平淡黃色或棕黃色丘疹,幾毫米至數釐米大小。此種黃色瘤常見於各種高脂血症,但也可見於血脂正常者。
上述不同形態的黃色瘤可見於不同類型的高脂血症,而在同一類型的高脂血症者又可出現多種形態的黃色瘤。經有效的降脂治療,多數黃色瘤可逐漸消退。
11.2.2 (2)脂性角膜弓
角膜弓(cornealarcus)又稱老年環,若見於40歲以下者,則多伴有高脂血症,以家族性高膽固醇血癥爲多見,但特異性並不很強。
11.2.3 (3)高脂血症眼底(retinal lipemia)改變
高脂血症眼底改變是由於富含三酰甘油的大顆粒脂蛋白沉積在眼底小動脈上引起光散射所致,常常是嚴重的高三酰甘油血癥並伴有乳糜微粒血癥的特徵表現。
此外,嚴重的高膽固醇血癥尤其是純合子家族性高膽固醇血癥可出現遊走性多關節炎,不過這種情況較爲罕見,且關節炎多爲自限性。
11.3 動脈粥樣硬化病變
11.3.1 (1)主動脈粥樣硬化
病變多見於主動脈後壁和其分支開口處,以腹主動脈最重,胸主動脈次之,升主動脈最輕,前述的各種病變均可見到。與梅毒性主動脈炎的動脈瘤相反,主動脈AS的動脈瘤主要見於腹主動脈,可於腹部觸及搏動性的腫塊,聽到雜音,並可因其破裂發生致命性大出血。由於主動脈壁彈性降低,患者的收縮壓升高,脈壓增寬,橈動脈觸診可類似促脈。
11.3.2 (2)冠狀動脈粥樣硬化
參見冠心病。
11.3.3 (3)頸動脈及腦動脈粥樣硬化
病變最常見於頸內動脈起始部、基底動脈、大腦中動脈和Willis環。纖維斑塊和粥樣斑塊常導致管腔狹窄,並可因復合病變而加重狹窄甚至形成閉塞。動脈瘤多見於Willis環部。長期供血不足可致腦實質萎縮,表現爲腦回變窄,皮質變薄,腦溝變寬變深,腦重量減輕。患者可有智力及記憶力減退,精神變態,甚至癡呆。急速的供血中斷可致腦梗死(腦軟化)。動脈及小的動脈瘤破裂可引起腦出血及相應的臨牀表現。
11.3.4 (4)腎動脈粥樣硬化
病變最常累及腎動脈開口處及其主幹近側端,亦可累及葉間動脈和弓形動脈。常因斑塊所致之管腔狹窄而引起頑固性腎血管性高血壓;亦可因斑塊合併血栓形成致腎組織梗死,引起腎區疼痛、無尿及發熱。梗死竈機化後遺留較大瘢痕,多個瘢痕可致腎臟縮小,稱爲AS性固縮腎。
11.3.5 (5)四肢動脈粥樣硬化
病變以下肢動脈爲重。當較大動脈管腔明顯狹窄時,可因供血不足致耗氧量增加時(如行走)可引起疼痛,休息後好轉,再走時再次出現劇痛,即所謂間歇性跛行。當動脈管腔完全阻塞側支循環又不能代償時,引起足趾部乾性壞疽。
11.3.6 (6)腸繫膜動脈粥樣硬化
13 實驗室檢查
13.1 血脂檢查的項目
血清TC、血清HDL-C、血清TG、血清LDL-C增高[用Friedewald公式計算:LDL-C(mmol/L)=TC-HDL-C-TG/2.2或LDL-C(mg/dl)=TC-HD L-C-TG/5但限於TG<4.5mmol/L,TG>4.5mmol/L時須用直接檢測法]。
13.2 複查
如首次檢測發現異常則宜複查禁食12~14h後的血脂水平,1~2周內血清膽固醇水平可有10%的變異,實驗室的變異容許在3%以內,在判斷是否存在高脂血症或決定防治措施之前,至少應有2次血標本檢查的記錄。
14 高脂蛋白血癥的診斷
血脂高於正常人上限即爲高脂血症。有多種分類方法,主要有4種。
14.1 高脂血症的分類
14.1.1 (1)高脂蛋白血癥表型分類
目前國際上通用的是以Fredrickson工作爲基礎經WHO修訂的分類系統,主要是基於各種血漿脂蛋白升高的程度不同而進行分型。該分類法不包括病因學,故稱爲表型分類。高脂蛋白血癥可分爲5型(連亞型在內,可分6型)(表3)。
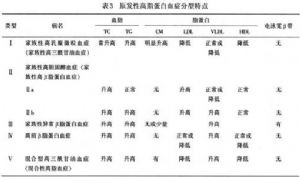
14.1.2 (2)臨牀分類
14.1.3 (3)病因分類
②繼發性高脂血症:常見的病因爲糖尿病、甲狀腺功能低下、腎病綜合徵等。
(4)基因分類:隨着分子生物技術的發展,發現一部分高脂血症患者存在單一或多個遺傳基因的缺陷,多具有家族基因聚集性,有明顯的遺傳傾向,臨牀上稱爲家族性高脂血症(包含家族性高膽固醇血癥;家族性載脂蛋白B100缺陷症;家族性混合型高脂血症;家族性異常β-脂蛋白血症等)。
14.2 調脂對象的檢出
應接受血脂檢查的對象:美國國家膽固醇教育計劃(NCEP)成人治療組指南Ⅲ(ATPⅢ)中推薦在人羣中進行血脂譜篩查,包括空腹總TC、LDL-C、HDL-C、TG。我國由於人力物力的限制,採取人羣血脂普查有困難,以下作爲應接受血脂檢查的對象:
(3)有冠心病或動脈粥樣硬化家族史者,尤其是直系親屬中有早發病或早病死者。
(4)有黃瘤或黃疣者。
(5)有家族性高脂血症者。以下可考慮作爲接受血脂檢查的對象:①40歲以上男性;②絕經期後女性。
14.3 結果的判斷
目前國際尚無一個統一的正常值。我國人羣血脂水平TC、TG都較歐美人羣低,其正常值不同於歐美。現將中國血脂防治建議和美國膽固醇教育計劃委員會成人治療組(ATP)所制定的高脂血症診斷標準分別列於表4和表5。


14.4 應接受調脂治療的人羣
(2)根據高脂血症發生的原因可分爲原發性高脂血症和繼發性高脂血症。繼發性高脂血症是指由於全身系統性疾病所引起的血脂異常,可引起血脂升高的系統性疾病有甲狀腺功能減退症、糖尿病、腎病綜合徵、腎功能衰竭、肝臟疾病、系統性紅斑狼瘡、糖原貯積症等。原發性高脂血症即未找到系統性疾病引起血脂異常,往往由於遺傳因素或後天環境因素,生活方式不良所致。這兩類血脂異常都需調脂,但繼發性血脂異常不僅需調脂而且需要治療原發病。
(3)冠心病及冠心病同等危險因素均是調脂治療重點對象。具有冠心病同等危險的情況稱爲冠心病等危症。有3種情況屬冠心病等危症:
①有其他臨牀表現的動脈粥樣硬化(周圍動脈疾病、腹主動脈瘤和症狀性頸動脈病等)。
②糖尿病。
③存在多項危險因素且預計10年冠心病危險性>20%。特別強調的是,ATPⅢ將糖尿病視爲冠心病等危症,要求對糖尿病如同對待冠心病一樣要進行強化降LDL-C治療。
15 鑑別診斷
15.1 家族性高膽固醇血癥(FH)
是一種常染色體顯性遺傳性疾病。本症的發病機制是細胞膜表面的LDL受體缺如或異常,導致體內LDL代謝異常,造成血漿總膽固醇(TC)水平和低密度脂蛋白-膽固醇(LDL-C)水平升高,臨牀上常有多部位黃色瘤和早發冠心病。
在男性雜合子型FH患者,30~40歲時可患有冠心病。男性預期23%患者在50歲以前死於冠心病,50%以上的男性患者在60歲時已有明顯的冠心病症狀。而在女性雜合子FH患者雖也易患冠心病,但發生冠心病的年齡較男性患者晚10年左右。
純合子FH患者是由於從其父母各遺傳獲得一個異常的LDL受體基因,患者體內無或幾乎無功能性的LDL受體,因而造成患者血漿膽固醇水平較正常人高出6~8倍。常較早發生動脈粥樣硬化,多在10歲時就出現冠心病的臨牀症狀和體徵,如得不到有效的治療,這些病人很難活到30歲。
常規診斷FH的實用方法是準確測定血漿膽固醇和三酰甘油濃度。如果爲單純性高膽固醇血癥,且血漿膽固醇濃度超過9.1mmol/L(350mg/dl),診斷FH幾乎無困難。若同時發現其他表現則更支持FH的診斷。這些表現包括病人或其第一級親屬中有肌腱黃色瘤,第一代親屬中有高膽固醇血癥者,患者家庭成員中有兒童期就被檢出有高膽固醇血癥者。對於雜合子FH,血漿膽固醇濃度6.5~9.1mmol/L(250~350mg/dl),若同時有上述其他特徵之一者,則可作出FH的診斷。
15.2 家族性載脂蛋白B100缺陷症
家族性載脂蛋白B100缺陷症(familial defective apolipoprotein B100,FDB)是由於Apo B100中3500位上的精氨酸(Arg)被谷酰胺(Gln)所置換(Arg3500→Gln),造成含有這種缺陷Apo B100的LDL與受體結合障礙。人類血漿中LDL顆粒僅含有一個分子Apo B100雜合子FDB者體內則應存在兩種LDL顆粒,即一種LDL顆粒含有正常的Apo B100,另一種LDL顆粒則含有突變的Apo B100。從FBD雜合子者血漿中分離出富含缺陷Apo B100的LDL與受體的親和力僅爲正常的10%。
現有資料尚不能確定FDB在一般人羣中的發生頻率,因爲已報道的FDB病例絕大多數是在對高膽固醇血癥患者進行研究時被發現的。在一般人羣中FDB的發生率估計爲1/700~1/500。
FDB患者的血脂異常改變似乎與雜合子FH者相類同,主要是血漿總膽固醇濃度和LDL膽固醇濃度中等或重度升高。
15.3 家族性混合型高脂血症
家族性混合型高脂血症(FCH)是於1973年首次被認識的一個獨立的病症。在60歲以下患有冠心病者中,這種類型的血脂異常最常見(佔11.3%)。在一般人羣中FCH的發生率爲1%~2%。另有研究表明,在40歲以上原因不明的缺血性腦卒中患者中,FCH爲最多見的血脂異常類型。
FCH的血脂異常特點是血漿膽固醇和三酰甘油均有升高,其生化異常類似於Ⅱb型高脂蛋白血癥。所以,曾有人將FCH與Ⅱb型高脂蛋白血癥相提並論。在作出FCH的診斷時,首先要注意排除繼發性高脂血症。
FCH最突出的特徵是,在同一家族中,發現有各種不同類型的高脂蛋白血癥患者,並有60歲以下發生心肌梗死者的陽性家族史。由於目前有關FCH的代謝異常和遺傳缺陷的基因尚不清楚,也未發現具有診斷意義的遺傳標記,所以要建立FCH的診斷,瞭解家族史是必不可少的。現將FCH的臨牀和生化特徵以及提示診斷的要點列出如下:①第一代親屬中有多種類型高脂蛋白症的患者;②早發性冠心病的陽性家族史;③血漿Apo B水平增高;④第一代親屬中無黃色瘤檢出;⑤家族成員中20歲以下者無高脂血症患者;⑥表現爲Ⅱa、Ⅱb、Ⅳ或Ⅴ型高脂血症;⑦LDL-膽固醇/Apo B比例變低;⑧HDL2-膽固醇水平降低。一般認爲,只要存在第1、2和3點就足以診斷FCH。
15.4 家族性異常β-脂蛋白血症
家族性異常β-脂蛋白血症(familial dysbetalipoproteinemia,FD)又名Ⅲ型高脂蛋白血癥。將病人的血漿脂蛋白經超速離心方法分離後,並進行瓊脂糖電泳,發現其極低密度脂蛋白(VLDL)電泳時常移至β位置,而不是正常的前β位置,因而稱之這種VLDL爲β-VLDL。對這些β-VLDL進行結構分析,發現其膽固醇的含量非常豐富。由於β-VLDL是Ⅲ型高脂蛋白血癥的最突出表現,且具有明顯的家族聚集性,所以稱之爲家族性異常β-脂蛋白血症。
血脂改變表現爲血漿膽固醇和三酰甘油濃度同時升高。血漿膽固醇濃度通常高於7.77mmol/L(300mg/dl),可高達26.0mmol/L。血漿三酰甘油濃度升高的程度(若以mg/dl爲單位)與血漿膽固醇水平大體相當或更高。一般認爲,若血漿膽固醇和三酰甘油濃度同時升高,且兩者相當時,應考慮到Ⅲ型高脂蛋白血癥的可能。
血漿中β-VLDL被認爲是診斷Ⅲ型高脂蛋白血癥的最重要依據。血漿中的VLDL富含膽固醇酯(大於25%,正常爲15%左右)即是β-VLDL的特徵之一。一般可通過測定兩種比值來反映VLDL中含膽固醇酯量的程度:①VLDL-膽固醇/血漿三酰甘油比值。這一比值≥0.3(mg/mg)對Ⅲ型高脂蛋白血癥幾乎有確診意義;而比值≥0.28(mg/mg)提示可能爲Ⅲ型高脂蛋白血癥。②VLDL-膽固醇/VIDL-三酰甘油比值。該比值≥1.0(mmol/mmol)對診斷Ⅲ型高脂蛋白血癥很有價值。
診斷Ⅲ型高脂蛋白血癥最可靠的生化標記是Apo E表型或Apo E基因型的測定。ApoE2與上述任何一個特徵同時存在,即可確立Ⅲ型高脂蛋白血癥的診斷。Apo E的表型或基因型不會因其他因素而發生改變。
16 高脂蛋白血癥的治療
16.1 調脂目標
16.1.1 (1)一級預防的調脂目標
①無動脈粥樣硬化疾病,也無冠心病危險因素者:TC< 5.72mmol/L(220mg/dl),TG<1.70mmol/L(150mg/dl),DLC-C<3.64mmol/L(140mg /dl)。
②無動脈粥樣硬化疾病,但有冠心病危險因素者:TC<5.20mmol/L(200mg/ dl),TG<1.70mmol/L(150mg/dl),LDL-C<3.12mmol/L(120mg/dl)。
16.1.2 (2)二級預防的調脂目標
有動脈粥樣硬化疾病者:TC<4.68mmol/L (180mg/dl),TG<1.70mmol/L(150mg/dl),LDL-C<2.60mmol/L(100mg/dl)。
目前美國膽固醇教育計劃(NCEP)和我國血脂防治建議均將冠心病患者的LDL-C目標水平定爲2.60mmol/L(100mg/dl),若LDL-C≥3.12~3.38mmol/L(120~130mg/dl)就應開始他汀類藥物治療。但目標水平下限尚未明確,曾有學者提出,就冠心病的防治而言,膽固醇降得越低越好。提出這一觀點是基於下列3點考慮:①在一定範圍內,膽固醇降低幅度愈大,則臨牀所獲益處會增大。②現有的藥物不可能使膽固醇降至極低。③目前大多數冠心病患者並沒有得到充分的降膽固醇治療。最近有些試驗表明將LDL-C水平控制在比2.60mmol/L(100mg/dl)更低時可能臨牀得益更大。冠狀動脈搭橋後試驗(Post-CABG)是首次比較了一般降脂與積極降脂臨牀療效。積極降脂者服用洛伐他汀40~80mg/d,以使LDL-C降至1.6~2.5mmol/L,追蹤觀察7.5年,積極降脂治療者的血管再建術減少30%。聯合終點減少24%,該研究結果支持積極降脂治療,使LDL-C降至2mmol/L(77mg/dl)左右。在AVERT(阿託伐他汀與血管再通療效比較)試驗中,用阿託伐他汀將穩定型心絞痛患者的LDL-C降至2mmol/L(77mg/dl)(積極降脂組),1.5年時死亡、腦卒中、心肌梗死等心血管事件比LDL-C降至3.09mmol/L(119mg/dl)者(常規降脂加PTCA治療組)減少36%,發現積極降脂能明顯降低心肌缺血事件發生率,其療效與PTCA基本相當甚或更好。另有研究發現將接受冠狀動脈旁路移植術患者的LDL-C水平降至平均2.2mmol/L(85mg/dl)時,臨牀效益更大,而且內膜增厚減輕。然而,CARE試驗結果表明,將LDL-C降至3.25mmol/L(125mg/dl)時,心血管事件降低最顯著,進一步降脂並未看到得益增加。因此,一些臨牀試驗正在進行之中,如TNT所驗證的LDL-C目標值爲2mmol/L(77mg/dl),IDEAL爲2.08mmol/L(80mg/dl),以探討LDL-C的新的目標值水平。
有人全面複習了膽固醇與冠心病相關研究的文獻後,推測TC<4.14mmol/L(相當於LDL-C<2.0mmol/L),可能很少發生冠心病。其依據是,在日本於1960~1970年,人羣平均TC爲4.14mmol/L,冠心病發病率非常低,因此,提出TC<4.14mmol/L(<160mg/dl)是一個很值得研究的目標值。中國心血管病流行病多中心協作研究綜合血清TC對冠心病、腦卒中、惡性腫瘤以及總死亡影響的定量分析結果,首次提出對於健康人羣來說,TC在3.64~5.17mmol/L是適宜的。高於5.2mmol/L,將會使發生冠心病、腦卒中的機會大大增加,並進一步造成死亡。低於3.64mmol/L,可能因惡性腫瘤發生的增加,造成相對過高的死亡機會。
調整TG及HDL-C的目標水平國內外有很大差異。從TG過高時使LDL-C亞型sLDL增多,到現在暫定目標值爲<1.7mmol/L(150mg/dl),對國人也是有待探索的。HDL-C目標值是越高越好,但亦無足夠證據,一般認爲至少應>1.04mmol/L(40mg/dl)爲宜。
16.2 血脂異常治療
降血脂治療方法包括兩大類:藥物性降脂治療和非藥物性降脂治療。通過採用藥物使過高的血脂降至正常,這在臨牀上較爲常用,其降脂效果肯定,病人常易於接受,但也有其侷限性。
非藥物性降脂治療包括飲食控制、血漿淨化、外科手術和基因治療等。其中飲食治療因爲是高脂血症治療的基礎,所以已被普遍採用。血漿淨化和外科手術治療則是藥物性降脂治療的補充,應用並不廣泛。基因治療僅適應於極少數嚴重的高脂血症。
16.2.1 (1)降脂藥物
16.2.1.1 ①膽酸螯合劑
膽酸螯合劑也稱爲膽酸隔置劑,主要爲鹼性陰離子交換樹脂,在腸道內能與膽酸呈不可逆結合,因而阻礙膽酸的腸肝循環,促進膽酸隨大便排出體外,阻斷膽汁酸中膽固醇的重吸收。同時伴有肝內膽酸合成增加,引起肝細胞內遊離膽固醇含量減少,反饋性上調肝細胞表面LDL受體表達,加速血漿LDL分解代謝,使血漿膽固醇和LDL-C濃度降低。本類藥物可使血漿總膽固醇(TC)水平降低15%~20%,使LDL-C降低20%~25%,但對三酰甘油(TG)無降低作用甚或稍有升高,故僅適應於單純高膽固醇血癥,或與其他降脂藥物合用治療混合型高脂血症。
A.考來烯胺(Cholestyramine)又名消膽胺,4~5g,3次/d,總量每天不超過24g。爲了減少副作用,增加病人的耐受性,可從小劑量開始用藥,1~3個月內達最大耐受量。該藥的主要缺點是含有異味,常引起消化道不良反應如噁心、厭食、便祕,大劑量時可致脂肪痢。
B.考來替泊(Colestipol)又名降膽寧,常用劑量爲10~20g,1~2次/d。該藥與煙酸長期聯合應用的效果良好。考來替泊的不良反應基本上與考來烯胺相似。
16.2.1.2 ②煙酸及其衍生物
煙酸及其衍生物屬B族維生素,當用量超過作爲維生素作用的劑量時,可有明顯的降脂作用。煙酸的降脂作用機制尚不十分明確,可能與抑制脂肪組織中的脂解和減少肝臟中極低密度脂蛋白(VLDL)合成和分泌有關。此外,煙酸還具有促進脂蛋白脂酶的活性,加速脂蛋白中三酰甘油的水解,因而其降TG的作用明顯。
臨牀上觀察到,煙酸既降低膽固醇又降低三酰甘油,同時還具有升高HDL-C的作用。常規劑量下,煙酸可使TC降低10%~15%,LDL-C降低15%~20%,TG降低20%~40%,並使HDL-C輕度至中度升高。所以,該類藥物的適用範圍較廣,可用於除純合子型家族性高膽固醇血癥及Ⅰ型高脂蛋白血癥以外的任何類型的高脂血症。
A.煙酸(Nicotinic acid,又名Niacin):常用劑量爲1~2g,3次/d。爲減少服藥的不良反應,可從小劑量開始,0.1~0.5g,3次/d,以後酌情漸增至常用劑量。有研究表明,煙酸3.0g/d ,使TC和TG分別下降9.9%和26.1%,尚未證實煙酸能降低冠心病患者死亡率。但可防止冠脈病變的進展,促使已有的冠脈病變逆轉,降低冠心病事件的發生率。本藥常見不良反應爲面紅、皮膚瘙癢及胃部不適。
B.阿昔莫司(Acipimox):又名氧甲吡甲吡嗪,樂脂平。常用劑量爲0.25g,2~3次/d。該藥是一種新合成的煙酸衍生物,其降脂作用機制與煙酸相同,臨牀適應範圍也與煙酸相似。可使TC降低25%,TG降低50%,HDL-C升高20%。阿昔莫司的常見不良反應與煙酸基本上相同,但發生率較低。服藥後部分病人可出現臉部潮紅,皮膚瘙癢或胃部灼熱感,上腹部不適和輕微頭痛。
16.2.1.3 ③苯氧芳酸類或稱貝特類
貝特類能增強脂蛋白脂酶的活性,加速VLDL分解代謝,並能抑制肝臟中VLDL的合成和分泌。這類藥物可降低三酰甘油22%~43%,而降低TC僅爲6%~15%,並有不同程度升高HDL-C作用。其適應證爲高三酰甘油血癥或以三酰甘油升高爲主的混合型高脂血症。
A.氯貝丁酯(氯貝特,安妥明,冠心平);0.25~0.5g,3次/d,是臨牀上應用最早的一種貝特類降脂藥物。由於早年的WHO試驗提示服用該藥者非心血管疾病的死亡危險增加,因而影響該藥在臨牀上的廣泛使用。
B.非諾貝特(Fenofibrate)0.1g,3次/d,有微粒化製劑,又名力平之,O.2g/d;微粒型非諾貝特可使TG下降15.2%~52%,TC下降12%~29%左右,LDL-C降低12%~25%,小而緻密的LDL-C(sLDL-C)降低21.5%,VLDL-C降低54%~63%,HDL-C升高26%~29%,Apo B下降22%~23%,並且降低Lp(a),升高Apo AⅠ。微粒化非諾貝特降低TG及LDL-C的效用與TG及LDL-C基礎水平成比例關係。少數患者使用微粒化非諾貝特後1周出現輕度腹脹,並於4周後消失。絕大多數病人服用微粒化非諾貝特耐受性較好。長期應用貝特類藥物可能誘發類似Ⅰ型自身免疫性慢性肝炎,停藥後可逐漸恢復。微粒型非諾貝特可引起穀草轉氨酶與谷丙轉氨酶的輕度升高,偶爾也可引起肌病。
C.吉非貝齊(Gemfibrozil)又名諾衡,康利脂0.6g,3次/d。赫爾辛基心臟研究(HHS)證實,吉非貝齊降低TG 43%,也降低冠心病事件發生率。退伍軍人管理局HDL-C干預試驗(VA-HIT)觀察到吉非貝齊(1200mg/d)治療後TG降低31%,HDL-C升高6%,LDL-C無明顯變化;非致死性心肌梗死或冠心病死亡(一級終點)發生的相對危險率下降22%;同時伴卒中發生的危險性下降;但總死亡的危險性下降(11%)無顯著性意義。
D.苯扎貝特(Bezafibrate)又名阿貝他或必降脂,0.2g,3次/d,緩釋長效製劑商品名爲脂康平。苯扎貝特在顯著降低TG後,能夠減慢侷限性冠狀動脈粥樣硬化的進程,尤其是基礎狹窄<50%的輕到中度的動脈粥樣硬化病竈,並降低心肌梗死後存活的年輕病人冠心病事件的發生率。苯扎貝特心肌梗死預防研究(BIP)觀察苯扎貝特緩釋製劑(400mg/d)對致死性和非致死性心肌梗死(猝死)(一級終點)發生率的作用。受試者爲3090例冠心病患者,苯扎貝特治療後,TG降低21%,TC降低4%,LDL-C降低6%,HDL-C升高18%。但治療組致死性和非致死性心肌梗死/猝死(一級終點)相對危險性僅降低9%。
16.2.1.4 ④三羥基三甲基戊二酰輔酶A(HMG-CoA)還原酶抑制劑(他汀類)
這類藥物是細胞內膽固醇合成限速酶即HMG-CoA還原酶的抑制劑,是目前臨牀上應用最廣泛的一類調脂藥,由於這類藥物的英文名稱均含有“statin”,故常簡稱爲他汀類。自1987年第1個他汀藥物即洛伐他汀(Lovastatin)被批准用於治療高脂血症以來,現已有5種他汀類藥物可供臨牀選用。他汀類降脂作用的機制目前認爲是由於該類藥能抑制細胞內膽固醇合成早期階段的限速酶即HMG-CoA還原酶,造成細胞內遊離膽固醇減少,並通過反饋性上調細胞表面LDL受體的表達,因而使細胞LDL受體數目增多及活性增強,加速了循環血液中VLDL殘粒(或IDL)和LDL的清除。
A.洛伐他汀(Lovastatin):商品名有美降之、羅華寧、洛特、洛之特,此外血脂康的主要成分也是洛伐他汀。常用劑量爲10~80mg/d,每晚頓服。對於Ⅱ型高脂蛋白血癥患者,洛伐他汀20mg/d使TC、LDL-C、TG分別降低17%、24% 10%,升高HDL-C 6.6%;洛伐他汀40mg/d 使TC、LDL-C、TG分別降低22%、30%和14%,升高HDL-C 7.2%;洛伐他汀80mg/d 使TC、LDL-C、TG分別降低29%、40%和19%,升高HDL-C 9.5%。空軍/得克薩斯冠狀動脈粥樣硬化預防研究 (AFCAPS/TexCAPS)表明,對於65歲以上的普通血脂濃度的健康者,洛伐他汀20~40mg/d(治療5.2年),使主要冠心病事件的危險性降低37%,心肌梗死(致死性或非致死性)發生的危險性降低40%。該藥副作用很少見,偶有腹痛、腹瀉、便祕、肌肉痙攣、疲乏無力、皮疹和視力模糊等。可有肝功能異常,CK升高。偶可出現肌病臨牀表現並伴顯著的CK升高(超過正常值上限10倍)。
B.辛伐他汀(Simvastatin):商品名爲舒降之、理舒達、京必舒新、澤之浩、蘇之。5~80mg;每晚頓服。辛伐他汀自1988年問世以來,在臨牀上應用已有10餘年,許多研究和臨牀觀察都證實該藥長期應用具有良好的安全性。辛伐他汀治療可使TC平均降低28%~30%;LDL-C平均降低36%~39%;TG平均降低11%~16%;HDL-C平均升高10%~14%。北歐辛伐他汀生存研究(4S)中63%患者服辛伐他汀20mg/d,37%服40mg/d。證實辛伐他汀有良好的降脂作用,使TC和LDL-C分別降低28%和38%,並能顯著降低總死亡和冠心病死亡的危險性。心臟保護研究(HPS)結果表明,辛伐他汀40mg/d治療使LDL-C平均降低37%,並使冠心病事件降低24%,卒中發生的危險性降低27%,總死亡率降低12%。受試人羣爲冠心病或心血管病高危者,血漿總膽固醇(TC)>3.5mmol/L。HPS發現,不論受試者的基礎LDL-C水平如何,即使受試者的基礎LDL-C已低於2.6mmol/L,通過辛伐他汀治療,LDL-C在降低1mmol/L後,都能獲得明顯的臨牀益處。所以,HPS重要貢獻在於拓寬了需要進行積極降脂治療的人羣:凡屬冠心病及心血管病高危者,都應給予積極降脂治療。
辛伐他汀不良反應少見,包括便祕、腹痛、消化不良、腹脹和噁心。辛伐他汀引起肝臟受損並不常見,主要表現爲血清轉氨酶輕度升高。大約5%患者接受辛伐他汀治療可出現肌酸磷酸激酶一過性輕度升高(大於正常參考值的3倍),通常無臨牀意義。極少數服用HMG-CoA還原酶抑制劑者可發生肌炎,伴或不伴血清CK水平升高,但這種肌炎常爲自限性。
C.普伐他汀(Pravastatin):商品名爲普拉固,美百樂鎮。10~80mg/d,每晚頓服。普伐他汀多國研究觀察1062例高膽固醇血癥患者的降脂效果,表明普伐他汀(20mg/d)治療13周,可使TC、LDL-C和TG分別降低19%、26%和12%。西蘇格蘭冠心病預防研究(WO-SCOPS)、膽固醇和冠心病復發事件試驗(CARE)和普伐他汀對缺血性心臟病的長期干預(LIPID)均證實普伐他汀40mg/d可使TC下降18%~20%,LDL-C降低25%~28%,HDL-C增加5%,TG降低11%~14%。同時明顯降低冠心病死亡率和致殘率。
主要不良反應主要表現爲肝臟轉氨酶升高,且與藥物劑量有關,但至今尚未見本藥所致的長久性肝損害的報道。服用普伐他汀者需監測轉氨酶,轉氨酶超過正常上限3倍時慎用。患者可出現肌病甚至無力,以致不能站立;CK可明顯升高,大於正常上限10倍。罕有橫紋肌溶解和免疫性肌病的報道。
D.氟伐他汀(Fluvastatin):又名來適可;20~80mg,每晚頓服。對原發性高膽固醇血癥病人每天給予20~40mg氟伐他汀可降低LDL-C 19%~3l%,降低TC 15%~21%,降低TG 1%~12%,增加HDL-C 2%~10%。氟伐他汀劑量增加至40~80mg/d,可使LDL-C繼續降低6%以上。LIPS研究是第1項針對首次經皮冠脈介入(PCI)術後立即開始降脂治療的臨牀試驗。該研究證實應用氟伐他汀(40mg,2次/d)治療,在4年的隨訪時間內可使冠心病患者在PCI術後的心臟事件絕對減少5.3%,相對減少22%。
氟伐他汀引起的副作用通常較輕且短暫,包括頭疼(8.9%)、消化不良(7.9%)、腹瀉(4.9%)、腹痛(4.9%)、噁心(3.2%)、失眠(2.7%)。臨牀試驗中因副作用而停用氟伐他汀的佔3.5%。雖然很少報道氟伐他汀的嚴重副作用,但仍有關於氟伐他汀引起肌痛(肌炎)的報道,服氟伐他汀的病人中,0.3%的病人出現無症狀性肌酸磷酸激酶升高(比正常上限高10倍),應迅速停藥。
E.阿伐他汀(Atorvastatin):又名立普妥、阿樂。2.5~20mg,每晚頓服。通常劑量下(10~80mg/d),阿伐他汀可使LDL-C降低40%~60%,TG降低23%~45%,HDL-C升高5%~9%,Apo B的變化和LDL-C的變化平行,對Lp(a)無明顯作用。對於原發性高三酰甘油血癥,單用阿伐他汀也能獲得療效顯著。AVERT試驗比較阿伐他汀(80mg/d)與PTCA治療穩定型心絞痛的療效,發現PTCA組21%(37例)患者發生缺血性事件,而阿伐他汀治療組僅13%(22例)發生此事件;並且後者發生第1次缺血性事件的時間較前者晚。此結果證實在預防冠心病患者缺血性事件發生方面,積極的降脂治療至少有和PTCA同樣的功效。積極降脂治療減少心肌缺血事件研究(MIRACL)是他汀類治療急性冠脈綜合徵的第1項大規模的臨牀試驗。受試對象爲3086例不穩定心絞痛或無ST段上抬的急性心肌梗死住院患者。於住院96h內隨機分爲阿伐他汀(80mg/d)治療組和安慰劑組。研究的主要聯合終點爲死亡、非致死性心肌梗死、心肺復甦或再次發作心絞痛並觀察證據需住院治療。平均觀察16周。研究結果阿伐他汀積極降脂治療可降低主要終點發生的危險性16%。盎格魯-斯堪的那維亞的心臟終點試驗(Anglo Scandinavian Cardiac Outcomes Trial,ASCOT)評價阿伐他汀(10mg/d)對膽固醇水平正常或輕度升高的高血壓患者的益處。主要終點是致死性冠心病和非致死性心肌梗死的聯合發生率,次級終點包括腦卒中發生率等。平均追蹤觀察3.3年的結果顯示,阿伐他汀治療組致死性冠心病和非致死性心肌梗死的聯合終點發生危險性降低36%,致死性和非致死性腦卒中發生的危險性降低27%。
阿伐他汀的耐受性好,不良反應的發生與藥物劑量無明顯相關性。約0.7%服藥者出現持續性轉氨酶升高超過正常3倍以上,多發生在治療後16周內,偶有肌病發生。
F.各種他汀類藥物調脂療效比較:目前在國內臨牀上可供選擇的他汀類降脂藥有5種製劑,他們各自的降脂效果和防治冠心病的作用可能有所不同,但在某種劑量範圍內,這5種他汀類藥的降低總膽固醇、LDL-C和三酰甘油以及升高HDL-C的療效具可比性(表6)。同時,也發現他汀類藥物降低總膽固醇和LDL-C的作用雖與藥物劑量有相關性,但並非呈直線相關關係。當他汀類藥物的劑量增大1倍時,其降低總膽固醇的幅度僅增加5%,降低LDL-C的幅度增加7%。

16.2.1.5 ⑤其他降脂藥物
A.普羅布考:又名丙丁酚。常用劑量爲0.5g,3次/d。本品吸收入體內後,可滲入到LDL顆粒核心中,因而有可能改變LDL的結構,使LDL易通過非受體途徑被清除。此外,該藥可能還具有使肝細胞LDL受體活性增加和抑制小腸吸收膽固醇的作用。有人觀察到,普羅布考(丙丁酚)還是一種強力抗氧化劑。可使血漿TC降低20%~25%,LDL-C降低5%~15%,而HDLC也明顯降低(可達25%)。主要適應於高膽固醇血癥尤其是純合子型家族性高膽固醇血癥。用藥期間,患者跟腱及皮膚黃色瘤可見消退。普羅布考(丙丁酚)的常見副作用包括噁心、腹瀉、消化不良等,亦可引起嗜酸細胞增多,血漿尿酸濃度增高,最嚴重的副作用是引起QT間期延長。有室性心律失常或QT間期延長者禁用。
B.魚油製劑:國內臨牀上應用的魚油製劑有多烯康、脈絡康及魚烯康製劑,用量爲1.8g,3次/d。主要含二十碳戊烯酸(EPA)和二十二碳乙烯酸(DHA)。其降低血脂的作用機制尚不十分清楚,可能與抑制肝臟合成VLDL有關。魚油製劑僅有輕度降低TG和稍升高HDL-C的作用,對TC和LDL-C無影響。主要用於高三酰甘油血癥。常見副作用爲魚腥味所致的噁心,一般難以長期堅持服用,服藥後約有2%~3%的病人出現消化道症狀如噁心、消化不良、腹脹、便祕,少數病例出現轉氨酶或肌酸激酶輕度升高,罕有引起肌病的報道。
16.2.2 (2)降脂藥物的臨牀應用
臨牀上目前主要是根據病人高脂血症的表型而選擇用藥。爲了方便起見,可分3種情況:
16.2.2.1 ①單純性高膽固醇血癥
單純性高膽固醇血癥是指血漿膽固醇水平高於正常,而血漿三酰甘油則正常。這種情況可選用膽酸螯合劑、他汀類、普魯布考、彈性酶和煙酸,其中以他汀類爲最佳選擇。
16.2.2.2 ②單純性高三酰甘油血癥
輕至中度高三酰甘油血癥常可通過飲食治療使血漿三酰甘油水平降至正常,不必進行藥物治療。而對於中度以上的高三酰甘油血癥,則可選用魚油製劑和貝特類調脂藥物。
16.2.2.3 ③混合型高脂血症
混合型高脂血症是指既有血漿膽固醇水平升高又有血漿三酰甘油水平升高。這種情況還可分爲兩種亞型:以膽固醇升高爲主或是以三酰甘油升高爲主。若是以膽固醇升高爲主,則首選他汀類;如果是以三酰甘油升高爲主,則可先試用貝特類。煙酸類製劑對於這種類型血脂異常也較爲適合。
16.2.2.4 ④聯合用藥
對於嚴重的高脂血症患者,單用一種調脂藥,可能難以達到理想的調脂效果,這時可考慮採用聯合用藥。簡單說來,只要不是同一類調脂藥物,均可考慮聯合用藥。而臨牀上常採用聯合用藥是:
A.對於嚴重高膽固醇血癥,若單種藥物的降脂效果不理想,可採用他汀類+膽酸螯合劑或+煙酸或+貝特類。
16.2.2.5 ⑤用藥注意事項
對於具體的病人,應根據其血脂異常的類型及其冠心病危險性的高低而選擇合適的降脂藥物。目前尚沒有確定合適的降脂藥物的公認標準,從冠心病防治的角度來說,一般認爲合適的降脂藥物應具備下列的特點:A.降脂效果尤其降膽固醇效果確切;應用常規劑量在4~6周內能使TC降低20%(LDL-C降低25%)以上,並具有降低TG和升高HDL-C的作用;B.病人耐受性好,不良反應少見,不產生嚴重的毒、副作用;C.已被證實能明顯地降低心血管病死率和致殘率,不增加非心血管病死亡率;D.具有良好的費用效益比。現有的大量臨牀證據表明,爲了防治冠心病,應首選他汀類降脂藥。
血脂異常的治療一般需要長期堅持,方可獲得明顯的臨牀益處。服藥期間應定期隨診,在開始藥物治療後4~6周內,應複查血漿膽固醇、三酰甘油和HDL-C,根據血脂改變而調整用藥。如果血脂未能降至正常,則應增加藥物的劑量或改用其他降脂藥物,也可考慮聯合用藥。若經治療後血脂已降至正常或已達到目標值,則繼續按同等劑量用藥,除非血脂已降至很低時,一般不要減少藥物的劑量。長期連續用藥時,應每3~6個月複查血脂,並同時複查肝腎功能和測肌酸激酶。
16.2.3 (3)冠心病防治中調脂治療指南
現有的大量研究證實,冠心病的防治中,降脂治療佔有很重要的地位。各國對冠心病預防時開始調脂治療的血脂水平和要求達到的目標值並不完全相同。有些國家建議根據冠心病的危險因素的多少進行分層治療。例如美國國立膽固醇教育計劃成人治療組(ATP)建議,對於少於2個冠心病危險因素的個體和對於已有2個或2個以上冠心病危險因素的個體,開始藥物降脂治療的血脂水平不同(表7)。我國於1997年發表了“血脂異常防治建議”,提出了有關冠心病預防的降脂治療的血脂水平與防治目標水平(表8)。歐洲也提出了冠心病防治指南中降脂治療的準則。
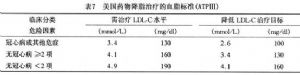
16.2.3.1 ①美國膽固醇教育計劃成人治療組第三次制定的標準(ATPⅢ)
這一標準(表7)已被世界許多國家借鑑並採納,對已患有冠心病的患者,血漿LDL-C>3.4mmol/L(TC>5.2mmol/L)就應進行調脂治療。
16.2.3.2 ②中國的血脂異常防治建議
我國的心血管病專家參考了美國的ATPⅡ方案及其他亞洲國家和地區的方案,結合中國的實際情況,制定出了適合我國醫藥衛生人員對血脂異常防治需要的統一指南(表8)。此外,在我國的血脂異常防治建議中,制定了將血漿三酰甘油降至1.70mmol/L(150mg/dl)的防治目標水平。

16.2.3.3 ③歐洲心臟病學會制定的冠心病預防指南中血脂干預建議
對於已患有冠心病或其他動脈粥樣硬化性疾病的患者,將血漿TC降至5.0 mmol/L(190mg/dl)以將血漿LDL-C降至3.0mmol/L(115mg/dl)以下。雖然認爲HDL-C<1.0 mmol/L(40mg/dl)和TG>2.0mmol/L(180mg/dl)是患冠心病危險性增加的標誌,但尚未制定出有關HDL-C和TG的治療目標值。
16.2.4 (4)非藥物降脂療法
16.2.4.1 ①飲食療法
飲食療法是各種高脂血症治療的基礎,尤其是對原發性高脂血症患者,更應首選飲食治療。即使是在進行藥物性降脂治療時,飲食療法仍然應同時進行。飲食治療除能使血清膽固醇降低2%~8%,以及使血脂調節劑更易發揮良好作用外,尚具有改善糖耐量、恢復胰島功能和減輕肥胖者體重等多方面功效。
A.飲食治療原則:合理的膳食應以維持身體健康和保持體重恆定爲原則。
B.飲食治療的標準與目標:需要進行飲食療法的血清LDL-C水平以及要達到的降低LDL-C的目標,還按是否患有CHO加以分類(表9)。

C.飲食療法方案:美國膽固醇教育規劃(ATPⅢ)提出的高膽固醇血癥的飲食治療方案,可供我國臨牀治療高膽固醇血癥時借鑑。ATPⅢ中的治療性生活方式改變(TLC)具有下列特點:a.少飽和脂肪酸攝入(<總熱量的7%)和膽固醇攝入(<200mg/d);b.提倡從飲食中補充stanols/固醇(2g/d)和增加黏性(可溶性)纖維(10~25g/d);c.減輕體重;d.增加體力活動。
16.2.4.2 ②血漿淨化療法
高脂血症血漿淨化療法亦稱血漿分離法,意指移去含有高濃度脂蛋白的血漿,也稱之血漿清除法或血漿置換。近年來發展起來了LDL去除法,其優點是特異性高,副作用少,不需補充血漿,但需每間隔7~14天進行1次,且需終身治療。
LDL去除法已成爲對於難治性高膽固醇血癥者的最有效的治療手段之一,可使血漿膽固醇水平降低到用藥物無法達到的水平。LDL去除法治療的適應證:
A.冠心病患者經最大限度飲食和藥物治療後,血漿LDL-C>4.92mmol/L(190mg/dl)。
B.無冠心病的30歲以上的男性和40歲以上的女性,經飲食和藥物治療後,血漿LDL-C>6.48mmol/L(250mg/dl)者,並在一級親屬中有早發性冠心病者,以及有一項或一項以上其他冠心病危險因素,包括血漿脂蛋白(a)>40mg/dl者。
C.純合子家族性高膽固醇血癥患者,即使無冠心病,若同時有血漿纖維蛋白水平升高者。
D.此外,對於純合子型家族性高膽固醇血癥患者,凡對降脂藥物治療反應差而血漿膽固醇水平又非常高者,均可考慮爲採用該法的適應證。
由於該療法的費用十分昂貴,且需反覆進行,故不宜在臨牀上推廣應用。
16.2.4.3 ③基因治療
通過利用特定的重組DNA,在基因水平治療遺傳性疾病。有多種方法,例如可將正常基因導入靶細胞並使之表達,以治療內源性基因所致的異常;或用同源重組的方法,用外源性正常基因代替突變的基因或序列;或將某種特殊功能的基因加入特定的靶細胞中,以對抗異常基因引起的病理狀態;也可利用反義核酸技術降低變異基因的表達。基因治療還未成熟,有待進一步深入研究和發展。
17 高脂蛋白血癥的預防
通過多種途徑進行廣泛、反覆的健康教育,提倡科學膳食、均衡膳食,規律的體育鍛煉,防止肥胖,戒菸、酒,並與心血管病、肥胖症、糖尿病等慢性病防治的衛生宣傳教育相結合,使人羣中的血脂保持在適當水平。此外,定期健康檢查亦有助於及早檢出血脂異常者,及時治療。