3 坎地沙坦酯藥典標準
3.1 品名
3.1.1 中文名
3.1.2 漢語拼音
Kandishatanzhi
3.1.3 英文名
Candesartan Cilexetil
3.2 結構式
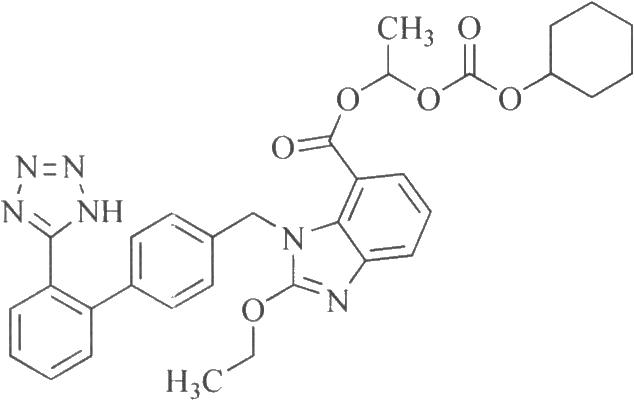
3.3 分子式與分子量
C33H34N6O6 610.67
3.4 來源(名稱)、含量(效價)
本品爲(±)-1-[(環己氧基)羰基氧基]乙基 2-乙氧基-1-[[2'-(1H-四氮唑基-5-基)聯苯基-4-基]甲基]-1H-苯並咪唑-7-羧酸酯。按乾燥品計算,含C33H34N6O6不得少於98.5%。
3.5 性狀
本品爲白色或類白色結晶性粉末。
3.6 鑑別
(1)取有關物質項下的對照溶液作爲供試品溶液;另取坎地沙坦酯對照品適量,用乙腈-水(3:2)溶解並稀釋製成每1ml中約含4μg的溶液作爲對照品溶液。照有關物質項下的色譜條件測定,供試品溶液主峯的保留時間應與對照品溶液主峯的保留時間一致。
(2)本品的紅外光吸收圖譜應與對照的圖譜(《藥品紅外光譜集》1147圖)一致。
3.7 檢查
3.7.1 氯化物
取本品0.40g,加水100ml,強力振搖10分鐘,濾過,取續濾液25ml,依法檢查(2010年版藥典二部附錄Ⅷ A),與標準氯化鈉溶液5.0ml製成的對照液比較,不得更深(0.05%)。
3.7.2 有關物質
取本品約20mg,置50ml量瓶中,加乙腈-水(3:2)溶解並稀釋至刻度,搖勻,作爲供試品溶液;精密量取1ml,置100ml量瓶中,用乙腈-水(3:2)稀釋至刻度,搖勻,作爲對照溶液。照高效液相色譜法(2010年版藥典二部附錄Ⅴ D)測定,用十八烷基硅烷鍵合硅膠爲填充劑(推薦Ecosil C18柱或Kromasil100-5 C18柱,4.6mm×250mm,5μm或效能相當的色譜柱);以乙腈-冰醋酸-水(57:1:43)爲流動相A,乙腈-冰醋酸-水(90:1:10)爲流動相B,檢測波長爲254nm。按下表進行線性梯度洗脫。取供試品溶液20ml,加0.1mol/L鹽酸溶液1.0ml,90℃水浴加熱10分鐘後,加0.1mol/L氫氧化鈉溶液1.0ml中和,作爲系統適用性溶液,取系統適用性溶液10μl注入液相色譜儀,記錄色譜圖,坎地沙坦酯峯保留時間約爲20分鐘,(±)-1-[[(環己氧代)羰基)氧代)乙基-2-氧代-3-[(2'-(1H-四氮唑基-5-基)聯苯基-4-基]甲基]-2,3-二氫-1H-苯並咪唑-4-羧酸酯(雜質Ⅰ)的相對保留時間約爲0.6;理論板數按坎地沙坦酯峯計不低於12000,拖尾因子不得過1.5。精密量取供試品溶液和對照溶液各10μl注入液相色譜儀,記錄色譜圖,供試品溶液的色譜圖中如有雜質峯,雜質Ⅰ峯面積不得大於對照溶液主峯面積的0.3倍(0.3%),其他單個雜質峯面積不得大於對照溶液主峯面積的0.2倍(0.2%),各雜質峯面積的和不得大於對照溶液主峯面積的0.6倍(0.6%)。供試品溶液色譜圖中任何小於對照溶液主峯面積0.05倍的峯可忽略不計。
時間(分鐘) | 流動相A(%) | 流動相B(%) |
0 | 100 | 0 |
3 | 100 | 0 |
33 | 0 | 100 |
40 | 0 | 100 |
41 | 100 | 0 |
50 | 100 | 0 |
3.7.3 殘留溶劑
3.7.3.1 乙醇、二氯甲烷、甲苯與N,N-二甲基甲酰胺
取本品適量,精密稱定,加二甲基亞碸溶解並定量稀釋製成每1ml中約含0.1g的溶液,作爲供試品溶液;另取乙醇、二氯甲烷、甲苯與N,N-二甲基甲酰胺各適量,精密稱定,加二甲基亞碸定量稀釋製成每1ml中含乙醇0.5mg、二氯甲烷60μg、甲苯89μg與N,N-二甲基甲酰胺88u g的溶液,作爲對照品溶液。精密量取供試品溶液和對照品溶液各5ml,置頂空瓶中,密封。照殘留溶劑測定法(2010年版藥典二部附錄Ⅷ P 第二法)測定。以6%氰丙基苯基-94%二甲基聚硅氧烷(或極性相近)爲固定液;起始溫度爲60℃,維持8分鐘,以每分鐘35℃的速率升溫至150℃,維持10分鐘;進樣口溫度爲200℃;檢測器溫度爲250℃;頂空瓶平衡溫度爲95℃,平衡時間爲60分鐘。取對照品溶液頂空進樣,各成分峯之間的分離度均應符合要求。再取供試品溶液和對照品溶液分別頂空進樣,記錄色譜圖。按外標法以峯面積計算,均應符合規定。
3.7.4 乾燥失重
取本品1.0g,在105℃乾燥至恆重,減失重量不得過0.5%(2010年版藥典二部附錄Ⅷ L)。
3.7.5 熾灼殘渣
取本品1.0g,依法檢查(2010年版藥典二部附錄Ⅷ N),遺留殘渣不得過0.1%。
3.7.6 重金屬
取熾灼殘渣項下遺留的殘渣,依法檢查(2010年版藥典二部附錄ⅧH 第二法),含重金屬不得過百萬分之十。
3.8 含量測定
取本品約0.45g,精密稱定,加冰醋酸-醋酐(1:1)40ml,振搖使溶解,照電位滴定法(2010年版藥典二部附錄Ⅶ A),用高氯酸滴定液(0.1mol/L)滴定,並將滴定的結果用空白試驗校正。每1ml高氯酸滴定液(0.1mol/L)相當於61.07mg的C33H34N6O6。
3.9 類別
3.10 貯藏
3.11 附
雜質Ⅰ:(±)-1-[(環己氧基)羰基氧基]乙基 2-氧代-3-[[2'-(1H-四氮唑-5-基)聯苯-4-基]甲基]-2,3-二氫-1H-苯並咪唑-4-羧酸酯
(1RS)-1-[[(cyclohexyloxy) carbonyl] oxy] ethyl-2-oxo-3-[[2'-(1H-tetrazol-5-yl)biphenyl-4-yl] methyl]-2,3-dihydro-1H -benzimidazole-4-carboxylate

C31H30N6O6 582.62
3.12 版本
《中華人民共和國藥典》2010年版 第三增補本