2 附錄XIII A 無特定病原體雞胚質量檢測要求
無特定病原體(SPF)雞係指在嚴格控制飼養條件下,符合所規定的微生物學檢測要求的雞。無特定病原體雞胚是指SPF雞生產的受精卵,在符合生物製品生產的條件下,經孵化後所生成的雞胚。通過對SPF雞蛋和SPF雞羣病原微生物的檢測,使SPF雞胚質量得以控制。
2.1 檢測項目與方法
檢測要求 | ||
雞白痢沙門菌Salmonella pullorum | ● | SPA, IA, TA |
● | AGP, HI | |
● | AGP, SN, HI | |
傳染性法氏囊病病毒 Infectious Bursal Disease Virus | ● | AGP, SN |
● | AGP, SN | |
新城疫病毒 Newcastle Disease Virus | ● | |
禽痘病毒 Fowl Pox Virus | ● | AGP |
馬立克病病毒 Marek's Disease Virus | ● | AGP |
副雞嗜血桿菌 Haemophilus paragallinarum | ● | SPA |
多殺巴斯德菌 Pasteurella multocida | ○ | AGP |
檢測要求 | ||
禽腺病毒Ⅲ羣(EDS)Avian Adenovirus Group Ⅲ | ● | |
雞毒支原體 Mycoplasma gallisePticum | ● | SPA, HI |
滑液囊支原體 Mycoplasma synoviae | ● | SPA, HI |
● | AGP, EST, SN | |
● | ||
● | AGP | |
● | AGP | |
禽腺病毒Ⅰ羣 Avian Adenovirus Group I | ● | AGP |
● | IFA |
2.2 【附註】
HI,血凝抑制試驗;
ELISA,酶聯免疫吸附試驗;
EST,胚敏感試驗;
SN,血清中和試驗;
TA,試管凝集試驗;
IFA.間接免疫熒光試驗。
2.3 檢測要求
(1)取樣 禽淋巴白血病病毒和禽腦脊髓炎病毒的檢測均應取新鮮雞蛋。其他病原微生物檢測一律檢測血清,每份供試品血清量應不少於1ml。必須按無菌操作程序取樣,防止污染。
(2)取樣數量 淋巴白血病病毒檢測,每個雞羣取雞蛋200枚(少於200只的雞羣從全羣中取樣),每隻雞取蛋1枚。禽腦脊髓炎病毒檢測,每個雞羣取雞蛋不少於50枚(少於50只雞的雞羣應從全羣中取樣),每隻雞取蛋1枚。其他病原微生物感染檢測,應採取隨機方式取樣,抽取每個雞羣的5%,少於200只雞的雞羣應按10%~15%抽樣。
(3)供試品的保存與運輸 取樣後應儘快將供試品送往檢測實驗室檢驗。不能及時運送的供試品,血清須在-15℃以下保存,雞蛋應在4~10℃保存。保存時間應不超過1周。供試品應有明顯的編號標誌,並附送檢單,寫明雞羣名稱、雞羣數量、供試品名稱及數量。供試品在運送過程中應避免溫度上升,防止破損。
2.4 結果判定
3 附錄XIII B 實驗動物微生物學檢測要求
本標準(引自GB 14922.2—2001)適用於豚鼠、地鼠、兔、犬、猴和清潔級及以上小鼠、大鼠。
3.1 1.實驗動物微生物學等級分類
(1)普通級動物Conventional (CV) Animal 不攜帶所規定的人獸共患病病原和動物烈性傳染病的病原。
(2)清潔動物Clean.(CL) Animal 除普通動物應排除的病原外,不攜帶對動物危害大和對科學研究干擾大的病原。
(3)無特定病原體動物Specific Pathogen Free (SPF)Animal 除清潔動物應排除的病原外,不攜帶主要潛在感染或條件致病和對科學實驗干擾大的病原。
(4)無菌動物Germ Free (GF) Animal 無可檢出的一切生命體。
3.2 2.檢測要求
(1)外觀指標 動物應外觀健康、無異常。


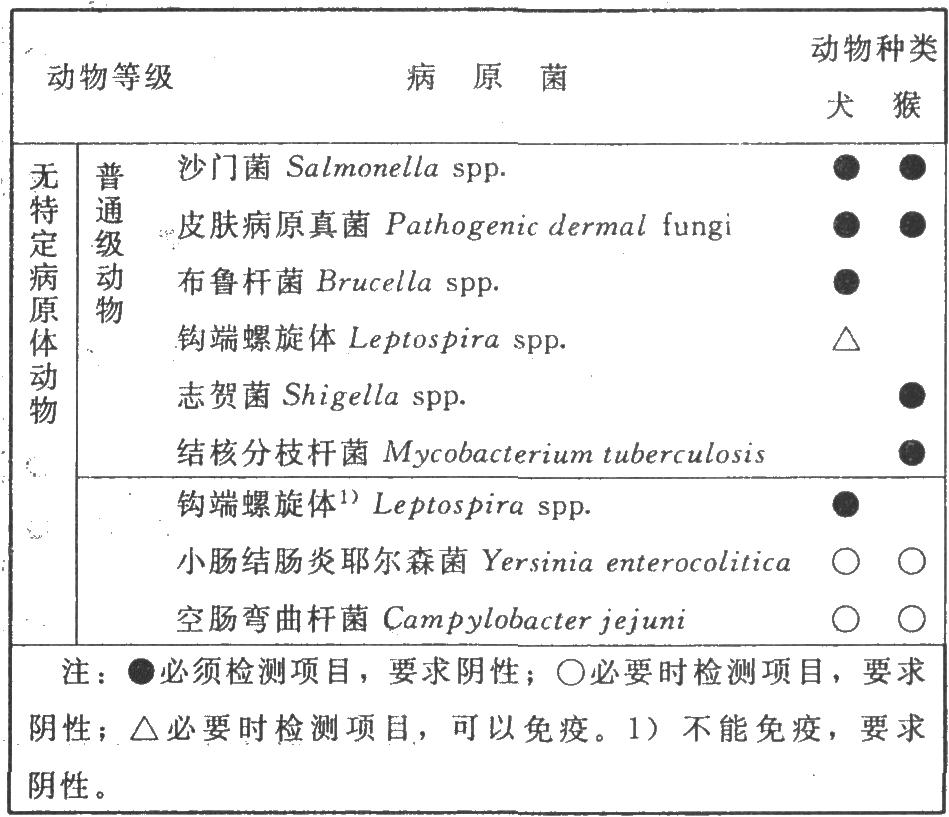



4 附錄XIII C 實驗動物寄生蟲學檢測要求
本標準(引自GB 14922.1—2001)適用於地鼠、豚鼠、兔、犬、猴和清潔級及以上小鼠、大鼠。
4.1 1.實驗動物寄生蟲學等級
(1)普通級動物Conventional (CV) Animal不攜帶所規定的人獸共患寄生蟲。
(2)清潔動物Clean (CL) Animal 除普通動物應排除的寄生蟲外,不攜帶對動物危害大和對科學研究干擾大的寄生蟲。
(3)無特定病原體動物Specific Pathogen Free (SPF)Animal除普通動物、清沽動物應排除的寄生蟲外,不攜帶主要潛在感染或條件致病和對科學實驗干擾大的寄生蟲。
(4)無菌動物Germ Free(GF)Animal 無可檢出的一切生命體。
4.2 2.檢測要求
(1)外觀指標 動物應外觀健康,無異常。

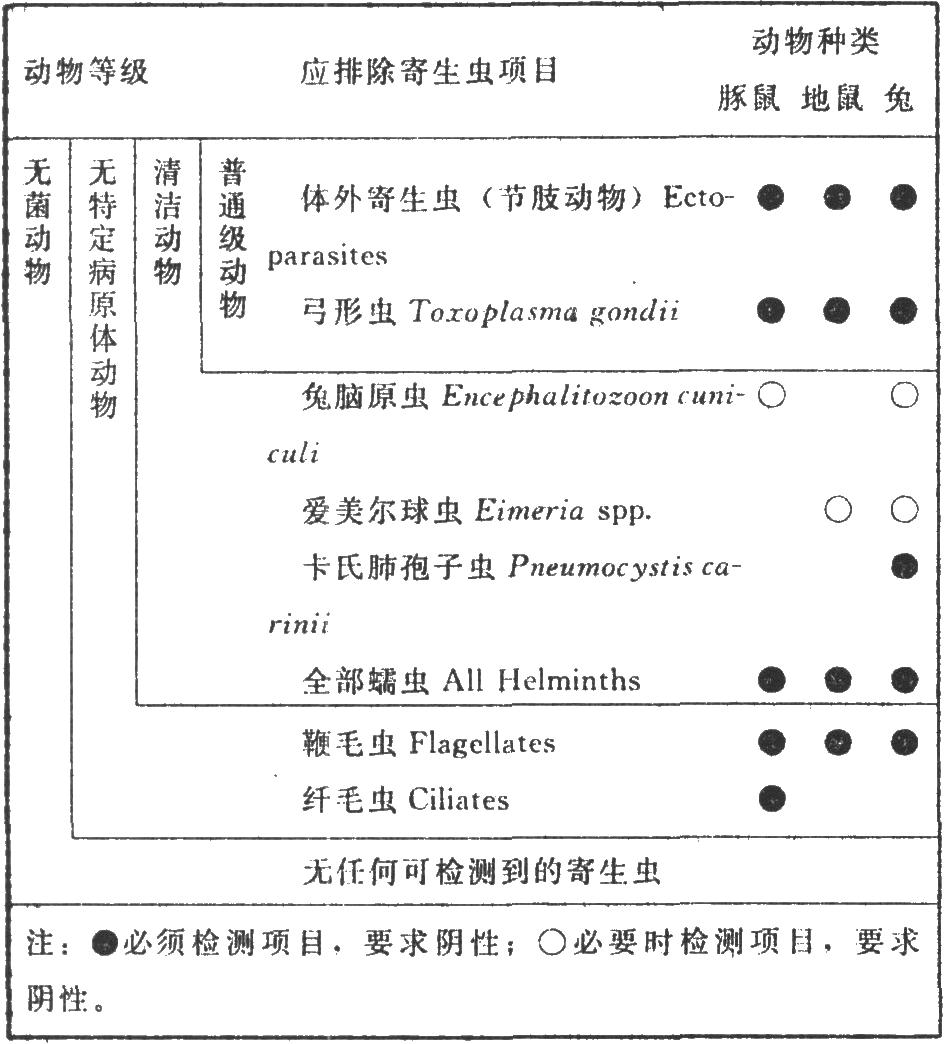

5 附錄XIII D 新生牛血清檢測要求
本品系從出生14小時內未進食的新生牛採血分離血清,經除菌過濾後製成。牛血清生產過程中不得任意添加其他物質成分。新生牛血清用於生產前應逐批進行以下檢查,並應符合規定。
5.1 蛋白質含量
應爲3.5%~5.0%(2010年版藥典三部附錄Ⅵ B 第一法)。
5.2 血紅蛋白
用氰化高鐵法或其他適宜的方法測定。應不高於0.02%。
5.3 大腸桿菌噬菌體
5.4 滲透壓摩爾濃度
應爲250~400mOsmol/kg(2010年版藥典三部附錄V H)。
5.5 無菌檢查
依法檢查(2010年版藥典三部附錄Ⅻ A),應符合規定。
5.6 支原體檢查
依法檢查(2010年版藥典三部附錄Ⅻ B),應符合規定。細菌內毒素檢查 應不高於10EU/ml(2010年版藥典三部附錄Ⅻ E 凝膠限度試驗)。
5.7 病毒檢查
5.7.1 1.細胞培養法
(1)非血吸附病毒檢查 將新生牛血清供試品分別接種到人源(如人二倍體細胞)、猴源(如Vero細胞)以及牛腎傳代細胞3種細胞,採用的牛腎傳代細胞系應證明無牛病毒的污染。每種細胞至少接種6瓶,每瓶細胞懸液接種量應不少於培養液總量的25%。置36℃±1℃培養21天。接種的每種細胞都應同時設立牛血清陰性對照和病毒陽性對照(陰性對照用牛血清應證明無牛病毒污染)。培養過程中可根據細胞生長情況更換細胞培養液,每次更換培養液前應觀察有無細胞病變出現。培養到期後,陰性對照應無任何細胞病變出現,陽性對照應出現典型的細胞病變,試驗成立。供試品檢查不出現任何細胞病變爲陰性,符合要求。
(2) 血吸附病毒檢查 將上述接種供試品的每種細胞取2瓶進行血吸附病毒檢查。用0.2%~0.5%雞和豚鼠紅細胞混合懸液覆蓋於細胞表面,置2~8℃30分鐘,然後置90~25℃作用30分鐘,分別進行鏡檢,觀察紅細胞吸附情況,供試品檢查結果均應爲陰性。試驗同時應設立血吸附陽性對照。
5.7.2 2.免疫熒光抗體檢查法
採用直接或間接免疫熒光抗體檢查法,至少應對牛腹瀉病毒、牛腺病毒、牛細小病毒、呼腸孤病毒、狂犬病病毒以及牛副流感病毒進行檢查,結果均應爲陰性。
支持細胞增殖檢查 用Sp2/O-Ag14或適宜的非貼壁傳代細胞進行。
(1)細胞生長曲線的測定 取供試品按10%濃度配製細胞培養液,按每1ml含104個細胞的細胞濃度接種細胞,每天計數活細胞,連續觀察1周,並繪製生長曲線,細胞的最大增殖濃度應不低於每1ml含106個細胞。
(2)細胞倍增時間的測定 按Sp2/O-Ag14細胞生長曲線計算細胞的倍增時間。取細胞峯值前一天的細胞計數(Y)、接種細胞數(X)及生長時間(T)計算。

細胞的倍增時間應不超過20小時。
(3)克隆率的測定 按有限稀釋法將細胞稀釋,並按每孔1個細胞的濃度接種於96孔細胞培養板,每板至少接種48孔,於37℃、5%二氧化碳條件下培養1周後計算克隆率,應不低於70%。
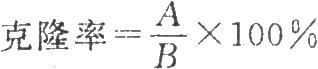
B爲接種細胞的總孔數。