1971年Engvall和Perlmann發表了酶聯免疫吸附劑測定(enzymelinkedimmunosorbentassay,ELISA)用於IgG定量測定的文章,使得1966年開始用於抗原定位的酶標抗體技術發展成液體標本中微量物質的測定方法。
1 ELISA基本原理
這一方法的基本原理是:①使抗原或抗體結合到某種固相載體表面,並保持其免疫活性。②使抗原或抗體與某種酶連接成酶標抗原或抗體,這種酶標抗原或抗體既保留其免疫活性,又保留酶的活性。在測定時,把受檢標本(測定其中的抗體或抗原)和酶標抗原或抗體按不同的步驟與固相載體表面的抗原或抗體起反應。用洗滌的方法使固相載體上形成的抗原抗體複合物與其他物質分開,最後結合在固相載體上的酶量與標本中受檢物質的量成一定的比例。加入酶反應的底物後,底物被酶催化變爲有色產物,產物的量與標本中受檢物質的量直接相關,故可根據顏色反應的深淺刊物定性或定量分析。由於酶的催化頻率很高,故可極大地地放大反應效果,從而使測定方法達到很高的敏感度。
2 方法類型和操作步驟
ELISA可用於測定抗原,也可用於測定抗體。在這種測定方法中有3種必要的試劑:①固相的抗原或抗體,②酶標記的抗原或抗體,③酶作用的底物。根據試劑的來源和標本的性狀以及檢測的具備條件,可設計出各種不同類型的檢測方法。
2.1 (一)雙抗體夾心法
雙抗體夾心法(圖15-4)是檢測抗原最常用的方法,操作步驟如下:

(1)將特異性抗體與固相載體連接,形成固相抗體:洗滌除去未結合的抗體及雜質。
(2)加受檢標本:使之與固相抗體接觸反應一段時間,讓標本中的抗原與固相載體上的抗體結合,形成固相抗原複合物。洗滌除去其他未結合的物質。
(3)加酶標抗體:使固相免疫複合物上的抗原與酶標抗體結合。徹底洗滌未結合的酶標抗體。此時固相載體上帶有的酶量與標本中受檢物質的量正相關。
(4)加底物:夾心式複合物中的酶催化底物成爲有色產物。根據顏色反應的程度進行該抗原的定性或定量。
根據同樣原理,將大分子抗原分別製備固相抗原和酶標抗原結合物,即可用雙抗原夾心法測定標本中的抗體。
2.2 (二)雙位點一步法
在雙抗體夾心法測定抗原時,如應用針對抗原分子上兩個不同抗原決定簇的單克隆抗體分別作爲固相抗體和酶標抗體,則在測定時可使標本的加入和酶標抗體的加入兩步並作一步(圖15-5)。這種雙位點一步不但簡化了操作,縮短了反應時間,如應用高親和力的單克隆抗體,測定的敏感性和特異性也顯著提高。單克隆抗體的應用使測定抗原的ELISA提高到新水平。
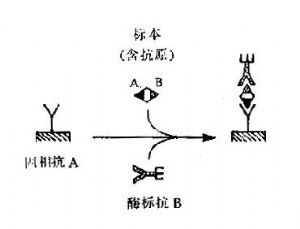
圖15-5雙位點一步法示意圖
在一步法測定中,應注意鉤狀效應(hookeffect),類同於沉澱反應中抗原過剩的後帶現象。當標本中待測抗原濃度相當高時,過量抗原分別和固相抗體及酶標抗體結合,而不再形成夾心複合物,所得結果將低於實際含量。鉤狀效應嚴重時甚至可出現假陰性結果。
2.3 (三)間接法測抗體
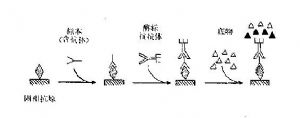
間接法(圖15-6)是檢測抗體最常用的方法,其原理爲利用酶標記的抗抗體以檢測已與固相結合的受檢抗體,故稱爲間接法。操作步驟如下:
(1)將特異性抗原與固相載體連接,形成固相抗原:洗滌除去未結合的抗原及雜質。
(2)加稀釋的受檢血清:其中的特異抗體與抗原結合,形成固相抗原抗體複合物。經洗滌後,固相載體上只留下特異性抗體。其他免疫球蛋白及血清中的雜質由於不能與固相抗原結合,在洗滌過程中被洗去。
(3)加酶標抗抗體:與固相複合物中的抗體結合,從而使該抗體間接地標記上酶。洗滌後,固相載體上的酶量就代表特異性抗體的量。例如欲測人對某種疾病的抗體,可用酶標羊抗人IgG抗體。
本法只要更換不同的固相抗原,可以用一種酶標抗抗體檢測各種與抗原相應的抗體。
2.4 (四)競爭法
競爭法(圖15-7)可用於測定抗原,也可用於測定抗體。以測定抗原爲例,受檢抗原和酶標抗原競爭與固相抗體結合,因此結合於固相的酶標抗原量與受檢抗原的量呈反比。操作步驟如下:
(2)待測管中加受檢標本和一定量酶標抗原的混合溶液,使之與固相抗體反應。如受檢標本中無抗原,則酶標抗原能順利地與固相抗體結合。如受檢標本中含有抗原,則與酶標抗原以同樣的機會與固相抗體結合,競爭性地佔去了酶標抗原與固相載體結合的機會,使酶標抗原與固相載體的結合量減少。參考管中只加酶標抗原,保溫後,酶標抗原與固相抗體的結合可達最充分的量。洗滌。
(3)加底物顯色:參考管中由於結合的酶標抗原最多,故顏色最深。參考管顏色深度與待測管顏色深度之差,代表受檢標本抗原的量。待測管顏色越淡,表示標本中抗原含量越多。
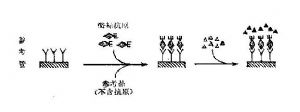
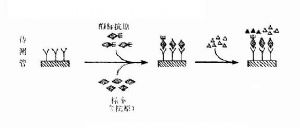
圖15-7競爭法測抗原示意圖
2.5 (五)捕獲法測IgM抗體
血清中針對某些抗原的特異性IgM常和特異性IgG同時存在,後者會干擾IgM抗體的測定。因此測定IgM抗本多用捕獲法(圖15-8),先將所有血清IgM(包括異性IgM和非特異性IgM)固定在固相上,在去除IgG後再測定特異性IgM。操作步驟如下:

圖15-8捕獲法測IgM抗體示意圖
(1)將抗人IgM抗體連接在固相載體上,形成固相抗人IgM。洗滌。
(2)加入稀釋的血清標本:保溫反應後血清中的IgM抗體被固相抗體捕獲。洗滌除去其他免疫球蛋白和血清中的雜質成分。
(3)加入特異性抗原試劑:它只與固相上的特異性IgM結合。洗滌。
(4)加入針對特異性的酶標抗體:使之與結合在固相上的抗原反應結合。洗滌。
(5)加底物顯色:如有顏色顯示,則表示血清標本中的特異性IgM抗體存在,是爲陽性反應。
2.6 (六)應用親和素和生物素的ELISA
親和素是一種糖蛋白,可由蛋清中提取。分子量60kD,每個分子由4個亞基組成,可以和4個生物素分子親密結合。現在使用更多的是從鏈黴菌中提取的鏈黴和素(strepavidin)。生物素(biotin)又稱維生素H,分子量244.31,存在於蛋黃中。用化學方法製成的衍生物,生物素-羥基琥珀亞胺酯(biotin-hydroxysuccinimide,BNHS)可與蛋白質、糖類和酶等多種類型的大小分子形成生物素化的產物。親和素與生物素的結合,雖不屬免疫反應,但特異性強,親和力大,兩者一經結合就極爲穩定。由於1個親和素分子有4個生物素分子的結合位置,可以連接更多的生物素化的分子,形成一種類似晶格的複合體。因此把親和素和生物素與ELIS偶聯起來,就可大提高ELISA的敏感度。
親和素-生物素系統在ELISA中的應用有多種形式,可用於間接包被,亦可用於終反應放大。可以在固相上先預包被親和素,原用吸附法包被固相的抗體或抗原與生物素結合,通過親和素-生物素反應而使生物素化的抗體或抗在相化。這種包被法不僅可增加吸附的抗體或抗原量,而且使其結合點充分暴露。另外,在常規ELISA中的酶標抗體也可用生物素化的抗體替代,然後連接親和素-酶結合物,以放大反應信號。橋聯法ABC-ELISA(avidinbiotincomplex-ELISA)夾心法測抗原的過程見圖15-9。

圖15-9橋連法ABC-ELISA夾心法測抗原示意圖
3 ELISA的技術要點
ELISA的技術要點包括三個方面:試劑的製備、反應條件的選擇和操作的標準化。
3.1 試劑的製備
ELISA的主要試劑爲固相的抗原或抗體、酶標記的抗原或抗體和與標記酶直接關聯的酶反應底物。以下敘述這些試劑的原料和製備方法。
3.1.1 (一)固相載體
可作ELISA中載體的物質很多,最常用的是聚苯乙烯。聚苯乙烯具有較強的吸附蛋白質的性能,抗體或蛋白質抗原吸附其上後保留原來的免疫活性。聚苯乙烯爲塑料,可製成各種形式。在ELISA測定過程中,它作爲載體和容器,不參與化學反應。加之它的價格低廉,所以被普遍採用。
ELISA載體的形狀主要有三種:小試管、小珠和微量反應板。小試管的特點是還能兼作反應的容器,最後放入分光光度計中比色。小珠一般爲直徑0.6cm的圓球,表面經磨砂處理後吸附面積大增加。如用特殊的洗滌器,在洗滌過程中使圓珠滾動淋洗,效果更好。最常用的載體爲微量反應板,專用於ELISA測定的產品也稱爲ELISA板,國際通用的標準板形是8×12的96孔式。爲便於作少量標本的檢測,有製成8聯或12聯孔條的,放入座架後,大小與標準ELISA板相同。ELISA板的特點是可以同時進行大量標本的檢測,並可在特定的比色計上迅速讀出結果。現在已有多種自動化儀器用於微量反應板型的ELISA檢測,包括加樣、洗滌、保溫、比色等步驟,對操作的標準化極爲有利。
良好的ELISA板應該是吸附性能好,空白值低,孔底透明度高,各板之間和同一板各孔之間性能相近。聚苯乙烯ELISA板由於配料的不同和製作工藝的差別,各種產品的質量差異很大。因此每一批號的聚苯乙烯製品在使用前須檢查其性能。常用的檢查方法爲:以一定濃度的人IgG(一般爲10ng/ml)包被ELISA板各孔後,每孔內加入適當稀釋的酶標抗人IgG抗人IgG抗體,保溫後洗滌,加底物顯色,終止酶反應後分別測每孔溶液的吸光度。控制反應條件,使各讀數在0.8左右。計算所有讀數的平均值。所有單個讀數與平均讀數之差應小於10%。
與聚苯乙烯類似的塑料爲聚氯乙烯。作爲ELISA固相載體,聚氯乙烯板的特點爲質軟板薄,可切割,價廉、但光潔度不如聚苯乙烯板。聚氯乙烯對蛋白質的吸附性能比聚苯乙烯高,但空白值有時也略高。
爲比較不同固相在某一ELISA測定中的優劣,可用以下方法加以檢驗:用其它免疫學測定方法選出一個典型的陽性標本和一個典型的陰性標本。將它們分別進行一系列稀釋後,在不同的固相載體上按預定的ELISA操作步驟進行測定,然後比較測定結果。在哪一種載體上陽性結果與陰性結果判別最大,這種載體就是這一ELISA測定的最合適的固相載體。
除塑料製品外,固相酶免疫測定的載體還有兩種材料:一是微孔濾膜,如硝酸纖維素膜、尼龍膜等,這類測定形式將在本章第五節“膜載體的酶免疫測定”中介紹。另一種載體是以含鐵的磁性微粒製作的,反應時固相微粒懸浮在溶液中,具有液相反應的速率,反應結束後用磁鐵吸引作爲分離的手段,洗滌也十分方便,但需配備特殊的儀器。
3.1.2 (二)抗原和抗體
在ELISA實施過程中,抗原和抗體的質量是實驗是否成功的關鍵因素。本法要求所用抗原純度高,抗體效價高、親和力強。
ELISA所用抗原有三個來源:天然抗原、重組抗原和合成多肽抗原。天然抗原取材於動物組織或體液、微生物培養物等,一般含有多種抗原成分,需經純化,提取出特定的抗原成分後纔可應用,因此也稱提純抗原(purifiedantigen)。重組抗原(recombinantantigen)和多肽抗原(peptideantigen)均爲人工合成品,使用安全,而且純度高,干擾物質少。因此雖然製備合成抗原有較高的技術難度且要求較爲昂貴的儀器設備和試劑,其應用仍十分普遍,特別是對那些天然抗原不易得到的試驗,更顯出其獨到之處。
用於ELISA的抗體有多克隆的和單克隆的。抗血清成分複雜,應從中提取IgG纔可用於包被固相或酶標記。含單克隆抗體的小鼠腹水中的特異性抗體含量較高,有時可適當稀釋後直接進行包被。製備酶結合物用的抗體的質量往往要求有較高的純度。經硫酸銨鹽析純化的IgG可進一步用各種分子篩層析提純。也可用親和層析法提純特異性IgG,如用酶消化IgG後提取的Fab片段,則效果更好。
3.1.3 (三)免疫吸附劑
固相的抗原或抗體稱爲免疫吸附劑。將抗原或抗體固相化的過程稱爲包被(coating)。由於載體的不同,包被的方法也不同。如以聚苯乙烯ELISA板爲載體,通常將抗原或抗體溶於緩衝液(最常用的爲pH9.6的碳酸緩衝液)中,加於ELISA板孔中在4℃過夜,經清洗後即可應用。如果包被液中的蛋白質濃度過低,固相載體表面有能被此蛋白質完全覆蓋,其後加入的血清標本和酶結合物中的蛋白質也會部分地吸附於固相載體表面,最後產生非特異性顯色而導致本底偏高。在這種情況下,如在包被後再用1%~5%牛血清白蛋白包被一次,可以消除這種干擾。這一過程稱爲封閉(blocking)。包被好的ELISA板在低溫可放置一段時間而不失去其免疫活性。
3.1.4 (四)酶和底物
ELISA中所用的酶要求純度高、催化反應的轉化率高、專一性強、性質穩定、來源豐富、價格不貴、製備成的酶標抗體或抗原性質穩定,繼續保留着它的活性部分和催化能力。最好在受檢標本中不存在與標記酶相同的酶。另外它的相應底物應易於製備和保存,價格低廉,有色產物易於測定,光吸收高。ELISA中最常用的酶爲辣根過氧化酶(HRP)和從牛腸粘膜或大腸桿菌提取的鹼性磷酸酶(AP)。
HRP在蔬菜作物辣根中含量很高,純化方法也不復雜。它是一種糖蛋白,含糖量約18%;分子量爲44kD;是一種複合酶,由主酶(酶蛋白)和輔基(亞鐵血紅素)結合而成的一種卟啉蛋白質。主酶爲無色糖蛋白,在275nm波長處有最高吸收峯;輔基是深棕色的含鐵卟啉環,在403nm波長處有最高吸收峯。HRP催化下列反應:
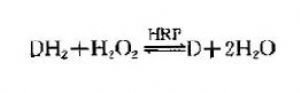
上式中DH2爲供氫體,H2O2O爲受氫體。HRP對受氫體的專一性很高,除H2O2外,僅作用於小分子醇的過氧化物和尿素的過氧化物。後者爲固體,作爲試劑較H2O2方便。許多化合物可作爲HRP的供氧體,在ELISA中常用的供氫體底物爲鄰苯二胺(orthopenylenediamine,OPD)、四甲基聯苯胺(3,3',5,5'-tetramethylbenzidine,TMB)和ABTS[2,2'-azino-bis(3-ethyl-benzthiazolinesulfonate-6)]。
OPD爲在ELISA中應用最多的底物,靈敏度高,比色方便。其缺點是配成應用液後穩定性差,而且具有致異變性。TMB無此缺點。TMB經酶作用後由無色變藍色,目測對比鮮明;加酸停止酶反應後變黃色,可在比色計中定量;因此應用日見增多。ABTS,雖然靈敏度不如OPD和TMB,但空白值很低。HRP催化OPD的反應如下:

HRP的純度用RZ(ReinheitZahl,意爲純度數)表示,是403nm的吸光度與280nm的吸光度之比,高純度的HRP的RZ≥3.0。應注意的是酶變性後,RZ可不變而活力降低,故重用酶製劑時更重要的指標爲活力。酶活力以單位表示:1min將1μmol的底物轉化爲產物的酶量爲1個單位。
在ELISA中另一常用的酶爲鹼性磷酸酶。從大腸桿菌提取的AP分子量爲80kD,酶作用的最適pH爲8.0;用小牛腸粘膜提取的AP分子量爲100kD,最適pH爲9.6。一般採用對硝基苯磷酸酯(p-nitrophenylphosphate,p-NPP)作爲底物。它可製成片狀試劑,使用方便。產物爲黃色的對硝基酚,在405nm有吸收峯。用NaOH終止酶反應後,黃色可穩定一段時間。反應式如下:
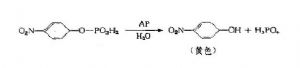
在ELISA中應用AP系統,其敏感性一般高於應用HRP系統,空白值也較低。但由於AP較難得到高純度製劑,穩定性較HRP低,價格較HRP高,製備酶結合物時得率較HRP低等原因,國內在ELISA中一般均採用HRP。
除HRP和AP以外,在商品ELISA試劑中應用的酶尚有葡萄糖氧化酶、β-半乳糖苷酶和脲酶等。β-半乳糖苷酸的底物常用4-甲基傘基-β-D半乳糖苷(4-mehtyumbelliferyl-β-D-galactoside),經酶水解後產生熒光物質4-甲基傘酮(4-mehtylumbelliferone),可用熒光計檢測。熒光的放大作用大大提高了方法的敏感度。AP也可應用可產生熒光的傘基磷酸酯作底物。其缺點是需要熒光計測定,而且如用固相載體直接作爲測定容器,此載體不可發出熒光。脲酶的特點是酶作用後反應液發生pH改變,可使指示劑變色;另外,在人體內沒有內源酶(酶的化學發光底物見第十八章)。
3.1.5 (五)結合物
酶標記的抗原或抗體稱爲結合物(conjugate)。抗原由於化學結構不同,可用不同的方法與酶結合。如爲蛋白質抗原,基本上可參考抗體酶標記的方法。製備抗體酶結合物的方法通常有以下幾種。
1.戊二醛交聯法戊二醛是一種雙功能團試劑,可以使酶與蛋白質或其他抗原的氨基通過它而偶聯。戊二醛交聯可用一步法(如連接AP),也可用二步法(如連接HRP)。舉例如下:
2~5mg純抗體與5mgAP混合於0.1mol/LpH6.8的磷酸緩衝液1ml中,4℃下對同上緩衝液透析平衡。磁力攪拌下,緩慢加入1%戊二醛0.05ml,在室溫下放置2小時。在4℃下對0.05mol/LpH8.0Tris緩衝液透析平衡,即得酶標抗體。
辣根過氧化物酶可溶解於50%飽和度硫酸銨中。用上法交聯後可用50%飽和度硫酸銨沉澱酶標抗體,棄去上清中游離酶。
戊二醛一步法操作簡便、有效,而且重複性好。缺點是交聯時分子間的比例不嚴格,大小也不一,影響效果。
製備HRP抗體結合物也可用二步法,即先將HRP與戊二醛作用,透析除去戊二醛,在pH9.5緩衝液中再與抗體作用而形成酶標抗體。此法的效率可高於一步法10倍左右。
2.過碘酸鹽氧化法本法只用於HRP的交聯。該酶含18%碳水化合物,過碘酸鹽將其分子表面的多糖氧化爲醛基。用硼氫化鈉(NaBH4)中和多餘的過碘酸。酶上的醛根很活潑,可與蛋白質結合,形成按摩爾比例結合的酶標結合物。有人認爲此法爲辣根過氧化物酶交聯最有效的方法。但也有隻認爲由於所用試劑較爲劇烈,各批實驗結果不易重複。
按以上方法製備的結合物一般混有未結合的酶和抗體。理論上結合物中混有遊離酶不影響ELISA中最後的酶活性測定,因經過洗滌,非特異性吸附於固相上的遊離酶已被洗去。但遊離的抗體則會與酶標抗體競爭相應的固相抗原,因而減低結合到固相上的酶標抗體量。因此製備的結合物應予以純化。純化的方法較多,分離大分子混合物的方法均可應用。硫酸銨鹽析法操作簡便,但效果不如用SephadexG-200凝膠過濾的好。
3.2 最適工作濃度的選擇
在建立某一ELISA測定中,應對包被抗原或抗體的濃度和酶標抗原或抗體的濃度予以選擇,以達到最合適的測定條件和節省測定費用。下面以間接法測抗體和夾心法測抗原爲例,介紹最適工作濃度的選擇方法。
3.2.1 (一)間接法測抗體
1.酶標抗抗體工作濃度的選擇
(2)將酶標抗人IgG用稀釋液作一系列稀釋後分別加入已包被的孔中,保溫、洗滌。
(3)加底物顯色。加酸終止反應後,讀取吸亮度(A),繪製曲線如圖15-10。讀取A值在1.0時的酶標抗體稀釋度,作爲酶標抗體的工作濃度。該酶標抗人IgG的工作濃度應爲1/1600。
(2)將強陽性參考血清、弱陽性參考血清和陰性參考血清用稀釋液作1:100稀釋,加樣,保溫,洗滌。
(3)加按工作濃度稀釋的酶標抗人IgG抗體,保溫,洗滌。
(4)加底物顯色。加酸終止反應後讀取A值。
(5)選擇強陽性參考血清的A值爲0.8左右、陰性參考血清的A值小於0.1的包被抗的的稀釋度作爲工作濃度。表15-1爲本例的測定結果,表中數字爲A值。從表中可見1:200爲最舒適的工作濃度。
| 各類血清 | 抗原稀釋度 | ||||
| 1:50 | 1:100 | 1:200 | 1:400 | 1:800 | |
| 強陽性 | 1.20 | 1.04 | 0.84 | 0.68 | 0.42 |
| 弱陽性 | 0.64 | 0.41 | 0.30 | 0.22 | 0.19 |
| 陰性 | 0.23 | 0.13 | 0.08 | 0.66 | 0.05 |
| 稀釋液 | 0.09 | 0.02 | 0.02 | 0.02 | 0.04 |
3.2.2 (二)夾心法測抗原
在夾心法ELISA法中可用棋盤滴定法同時選擇包被抗體和酶標抗體的工作濃度,舉例如下(表15-2):
| 包被抗體的濃度及酶標抗體稀釋度 | 參考抗原 | ||
| 強陽性(25ng/ml) | 弱陽性(1.5ng/ml) | 陰性 | |
| 10μg/ml | |||
| 1:1000 | 1.17 | 0.15 | 0.09 |
| 1:5000 | 0.46 | 0.03 | 0 |
| 1:25000 | 0.12 | 0 | 0 |
| 1μg/ml | |||
| 1:1000 | >2 | 0.25 | 0.10 |
| 1:5000 | 0.91 | 0.12 | 0.01 |
| 1:25000 | 0.25 | 0.01 | 0 |
| 0.1μg/ml | |||
| 1:1000 | 0.42 | 0.13 | 0.13 |
| 1:5000 | 0.11 | 0.03 | 0.02 |
| 1:25000 | 0.03 | 0 | 0 |
(1)抗體免疫球蛋白用包被緩衝液稀釋至蛋白濃度爲10、1和0.1μg/ml,分別在ELISA板上進行包被,每一濃度包括三個縱行,洗滌。
(2)在一個橫行各包被孔中加入強陽性抗原液,另一橫行加入弱陽性抗原液,第三橫行加入陰性對照液,保溫,洗滌。
(3)將酶標抗體用稀釋液稀釋成三個濃度,例如1:1000、1:5000和1:25000。分別加入每一包被濃度的一個縱行中,保溫,洗滌。
(4)加底物顯色。加酸終止反應後,讀取A值。
(5)以強陽性抗原的A值在0.8左右、陰性參考的A值小於0.1的條件作最適條件,據此選擇包被抗體和酶標抗體的工作濃度。從表15-2可看出包被抗體濃度可選用1μg/ml,酶標抗體的稀釋度可選爲1:5000。爲了進一步節省試劑,可以此濃度爲基點,縮小間距再做進一步的棋盤滴定。
3.3 測定方法的標準化
要使ELISA測定得到準確的結果,不論是定性的還是定量的,必須嚴格按照規定的方法製備試劑和實施測定。主要試劑的製備要點已如前述,其他一般性試劑,如包被緩衝液、洗滌液、標本稀釋液、結合物稀釋液、底物工作液和酶反應終止液等,配製時不可掉以輕心。緩衝液可於冰箱中短期保存,使用前應觀察是否變質。蒸餾水的質量在ELISA中也至關重要,最好使用新鮮重蒸餾的。不合格的蒸餾水可使空白值升高。
測定的實施中,應力求各個步驟操作的標準化,下面以板式ELISA爲例,介紹有關注意事項。
3.3.1 (一)加樣
在ELISA中除了包被外,一般需進行45加樣。在定性測定中有時不強調加樣量的準確性,例如規定爲加樣一滴。此時應該使用相同口徑的滴管,保持準確的加樣姿勢,使每滴液體的體積基本相同。在定量測定中則加樣量應力求準確。標本和結合物的稀釋液應按規定配製。加樣時應將液體加在孔底,避免加在孔壁上部,並注意不可出現氣泡。
3.3.2 (二)保溫
在ELISA中一般有二次抗原抗體反應,即加標本後和加結合物後,此時反應的溫度和時間應按規定的要求,保溫容器最好是水浴箱,可使溫度迅速平衡。各ELISA板不應疊在一起。爲避免蒸發,板上應加蓋,或將板平放在底部墊有溼紗布的溼盒中。溼盒應該是金屬的,傳熱容易。如用保溫箱,空溼盒應預先放在其中,以平衡溫度,這在室溫較低時更爲重要。加入底物後,反應的時間和溫度通常不做嚴格要求。如室溫高於20℃,ELISA板可避光放在實驗臺上,以便不時觀察,待對照管顯色適當時,即可終止酶反應。
3.3.3 (三)洗滌
洗滌在ELISA過程中不是反應聚,但卻是決定實驗成敗的關鍵。洗滌的目的是洗去反應液中沒有與固相抗原或抗體結合的物質以及在反應過程中非特異性吸附於固相載體的干擾物質。聚苯乙烯待塑料對蛋白質的吸附作用是普遍性的。因此在ELISA測定的反應過程中應儘量避免非特異性吸附,而在洗滌時又應把這種非特異性吸附的干擾物質洗滌下來。在標本和結合物的稀釋液和洗滌液中加入聚山梨酯(吐溫,Tween)一類物質即右達到此目的。聚山梨酯是聚氧乙烯去水山梨醇脂肪酸酯,爲非離子型的表面張力物質,常作爲助溶劑。根據脂肪酸的種類而對聚山梨酯編號,結合月桂酸的爲聚山梨酯20,在ELISA中最爲常用。它的洗滌效果好,並具有減少非特異性吸附和增強抗原抗體結合的作用。
洗滌如不徹底,特別在最後一次,如有酶結合物的非特異性吸附,將使空白值升高。另外,在間接法中如血清標本內的非特異性IgG吸附在固相上而未被洗淨,也將與酶標抗體作用而產生干擾。
ELISA板的洗滌一般可採用以下方法:①吸乾孔內反應液;②將洗滌液注滿板孔;③放置2min,略作搖動;④吸乾孔內液,也可傾去液體後在吸水紙上拍幹。洗滌的次數一般爲3~4次,有時甚至需洗5~6次。
3.3.4 (四)比色
如陰性對照顏色極淺,在定性測定中一般可採用目視比色。如用比色計測定結果,準確性決定於ELISA板底的平整與透明度和比色計的質量。