7 概述
古典式剖宮產術(classic cesarean section)又稱體位剖宮產術,由於其併發症多,目前已少用或不用。其特點是操作簡易迅速,可在緊急情況下迅速娩出胎兒,爭取搶救機會。缺點是切口部肌肉組織厚,縫合常不理想,出血多,再孕時子宮破裂率高,術後粘連發生率高。
剖宮產術到底起源何時,已很難考據。遠在公元前715~672年,古羅馬天主教就頒佈過法令,規定死亡的臨產婦或孕婦,未經剖腹取胎兒者禁止埋葬,這是屍體剖宮產術的起源。至16世紀初,見到有爲活孕婦施行剖宮產的記載。但在以後的300年內,剖宮產孕婦死亡率高達52%~100%,因手術不縫合子宮切口,死亡原因主要爲出血及感染。因爲手術非常危險,所以很少有人施行。至1876年意大利產科醫生波羅(Porro)於剖宮產同時從宮頸上切除了子宮,避免了產後出血及感染,成爲當時處理難產的一大進展。至1882年馬克斯·桑格(Maxsanger)首創了子宮底縱切口及縫合法,減少了出血,促進了癒合還保留了子宮,做出了革命性的貢獻。此手術名爲“保守性剖宮產術”或“古典式剖宮產術”(Classic Cesarena Section)。1907年弗蘭克(Frank)首先應用經腹腹膜外剖宮產,橫切口切開壁層腹膜,再切開膀胱腹膜反折,將壁層腹膜之上緣與髒層腹膜切口之上緣縫合關閉腹腔,然後切開子宮下段,減少了感染性病例併發腹膜炎的機會。至1908年拉茲科(Latzko)設計了從膀胱側窩進入子宮下段的途徑,後經諾頓(Norton)等人改進及描述,就是目前常用的側入式腹膜外剖宮產術。至1940年沃特斯(Waters)又首先找到了從膀胱頂進入子宮下段的途徑,於是產生了頂入式腹膜外剖宮產術。腹膜外剖宮產術,在防止感染上起了重要作用,但其操作複雜,容易損傷膀胱。克羅尼克(Kronig)分析了腹膜外剖宮產的特點是利用非收縮性的子宮下段以及用腹膜遮蓋切口,他應用這些原則於1912年提出切開膀胱子宮反折腹膜,暴露子宮下段而剖宮取胎的術式,即目前應用最廣泛的“子宮下段剖宮產術”。
目前,由於麻醉、剖宮手術技術的提高,輸血的進展,又受到圍生醫學、優生學、計劃生育等方面的影響。剖宮產的死亡率及圍生兒的死亡率均大大降低。剖宮產術已代替了困難的陰道助產術,併成爲諸多妊娠合併症的主要分娩途徑。剖宮產雖然是一種較安全的手術,但可增加出血和感染,也有因子宮切口感染而致產後晚期大出血者,有時需切除子宮,個別危及生命;亦有術中發生意外損傷和麻醉意外的,因此應嚴格掌握手術適應證。
古典式剖宮產,由於剖宮切口在子宮體部,該處肌肉組織厚,切開及縫合均不易,且出血多,術後粘連發生率高,再次妊娠時子宮破裂機會多,因此,不作爲主要選擇的術式(圖11.2.9.2-1~11.2.9.2-6)。
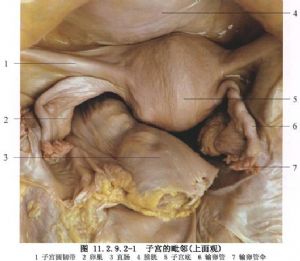
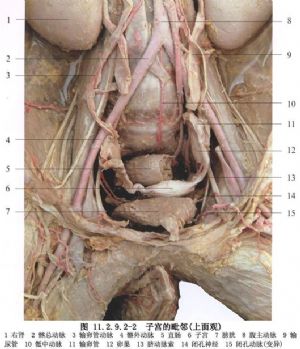
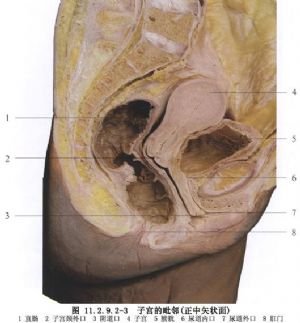

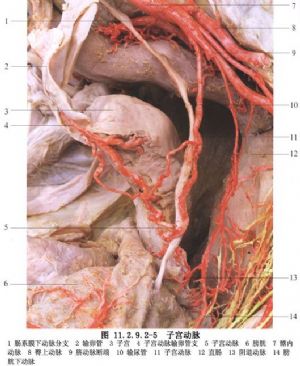

8 適應症
古典式剖宮產術適用於:
因各種原因如:①子宮下段嚴重粘連;②子宮下段形成不良;③子宮下段有肌瘤或被腫瘤侵蝕難分;④子宮極度前傾無法暴露子宮下段;⑤橫位,胎背在下者更易於取胎;⑥前置胎盤或部分前置胎盤附着於下段前壁,爲避免胎盤打洞者。
剖宮產指徵掌握恰當與否,是衡量產科工作水平的重要標誌。產科情況複雜,有些指徵很明確稱絕對指徵,如中央性前置胎盤、骨盆狹窄、產道梗阻等。而有些情況需仔細權衡方能做出判斷。總的原則是當分娩不可能經陰道完成,或經陰道分娩對母、嬰將有危險時應選擇剖宮產。
8.1 1.絕對指徵
(1)骨盆狹窄:骨盆經內、外測量其入口、中腔或出口中度以上狹窄者。
(2)頭盆不稱:是指骨盆徑線在正常範圍,但胎兒過大或胎頭與骨盆比例不相適應而使產程受阻,是目前剖宮產的主要指徵。
(4)軟產道異常:因軟產道異常而行剖宮產者較少見,但主要有下列情況:①軟產道梗阻,宮頸、陰道或外陰由於創傷或手術致嚴重瘢痕攣縮,可使分娩梗阻。此外,如子宮頸肌瘤、卵巢腫瘤、巨大生殖道疣、陰道先天發育異常阻礙先露下降者均需行剖宮產術。②宮頸癌陰道分娩可引起產道裂傷而有大出血的危險,宮頸癌還可導致癌腫擴散,應剖宮產。
(5)中央性前置胎盤:若孕齡達36周胎兒可活,應行選擇性剖宮產;若孕齡不足36周,陰道大出血不止者,亦應立即行剖宮產止血。
(7)臍帶脫垂:臍帶脫垂時胎兒生命有嚴重威脅,只要宮口未開全,不可能經陰道迅速分娩者。
8.2 2.相對指徵
(1)胎兒窘迫:引起胎兒窘迫的原因很多,對此指徵要慎重掌握,多觀察、多分析,但也不要猶豫而失去搶救時機。
(2)臀位:臀位足先露、初產婦年齡35歲以上、胎兒估計體重3.5kg以上、胎頭過度仰伸、合併過期妊娠等,應放寬剖宮產指徵。
(3)部分性前置胎盤或低置胎盤:當陰道流血多或胎兒窘迫者應剖宮產。有的臨牀表現爲反覆少量陰道流血,因一旦臨產宮口開大後有可能大出血,若醫院無充足血源條件,只要胎兒成熟可存活時,應及時剖宮產。
(4)過期妊娠:胎兒常不能耐受宮縮壓力而致窘迫甚至宮內死亡,若合併羊水過少或羊水明顯糞染,或檢測胎盤功能異常,或有胎兒宮內窘迫者應及時行剖宮產。
(5)早產、胎兒生長遲緩:這類胎兒對分娩時宮縮壓力難以耐受,且陰道分娩時易引起顱內損傷,若新生兒監護系統完善,早產兒存活率高可行剖宮產,而在胎兒無存活把握情況下,對剖宮產要慎重。
(6)妊娠高血壓綜合徵:子癇抽搐控制4h以後,不能迅速由陰道娩出者,先兆子癇經治療無效而引產條件不成熟者。
(7)心臟病:嚴重心臟功能代償不全達Ⅲ級以上者,應擇期剖宮產。
(8)其他妊娠合併症:如糖尿病、重症肝炎、甲狀腺功能亢進、血液疾病等常常不能耐受陰道分娩,可在內科醫生配合下,適時施術。
9 禁忌症
1.死胎 除產婦大出血、宮口尚未擴張、短期內不能娩出死胎,爲挽救產婦生命者外皆應設法令其陰道分娩,必要時碎胎。
2.畸胎 一般不考慮剖宮產。但若有危及孕婦生命的疾病,必須立刻終止分娩而經陰道又無法完成者,或少數畸形如聯體雙胎經陰道碎胎困難等,仍需剖宮取胎。
10 術前準備
10.1 1.手術時機的選擇
剖宮產手術時機選擇是否恰當,直接關係到母、嬰的安全。據統計,急診剖宮產母、嬰病率較擇期手術者高2~3倍,因此,儘可能減少急診剖宮產。一般而言,足月妊娠臨產後,子宮下段已形成、宮口部分開大、產婦尚不覺疲乏、胎兒無缺氧徵象,爲施行手術的最佳時機。
10.2 2.擇期剖宮產的術前準備
①需提前入院,對產前檢查時已有明確的手術指徵,或有可能施行剖宮產術的產婦,應在預產期前入院。②積極治療併發症,對有併發症者,應先積極治療,如妊娠高血壓綜合徵,應在經過治療而尚不能完全控制時選擇有利時機手術。孕婦貧血,應檢查原因及糾正貧血。孕婦合併心臟病有心力衰竭時應先控制心衰。合併感染時需積極抗感染等。③積極促胎兒成熟,對胎兒未成熟而又必須分娩的,及時促進胎肺成熟。擇期手術可以在做好一切準備下,待臨產開始後及早手術,亦可在臨產前認爲適合的時機進行。
10.3 3.急診剖宮產術前準備
急診剖宮產大都是在產程中遇到了困難,或因妊娠併發症病情突然變化而須立即終止妊娠的,約佔全部剖宮產的半數以上,其中一部分因入院較早,多已有相應處理。若爲急診入院,醫生應抓緊時間重點複習病史,做系統體格檢查及必要的輔診檢查,充分估計母、嬰情況,明確手術指徵。
10.4 4.具體準備事項
①糾正全身情況,根據不同病情予以相應處理,特別注意糾正產婦脫水,電解質紊亂,積極處理胎兒窘迫。如有失血性休克,應及時補足血容量。②備血,產科出血常常很急且量大,要隨時做好輸血的準備。產前已有出血者應在輸血同時手術,因產前大出血者都需手術纔能有效止血,故不可久待而延誤搶救時機。③備皮,按婦科腹部手術範圍準備。④置導尿管。⑤術前用藥,對感染或可能感染的產婦,應在手術前給予抗生素。對未成熟的胎兒。術前用藥促胎肺成熟。⑥做好搶救嬰兒的準備,包括氣管插管、臍血管注射等。最好有新生兒科醫師參加搶救。
11 麻醉和體位
1.硬膜外麻醉 方法簡單、肌肉鬆弛好,止痛完全,是目前國內剖宮產的首選麻醉。
2.局部麻醉 局部浸潤麻醉和神經阻滯麻醉對母、嬰安全,但肌肉鬆弛不良,止痛不全,情況緊急時可選用。
3.笑氣-氧氣平衡麻醉 對母、嬰無不良反應,止痛及肌肉鬆弛均較滿意,特別適用於有併發症的孕婦,如妊娠高血壓綜合徵、血液病及心臟病等。
傳統體位爲垂頭仰臥位,心臟病或呼吸功能不全者,可取平臥位。爲防止“仰臥位低血壓綜合徵”,應向左側臥傾斜10°~15°,被認爲是剖宮產最佳體位。
12 手術步驟
12.1 1.切開腹壁
古典式剖宮產腹壁切口位置應比下段剖宮產術高,常常需要超過臍部,可採用腹中線切口繞過臍部達臍上,但更宜取中線旁切口,全長之1、3在臍上,2、3在臍下。有利於暴露宮體,且可避免術後腹壁切口與子宮切口粘連。操作方法與子宮下段剖宮產相同。
12.2 2.顯露子宮、保護腹腔
術者沖洗手套後,探查腹腔,扶正子宮,然後於腹壁與子宮壁之間填塞紗布墊,藉以推開腸管、固定子宮便於操作,並完全遮閉腹腔,防止宮腔內容物溢入腹腔。
12.3 3.切開子宮
取子宮壁正中縱切口(圖11.2.9.2-7),位於兩側圓韌帶之間,其下端達腹膜反折以上。根據需要可向上延長,全長約12~13cm。先在宮體正中切一長約4~5cm的小口(圖11.2.9.2-8),注意保持胎囊完整,以左手示、中兩指伸入宮壁與胎囊之間作引導,右手握鈍頭剪刀向上、下延長切口(圖11.2.9.2-9)。刺破胎膜時要及時吸淨溢出的羊水。除作體部正中縱行切口外,有些特殊情況可以採用宮體橫切口、子宮底部切口、子宮後壁切口及子宮側壁切口等。

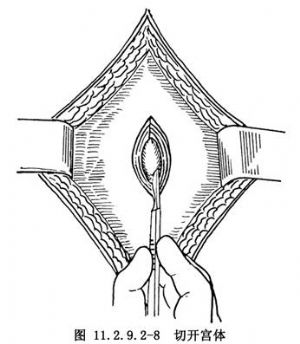

12.4 4.娩出胎兒
不論何種胎位,擴大胎膜破口後,術者右手伸入宮腔,握住胎足(單足或雙足),以臀牽引方式娩出胎兒。如爲單臀,則術者用手指勾胎兒腹股溝向外牽引,娩出臀部後按臀助產完成分娩。
12.5 5.娩出胎盤
因胎盤大部分附着於宮體部,故切口下遇到胎盤的機會較多,應迅速將胎盤推向一側娩出胎兒,一般都無困難。若切口下沒有胎盤也無大出血,應等待宮縮,待胎盤自然剝離後娩出。傳統操作系用卵圓鉗鉗夾創緣止血,但因子宮壁肌層厚,鉗夾止血對組織創傷大,使解剖關係破壞以致難於對合,影響切口癒合。現主張用小拉鉤或助手用示指鉤住切口上端,將整個切口拉緊,或在切口兩端各縫一針腸線提起拉緊,迫使血管及血竇閉合止血。
12.6 6.縫合子宮切口
用大圓針及1-0號鉻制腸線。有三種縫法。
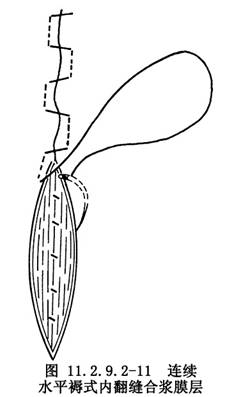
(1)連續+間斷+連續縫合法:第一層縫合肌層的內2/3(圖11.2.9.2-10),不穿透內膜,在子宮肌層與內膜交界處出針及進針,助手必須拉緊縫線,使內膜既不被縫入而又需能包蓋肌組織。第二層間斷縫合漿肌層,由漿膜面距切緣0.5cm進針,深達肌層2/3,在對側相應處出針,要包括第一層縫合的肌肉,縫在第一層兩針距之間。爲減少線結及節省時間,亦可採用“8”字形間斷縫合。第三層連續褥式內翻縫合漿膜層(圖11.2.9.2-11),進針應稍深,進針與出針間距不宜過長,保證漿膜內翻而不被撕裂。第三層也可用倫勃特(Lembert)連續縫合法,使切口邊緣內翻幷包埋縫線。若遇到子宮肌層水腫、組織脆弱,內翻縫合組織易被縫線切斷時,可採用“棒球縫合法”(圖11.2.9.2-12)。


(2)間斷+連續+連續縫合法:第一層間斷縫合肌層內2/3,一針一線先縫不打結,待全部縫完後再結紮(圖11.2.9.2-13),以免肌層過厚,最後縫合困難。另一種方法爲從黏膜面進針於肌層中部出針,對側於肌層中部進針,黏膜面出針,將結打在宮腔內,可避免線結對切口的刺激,有利癒合,但操作稍困難。第二層連續縫合肌層,恰於漿膜切緣內進針及出針,但不縫漿膜,深度要包括第一部分第一層包縫的肌肉,縫合完畢漿膜切緣幾乎完全對合,使第三層縫合易於進行(圖11.2.9.2-14)。第三層用連續褥式內翻縫合法。
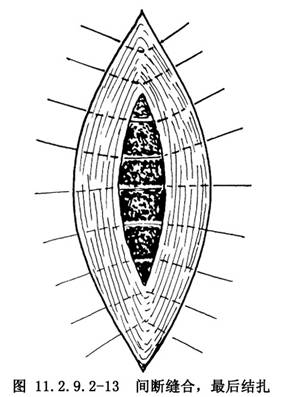

(3)三層連續縫合法:第一層連續縫合肌層內2/3;第二層連續縫肌層外2/3,於漿膜切緣進、出針,不縫漿膜;第三層連續褥式內翻縫合。三層連續縫合的方法簡單、迅速、止血良好,特別適合病情危重,急於結束手術的病例。
12.7 7.清理腹腔
吸淨溢入腹腔內的羊水及血液,若有胎便或感染性宮腔內容物溢入腹腔時,需用生理鹽水沖洗,然後扶正子宮,檢查兩側附件,用大網膜遮蓋子宮切口。清點紗布、敷料。
12.8 8.縫合腹壁。
13 術中注意要點
2.充分估計腹壁厚度,不可用力過猛一刀直入腹腔,甚至誤切子宮、損傷胎兒。
3.防止損傷膀胱及腸管,對產程時間長、子宮下段伸長的產婦,膀胱可隨子宮下段擴張而升高,腸管亦因脹氣而移向子宮前方,在切開腹膜時,必須辨認清楚。
4.刺破胎膜後要及時吸淨羊水,否則因宮壁血竇開放,易導致羊水栓塞。
5.因宮壁肌層較厚,切開時注意使兩側肌層等厚,否則影響縫合。
6.子宮壁切口宜先向下延長,然後向上,因下方子宮壁較薄易於剪開,也避免先剪開上方時血液向下流影響視野。
7.子宮切口下遇到胎盤時,應推開而避免在胎盤上打洞,以防出血過多。
8.宮壁切口厚,縫合難度較大,原則是先縫宮底部,後縫近下段的部分,由厚向薄,對合準確,不留空隙或死腔。
14 術後處理
古典式剖宮產術術後做如下處理:
14.1 1.一般處理
除觀察體溫、脈搏、呼吸及血壓外,特別要注意陰道流血及腹部傷口情況,定時按摩子宮,促進宮縮,壓出宮腔積血。
14.2 2.應用縮宮劑
術後輸液時,每日應用縮宮素10U,連續2~3d,對改善子宮收縮、促進術後恢復和減少出血均有利。
14.3 3.體位
術後平臥6h即可改爲半臥位,鼓勵早期下地活動。一般術後24h即可起牀下地走動。
14.4 4.輸液
手術後一般不需禁食,但在肛門尚未排氣前暫進流質飲食,故需適量補液。排氣後改進半流質,酌情決定是否輸液。
14.5 5.留置尿管
原則上術後可不必留置尿管,必要時酌情留置12~24h。
14.6 6.抗生素預防感染
迄今尚無統一看法,應根據產婦的情況如術前肛門指檢或陰道檢查的次數、產程長短、胎膜早破、有無併發症等來決定是否應用。若需用藥,則主張選用廣譜抗生素,要求量足、療程短、且在術前即用第一次,維持2~3d即可。
15 併發症
15.1 術中併發症及處理
原因:①由於仰臥位妊娠子宮壓迫下腔靜脈使回心血量不足;②硬膜外麻醉範圍過廣,交感神經廣泛阻滯導致周圍血管擴張,靜脈回心血量減少,甚至因交感神經阻滯而使心肌收縮力減弱。有效循環血量減少,引起血壓下降或伴有頭暈眼花、甚至暈厥等症狀。
防治:①術前對脫水、失血者儘量補足血容量;②選腰L2~L3間隙進針防止麻醉平面過高;③施行椎管內阻滯時應先建立靜脈通道,及時補充血容量;④術時取左側15°~30°臥位,或仰臥位血壓下降後改左側臥位;⑤進入腹腔後操作應輕巧,避免牽拉刺激;⑥吸氧;⑦當血壓降至90/60mmHg或下降原值的20%時,可發生胎兒窘迫,應進行必要的升壓處理,如限制麻醉用藥,加快補液速度,使用麻黃鹼15~20mg靜脈注射等,並停止操作,待血壓回升後儘快娩出胎兒。
(1)子宮切口出血:施行子宮下段剖宮產術時,若切口部位有較粗大血管,或前置胎盤附着於子宮前壁或與切口鄰近時,則切口出血較多。
處理:術中如發現子宮壁切口表面有粗大曲張血管時可先在預定切口上下將血管縫扎,可避免切開宮壁時出血。遇有子宮切口出血時,可先鉗夾出血部位,待娩出胎盤,拭淨宮腔後迅速縫合子宮切口止血。通常按常規縫合子宮切口後即可止血,如仍有出血可用腸線或絲線縫合止血,注意縫線不應穿透子宮內膜層。縫合切口兩側角均應超越0.5cm左右,以免因血管退縮而漏縫。
(2)子宮切口裂傷及血管破裂出血:剖宮產術中子宮切口裂傷常見於子宮下段橫切口剖宮產術。切口裂傷可沿宮頸向下,甚至延長至陰道壁上段,或向兩側橫行撕裂,裂傷可以波及子宮血管,甚至延伸向闊韌帶。
子宮切口裂傷出血的常見原因有子宮切口過小,子宮切口過低,胎頭過大,胎頭過低,產程延長局部受壓致組織水腫,娩頭過急,用力不當或手法粗暴等。
預防:子宮切口的高度一般在反折腹膜下1.5~2.0cm,胎頭深陷者切口應稍低,可選擇在反折腹膜下3cm處,切口大小通常以10~12cm長度爲宜,兩端應呈向上的弧形。對於胎頭嵌頓骨盆者,應在術前做好外陰消毒,一旦胎頭娩出困難可由助手自陰道上推胎頭,可減少術者娩頭的困難,娩頭時可將胎頭轉成枕前位或枕橫位以縮小胎頭娩出徑線,轉胎頭時要輕柔。也可置入雙葉產鉗,將胎頭牽出,以免因暴力娩頭造成子宮切口撕裂。
處理:迅速鉗夾切口撕裂的尖端及出血血管,及時縫扎止血,不可縫合過密,造成血供不良引起晚期產後出血。當裂傷延及闊韌帶時,注意勿損傷輸尿管,必要時遊離輸尿管後再結紮止血。
(3)宮腔內表面局部出血:多是胎盤剝離出血,尤其是前置胎盤的剝離面,其特點是即使宮縮良好,局部仍有明顯出血。可在看清出血部位後迅速採用1號腸線“8”字縫合出血部位,但要注意勿穿透子宮全層而誤傷周圍組織。
(4)子宮弛緩性出血:是產後出血的最常見原因,可採用以下措施:
藥物治療:縮宮素20U宮體及子宮下段多點注射,或麥角新鹼0.2mg靜脈注入或注射於子宮下段,或(和)卡孕栓1mg口含或納肛。
按摩子宮:將子宮提出腹腔,雙手按摩子宮或溫鹽水紗布按摩子宮,多能奏效。
填塞宮紗:上述方法無效時可填塞宮紗,證實有效後將一端經宮口放置於陰道內,隨後縫合子宮切口,12~24h後可取出紗條。
縫扎大血管:上述方法無效時,可結紮子宮動脈上行支或結紮髂內動脈。日後血管可再通,仍可保留生育功能。
切除子宮:上述方法無效時要當機立斷切子宮,避免出現難以逆轉的休克。
(5)胎盤粘連或植入出血:一般對剝離面採用腸線“8”字縫合止血,如無效可結紮子宮動脈,宮腔填塞紗條等,必要時切除子宮。
3.臟器損傷
(1)膀胱損傷:剖宮產時膀胱損傷見於以下情況:切開壁層腹膜時因粘連或膀胱位置高而誤傷;子宮下段剖宮產分離膀胱時因粘連而損傷;腹膜外剖宮產分離膀胱筋膜時損傷;娩出胎頭時子宮切口撕裂而累及膀胱。一旦發生損傷要及時修補。用2-0或3-0腸線縫合膀胱肌層及漿肌層,最好不穿透黏膜,以免日後形成結石。術後持續導尿7~14d,抗生素預防感染。及時發現,及時修補則預後較好。
(2)腸管損傷:剖宮產術中腸管損傷罕見,見於前次腹腔手術史或盆腹腔嚴重感染致盆腹腔廣泛粘連者。處理:發現爲小腸損傷立即修補,術後胃腸減壓,給予廣譜抗生素。如爲結腸損傷,可先行造瘻,控制腹腔感染,待損傷癒合後,再閉合結腸瘻,損傷小者也可以直接修補。
(3)輸尿管損傷:剖宮產中輸尿管損傷少見,發生於子宮切口撕裂累及輸尿管,或因裂傷處出血,盲目鉗夾、縫扎止血所致,也可見於剖宮產產後出血切除子宮時。損傷後及時發現、及時修補非常重要,一旦形成輸尿管陰道瘻等會給產婦帶來很大痛苦。
4.羊水栓塞 剖宮產術中羊水栓塞的原因:①宮腔內壓力過高如強直性子宮收縮,擠壓宮底使宮腔內壓力過高,羊水沿裂傷的宮頸內靜脈或胎盤邊緣血竇進入母體血循環;②子宮血管異常開放如子宮破裂、前置胎盤、胎盤早剝等使子宮血管異常開放,羊水由此進入母體血循環;③子宮切口血管開放,古典式剖宮產更易發生。
臨牀表現與進入母血的羊水量及性狀有關,輕者僅表現爲一過性的寒戰,胸悶,嚴重者可引起呼吸困難、紫紺、休克、DIC等。
預防措施:切開子宮及破膜後,及時吸淨羊水,然後娩出胎頭,子宮切口足夠大,以防擠壓宮底時因阻力過大而使宮腔內壓增高,胎兒娩出後,待吸淨殘留羊水後再娩出胎盤。
15.2 術後併發症及處理
(1)術後病率與感染:剖宮產術後病率與感染是陰道分娩的10~20倍。細菌通過各種途徑侵入手術切口及胎盤剝離面而引起產褥期生殖器及全身的感染。剖宮產術後感染除與細菌種類、數量和毒性有關外,機體的抗病能力是一重要因素。
易感因素:妊娠合併營養不良、貧血、糖尿病、生殖道感染和胎膜早破、產程延長、頻繁的陰道檢查及肛查和胎兒內監護、止凝血功能不佳、消毒不嚴、器械污染等。
處理:對有易感因素者手術前後預防性應用抗生素,宜行腹膜外剖宮產,已感染者應給予敏感或廣譜抗生素治療。
(2)腹壁與子宮切口感染、子宮腹壁瘻:腹壁與子宮切口感染除與一般易感因素有關外,還與縫線反應,縫合部組織壞死,血腫形成等有關。子宮腹壁瘻系由子宮切口感染,壞死,並與腹壁粘連形成瘻管所致。子宮腹壁瘻的診斷主要依據碘油造影或向瘻道內注入亞甲藍液觀察是否經陰道流出。對腹壁切口感染範圍小者可行清除術,範圍大者應行擴創,儘量切除壞死組織和縫線,促使傷口癒合。對已形成子宮腹壁瘻者,治療方法有:局部引流,搔刮,碘仿紗條填塞,配合抗生素治療,促使瘻道閉合;開腹探查並切除瘻管;病情嚴重者需切除子宮。
(3)子宮切口癒合不良:影響子宮切口癒合的因素:①全身因素:貧血、感染、低蛋白血症、維生素B及C族缺乏以及不適當的應用皮質激素等都不利於切口的癒合。②切口部位:子宮下段橫切口優於子宮體部各類切口,但如在子宮下段與體部交界處切開也妨礙切口癒合。③操作:縫合的鬆緊疏密應適度,對合應整齊,止血牢靠,但應避免多次盲目縫扎。
處理:加強支持治療,應用廣譜抗生素及縮宮劑,對造成嚴重晚期產後出血保守治療無效者,需清除壞死組織再縫合,如感染嚴重者可考慮子宮切除。
(4)剖宮產術後晚期出血:指手術分娩24h後,在產褥期內發生的大出血,一般發生在術後2~6周,多發生在術後10~19d內。
原因:①胎盤附着部位復舊不全:多因感染而影響胎盤附着部位復舊,當局部蛻膜脫落時出血。②子宮切口癒合不佳或感染裂開:常因術中子宮切口出血,反覆縫合過密過緊所致。③胎盤、胎膜殘留出血:少見。④子宮內膜炎。
處理:①使用一種或多種宮縮劑。②應用廣譜抗生素。③疑有胎盤胎膜殘留時可在上述治療3~5d,在做好開腹手術準備後行清宮術。④上述治療無效時,可行血管栓塞術或切除子宮。
(5)栓塞性靜脈炎:剖宮產術後血栓栓塞性靜脈炎有兩類,即由感染引起的膿毒性盆腔血栓靜脈炎和非感染因素所致的盆腔、下肢靜脈血栓栓塞。
①膿毒性血栓性靜脈炎:是一種嚴重而少見的盆腔感染性合併症,常見於產褥感染或剖宮產術後感染,分爲盆腔內血栓性靜脈炎及下肢血栓性靜脈炎。
患者術後盆腔及下肢靜脈血流緩慢,若有感染因素存在則可能引起盆腔靜脈炎。
臨牀表現及診斷:盆腔血栓性靜脈炎常爲單側,多在產後1~2周出現寒戰、高熱及下腹疼痛,宮頸舉痛,宮體壓痛,宮旁深壓痛。婦科檢查後可因促發菌血症而引起急劇的高熱。血細菌培養爲陽性。下肢血栓性靜脈炎患側疼痛、腫脹,皮膚發白,局部溫度升高,有時可觸及靜脈栓塞所致的硬條索狀物及壓痛。小腿深部靜脈栓塞時出現腓腸肌及足底疼痛及壓痛,背屈踝關節可引起小腿深部肌肉牽拉性疼痛。還可以通過測下肢靜脈壓或超聲多普勒測下肢血管血流圖而協助診斷。下肢血栓性靜脈炎病程長,往往需待側支循環建立後腫脹才逐漸消失。
處理:臥牀、抬高患肢;選用強有效的抗菌藥物;肝素50mg加入5%葡萄糖溶液200ml中,靜滴6h,連續用10d,一般用藥後1~2d病情即可改善,肝素治療無效者應多考慮有無盆腔膿腫形成;下肢靜脈血栓可在使用肝素的基礎上應用尿激酶及低分子右旋糖酐。手術治療僅適用於藥物治療無效、膿毒性血栓繼續擴展及禁忌使用抗凝治療者。手術範圍包括下腔靜脈結紮、卵巢靜脈結紮和下肢靜脈結紮。術後繼續使用抗生素及抗凝治療。
病因:妊娠晚期血液呈高凝狀態,盆腔及下肢靜脈血流緩慢;妊娠併發妊高徵時血液濃縮、血管壁受損;剖宮產體位及硬膜外麻醉時下肢靜脈擴張、血流淤滯;術後仰臥位、活動少;靜脈輸注液體。
臨牀表現及診斷:除因感染因素所致的高熱外,臨牀表現與膿毒血栓性靜脈炎相似。“股白腫”是因下肢深、淺靜脈均形成血栓所致,表現特異。小腿深靜脈血栓的症狀隱蔽,水腫不明顯。
處理:與膿毒性血栓性靜脈炎相似,對有動脈痙攣而致劇痛者,可應用血管解痙劑,如罌粟鹼、妥拉蘇林等。對保守治療無效者,可行深部靜脈血栓摘除術。
(6)腸梗阻:偶有發生,機械性腸梗阻多由腸粘連所致,麻痹性腸梗性腸梗阻可可由嚴重的腹脹或機械性腸梗阻發展而來。治療以胃腸減壓、補液、抗炎爲主,保守治療無效時,應儘早剖腹探查。
(7)子宮內膜異位症:剖宮產術後子宮內膜異位症常見於腹壁切口處,硬結隨月經週期增大伴疼痛,保守治療效果不佳。縫合子宮切口時不縫子宮內膜,認真沖洗切口有可能避免剖宮產術後的子宮內膜異位症。
(8)剖宮產兒綜合徵:剖宮產娩出之新生兒,由於未受產道擠壓,體內缺乏纖溶酶和免疫因子,容易發生肺透明膜病而致呼吸窘迫,稱之爲剖宮產兒綜合徵。其臨牀特點爲出生時正常,生後4~6h發病,出現進行性呼吸困難,逐漸出現發紺伴呼氣性呻吟等缺氧爲主症的徵候羣。更易發生於早產、IUGR和糖尿病產婦之新生兒。爲預防剖宮產兒綜合徵,術時採取左側傾斜15°~30°,注意掌握麻醉深度,對於高危新生兒產後可給予卵磷脂製劑氣管內滴入或超聲霧化吸入。治療包括保溫、保持呼吸道通暢、吸氧、糾正水、電解質及酸鹼平衡,預防性應用抗生素等措施。