2 一、概述
近年來,隨着人民生活水平的不斷提高,飲食習慣和飲食結構的改變以及人口老齡化,我國結直腸癌(colorectal cancer,CRC)的發病率和死亡率均保持上升趨勢。其中,結腸癌的發病率上升尤爲顯著。大多數患者發現時已屬於中晚期。
爲進一步規範我國結直腸癌診療行爲,提高醫療機構結直腸癌診療水平,改善結直腸癌患者預後,保障醫療質量和醫療安全,特制定本規範。
3 二、診斷技術與應用
3.1 (一)臨牀表現。
早期結直腸癌可無明顯症狀,病情發展到一定程度纔出現下列症狀:
3.腹痛或腹部不適。
4.腹部腫塊。
5.腸梗阻。
3.2 (二)體格檢查。
1.一般狀況評價、全身淺表淋巴結情況。
3.直腸指檢:凡疑似結直腸癌者必須常規作肛門直腸指診。瞭解腫瘤大小、質地、佔腸壁周徑的範圍、基底部活動度、距肛緣的距離、腫瘤向腸外浸潤狀況、與周圍臟器的關係等。指檢時必須仔細觸摸,避免漏診;觸摸輕柔,切忌擠壓,觀察是否指套血染。
3.3 (三)實驗室檢查。
2.尿常規:觀察有無血尿,結合泌尿系影像學檢查瞭解腫瘤是否侵犯泌尿系統。
3.4 (四)內窺鏡檢查。
所有疑似結直腸癌患者均推薦纖維結腸鏡或電子結腸鏡檢查,但以下情況除外:
1.一般狀況不佳,難以耐受;
內窺鏡檢查之前,必須做好準備,檢查前進流質飲食,服用瀉劑,或行清潔洗腸,使腸腔內糞便排淨。
內窺鏡檢查報告必須包括:進鏡深度、腫物大小、距肛緣位置、形態、局部浸潤的範圍,結腸鏡檢時對可疑病變必須病理學活組織檢查。
由於結腸腸管在檢查時可能出現皺縮,因此內窺鏡所見腫物距離肛門距離可能存在誤差,建議結合CT或鋇劑灌腸明確病竈部位。
3.5 (五)影像檢查。
1.結腸鋇劑灌腸檢查,特別是氣鋇雙重造影檢查是診斷結直腸癌的重要手段。但疑有腸梗阻的患者應當謹慎選擇。
2.B型超聲:超聲檢查可瞭解患者有無復發轉移,具有方便快捷的優越性。
3.CT檢查:CT檢查的作用在於明確病變侵犯腸壁的深度,向壁外蔓延的範圍和遠處轉移的部位。目前,結直腸病變的CT檢查推薦用於以下幾個方面:
(2)發現復發腫瘤;
(4)闡明鋇劑灌腸或內窺鏡發現的腸壁內和外在性壓迫性病變的內部結構,明確其性質;
(5)對鋇劑檢查發現的腹內腫塊作出評價,明確腫塊的來源及其與周圍臟器的關係。
4.MRI檢查:MRI檢查的適應證同CT檢查。推薦以下情況首選MRI檢查:(1)直腸癌的術前分期;(2)結直腸癌肝轉移病竈的評價;(3)懷疑腹膜以及肝被膜下病竈。
5. 經直腸腔內超聲:推薦直腸腔內超聲或內鏡超聲檢查爲中低位直腸癌診斷及分期的常規檢查。
6.PET-CT:不推薦常規使用,但對於常規檢查無法明確的轉移復發病竈可作爲有效的輔助檢查。
7.排泄性尿路造影:不推薦術前常規檢查,僅適用於腫瘤較大可能侵及尿路的患者。
3.6 (六)血清腫瘤標誌物。
結直腸癌患者在診斷、治療前、評價療效、隨訪時必須檢測CEA、CA19-9;建議檢測CA242、CA72-4;有肝轉移患者建議檢測AFP;有卵巢轉移患者建議檢測CA125。
3.7 (七)病理組織學檢查。
病理活檢明確佔位性質是結直腸癌治療的依據。活檢診斷爲浸潤性癌的病例進行規範性結直腸癌治療。如因活檢取材的限制,活檢病理不能確定浸潤深度,診斷爲高級別上皮內瘤變的病例,建議臨牀醫師綜合其他臨牀情況,確定治療方案。確定爲復發或轉移性結直腸癌時,檢測腫瘤組織K-ras基因狀態。
3.8 (八)開腹探查。
如下情況,建議行開腹探查:
2.出現腸梗阻,進行保守治療無效。
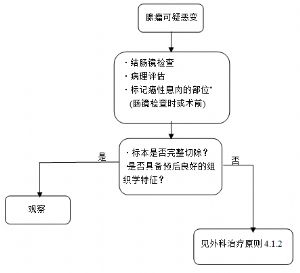
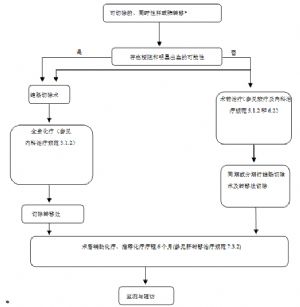
3.9 (九)結直腸癌的診斷步驟。
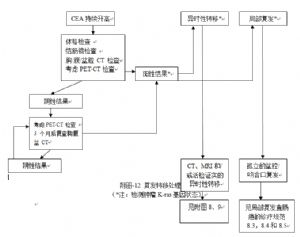
結直腸癌診斷步驟參見附圖-1。
3.10 (十)結直腸癌的鑑別診斷。
1.結腸癌應當主要與以下疾病進行鑑別:
(1)潰瘍性結腸炎。本病可以出現腹瀉、黏液便、膿血便、大便次數增多、腹脹、腹痛、消瘦、貧血等症狀,伴有感染者尚可有發熱等中毒症狀,與結腸癌的症狀相似,纖維結腸鏡檢查及活檢是有效的鑑別方法。
(2)闌尾炎。回盲部癌可因局部疼痛和壓痛而誤診爲闌尾炎。特別是晚期回盲部癌,局部常發生壞死潰爛和感染,臨牀表現有體溫升高,白細胞計數增高,局部壓痛或觸及腫塊,常診斷爲闌尾膿腫,需注意鑑別。
(3)腸結核。在我國較常見,好發部位在迴腸末端、盲腸及升結腸。常見症狀有腹痛、腹塊、腹瀉、便祕交替出現,部分患者可有低熱、貧血、消瘦、乏力,腹部腫塊,與結腸癌症狀相似。但腸結核患者全身症狀更加明顯,如午後低熱或不規則發熱、盜汗、消瘦乏力,需注意鑑別。
(4)結腸息肉。主要症狀可以是便血,有些患者還可有膿血樣便,與結腸癌相似,鋇劑灌腸檢查可表現爲充盈缺損,行纖維結腸鏡檢查並取活組織送病理檢查是有效的鑑別方法。
(5)血吸蟲性肉芽腫。多見於流行區,目前已少見。少數病例可癌變。結合血吸蟲感染病史,糞便中蟲卵檢查,以及鋇劑灌腸和纖維結腸鏡檢查及活檢,可以與結腸癌進行鑑別。
(6)阿米巴肉芽腫。可有腸梗阻症狀或查體捫及腹部腫塊與結腸癌相似。本病患者行糞便檢查時可找到阿米巴滋養體及包囊,鋇劑灌腸檢查常可見巨大的單邊缺損或圓形切跡。
2.直腸癌應當與以下疾病進行鑑別:
(1)痔。痔和直腸癌不難鑑別,誤診常因未行認真檢查所致。痔一般多爲無痛性便血,血色鮮紅不與大便相混合,直腸癌便血常伴有黏液而出現黏液血便和直腸刺激症狀。對便血病人必須常規行直腸指診。
(2)肛瘻。肛瘻常由肛竇炎而形成肛旁膿腫所致。患者有肛旁膿腫病史,局部紅腫疼痛,與直腸癌症狀差異較明顯,鑑別比較容易。
(3)阿米巴腸炎。症狀爲腹痛、腹瀉,病變累及直腸可伴裏急後重。糞便爲暗紅色或紫紅色血液及黏液。腸炎可致肉芽及纖維組織增生,使腸壁增厚,腸腔狹窄,易誤診爲直腸癌,纖維結腸鏡檢查及活檢爲有效鑑別手段。
4 三、病理評估
4.1 (一)標本固定標準。
1.固定液:推薦使用10~13% 中性福爾馬林固定液,避免使用含有重金屬的固定液。
2.固定液量:必須 ≥ 所固定標本體積的10倍。
3.固定溫度:正常室溫。
4.固定時間:內鏡下切除腺瘤或活檢標本:≥6小時,≤48小時。
手術標本:≥12小時,≤48小時。
4.2 (二)取材要求。
(3)將標本包於紗布或柔軟的透水紙中以免丟失。
(3)垂直於腸壁,每間隔0.3cm平行切開標本,分成適宜大小的組織塊,推薦按同一包埋方向全部取材。記錄組織塊對應的方位。
3. 手術標本。
(1)腸壁及腫瘤。
①沿腸壁長軸、垂直於腸壁切取腫瘤標本,腫瘤組織充分取材,視腫瘤大小、浸潤深度、不同質地、顏色等區域分別取材(常規4塊),腫瘤浸潤最深處至少1塊全層厚度腫瘤及腸壁組織,以判斷腫瘤侵犯的最深層次。切取能夠顯示腫瘤與鄰近粘膜關係的組織(常規2塊)。
②切取遠側、近側手術切緣。環周切緣按手術醫師標記的部分切取。
③記錄腫瘤距遠側及近側切緣的距離。
④腸標本如包含回盲部或肛管、肛門,應當於迴盲瓣、齒狀線、肛緣取材(常規各1塊)及闌尾(常規3塊:環形2塊+盲端1塊);如腫瘤累及上述部位,應當切取充分顯示病變程度的組織塊。
⑤行中低位直腸癌根治術時需要完整切除直腸系膜,因此病理醫師需要對手術標本進行系統檢查,包括系膜的完整性、環周切緣是否有腫瘤侵犯,這是評價全直腸系膜切除手術效果的重要指標。
(2)淋巴結。
建議外科醫師根據局部解剖體徵和術中所見,分組送檢淋巴結,有利於淋巴結引流區域的定位;在未接到手術醫師分組送檢醫囑或標記的情況下,病理醫師按照以下原則檢出標本中的淋巴結:
全部淋巴結均需取材(建議檢出至少12枚淋巴結。接受過術前治療患者的淋巴結可以低於12枚)。所有肉眼陰性的淋巴結應當完整送檢,肉眼陽性的淋巴結可部分切取送檢。
(3)推薦取材組織塊體積:不大於2×1.5×0.3cm。
4.3 (三)取材後標本處理原則和保留時限。
1.剩餘標本的保存。取材剩餘組織保存在標準固定液中,並始終保持充分的固定液量和甲醛濃度,避免標本乾枯或因固定液量不足或濃度降低而致組織腐變;以備根據鏡下觀察診斷需求而隨時補充取材;以備在病理診斷報告簽發後接到臨牀反饋信息時複查大體標本或補充取材。
2.剩餘標本處理的時限。建議在病理診斷報告簽發1個月後,未接到臨牀反饋信息,未發生因外院會診意見分歧而要求複審等情形後,可由醫院自行處理。
4.4 (四)病理類型。
1.早期結直腸癌。
癌細胞限於結直腸黏膜下層者稱早期結直腸癌(pT1)。WHO消化道腫瘤分類將黏膜層內有浸潤的病變亦稱之爲“高級別上皮內瘤變”。
2.進展期結直腸癌的大體類型。
(3)浸潤型。腫瘤向腸壁各層瀰漫浸潤,使局部腸壁增厚,但表面常無明顯潰瘍或隆起。
3. 組織學類型。
(1)腺癌:①乳頭狀腺癌;②管狀腺癌;③黏液腺癌;④印戒細胞癌;
(2)未分化癌;
(3)腺鱗癌;
(4)鱗狀細胞癌;
(5)小細胞癌;
(6)類癌。
4. 分級與組織學類型的關係。
表1 分級與組織學類型的關係
4.5 (五)病理報告內容。
(2)如有上皮內瘤變(異型增生),報告分級。
(3)如有癌變,區分組織學類型。
臨牀醫師應當瞭解受活檢取材深度限制,活檢病理不能完全確定浸潤深度,故癌變組織可能爲侷限於粘膜內的癌(高級別上皮內瘤變或粘膜內癌)。
(3)上皮內瘤變(異型增生)的分級。
如有癌變,報告癌變組織的組織學分型、分級、浸潤深度、切緣情況、脈管侵犯情況。
pT1、Ⅲ與Ⅳ級分化、脈管侵犯、切緣陽性,臨牀應當再行外科手術擴大切除範圍。其他情況腸鏡下切除已足夠,但術後需定期隨訪。
①癌變的腺瘤中有癌細胞浸潤穿透黏膜肌層到達黏膜下層(pT1)。
②預後良好的組織學特徵包括:Ⅰ或Ⅱ級分化,無血管、淋巴管浸潤,“切緣陰性”。
③預後不良的組織學特徵包括:Ⅲ或Ⅳ級分化,血管、淋巴管浸潤,“切緣陽性”。
④陽性切緣定義爲:腫瘤距切緣小於1mm或電刀切緣可見癌細胞。
3. 手術標本的病理報告內容和要求:
(2)大體情況:腫瘤大小、大體類型、肉眼所見浸潤深度、切除腸管兩端距腫瘤遠近端的長度。
(4)腫瘤浸潤深度(T分期)(T分期或ypT是根據有活力的腫瘤細胞來決定的,經過新輔助治療的標本內無細胞的黏液湖不認爲是腫瘤殘留)。
(6)近端切緣、遠端切緣的狀況。
(7)建議報告環周切緣的狀況(如果腫瘤距切緣很近,應當在顯微鏡下測量並報告腫瘤與切緣的距離,腫瘤距切緣1mm以內報切緣陽性)。
(8)脈管侵犯情況(以V代表血管,V1爲鏡下血管浸潤,V2爲肉眼血管浸潤,L代表淋巴管)。
(9)神經侵犯。
(10)K-ras基因狀態,確定爲復發或轉移性結直腸癌時。如無手術切除標本可從活檢標本中測定。
完整的病理報告的前提是臨牀醫師填寫詳細的病理診斷申請單,詳細描述手術所見及相關臨牀輔助檢查結果並清楚標記淋巴結。臨牀醫師與病理醫師的相互交流、信任和配合是建立正確分期和指導臨牀治療的基礎。
4.6 附:結直腸癌TNM分期
美國癌症聯合委員會(AJCC)/國際抗癌聯盟(UICC)結直腸癌TNM分期系統(2010年第七版)
原發腫瘤(T)
Tx 原發腫瘤無法評價
T0 無原發腫瘤證據
Tis 原位癌:侷限於上皮內或侵犯黏膜固有層
T1 腫瘤侵犯黏膜下層
T2 腫瘤侵犯固有肌層
T3 腫瘤穿透固有肌層到達漿膜下層,或侵犯無腹膜覆蓋的結直腸旁組織
區域淋巴結(N)
Nx 區域淋巴結無法評價
N1c 漿膜下、腸繫膜、無腹膜覆蓋結腸/直腸周圍組織內有腫瘤種植(TD, tumor deposit),無區域淋巴結轉移
遠處轉移(M)
M0 無遠處轉移
M1 有遠處轉移
M1a 遠處轉移侷限於單個器官或部位(如肝,肺,卵巢,非區域淋巴結)
解剖分期/預後組別
期別 T N M Dukes MAC 0 Tis N0 M0 - - Ⅰ T1 N0 M0 A A T2 N0 M0 A B1 ⅡA T3 N0 M0 B B2 ⅡB T4a N0 M0 B B2 ⅡC T4b N0 M0 B B3 ⅢA T1-2 N1/N1c M0 C C1 T1 N2a M0 C C1 ⅢB T3-4a N1/N1c M0 C C2 T2-3 N2a M0 C C1/C2 T1-2 N2b M0 C C1 ⅢC T4a N2a M0 C C2 T3-4a N2b M0 C C2 T4b N1-2 M0 C C3 ⅣA 任何T 任何N M1a - - ⅣB 任何T 任何N M1b - -
注:1.cTNM是臨牀分期,pTNM是病理分期;前綴y用於接受新輔助(術前)治療後的腫瘤分期(如ypTNM),病理學完全緩解的患者分期爲ypT0N0cM0,可能類似於0期或1期。前綴r用於經治療獲得一段無瘤間期後復發的患者(rTNM)。
Dukes B期包括預後較好(T3N0M0)和預後較差(T4N0M0)兩類患者,Dukes C期也同樣(任何TN1M0和任何TN2M0)。MAC是改良Astler-Coller分期。
2.Tis包括腫瘤細胞侷限於腺體基底膜(上皮內)或黏膜固有層(黏膜內),未穿過黏膜肌層到達黏膜下層。
3.T4的直接侵犯包括穿透漿膜侵犯其他腸段,並得到鏡下診斷的證實(如盲腸癌侵犯乙狀結腸),或者位於腹膜後或腹膜下腸管的腫瘤,穿破腸壁固有基層後直接侵犯其他的臟器或結構,例如降結腸後壁的腫瘤侵犯左腎或側腹壁,或者中下段直腸癌侵犯前列腺、精囊腺、宮頸或陰道。
4.腫瘤肉眼上與其他器官或結構粘連則分期爲cT4b。但是,若顯微鏡下該粘連處未見腫瘤存在則分期爲pT3。V和L亞分期用於表明是否存在血管和淋巴管浸潤,而PN則用以表示神經浸潤(可以是部位特異性的)。
5 四、外科治療
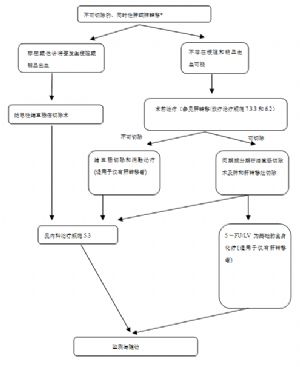
5.1 (一)結腸癌的外科治療規範。
1.結腸癌的手術治療原則。
(1)全面探查,由遠及近。必須探查記錄肝臟、胃腸道、子宮及附件、盆底腹膜,及相關腸繫膜和主要血管淋巴結和腫瘤臨近臟器的情況。
(2)建議切除足夠的腸管,清掃區域淋巴結,整塊切除。
(3)推薦銳性分離技術。
(5)推薦手術遵循無瘤原則。
(7)如果患者無出血、梗阻、穿孔症狀,且已失去根治性手術機會,則無首先姑息性切除原發竈必要。
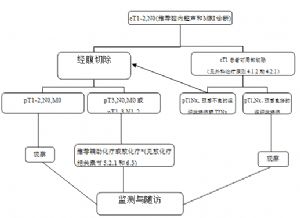
2. 早期結腸癌的手術治療。
(1)T1N0M0結腸癌:建議局部切除。術前直腸腔超聲波檢查屬T1或局部切除術後病理提示T1,如果切除完整而且具有預後良好的組織學特徵(如分化程度良好、無脈管浸潤),則無論是廣基還是帶蒂,不推薦再行手術切除。如果是帶蒂但具有預後不良的組織學特徵,或者非完整切除,標本破碎切緣無法評價,推薦行結腸切除術加區域淋巴結清掃。
(2)直徑超過2.5cm的絨毛狀腺瘤癌變率高,推薦行結腸切除加區域淋巴結清掃。
(3)所有患者術後均須定期行全結腸鏡檢查以排除是否存在多發腺瘤或多發腸癌。
注:局部切除標本必須由手術醫師展平、固定,標記方位後送病理檢查。
3. T2-4,N0-2,M0結腸癌。
(1)首選的手術方式是相應結腸切除加區域淋巴結清掃。區域淋巴結清掃必須包括腸旁,中間和系膜根部淋巴結三站。建議標示系膜根部淋巴結並送病理學檢查;如果懷疑清掃範圍以外的淋巴結有轉移必須完整切除,無法切除者視爲姑息切除。
(2)對具有遺傳性非息肉病性結直腸癌(hereditary nonpolyposis colorectal cancer, HNPCC)家族史,或有明顯的結腸癌家族史,或同時多原發結腸癌的患者建議行更廣泛的結腸切除術。
(4)結腸新生物臨牀診斷高度懷疑惡性腫瘤,由於某些原因無得到病理學診斷,如患者可耐受手術,建議行剖腹探查。
(5)行腹腔鏡輔助的結腸切除術推薦滿足如下條件:①由有經驗的外科醫師實施手術;
②原發竈不在橫結腸(除非進行臨牀試驗);
③無嚴重影響手術的腹腔粘連;
④無局部進展期或晚期病變的表現;
⑥保證能進行全腹腔的探查。
(6)對於已經引起梗阻的可切除結腸癌,推薦行Ⅰ期切除吻合,或Ⅰ期腫瘤切除近端造口遠端閉合,或造瘻術後Ⅱ期切除,或支架植入術後Ⅱ期切除。如果腫瘤局部晚期不能切除或者臨牀上不能耐受手術,建議給予姑息性治療。
(1)原發竈必須能根治性切除(R0)。
(2)有肺外可切除病竈並不妨礙肺轉移瘤的切除。
(3)完整切除必須考慮到腫瘤範圍和解剖部位,肺切除後必須能維持足夠功能。
(4)某些患者可考慮分次切除。
(5)不管肺轉移瘤能否切除,均應當考慮聯合化療(術前化療和/或術後輔助化療)。
5.2 (二)直腸癌的外科治療。
1.直腸癌局部切除(T1N0M0)。
早期直腸癌(T1N0M0)如經肛門切除必須滿足如下要求:(1)侵犯腸周徑<30%;
(4)活動,不固定;
(5)距肛緣8cm以內;
(6)僅適用於T1腫瘤;
(9)高-中分化;
注:局部切除標本必須由手術醫師展平、固定,標記方位後送病理檢查。
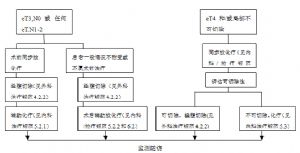
2.直腸癌(T2-4,N0-2,M0)。
必須爭取根治性手術治療。中上段直腸癌推薦行低位前切除術;低位直腸癌推薦行腹會陰聯合切除術或慎重選擇保肛手術。中下段直腸癌必須遵循直腸癌全系膜切除術原則,儘可能銳性遊離直腸系膜,連同腫瘤遠側系膜整塊切除。腸壁遠切緣距離腫瘤≥2cm,直腸系膜遠切緣距離腫瘤≥5cm或切除全直腸系膜。在根治腫瘤的前提下,儘可能保持肛門括約肌功能、排尿和性功能。治療原則如下:
(1)切除原發腫瘤,保證足夠切緣,遠切緣至少距腫瘤遠端2cm。下段直腸癌(距離肛門小於5cm)遠切緣距腫瘤1~2cm者,建議術中冰凍病理檢查證實切緣陰性。
(4)新輔助(術前)放化療後推薦間隔4~8周進行手術。
(6)合併腸梗阻的直腸新生物,臨牀高度懷疑惡性,而無病理診斷,不涉及保肛問題,並可耐受手術的患者,建議剖腹探查。
(7)對於已經引起腸梗阻的可切除直腸癌,推薦行Ⅰ期切除吻合,或Hartmann手術,或造瘻術後Ⅱ期切除,或支架植入解除梗阻後II期切除。Ⅰ期切除吻合前推薦行術中腸道灌洗。如估計吻合口瘻的風險較高,建議行Hartmann手術或Ⅰ期切除吻合及預防性腸造口。
(8)如果腫瘤局部晚期不能切除或臨牀上不能耐受手術,推薦給予姑息性治療,包括選用放射治療來處理不可控制的出血、支架植入來處理腸梗阻以及支持治療。
6 五、內科治療
6.1 (一)結直腸癌的新輔助治療。
新輔助治療目的在於提高手術切除率,提高保肛率,延長患者無病生存期。推薦新輔助放化療僅適用於距肛門<12cm的直腸癌。除結腸癌肝轉移外,不推薦結腸癌患者術前行新輔助治療。
1.直腸癌的新輔助放化療。
(1)直腸癌術前治療推薦以氟尿嘧啶類藥物爲基礎的新輔助放化療。
(2)T1-2N0M0或有放化療禁忌的患者推薦直接手術,不推薦新輔助治療。
(3)T3和/或N+的可切除直腸癌患者,推薦術前新輔助放化療。
(4)T4或局部晚期不可切除的直腸癌患者,必須行新輔助放化療。治療後必須重新評價,並考慮是否可行手術。
新輔助放化療中,化療方案推薦首選持續灌注5-FU,或者5-FU/ LV,或者卡培他濱單藥。建議化療時限2-3個月。放療方案請參見放射治療原則。
結直腸癌患者合併肝轉移和/或肺轉移,可切除或者潛在可切除,推薦術前化療或化療聯合靶向藥物治療:西妥昔單抗(推薦用於K-ras基因狀態野生型患者),或聯合貝伐珠單抗。
化療方案推薦FOLFOX(奧沙利鉑+氟尿嘧啶+醛氫葉酸),或者FOLFIRI(伊立替康+氟尿嘧啶+醛氫葉酸),或者CapeOx(卡培他濱+奧沙利鉑)。建議治療時限2-3個月。
治療後必須重新評價,並考慮是否可行手術。
6.2 (二)結直腸癌輔助治療。
I期(T1-2N0M0)或者有放化療禁忌的患者不推薦輔助治療。
1.結直腸癌輔助化療。
(1)Ⅱ期結直腸癌的輔助化療。Ⅱ期結直腸癌患者,應當確認有無以下高危因素:組織學分化差(Ⅲ或Ⅳ級)、T4、血管淋巴管浸潤、術前腸梗阻/腸穿孔、標本檢出淋巴結不足(少於12枚)。
①Ⅱ期結直腸癌,無高危因素者,建議隨訪觀察,或者單藥氟尿嘧啶類藥物化療。
②Ⅱ期結直腸癌,有高危因素者,建議輔助化療。化療方案推薦選用5-FU/LV、卡培他濱、5-FU/LV/奧沙利鉑或 CapeOx方案。化療時限應當不超過6個月。有條件者建議檢測組織標本MMR或MSI,如爲dMMR或MSI-H,不推薦氟尿嘧啶類藥物的單藥輔助化療。
(1)Ⅱ期結直腸癌的輔助化療。Ⅲ期結直腸癌患者,推薦輔助化療。化療方案推薦選用5-FU/CF、卡培他濱、FOLFOX或FLOX(奧沙利鉑+氟尿嘧啶+醛氫葉酸)或CapeOx方案。化療不應超過6個月。
2.直腸癌輔助放化療。
T3-4或N1-2距肛緣≤12cm直腸癌,推薦術前新輔助放化療,如術前未行新輔助放療,建議輔助放化療,其中化療方案推薦氟尿嘧啶類單藥。放療方案請參見放射治療原則。
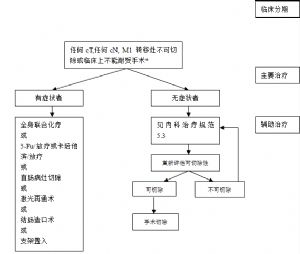
6.3 (三)晚期/轉移性結直腸癌化療。
目前,治療晚期或轉移性結直腸癌使用的藥物:5-FU/LV、伊立替康、奧沙利鉑、卡培他濱和靶向藥物,包括西妥昔單抗(推薦用於K-ras基因野生型患者)和貝伐珠單抗。
1.在治療前檢測腫瘤K-ras基因狀態,EGFR不推薦作爲常規檢查項目。
2.聯合化療應當作爲能耐受化療的轉移性結直腸癌患者的一、二線治療。推薦以下化療方案:FOLFOX/ FOLFIRI/CapeOx±西妥昔單抗(推薦用於K-ras基因野生型患者) ,FOLFOX/ FOLFIRI/CapeOx±貝伐珠單抗。
3.三線以上化療的患者推薦進入臨牀研究。對在一、二線治療中沒有選用靶向藥物的患者也可考慮伊立替康聯合靶向藥物治療。
4.不能耐受聯合化療的患者,推薦方案5-FU/LV±靶向藥物,或5-FU持續灌注,或卡培他濱單藥。
5.晚期患者若一般狀況或器官功能狀況很差,推薦最佳支持治療,不建議化療。
7.結直腸癌局部復發者,推薦進行多學科評估,判定能否有機會再次切除,是否適合術前放化療。如與放療聯合,可以根據患者身體狀況選擇氟尿嘧啶類單藥或聯合化療,如僅適於化療,則採用上述晚期患者藥物治療原則。
6.4 (四)局部/區域化療。
術中或術後區域性緩釋化療與腹腔熱灌注化療目前不常規推薦應用。
7 六、直腸癌放射治療規範
7.1 (一)直腸癌放射治療適應證。
直腸癌放療或放化療的主要目的爲輔助治療和姑息治療。輔助治療的適應證主要針對Ⅱ~Ⅲ期直腸癌;姑息性治療的適應證爲腫瘤局部區域復發和/或遠處轉移。對於某些不能耐受手術或者有強烈保肛意願的患者,可以試行根治性放療或放化療。
1.I期直腸癌不推薦放療。但局部切除術後,有以下因素之一,推薦行根治性手術;如拒絕或無法手術者,建議術後放療。
(1)術後病理分期爲T2;
(2)腫瘤最大徑大於4cm;
(3)腫瘤佔腸周大於1/3者;
(4)低分化腺癌;
2.臨牀診斷爲Ⅱ/Ⅲ期直腸癌,推薦行術前放療或術前同步放化療。
3.根治術後病理診斷爲Ⅱ/Ⅲ期直腸癌,如果未行術前放化療者,必須行術後同步放化療。
4.局部晚期不可手術切除的直腸癌(T4),必須行術前同步放化療,放化療後重新評估,爭取根治性手術。
5.局部區域復發的直腸癌,首選手術;如無手術可能,推薦放化療。
6.Ⅳ期直腸癌:對於初治Ⅳ期直腸癌,建議化療±原發病竈放療,治療後重新評估可切除性;轉移竈必要時行姑息減症放療。
7.復發轉移直腸癌:可切除的局部復發患者,建議先行手術切除,然後再考慮是否行術後放療。不可切除局部復發患者,推薦行術前同步放化療,並爭取手術切除。
7.2 (二)放射治療技術。
1.靶區定義。
(1)原發腫瘤高危復發區域包括腫瘤/瘤牀、直腸系膜區和骶前區,中低位直腸癌靶區應包括坐骨直腸窩。
(2)區域淋巴引流區包括真骨盆內髂總血管淋巴引流區、直腸系膜區、髂內血管淋巴引流區和閉孔淋巴結區。
(4)盆腔復發病竈的放療。
①既往無放療病史,建議行原發腫瘤高危復發區域、區域淋巴結引流區(真骨盆區)照射和腫瘤局部加量放療。
②既往有放療史,根據情況決定是否放療。
2.照射技術。
根據醫院具有的放療設備選擇不同的放射治療技術,如常規放療、三維適形放療、調強放療、圖像引導放療等。
(1)推薦CT模擬定位,如無CT模擬定位,必須行常規模擬定位。建議俯臥位或仰臥位,充盈膀胱。
(2)必須三野及以上的多野照射。
(3)如果調強放療,必須進行計劃驗證。
(4)局部加量可採用術中放療或外照射技術。
(5)放射性粒子植入治療不推薦常規應用。
3.照射劑量。
無論使用常規照射技術還是三維適形放療或調強放療等新技術,都必須有明確的照射劑量定義方式。三維適形照射和調強放療必須應用體積劑量定義方式,常規照射應用等中心點的劑量定義模式。
(1)原發腫瘤高危復發區域和區域淋巴引流區推薦DT45-50.4Gy,每次1.8-2.0Gy,共25或28次。術前放療如採用5x5 Gy/5次/1周或其他劑量分割方式,有效生物劑量必須≥30 Gy。
(2)有腫瘤和/或殘留者,全盆腔照射後局部縮野加量照射DT10-20Gy。
7.3 (三)同步放化療的化療方案和順序。
1.同步化放療的化療方案。推薦5-FU或5-FU類似物爲基礎方案。
2.術後放化療和輔助化療的順序。Ⅱ~Ⅲ期直腸癌根治術後,推薦先行同步放化療再行輔助化療或先行1-2週期輔助化療、同步放化療再輔助化療的夾心治療模式。
8 七、結直腸癌肝轉移治療規範
8.1 (一)結直腸癌肝轉移的定義。
1.國際通用分類:
①同時性肝轉移。結直腸癌確診時發現的或結直腸癌原發竈根治性切除術後6個月內發生的肝轉移。
2.結直腸癌確診時合併肝轉移與結直腸癌原發竈根治術後的肝轉移在診斷和治療上有較大差異,因此本規範按“結直腸癌確診時合併肝轉移”和“結直腸癌根治術後發生肝轉移”兩方面闡述。
8.2 (二)結直腸癌肝轉移的診斷。
(1)對已確診結直腸癌的患者,應當進行肝臟超聲和/或增強CT影像檢查,對於懷疑肝轉移的患者加行血清AFP和肝臟MRI檢查。PET-CT檢查不作爲常規推薦,可在病情需要時酌情應用。
(3)結直腸癌手術中必須常規探查肝臟以進一步排除肝轉移的可能,對可疑的肝臟結節可考慮術中活檢。
結直腸癌根治術後的患者,應當定期隨訪肝臟超聲或/和增強CT掃描,懷疑肝轉移的患者應當加行肝臟MRI檢查,PET-CT掃描不作常規推薦。
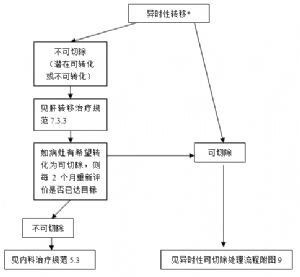
8.3 (三)結直腸癌肝轉移的治療。
手術完全切除肝轉移竈仍是目前能治癒結直腸癌肝轉移的最佳方法,故符合條件的患者均應當在適當的時候接受手術治療。對部分最初肝轉移竈無法切除的患者應當經多學科討論慎重決定新輔助化療和手術時機,創造一切機會使之轉化爲可切除病竈。
(1)適應證:
①結直腸癌原發竈能夠或已經根治性切除。
②根據肝臟解剖學基礎和病竈範圍肝轉移竈可完全(R0)切除,且要求保留足夠的肝臟功能,肝臟殘留容積≥50%(同步原發竈和肝轉移竈切除)或≥30%(分階段原發竈和肝轉移竈切除)。
(2)禁忌證:
①結直腸癌原發竈不能取得根治性切除;
②出現不能切除的肝外轉移;
③預計術後殘餘肝臟容積不夠;
④患者全身狀況不能耐受手術。
(1)手術治療。
在下列情況下,建議結直腸癌原發竈和肝轉移竈同步切除:肝轉移竈小、且多位於周邊或侷限於半肝,肝切除量低於50%,肝門部淋巴結、腹腔或其他遠處轉移均可手術切除時可考慮應用。
a先手術切除結直腸癌原發病竈,分階段切除肝轉移竈,時機選擇在結直腸癌根治術後4~6周。
b若在肝轉移竈手術前進行治療,肝轉移竈的切除可延至原發竈切除後3個月內進行。
d可根治的複發性結直腸癌伴有可切除肝轉移竈傾向於進行分階段切除肝轉移竈。
既往結直腸原發竈爲根治性切除且不伴有原發竈復發,肝轉移竈能完全切除且肝切除量低於70%(無肝硬化者),應當予以手術切除肝轉移竈,可先行新輔助治療。
③肝轉移竈切除術後復發。
在全身狀況和肝髒條件允許的情況下,對於可切除的肝轉移竈術後的復發病竈,可進行二次、三次甚至多次的肝轉移竈切除。
④肝轉移竈手術方式的選擇。
a肝轉移竈切除後至少保留3根肝靜脈中的1根且殘肝容積≥50%(同步原發竈和肝轉移竈切除)或≥30%(分階段原發竈和肝轉移竈切除)。
b轉移竈的手術切緣一般應當有1cm正常肝組織,若轉移竈位置特殊(如緊鄰大血管)時則不必苛求,但仍應當符合R0原則。
c如是侷限於左半或右半肝的較大肝轉移竈且無肝硬化者,可行規則的半肝切除。
d建議肝轉移手術時採用術中超聲檢查,有助於發現術前影像學檢查未能診斷的肝轉移病竈。
(2)術前治療。
①結直腸癌確診時合併肝轉移。在原發竈無出血、梗阻或穿孔時推薦術前治療,方案可選FOLFOX、FOLFIRI或CapeOX,可聯合分子靶向藥物治療;一般建議2~3個月內完成。西妥昔單抗推薦用於K-ras基因野生型患者。使用貝伐珠單抗時,建議手術時機選擇在最後一次使用貝伐珠單抗6周以後。不建議多種靶向藥物聯合應用。
②結直腸癌根治術後發生的肝轉移。原發竈切除術後未接受過化療的患者,或者發現肝轉移12個月前已完成化療的患者,可採用術前治療(方法同上);肝轉移發現前12個月內接受過化療的患者,也可直接切除肝轉移竈。
(3)切除術後的輔助治療。
肝轉移竈完全切除的患者推薦接受術後輔助化療,建議手術前後化療時間共爲6個月。術後化療方案建議可選5-FU/LV、卡培他濱、5-FU/LV/奧沙利鉑或 CapeOx方案。術前治療有效的患者建議沿用術前方案。
(1)除合併出血、穿孔或梗阻等急症需要手術切除原發竈以外的不可切除的結直腸癌肝轉移患者,應當經多學科討論,慎重選擇方案及藥物(原則同7.3.2中的術前治療)進行系統治療,創造一切機會轉化爲可手術治療。治療過程中每6-8周評估療效,一旦達到可手術切除條件,儘早爭取手術治療。轉化爲可切除的結直腸癌肝轉移患者等同於7.3.2相關原則。
(2)射頻消融。
①一般情況不適宜或不願意接受手術治療的可切除結直腸癌肝轉移患者推薦使用射頻消融,射頻消融的肝轉移竈的最大直徑小於3cm且一次消融最多3枚。
②預期術後殘餘肝臟體積過小時,建議先切除部分較大的肝轉移竈,對剩餘直徑小於3cm的轉移病竈進行射頻消融。
(3)放射治療。
無法手術切除的肝轉移竈,若全身化療、肝動脈灌注化療或射頻消融無效,建議放射治療。
(5)其他治療方法。
9 八、局部復發直腸癌的治療規範
9.1 (一)分型。
目前,局部復發的分型建議使用以下分類方法: 根據盆腔受累的解剖部位分爲中心型(包括吻合口、直腸系膜、直腸周圍軟組織、腹會陰聯合切除術後會陰部)、前向型(侵及泌尿生殖系包括膀胱、陰道、子宮、精囊腺、前列腺)、後向型(侵及骶骨、骶前筋膜)、側方型(侵犯盆壁軟組織或骨性骨盆)。
9.2 (二)治療原則。
根據患者和病變的具體情況評估,可切除或潛在可切除患者爭取手術治療,並與術前放化療、術中放療、輔助放化療等結合使用;不可切除的患者建議放、化療結合的綜合治療。
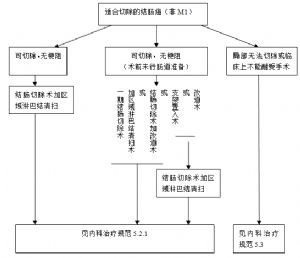
9.3 (三)手術治療。
1.可切除性的評估。
必須在術前評估復發病竈得到根治切除的可能性。推薦根據復發範圍考慮決定是否使用術前放化療。建議根據術中探查結果核實病竈的可切除性,必要時可行術中冰凍病理檢查。
不可切除的局部復發病竈包括:
①廣泛的盆腔側壁侵犯;
②骨性盆腔受侵;
③髂外血管受累;
⑤侵犯第2骶骨水平及以上。
2. 手術原則。
(1)推薦由結直腸外科專科醫師根據患者和病變的具體情況選擇適當的手術方案,並與術前放化療、術中放療、輔助放化療等結合使用。
(2)推薦必要時與泌尿外科、骨科、血管外科、婦產科醫師等共同制訂手術方案。
(4)必須遵循整塊切除原則,儘可能達到R0切除。
(5)術中注意保護輸尿管(酌情術前放置輸尿管支架)以及尿道。
3.可切除的病竈手術方式。
手術方式包括低位前切除術(LAR)、腹會陰聯合切除(APR)、盆腔清掃術等。
(1)中心型:建議行APR以保證達到R0切除;既往行保肛手術的在病變較爲侷限的情況下可考慮LAR。APR術後會陰部術野復發如病變侷限可考慮行經會陰或經骶切除術。
(2)前向型:在患者身體情況允許的情況下,可考慮切除受侵犯器官,行後半盆清掃或全盆清掃術。
(4)後向型:腹骶聯合切除受侵骶骨。會陰部切口可使用大網膜覆蓋或一期縫合。必要時使用肌皮瓣(股薄肌、臀肌、橫行腹直肌皮瓣、背闊肌等)。
9.4 (四)放射治療原則。
可切除的局部復發患者,建議先行手術切除,然後再考慮是否行術後放療。不可切除局部復發患者,推薦行術前同步放化療,並爭取手術切除。參見放射治療相關章節。
9.5 (五)化療原則。
10 九、腸造口康復治療
10.1 (一)人員、任務、架構。
有條件的醫院推薦配備造口治療師(專科護士)。造口治療師的職責包括所有造口(腸造口、胃造口、尿路造口、氣管造口等)術前術後的護理、複雜傷口的處理、大小便失禁的護理、開設造口專科門診、聯絡患者及其他專業人員和造口用品商、組織造口聯誼會並開展造口訪問者活動。
10.2 (二)術前心理治療。
推薦向患者充分解釋有關的診斷、手術和護理知識,讓患者接受患病的事實,並對即將發生的事情有全面的瞭解。
10.3 (三)術前造口定位。
1.要求:患者自己能看到,方便護理;有足夠的粘貼面積;造口器材貼於造口皮膚時無不適感覺。
2.常見腸造口位置如圖1
 |
圖1:常見腸造口位置 |
10.4 (四)腸造口術後護理。
11 十、隨訪
結直腸癌治療後一律推薦規律隨訪。
(一)病史和體檢,每 3-6個月 1次,共 2年,然後每 6個月 1次,總共 5年,5年後每年1次。
(二)監測CEA、CA19-9,每3-6個月 1次,共 2年,然後每 6個月1 次,總共 5年,5年後每年1次。
(三)腹/盆超聲、胸片每3-6個月 1次,共 2年,然後每 6個月1 次,總共 5年,5年後每年1次。
(四)腹/盆CT或MRI每年1次。
(五)術後1年內行腸鏡檢查,如有異常,1年內複查;如未見息肉,3年內複查;然後5年1次,隨診檢查出現的大腸腺瘤均推薦切除。
(六)PET-CT不是常規推薦的檢查項目。