2 英文參考
chronic obstructive pulmonary disease[湘雅醫學專業詞典]
chronic obstructive pulmonary disease,COPD[國家基本藥物臨牀應用指南:2012年版.化學藥品和生物製品]
3 概述
慢性阻塞性肺病(chronic obstructive pulmonary disease,COPD)簡稱“慢阻肺”[1],是一種慢性氣道阻塞性疾病的統稱,是以氣流受限爲特徵的肺部疾病。可以預防和治療[1]。氣流受限不完全可逆,呈進行性發展,與肺部對香菸煙霧等有害氣體或有害顆粒的異常炎症反應有關[1]。慢阻肺與慢性支氣管炎和肺氣腫密切相關[1]。慢性阻塞性肺病主要指具有不可逆性氣道阻塞的慢性支氣管炎和肺氣腫兩種疾病。當慢性支氣管炎、肺氣腫患者肺功能檢查出現氣流受限,並且不能完全可逆時,則能診斷爲慢阻肺[1]。
4 慢性支氣管炎
慢性支氣管炎(chronic bronchitis)是40歲以上男性人羣中最常見的疾病之一,臨牀上以反覆發作咳嗽、咳痰或伴有喘息症狀爲特徵,且症狀每年持續約3個月,連續兩年以上。病情進展,常常併發肺氣腫和慢性肺源性心臟病。是一種嚴重影響健康的慢性病。
4.1 病因和發病機制
慢性支氣管炎往往是因多種因素長期綜合作用所致。起病與感冒有密切關係,多在氣候變化比較劇烈的季節發病。呼吸道反覆病毒感染和繼發性細菌感染是導致慢性支氣管炎病變發展和疾病加重的重要原因。吸菸與慢性支氣管炎的關係也是肯定的,吸菸者比不吸菸者的患病率高2~8倍,吸菸時間愈久,日吸菸量愈大,患病率愈高,戒菸可使病情減輕。此外,長期接觸工業粉塵、大氣污染和過敏因素也常是引起慢性支氣管炎的原因,而機體抵抗力降低,呼吸系統防禦功能受損則是發病的內在因素。
4.2 病理變化
各級支氣管均可受累,受累的細支氣管愈多,病變愈重,後果也愈嚴重。主要的病變有:①粘膜上皮纖毛倒伏,甚至脫失。上皮細胞變性、壞死脫落。上皮再生時,杯狀細胞增多,並可發生鱗狀上皮化生(圖1);②粘液腺肥大、增生,分泌亢進,漿液腺發生粘液化(圖2);③管壁充血,淋巴細胞、漿細胞浸潤;④管壁平滑肌束斷裂、萎縮,而喘息型患者,平滑肌束可增生、肥大,管腔變窄;⑤軟骨可發生變性、萎縮,鈣化或骨化。支氣管炎反覆發作的結果,病變不僅逐漸加重,而且逐級向縱深發展蔓延,受累的細支氣管數量也不斷增多。細支氣管因管壁薄,炎症易向管壁周圍組織及肺泡擴展,導致細支氣管周圍炎,而且還可發生纖維閉塞性細支氣管炎,是引起慢性阻塞性肺氣腫的病變基礎。

圖1 慢性支氣管炎

圖2 慢性支氣管炎
支氣管粘膜上皮出現較多杯狀細胞,固有層及粘膜下層內有慢性炎性細胞浸潤,腺體呈粘液化
4.3 臨牀病理聯繫
患者因支氣管粘膜的炎症和分泌物增多,而出現咳嗽、咳痰症狀。痰一般呈白色粘液泡沫狀。在急性發作期,咳嗽加重,並出現粘液膿性或膿性痰。由於支氣管痙攣或支氣管狹窄及粘液、滲出物阻塞而引起喘息。檢查時,兩肺可聞及哮鳴音、幹溼囉音。有的患者因粘膜和腺體萎縮(慢性萎縮性支氣管炎),分泌物減少,痰量減少甚或無痰。病變導致小氣道狹窄或阻塞時,出現阻塞性通氣障礙,表現爲第1秒用力呼吸量和最大通氣量明顯降低,合併肺氣腫時,肺殘氣量明顯增多,肺總量也增大。
5 肺氣腫
肺氣腫(pulmonary emphysema)是指呼吸細支氣管以遠的末梢肺組織因殘氣量增多而呈持久性擴張,並伴有肺泡間隔破壞,以致肺組織彈性減弱,容積增大的一種病理狀態。在成人屍檢例中,約50%可發現不同程度的肺氣腫,其中約6.5%的患得因此病死亡。
5.1 病因和發病機制
肺氣腫是支氣管和肺疾病常見的併發症。與吸菸、空氣污染、小氣道感染、塵肺等關係密切,尤其是慢性阻塞性細支氣管炎是引起肺氣腫的重要原因。發病機制與下列因素有關:
1.阻塞性 通氣障礙慢性細支氣管炎時,由於小氣道的狹窄、阻塞或塌陷,導致了阻塞性通氣障礙,使肺泡內殘氣量增多,而且,細支氣管周圍的炎症,使肺泡壁破壞、彈性減弱,更影響到肺的排氣能力,末梢肺組織則因殘氣量不斷增多而發生擴張,肺泡孔擴大,肺泡間隔也斷裂,擴張的肺泡互相融合形成氣腫囊腔。
此外,細支氣閉塞時,吸入的空氣可經存在於細支氣管和肺泡之間的Lambert孔進入閉塞遠端的肺泡內(即肺泡側流通氣),而呼氣時,Lambert孔閉合,空氣不能排出,也是導致肺泡內儲氣量增多、肺泡內壓增高的因素。
2.彈性蛋白酶增多、活性增高與肺氣腫發生有關的內源性蛋白酶主要是中性粒細胞和單核細胞釋放的彈性蛋白酶。此酶能降解肺組織中的彈性硬蛋白、結締組織基質中的膠原和蛋白多糖,破壞肺泡壁結構。慢性支氣管炎伴有肺感染、尤其是吸菸者,肺組織內滲出的中性粒細胞和單核細胞較多,可釋放多量彈性蛋白酶。同時,中性粒細胞和單核細胞還可生成大量氧自由基,能氧化α1-抗胰蛋白酶活性中心的蛋氨酸使之失活。α1-抗胰蛋白酶乃彈性蛋白酶的抑制物,失活後則增強了彈性蛋白酶的損傷作用。
α1-抗胰蛋白酶由肝細胞產生,是一種分子量爲45000~56000的糖蛋白,它能抑制蛋白酶、彈性蛋白酶、膠原酶等多種水解酶的活性。遺傳性α1-抗胰蛋白酶缺乏是引起原發性肺氣腫的原因,α1-抗胰蛋白酶缺乏的家族,肺氣腫的發病率比一般人高15倍,主要是全腺泡型肺氣腫。但是,在我國因遺傳性α1-抗胰蛋白酶缺乏引起的原發性肺氣腫非常罕見,並不重要。而最重要的也是最常見的是慢性阻塞性肺氣腫(繼發性肺氣腫)。
5.2 類型及其病變特點
肺氣腫病變發生在肺腺泡(acinus),即Ⅰ級呼吸細支氣管所分佈的肺組織範圍內。屬肺泡性肺氣腫(alveolar emphysema)。根據病變的確切解剖部位及分佈範圍的不同可分爲:
1.瀰漫性肺氣腫
(1)腺泡中央型肺氣腫:腺泡中央型肺氣腫(centriacinar emphysema)病變累及肺腺泡的中央部分,呼吸細支氣管病變最明顯,呈囊狀擴張(圖3)。而肺泡管、肺泡囊變化則不明顯。
(2)全腺泡型肺氣腫:全腺泡型肺氣腫(panacinar emphysema)病變累及肺腺泡的各個部位,從終末呼吸細支氣管直至肺泡囊和肺泡均呈瀰漫性擴張,遍佈於肺小葉內(圖4)。如果肺泡間隔破壞較嚴重,氣腫囊腔可融合成直徑超過1cm的大囊泡,形成大泡性肺氣腫(圖5)。
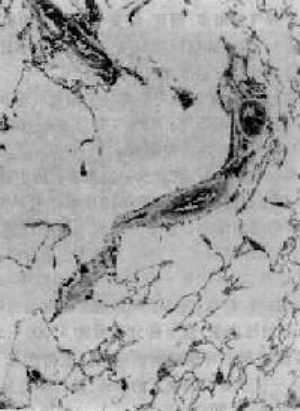
圖3 腺泡中央型肺氣腫
呼吸細支氣管呈囊狀擴張,伴行肺動脈(徑80μm)管壁增厚,其分支內膜增厚,管腔極度狹窄

圖4 全腺泡型肺氣腫
末梢呼吸道瀰漫性擴張,呈小囊狀遍佈於肺小葉內(徑>200μm)

圖5 左肺下葉大泡性肺氣腫
在全腺泡型肺氣腫基礎上,胖有直徑超過1cm的大囊泡
(3)腺泡周圍型肺氣腫:腺泡周圍型肺氣腫(periacinar emphysema)也稱隔旁肺氣腫(paraseptal emphysema),病變主要累及肺腺泡遠端部位的肺泡囊,而近端部位的呼吸細支氣管和肺泡管基本正常。常合併有腺泡中央型和全腺泡型肺氣腫。
2.侷限性肺氣腫
(1)不規則型肺氣腫:不規則型肺氣腫(irregular emphysema)也稱瘢痕旁肺氣腫(paracicatricial emphysema),病變主要發生在瘢痕附近的肺組織,肺腺泡不規則受累,確切部位不定,一般是發生在呼吸細支氣管遠側端,肺泡囊有時也受累。
(2)肺大泡:肺大泡(bullae of lung)病變特點是局竈性肺泡破壞,小葉間隔也遭破壞,往往形成直徑超過2cm的大囊泡,常爲單個孤立位於髒層胸膜下。而其餘肺結構可正常。
間質性肺氣腫(interstitial emphysema)是由於肺泡壁或細支氣壁破裂,氣體逸入肺間質內,在小葉間隔與肺膜連接處形成串珠狀小氣泡,呈網狀分佈於肺膜下。
5.3 病理變化
肉眼觀:氣腫肺顯著膨大,邊緣鈍圓,色澤灰白,表面常可見肋骨壓痕,肺組織柔軟而彈性差,指壓後的壓痕不易消退,觸之捻發音增強。
鏡下:肺泡擴張,間隔變窄,肺泡孔擴大,肺泡間隔斷裂,擴張的肺泡融合成較大的囊腔。肺毛細血管牀明顯減少,肺小動脈內膜呈纖維性增厚。小支氣管和細支氣管可見慢性炎症。腺泡中央型肺氣腫的氣腫囊泡爲擴張的呼吸細支氣管,在近端囊壁上常可見呼吸上皮(柱狀或低柱狀上皮)及平滑肌束的殘跡。全腺泡型肺氣腫的氣腫囊泡主要是擴張變圓的肺泡管和肺泡囊,有時還可見到囊泡壁上殘留的平滑肌束片斷,在較大的氣腫囊腔內有時還可見含有小血管的懸樑。
5.4 臨牀病理聯繫
肺氣腫患者的主要症狀是氣短,輕者僅在體力勞動時發生,隨着氣腫程度加重,氣短逐漸明顯,甚至休息時也出現呼吸困難,並常感胸悶。每當合併呼吸道感染時,症狀加重,並可出現缺氧、酸中毒等一系列症狀。肺功能檢查診斷肺氣腫的標準是殘氣量超過肺總量的35%,最大通氣量低於預計值的80%,肺總量超過預計值的100%,1秒用力呼吸量低於肺活量的60%。典型肺氣中患者的胸廓前後徑增大,呈桶狀胸。胸廓呼吸運動減弱。叩診呈過清音,心濁音界縮小或消失,肝濁音界下降。語音震顫減弱。聽診時呼吸音減弱,呼氣延長,用力呼吸時兩肺底部可聞及溼囉音和散在的幹囉音。劍突下心音增強,肺動脈瓣第二音亢進。
肺氣腫的嚴重後果有①肺源性心臟病及衰竭。②肺大泡破裂後引起自發性氣胸,並可導致大面積肺萎陷。③呼吸衰竭及肺性腦病。由於外呼吸功能嚴重障礙,導致動脈血PaO2<8kPa(60mmHg),伴有或不伴有PaCO2<6.67kPa(50mmHg)的病理過程,稱爲呼吸衰竭(respiratory failure)。呼吸衰竭時發生的低氧血癥和高碳酸血癥會引起各系統的代謝功能嚴重紊亂。中樞神經系統對缺氧最爲敏感,愈是高級部位敏感性愈高。隨着缺氧程度的加重,可出現一系列中樞神系統功能障礙,由開始的大腦皮層興奮性增高而後轉入抑制狀態。病人表現由煩燥不安、視力和智力的輕度減退,逐漸發展爲定向和記憶障礙,精神錯亂,嗜睡,驚厥以至意識喪失。迅速發生的CO2瀦留也能引起中樞神經功能障礙,病人常出現頭痛、頭暈、煩燥不安、言語不清、撲翼樣震顫、精神錯亂以及嗜睡、昏迷、呼吸抑制等“二氧化碳麻醉”症狀。由呼吸衰竭造成的以腦功能障礙爲主要表現的綜合徵,稱爲肺性腦病(pulmonary encephalopathy),可能是由於低氧血癥、高碳酸血癥,以及酸鹼平衡紊亂導致神經細胞變性、壞死和腦血液循環障礙引起腦血管擴張、腦水腫、竈性出血、顱內壓升高甚至腦疝形成等因素綜合作用所致。
6 慢性阻塞性肺病的診斷
6.1 典型症狀
③全身性症狀,包括體重下降、食慾減退、外周肌肉萎縮和功能障礙、精神抑鬱和(或)焦慮等[1]。
6.2 體徵
慢阻肺早期體徵可不明顯。隨疾病進展可有桶狀胸、發紺,伴右心衰竭者可見下肢水腫、肝臟增大,兩肺底或其他肺野可聞及溼囉音[1]。
6.3 診斷
應根據臨牀表現、危險因素接觸史、體徵及實驗室檢查等資料綜合分析確定[1]。考慮慢阻肺的主要症狀爲慢性咳嗽、咳痰和(或)呼吸困難及危險因素接觸史;存在不完全可逆性氣流受限是診斷慢阻肺的必備條件[1]。肺功能測定指標是診斷慢阻肺的金標準[1]。用支氣管舒張劑後FEV1/FVC<70%,而FEV1<80%預計值可確定爲不完全可逆性氣流受限[1]。
6.4 臨牀分級
慢阻肺患者根據以肺功能爲主的指標分爲Ⅰ~Ⅳ級(輕~極重度),具體見下表[1]。
分級 | 特徵 | 推薦治療方案 |
Ⅰ級(輕度) | FEV1/FVC<70%,FEV1佔預計 值百分比≥80% | 避免危險因素;接種流感疫苗;按需使 用短效支氣管舒張劑 |
Ⅱ級(中度) | FEV1/FVC<70%,50%≤FEV1 佔預計值百分比<80% | 在上一級治療基礎上,規律應用一種 |
Ⅲ級(重度) | FEV1/FVC<70%,30%≤FEV1 佔預計值百分比<50% | 在上一級治療基礎上,反覆急性發作, |
Ⅳ級(極重度) | FEV1/FVC<70%,FEV1佔預計 值百分比<30%,或伴有慢性 | 在上一級治療基礎上,如有呼吸衰竭, 長期氧療,可考慮外科治療 |
6.5 臨牀分期
(1)急性加重期:是指患者出現超越日常狀況的持續惡化,並需改變基礎慢阻肺的常規用藥者。患者出現短期內咳嗽、氣急加重,痰量增多呈膿性或黏膿性[1]。
7 慢性阻塞性肺病的治療方案
7.1 穩定期慢阻肺患者治療的方案
穩定期慢阻肺患者根據肺功能進行嚴重程度分級後,不同級別推薦的治療方案見下表[1]。
分級 | 特徵 | 推薦治療方案 |
Ⅰ級(輕度) | FEV1/FVC<70%,FEV1佔預計 值百分比≥80% | 避免危險因素;接種流感疫苗;按需使 用短效支氣管舒張劑 |
Ⅱ級(中度) | FEV1/FVC<70%,50%≤FEV1 佔預計值百分比<80% | 在上一級治療基礎上,規律應用一種 |
Ⅲ級(重度) | FEV1/FVC<70%,30%≤FEV1 佔預計值百分比<50% | 在上一級治療基礎上,反覆急性發作, |
Ⅳ級(極重度) | FEV1/FVC<70%,FEV1佔預計 值百分比<30%,或伴有慢性 | 在上一級治療基礎上,如有呼吸衰竭, 長期氧療,可考慮外科治療 |
7.2 支氣管舒張劑
支氣管舒張劑可鬆弛支氣管平滑肌、擴張支氣管、緩解氣流受限,是控制慢阻肺症狀的主要治療措施[1]。短期按需應用可緩解症狀,長期規則應用可預防和減輕症狀,增加運動耐力,但不能使所有患者的FEV1都得到改善[1]。
主要的支氣管舒張劑有:
7.2.1 沙丁胺醇
沙丁胺醇主要用於緩解症狀,按需使用[1]。沙丁胺醇爲短效定量霧化吸入劑,數分鐘內開始起效,15~30分鐘達到峯值,持續療效4~5小時[1]。每次劑量100~200μg(每噴100μg),24小時內不超過8~12噴[1]。
沙丁胺醇使用的常見不良反應主要是肌肉震顫、心悸等,過量可致心律失常,24小時內不超過8~12噴[1]。
7.2.2 異丙託溴銨(ipratropium bromide)氣霧劑
異丙託溴銨(ipratropium bromide)氣霧劑爲抗膽鹼藥物,可阻斷M膽鹼受體[1]。
定量吸入時,開始作用時間比沙丁胺醇等短效β2受體激動劑慢,但持續時間長,30~90分鐘達最大效果[1]。維持6~8小時,劑量爲40~80μg(每撳40μg)一日3~4次[1]。
該藥副作用小,長期吸入可改善慢阻肺患者健康狀況[1]。長期吸入可增加深吸氣量(IC),減低呼吸末肺容積(EELV),進而改善呼吸困難,提高運動耐力和生活質量,也可減少急性加重頻率[1]。對於輕症患者效果可能會更好[1]。
異丙託溴銨對於妊娠早期婦女和患有青光眼及前列腺肥大的患者應慎用[1]。
7.2.3 氨茶鹼
茶鹼類藥物可解除氣道平滑肌痙攣,廣泛用於慢阻肺的治療[1]。
靜脈用藥一次0.25~0.5g加入5%或10%葡萄糖注射液250ml後緩慢滴注[1]。靜脈給藥極量:一次0.5g,一日1g[1]。
氨茶鹼過量會引起中毒,吸菸、飲酒、服用抗驚厥藥、利福平等可縮短茶鹼半衰期;老人、持續發熱、心力衰竭和肝功能明顯障礙者,同時應用西咪替丁、大環內酯類藥物(紅黴素等)、氟喹諾酮類藥物(環丙沙星等)和口服避孕藥等都可能使茶鹼血藥濃度增加[1]。
7.3 糖皮質激素
儘管長期應用糖皮質激素吸入治療並不能阻止慢阻肺穩定期患者FEV1的下降趨勢,但對於FEV1<60%預計值並且反覆急性加重的慢阻肺患者而言,長期規律的吸入糖皮質激素能夠減少其急性加重的發生頻率,改善生活質量[1]。
聯合吸入激素和β2激動劑,比各自單用效果好,對於 FEV1<60%預計值的患者,聯合給藥可以延緩肺功能的下降速率[1]。具體方法:丙酸倍氯米松100~200μg(每撳50μg)吸入,一日3~4次[1]。可與沙丁胺醇聯合使用[1]。
對加重期患者,全身使用糖皮質激素可促進病情緩解和肺功能的恢復,可考慮口服糖皮質激素,潑尼松20mg,一日2次,用5~7天后逐漸減量[1]。
大劑量使用糖皮質激素容易併發高血糖、骨質疏鬆、高血壓病、腎上腺皮質功能減退等。口服劑量較大或療程長達2周以上者,易出現反跳現象,建議逐步減少劑量。需長期口服糖皮質激素者,潑尼松用量每日少於10mg[1]。
7.4 祛痰藥
常用藥物有氨溴索30mg,一日3次口服,或溴己新8~16mg,一日3次口服[1]。
7.5 抗菌藥物
慢阻肺症狀加重,特別是痰量增多並呈膿性時應積極給予抗菌藥物治療[1]。
急性加重期常見病原體以呼吸道病毒、流感嗜血桿菌及銅綠假單胞菌等革蘭陰性桿菌爲主。如考慮革蘭陽性球菌感染,可選擇大劑量青黴素(400萬單位,每8小時1次)靜脈滴注或頭孢呋辛(2.25g,一日2次)靜脈滴注;革蘭陰性桿菌感染,可使用頭孢曲松(2.0g,一日1次)靜脈滴注,或頭孢他啶(1.0~2.0g,一日2~3次),或左氧氟沙星(0.5g,一日1次),或阿米卡星(0.4g,一日1次),靜脈滴注。療程5~7天。臨牀症狀改善3天后可改用口服抗菌藥物序貫治療。[1]
7.6 住院標準
②出現新的體徵或原有體徵加重(如發紺、外周水腫);
④有嚴重的伴隨疾病;
⑤初始治療方案失敗;
⑦診斷不明確;
⑧院外治療條件欠佳或治療不力。
8 參考資料
- ^ [1] 國家基本藥物臨牀應用指南和處方集編委會主編.國家基本藥物臨牀應用指南:2012年版[M].北京:人民衛生出版社,2013:72-75.