版本:國家藥品監督管理局2001年公佈的第一批化學藥品說明書塞替派注射液說明書由國家藥品監督管理局於2001年12月31日國藥監注[2001]586號《關於印發第一批化學藥品說明書的通知》發佈。國家藥品監督管理局公佈的說明書是規範修訂後的建議參考樣稿,企業如有疑異,可提出修改意見。〔適應症〕應與原批准的內容一致;〔不良反應〕、〔藥物相互作用〕等項內容,企業提供的說明書不能比樣稿所列的少。對於說明書樣稿中的空項或未列全的項目,應要求企業根據實際情況填寫,如商品名、規格等。
塞替派注射液說明書
【藥品名稱】
通用名:塞替派注射液
曾用名:
商品名:
英文名:Thiotepa Injection
漢語拼音:Saitipai Zhusheye
本品主要成分及其化學名稱爲:1,1′,1″-硫次膦基三氮丙啶。
其結構式爲:
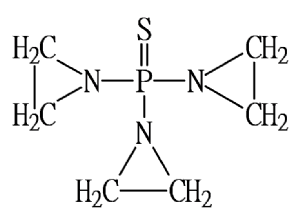
分子式:C6H12N3PS
分子量:189.22
【性狀】
本品爲無色或幾乎無色的黏稠澄明液體
【藥理毒理】
塞替派爲細胞週期非特異性藥物,在生理條件下,形成不穩定的亞乙基亞胺基,具有較強的細胞毒作用。塞替派是多功能烷化劑,能抑制核酸的合成,與DNA發生交叉聯結,干擾DNA和RNA的功能,改變DNA的功能,故也可引起突變。體外試驗顯示可引起染色體畸變,在小鼠的研究中可清楚看到有致癌性,但對人尚不十分清楚。近年來證明本品對垂體促卵泡激素含量有影響。
【藥代動力學】
本品不宜從消化道吸收。注射後廣泛分佈在各組織內。1~4小時後血漿濃度下降90%,24~48小時大部分藥物通過腎臟排出。注射藥物後血漿蛋白結合率爲10%,主要和白蛋白、脂蛋白結合,對白蛋白親和力最大。T1/2約3小時。尚無資料說明藥物能否通過胎盤屏障。
【適應症】
主要用於乳腺癌、卵巢癌、癌性體腔積液的腔內注射以及膀胱癌的局部灌注等,也可用於胃腸道腫瘤等。
【用法用量】
靜脈或肌肉注射(單一用藥):一次10mg(0.2mg/kg)每日一次,連續5天后改爲每週3次,一療程總量300mg。
胸腹腔或心包腔內注射:一次10~30mg,每週1~2次。
膀胱腔內灌注:每次排空尿液後將導尿管插入膀胱內向腔內注入60mg,溶於生理鹽水60ml,每週1~2次,10次爲一療程。
【不良反應】
骨髓抑制是最常見的劑量限制毒性,多在用藥後l~6周發生,停藥後大多數可恢復。有些病例在療程結束時開始下降,少數病例抑制時間較長。可有食慾減退、噁心及嘔吐等胃腸反應。
個別報道用此藥後再接受手術麻醉時,用琥珀酰膽鹼後出現呼吸暫停。少見過敏,個別有發熱及皮疹。有少量報告有出血性膀胱炎,注射部位疼痛,頭痛、頭暈,閉經、影響精子形成。
【禁忌症】
【注意事項】
1、妊娠初期的3個月應避免使用此藥,因其有致突變或致畸胎作用,可增加胎兒死亡及先天性畸形。
2、下列情況應慎用或減量使用:骨髓抑制、肝功能損害、感染、腎功能損害、腫瘤細胞浸潤骨髓、有泌尿繫結石史和痛風病史。
3、用藥期間每週都要定期檢查外周血象,白細胞與血小板及肝、腎功能。停藥後3周內應繼續進行相應檢查,已防止出現持續的嚴重骨髓抑制
5、在白血病、淋巴瘤病人中爲防止尿酸性腎病或高尿酸血癥,可給予大量補液(或)給予別嘌呤醇。
6、儘量減少與其它烷化劑聯合使用,或同時接受放療。
【孕婦及哺乳期婦女用藥】
不向孕婦推薦此藥,可能有致畸性。尚沒有對受乳嬰兒影響的報道。
【藥物相互作用】
1、塞替派可增加血尿酸水平,爲了控制高尿酸血癥可給予別嘌呤醇。
2、與放療同時應用時,應適當調整劑量。
3、與琥珀膽鹼同時應用可使呼吸暫停延長,在接受塞替派治療的病人,應用琥珀膽鹼前必須測定血中假膽鹼酯酶水平。
4、與尿激酶同時應用可增加塞替派治療膀胱癌的療效,尿激酶爲纖維蛋白溶酶原的活化劑,可增加藥物在腫瘤組織中的濃度。
【藥物過量】
藥物過量後沒有解毒藥物。以往出現骨髓毒性後建議輸注全血或白細胞、血小板懸液。目前,白細胞下降可使用粒細胞集落刺激因子。
【規格】
1ml∶10mg
【貯藏】
【包裝】
【有效期】
【批准文號】
【生產企業】
企業名稱:
地 址:
郵政編碼:
電話號碼:
傳真號碼:
網 址: