1 拼音
W S / T 6 1 5 — 2 0 1 8 fú shè shēng wù jì liàng gū suàn zǎo shú rǎn sè tǐ níng jí huán fēn xī fǎ
3 基本信息
ICS 13.100
C 60
中華人民共和國衛生行業標準WS/T 615—2018《輻射生物劑量估算 早熟染色體凝集環分析法》(Estimation of radiation biological dose—analyzing premature chromosome condensation ring)由中華人民共和國國家衛生健康委員會於2018年06月15日《關於發佈〈公衆成員的放射性核素年攝入量限值〉等3項推薦性衛生行業標準的通告》(國衛通〔2018〕12號)發佈,自2018年12月01日起實施。
4 發佈通知
關於發佈《公衆成員的放射性核素年攝入量限值》等3項推薦性衛生行業標準的通告
國衛通〔2018〕12號
現發佈《公衆成員的放射性核素年攝入量限值》等3項推薦性衛生行業標準,編號和名稱如下:
WS/T 613—2018 公衆成員的放射性核素年攝入量限值
WS/T 614—2018 應急情況下放射性核素的γ能譜快速分析方法
WS/T 615—2018 早熟染色體凝集環輻射生物劑量估算方法
上述標準自2018年12月1日起施行。
特此通告。
國家衛生健康委員會
2018年6月15日
5 前言
本標準按照 GB/T 1.1—2009 給出的規則起草。
本標準起草單位:中國疾病預防控制中心輻射防護與核安全醫學所、中國醫學科學院放射醫學研究所、蘇州大學。
本標準主要起草人: 劉青傑、趙驊、陸雪、劉強、朱巍。
6 標準正文
6.1 1 範圍
本標準規定了通過分析早熟染色體凝集環,對電離輻射外照射受照人員進行生物劑量估算的方法。
本標準適用於發生在受照後1個月內、吸收劑量在4 Gy~20 Gy範圍內的X或γ射線、急性全身均勻或近似均勻外照射的受照人員的生物劑量估算。
6.2 2 規範性引用文件
下列文件對於本文件的應用是必不可少的。凡是注日期的引用文件,僅注日期的版本適用於本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
6.3 3 術語和定義
GB/T 28236一2011界定的以及下列術語和定義適用於本文件。
3.1
早熟染色體凝集 premature chromosome condensation;PCC
利用化學或生物的方法,間期淋巴細胞核被誘導提前進入有絲分裂期,使間期淋巴細胞核內極度分散狀態的染色質凝縮成細纖維狀的染色體樣結構。
3.2
早熟染色體凝集環 premature chromosome condensation ring;PCC-R
當早熟染色體凝集斷裂後,一條染色體的兩個斷裂末端重接形成的環狀染色體。
3.3
劑量-效應曲線 dose-effect curve
某種生物體系受到照射後的反應與受照射劑量之間存在着某種定量關係,可用適當的數學模式描述,製備出相應的反應效應與受照劑量之間關係的刻度曲線,可用其估算受照劑量。
6.4 4 早熟染色體凝集標本製備
6.4.1 4.1 主要儀器和試劑配製
主要儀器和試劑配製參見附錄A。
6.4.2 4.2 早熟染色體凝集標本製備
6.4.2.1 4.2.1 樣品採集
6.4.2.2 4.2.2 樣品接種和細胞培養
將0.5 mL肝素抗凝全血加入到4.5 mL含有20%胎牛血清的全培養基(RPMI 1640)中,每個樣品設2個平行樣,37℃恆溫培養箱中培養46 h~47 h後,加入終濃度爲50 nmol/L的花萼海綿體誘癌素A(Calyculin A)或終濃度爲500 nmol/L的岡田酸(Okadaic acid),繼續培養1 h~2 h。
6.4.2.3 4.2.3 收穫細胞
用吸管吹打培養物,轉入15 mL刻度離心管中,水平離心機250 g離心10 min,棄上清液,約留1 mL剩餘沉澱物。
6.4.2.4 4.2.4 低滲
每離心管中加入37℃預溫的0.075 mol/L氯化鉀(KCl)至8 mL~10 mL,用吸管吹打均勻,置37℃低滲10 min~30 min。
6.4.2.5 4.2.5 預固定
每離心管中加入1 mL~2 mL新配製的固定液 [甲醇/冰乙酸 = 3/1(體積比)],用吸管輕輕吹吸混勻,250 g離心10 min,棄上清液。
6.4.2.6 4.2.6 固定
每離心管中加入8 mL固定液,輕輕吹吸混勻,室溫固定20 min,250 g離心10 min,棄上清液。
6.4.2.7 4.2.7 第二次固定
加入8 mL固定液,輕輕吹吸混勻,室溫固定15 min,250 g離心10 min,棄去大部分上清液,留適量上清液。
6.4.2.8 4.2.8 細胞懸液的製備
6.4.2.9 4.2.9 製片
將2滴~3滴細胞懸液滴在預冷玻片上,過火2 s~3 s,室溫自然乾燥。
6.4.2.10 4.2.10 染色
用pH 6.8的磷酸緩衝液將吉姆薩染液(Giemsa)稀釋成8%溶液,染色8 min ~10 min,自來水沖洗後晾乾。
6.5 5 早熟染色體凝集環的分析和記錄
6.5.1 5.1 光學顯微閱片
在光學顯微鏡的低倍鏡(10倍)下,尋找合適的早熟染色體凝集分裂相;然後在油鏡(100倍)下將早熟染色體凝集分裂相調至視野正中間,計數早熟染色體凝集環的數量。
6.5.2 5.2 早熟染色體凝集環判定標準及計數標準
早熟染色體凝集環分爲空心環和實心環。空心環是呈中空的圓環形或不規則環形結構。實心環是呈實心球狀的結構,稍緻密,直徑大於早熟凝集染色單體的橫徑。在分析時不計數實心環。早熟染色體凝集環示例參見附錄B。
兩條姐妹染色單體排在一起的分裂相稱作G2/M期早熟染色體凝集分裂相,這種分裂相中出現的環稱作G2/M期早熟染色體凝集環。G2/M期早熟染色體凝集分裂相中排在一起的2個大小相近的環狀結構,計數1個早熟染色體凝集環。兩條染色單體明顯處於分開狀態的分裂相稱作M/A期早熟染色體凝集分裂相,這種分裂相中出現的環稱作M/A期早熟染色體凝集環。M/A期早熟染色體凝集分裂相中的每個環狀結構,計數1個早熟染色體凝集環。
6.5.3 5.3 結果數據的記錄和保存
檢測到早熟染色體凝集環時,需要進行拍照。將選擇分析的每一個早熟染色體凝集分裂相記錄在早熟染色體凝集環分析記錄表中。早熟染色體凝集環分析記錄表參見附錄C。
6.6 6 劑量-效應曲線的建立
6.6.1 6.1 樣品採集
6.6.2 6.2 供血者要求
2名~3名健康成年人,非放射工作者,男女均可,年齡在18歲~60歲,半年內無急慢性疾病、無射線和化學毒物接觸史,近一個月內無病毒感染史。
6.6.3 6.3 照射條件
樣品均勻照射;X或γ射線照射劑量範圍在4 Gy~20 Gy;照射劑量率選擇0.3 Gy/min~1 Gy/min,照射劑量點在6個~8個(均勻布點);37℃進行照射。照射後將樣品置37℃恆溫培養箱中修復2 h,然後進行細胞培養。
6.6.4 6.4 早熟染色體凝集標本製備、分析及記錄
早熟染色體凝集標本製備、分析和記錄按照第4章~第5章中所述方法進行。
6.6.5 6.5 數據處理
兩組間早熟染色體凝集環每細胞數的比較用泊松分佈的U檢驗,多組間早熟染色體凝集環每細胞數的比較用卡方檢驗;早熟染色體凝集環每細胞數與照射劑量的關係進行曲線擬合,對擬合迴歸方程進行假設檢驗用卡方檢驗。
6.6.6 6.6 劑量-效應曲線擬合
參照GB/T 28236-2011中4.3,對X或γ射線誘導的早熟染色體凝集環與受照射劑量之間的劑量-效應關係以擬合二次多項式爲宜,按照式(1)進行擬合:

式中:
c —— 常數項,早熟染色體凝集環每細胞數本底值(PCC環/分裂相);
α —— 劑量一次項係數;
D —— 照射劑量,單位爲戈瑞(Gy);
β —— 劑量二次項係數。
6.6.7 6.7 建立劑量-效應曲線
進行劑量估算的實驗室應建立劑量-效應曲線;有條件的實驗室可建立不同輻射類型、不同劑量率的劑量-效應曲線。
6.7 7 劑量估算
6.7.1 7.1 早熟染色體凝集標本的製備
所要估算劑量樣品的早熟染色體凝集標本製備方法均應與建立劑量-效應曲線的方法相同。
6.7.2 7.2 分析早熟染色體凝集分裂相數的確定
可先分析200個早熟染色體凝集分裂相,將得到的早熟染色體凝集環每細胞數p,代入式(2)計算出需要分析的分裂相數。

式中:
96.04 —— 採用20%的允許誤差,令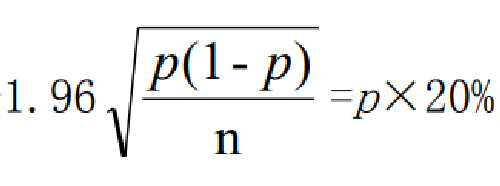 ,根據95%可信區間計算獲得的常數。
,根據95%可信區間計算獲得的常數。
6.7.3 7.3 檢測早熟染色體凝集環每細胞數和 95%可信區間的計算
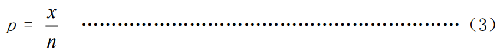
式中:
檢測早熟染色體凝集環每細胞數的95%可信區間按照式(4)計算:
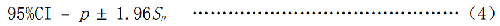
式中:
95%CI ——95%可信區間;
Sp —— 早熟染色體凝集環每細胞數的標準誤,按照式(5)計算:

式中:
6.7.4 7.4 受照劑量的估算
將所要估算劑量的標本中得到的早熟染色體凝集環每細胞數及95%可信區間的上下限代入建立的劑量-效應曲線,估算出受照劑量。事故受照人員生物劑量估算示例參見附錄D。
6.8 8 質量控制
8.1 進行早熟染色體凝集製備與分析的實驗室應有 2 名(含)以上專業技術人員,掌握電離輻射生物效應和細胞遺傳學基礎知識,熟練掌握早熟染色體凝集環顯微鏡下分析技術。每個早熟染色體凝集環需2 名專業技術人員相互確認。
8.2 標本應有唯一性編號。
7 附錄A(資料性附錄)主要儀器設備和試劑配製
7.1 A.1 主要儀器設備
A.1.4 恆溫水浴箱:用於收穫細胞。
A.1.5 低溫冰箱(-20℃)和普通冰箱:用於貯存少量實驗用試劑。
7.2 A.2 主要試劑的配製
A.2.1 Calyculin A工作液:將1 mL無水乙醇加入到10 μg花萼海綿體誘癌素A粉末中,混勻後置於-20℃低溫冰箱保存。
A.2.2 岡田酸工作液:將1 mL二甲基亞碸加入到25 μg岡田酸粉末中,混勻後置於-20℃低溫冰箱保存。
A.2.3 RPMI1640 全培養基:1L RPMI1640 培養基中含有10.4 gRPMI1640 粉末、1.3 g無水碳酸氫鈉,pH在7.0~7.2之間。RPMI1640 全培養基中含20%胎牛血清、青黴素100 IU/mL、鏈黴素100 mg/mL、植物血球凝集素200 μg/mL。
A.2.4 低滲液:稱取5.59 g氯化鉀(KCl)雙蒸水溶解後定容到1 L,終濃度爲0.075 mol/L,37℃保存。
A.2.5 固定液:將甲醇與冰乙酸以3/1(體積比)的比例混勻,使用前新鮮配製。
A.2.6 磷酸緩衝液:稱取4.705 g磷酸氫二鉀及4.54 g磷酸二氫鈉雙蒸水溶解後定容到1 L,pH爲6.8,終濃度爲1/15 mol/L,4℃保存。
A.2.7 Giemsa染液:稱取1.0 g吉姆薩粉末放入研鉢中,加入少量甘油混勻研磨,邊研磨邊加入甘油至66 mL,充分混勻後,置於60℃水浴箱中2 h。冷卻至室溫後,加入66 mL甲醇,充分攪拌混勻,避光密閉保存。
注:試劑級別爲分析純。
8 附錄B(資料性附錄)早熟染色體凝集環示例
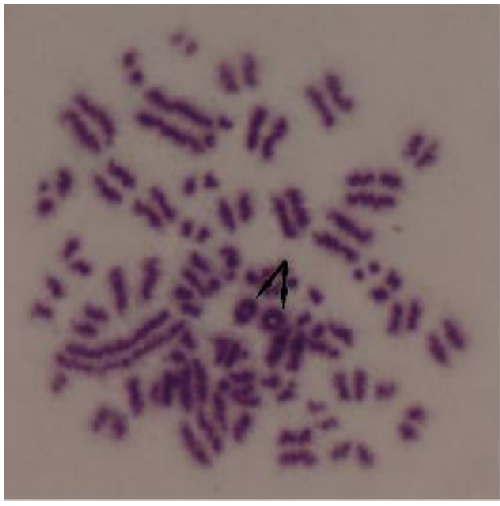
a) G2/M–PCC細胞中的1對空心環
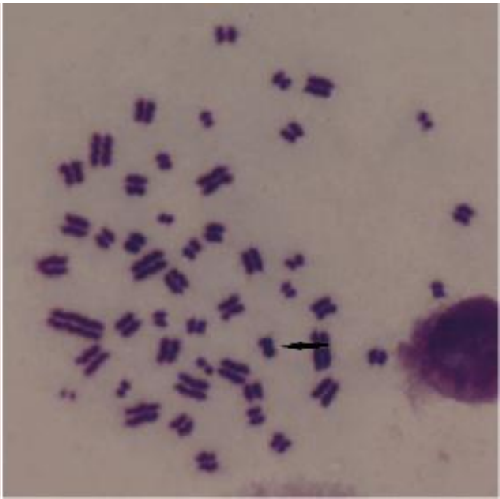
b) G2/M–PCC細胞中的1對實心環
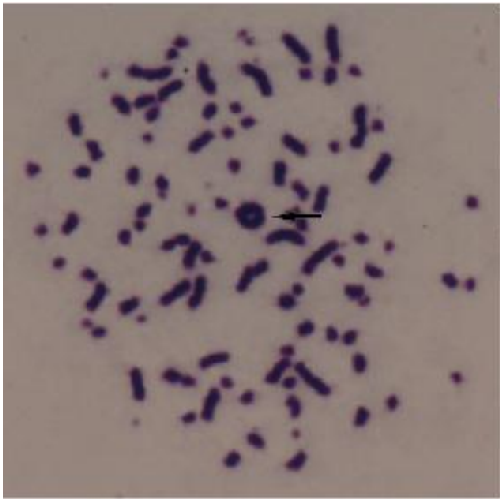
c) M/A–PCC細胞中的1個空心環
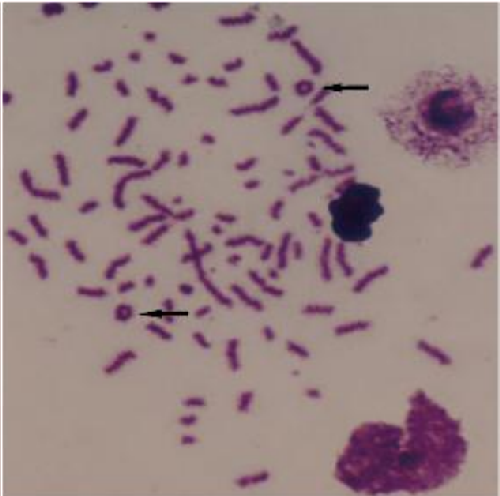
d) M/A–PCC細胞中的2個空心環
10 附錄D(資料性附錄)劑量估算應用示例
某男性受到60Coγ射線事故照射,受照後24 h內取外周血,分析1000個早熟染色體凝集分裂相,觀察到57個早熟染色體凝集環。
95%可信區間:p±1.96Sp=0.057±1.96×0.0075,因此,檢測早熟染色體凝集環每細胞數可信區間爲(0.0423,0.0717)。
根據本實驗室所建立的60Coγ射線照射離體血建立的早熟染色體凝集環的劑量-效應曲線:Y=0.0033+0.0083D+0.00022D2(劑量率爲1 Gy/min) 其中Y 爲早熟染色體凝集環每細胞數,D 爲劑量(Gy)。
將0.057、0.0423和0.0717分別代入Y 項,解方程後求出平均劑量爲5.63 Gy,下限爲4.23 Gy,上限爲6.95 Gy,估算的劑量爲5.63(4.23,6.95)Gy。


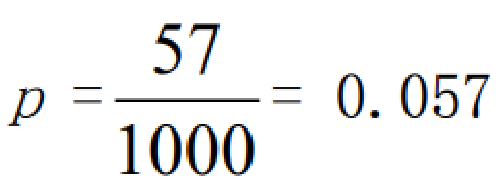 ,標準誤
,標準誤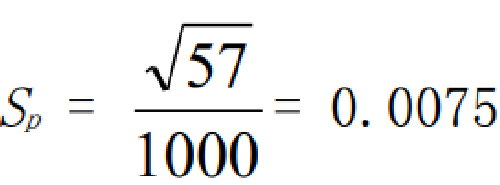 。
。