3 註解
剛地弓形蟲(Toxoplasma gondii Nicolle &Manceaux, 1908)是貓科動物的腸道球蟲,由法國學者Nicolle及Manceaux在剛地梳趾鼠(Ctenodactylus gondii)的脾臟單核細胞內發現,蟲體呈弓形,故命名爲剛地弓形蟲。該蟲呈世界性分佈,人和許多動物都能感染,引起人獸共患的弓形蟲病(toxoplasmosis),尤其在宿主免疫功能低下時,可致嚴重後果,是一種重要的機會致病原蟲(opportunistic protozoan)。我國首例弓形蟲感染是鍾惠瀾(1957)從一例患者的肝穿刺塗片中發現,之後有關弓形蟲病的報道逐漸增多。
4 剛地弓形蟲的形態
弓形蟲發育的全過程有5種不同形態的階段:滋養體、包囊、裂殖體、配子體和卵囊。其中滋養體、包囊和卵囊與傳播和致病有關。
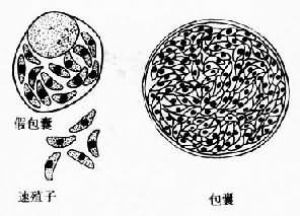
4.1 滋養體
指在中間宿主細胞內營分裂繁殖的蟲體,包括速殖子(tachyzoite)和緩殖子(bradyzoite)。遊離的速殖子呈香蕉形或半月形,一端較尖,一端鈍圓;一邊扁平,另一邊較膨隆。速殖子長4-7μm,最寬處2-4μm。經姬氏染劑染色後可見胞漿呈藍色,胞核呈紫紅色、位於蟲體中央;在覈與尖端之間有染成淺紅色的顆粒,稱副核體。細胞內寄生的蟲體呈紡錘形或橢圓形,以內二芽殖法不斷繁殖,一般含數個至20多個蟲體,這個由宿主細胞膜包繞的蟲體集合體稱假包囊(pseudocyst),內含的蟲體稱速殖子(圖2)。
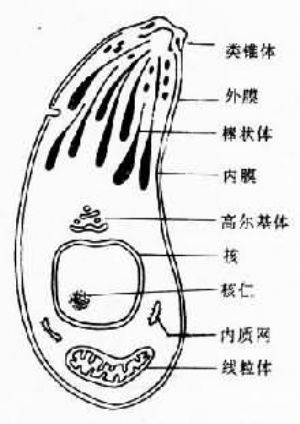
圖2 弓形蟲速殖子模式圖
4.2 包囊
圓形或橢圓形,直徑5-100μm,具有一層富有彈性的堅韌囊壁。
囊內含數個至數千個滋養體,囊內的滋養體稱緩殖子,可不斷增殖,其形態與速殖子相似,但蟲體較小,核稍偏後。包囊可長期在組織內生存。
4.3 卵囊(oocyst)
圓形或橢圓形,大小爲10-12μm,具兩層光滑透明的囊壁,其內充滿均勻小顆粒。成熟卵囊內含2個孢子囊,分別含有4個新月形的子孢子。
4.4 裂殖體
在貓科動物小腸絨毛上皮細胞內發育增殖,成熟的裂殖體爲長橢圓形,內含4-29個裂殖子,一般爲10-15個,呈扇狀排列,裂殖子形如新月狀,前尖後鈍,較滋養體爲小。
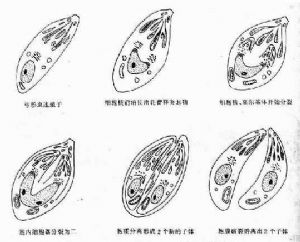
圖3 弓形蟲速殖子內二芽殖分裂過程模式圖
4.5 配子體
遊離的裂殖子侵入另外的腸上皮細胞發育形成配子母細胞、進而發育爲配子體。配子體有雌雄之分,雌配子體積可達10-20μm,核染成深紅色,較大,胞質深藍色;雄配子體量較少,成熟後形成12-32個雄配子,其兩端尖細,長約3μm。雌雄配子受精結合發育爲合子(zygote),而後發育成卵囊。
5 剛地弓形蟲的生活史
弓形蟲生活史比較複雜,全過程需要兩個宿主,分別進行無性生殖和有性生殖。在貓科動物體內完成有性生殖,同時也進行無性生殖,因此貓是弓形蟲的終宿主兼中間宿主。在人或其它動物體內只能完成無性生殖,爲中間宿主。有性生殖只限於貓科動物小腸上皮細胞內進行,稱腸內期發育,無性生殖階段可在腸外其它組織、細胞內進行,稱腸外期發育。弓形蟲對中間宿主的選擇極不嚴格,除哺乳動物外,鳥類和人等都是中間宿主,對組織的選擇也無特異親嗜性,可寄生在除紅細胞外的幾乎所有有核細胞中(圖4)。
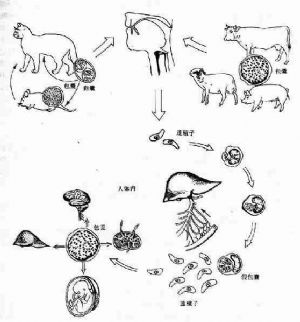
5.1 宿主體內的發育
有弓形蟲的包囊或假包囊吞入消化道而感染。此外食入或飲入被成熟卵囊污染的食物或水也可遭致感染。包囊內的速殖子、假包囊的緩殖子或卵囊內的子孢子在小腸腔逸出,主要在迴腸部侵入小腸上皮細胞發育增殖,經3-7天,上皮細胞內的蟲體形成裂殖體,成熟後釋出裂殖子,侵入新的腸上皮細胞形成第二、三代裂殖體,經數代增殖後,部分裂殖子發育爲雌雄配子體,繼續發育爲雌雄配子,雌雄配子受精成爲合子,最後形成卵囊。卵囊破上皮細胞進入腸腔,隨糞便排出體外。在適宜的溫、溼度環境中經2~4天即發育爲具有感染性的成熟卵囊。貓吞食不同發育階段蟲體後排出卵囊的時間也不同,通常吞食包囊後約3~10天就能排出卵囊,而吞食假包囊或卵囊後約需19~48天才能排出卵囊。受染貓每天可排出卵囊1,000萬個,持續10~20天.成熟卵囊是重要的感染階段。
5.2 中間宿主體內的發育
中間宿主如人、牛、羊、豬等吞食後,在腸內逸出子孢子、速殖子或緩殖子,隨即侵入腸壁經血或淋巴進入單核巨噬細胞系統的細胞內寄生,並擴散至全身各器官組織,如腦、淋巴結、肝、心、肺、肌肉等,進入細胞內並發育增殖,形成假包囊。當速殖子增殖到一定數量,胞膜破裂,速殖子侵入新的組織細胞,反覆增殖。速殖子侵入宿主細胞是一個主動的過程,包括粘附、穿入和內在化三個階段,其機制是相當複雜的。在免疫功能正常的機體,部分速殖子侵入宿主細胞後,特別是腦、眼、骨骼肌的蟲體增殖速度減慢,轉化爲緩殖子,並分泌成囊物質,形成包囊。包囊在宿主體內可存活數月、數年或更長。當機體免疫功能低下或長期應用免疫抑制劑時,組織內的包囊可破裂,釋出緩殖子,進入血流和其它新的組織細胞繼續發育增殖形成包囊,當宿主免疫力低下時則形成假包囊。假包囊和包囊是中間宿主之間或中間宿主與終宿主之間互相傳播的主要感染階段。
6 剛地弓形蟲的致病
6.1 致病機制
根據蟲株的侵襲力、增殖速度、包囊形成與否以及對宿主的致死率等,剛地弓形蟲可分爲強毒株和弱毒株。目前國際上公認的強毒株代表爲RH株,弱毒株代表爲Beverley株。在動物身上連續傳代後,可提高其毒力。有研究表明,蟲株毒力與蟲體棒狀體分泌的磷酸脂酶A2有關。絕大多數哺乳動物、人及家畜等對弓形蟲都是易感中間宿主,易感性則因宿主的種類而有所差異。
速殖子是弓形蟲的主要致病階段,在細胞內寄生並迅速增殖,以致破壞細胞,速殖子逸出後又侵犯鄰近的細胞,如此反覆破壞,因而引起組織的炎症反應、水腫、單核細胞及少數多核細胞浸潤。
包囊內緩殖子是引起慢性感染的主要階段。包囊因緩殖子增殖而體積增大,擠壓器官,可致功能障礙。包囊增大到一定程度,可因多種因素而破裂,釋放出緩殖子。釋出的緩殖子多數被宿主免疫系統所破壞,一部分緩殖子可侵入新的細胞並形成包囊。死亡的緩殖子可誘導機體產生遲髮型超敏反應,並形成肉芽腫病變,後期的纖維鈣化竈多見於腦、眼部等。宿主感染弓形蟲後,正常情況下可產生有效的保護性免疫,多數無明顯症狀,當宿主有免疫缺陷或免疫功能低下時才引起弓形蟲病。
6.2 臨牀表現
弓形蟲感染通常是無症狀的,但先天性感染和免疫功能低下者的獲得性感染常引起嚴重的弓形蟲病。
先天性弓形蟲病:感染弓形蟲的初孕婦女,可經胎盤血流將弓形蟲傳播給胎兒。在孕前3個月內感染,可造成流產、早產、畸胎或死胎,畸胎發生率高,如無腦兒、小頭畸形、小眼畸形、脊柱裂等。受染胎兒或嬰兒多數表現爲隱性感染,有的出生後數月甚至數年纔出現症狀。據研究表明,嬰兒出生時出現症狀或發生畸形者病死率爲12%,而存活者中90%有精神發育障礙,典型臨牀表現爲腦積水、大腦鈣化竈、腦膜腦炎和運動障礙;其次表現爲弓形蟲眼病,如視網膜脈絡膜炎。此外,還可伴有發熱、皮疹、嘔吐、腹瀉、黃疸、肝脾腫大、貧血、心肌炎、癲癇等。
獲得性弓形蟲病:可因蟲體侵襲部位和機體的免疫應答程度的不同而呈現不同的臨牀表現,因而無特異的症狀與體徵,需與有關疾病相鑑別。淋巴結腫大是獲得性弓形蟲病最常見的臨牀表現,多見於頜下和頸後淋巴結。弓形蟲常累及腦和眼部,引起中樞神經系統損害,如腦炎、腦膜腦炎、癲癇和精神異常,弓形蟲眼病以視網膜脈絡膜炎爲多見,成人表現爲視力突然下降,嬰幼兒可見手抓眼症,對外界事物反應遲鈍,也有出現斜視、虹膜睫狀體炎、色素膜炎等,多爲雙側性病變。
隱性感染者若患有惡性腫瘤、因長期接受免疫抑制劑和放射治療等引起的醫源性免疫受損或先天性、後天性免疫缺陷者,如艾滋病患者,都可使隱性感染轉變爲急性或亞急性,從而出現嚴重的全身性弓形蟲病,其中多因併發弓形蟲腦炎而死亡。
7 剛地弓形蟲的免疫
弓形蟲是一種機會致病性原蟲,機體的免疫狀態,尤其是細胞免疫狀態與感染的發展和轉歸密切相關。
弓形蟲在免疫功能健全的宿主,細胞免疫主要起保護性作用,其中T細胞、巨噬細胞、NK細胞及其它細胞介導的免疫應答起主導作用。致敏的T細胞能產生多種具有多種生物活性的細胞因子發揮免疫調節作用。弓形蟲感染可誘導Th1細胞和巨噬細胞產生免疫上調因子(IL-4、IL-6、IL-10)。
IFN-γ是抗弓形蟲免疫中起主導作用的細胞因子,可活化巨噬細胞產生一氧化氮殺傷蟲體。IL-4和IL-10可抑制IFN-γ的表達,尤其是IL-10、是IFN-γ的有力拮抗劑,從而在弓形蟲感染的宿主體內發揮重要的免疫抑制作用。在弓形蟲感染的不同時期,免疫上調因子和免疫下調因子的表達水平及出現時間有所不同,從而構成免疫調節網絡,調節弓形蟲感染及其結局。
人類感染弓形蟲後能誘導特異性抗體。感染早期IgM和IgA升高,前者在4個月後逐漸消失,後者消失較快,感染一個月後即被高滴度的IgG所替代,並維持較長時間。IgG能通過胎盤傳至胎兒,因此新生兒血清檢查常可出現陽性結果,這種抗體通常在出生後5~10月消失,抗感染的免疫保護作用不明顯。近來有研究證實,特異性抗體與速殖子結合,在補體參與下可使蟲體溶解或促進速殖子被巨噬細胞吞噬。
8 剛地弓形蟲的實驗診斷
8.1 病原學檢查
具有確診意義。
(1)塗片染色法 可取急性期患者的腹水、胸水、羊水、腦脊液、骨髓或血液等,離心後取沉澱物作塗片,或採用活組織穿刺物塗片,經姬氏染液染色,鏡檢弓形蟲滋養體。該法簡便,但陽性率不高,易漏檢。此外也可切片用免疫酶或熒光染色法,觀察特異性反應,可提高蟲體檢出率。
(2)動物接種分離法或細胞培養法 將待檢樣本接種於小鼠腹腔,一週後剖殺,取腹腔液,鏡檢滋養體,陰性需盲目傳代至少3次;待檢樣本亦可接種於離體培養的單層有核細胞。動物接種分離法或細胞培養法是目前比較常用的病原檢查法。
8.2 血清學試驗
由於弓形蟲病原學檢查比較困難,陽性率又不高,所以血清學試驗是目前廣泛應用的重要輔助診斷手段。幾種常用的方法簡要介紹如下。
(1)染色試驗(dye test,DT) 爲經典血清學方法,具有良好的特異性、敏感性和重複性。其原理是:活滋養體在有致活因子的參與下,與樣本的特異性抗體作用,使蟲體表膜破壞而不爲美藍所染。鏡檢時60%蟲體不着色者爲陽性,如測定滴度,則以50%蟲體不着色者爲血清最高滴度。蟲體多數着色者爲陰性。
(2)間接血凝試驗(IHA) 該法有較好的特異性和敏感性,操作簡易,適用於流行病學調查,應用廣泛。
(3)間接免疫熒光抗體試驗(IFA) 以整蟲爲抗原,採用熒光標記的二抗檢測特異性抗體。該法可測同型及亞型抗體,其中檢測IgM具有早期診斷價值。
(4)酶聯免疫吸附試驗驗 用於檢測宿主的特異循環抗體和抗原,已有多種改良法廣泛用於早期急性感染和先天性弓形蟲病的診斷。
9 剛地弓形蟲的流行病學
9.1 流行概況
該蟲呈世界性分佈,廣泛存在於多種哺乳動物體內,人羣感染也較普遍。據血清學調查,人羣抗體陽性率爲25%~50%,估計全球約有10億人感染弓形蟲,絕大多數屬隱性感染。我國在1983-1986年採用統一的IFA法調查了19個省(市、區),36個市,23個地區(州),141個縣的81968人,平均陽性率爲5.16%。弓形蟲感染常與生活習慣、生活條件、接觸貓科動物等因素有關。易感家畜有豬、貓、牛、羊、犬、馬、兔等;野生動物有猩猩、狼、狐狸、野豬等至少32種以上;曾在52種齧齒類體內發現弓形蟲。家畜的感染率可達10%~50%,可食用的肉類感染相當普遍,嚴重影響畜牧業發展,亦威脅人類健康。
造成弓形蟲病廣泛流行的原因有:①生活史各階段都具感染性;②中間宿主廣泛,140餘種哺乳動物易感;③在終宿主之間、中間宿主之間以及終宿主與中間宿主間均可互相傳播;④包囊在中間宿主組織內可長期生存;⑤卵囊排放量大,被感染的貓可持續10~20天每天排放約10000萬個卵囊;⑥滋養體、包囊和卵囊均具有較強的抵抗力。滋養體在低溫冷凍下可保持較長時間而不喪失活力;卵囊在室溫下可活3個月,在潮溼的泥土中可存活117天,糞便中的卵囊在自然界常溫常溼條件下可存活1~1.5年;豬肉中的包囊在冰凍狀態下可活35天。
9.2 流行環節
(1)傳染源 動物是本病的傳染源,貓及貓科動物是重要傳染源。人經胎盤的垂直傳播也具有傳染源的意義。
(2)傳播途徑 食入未煮熟的含各發育期弓形蟲的肉製品、蛋品、乳類或被卵囊污染的食物和水可致感染;肉類加工人員和實驗室工作人員有可能經口、鼻、眼結合膜或破損的皮膚、粘膜感染;輸血或器官移植也可能引起感染;節肢動物攜帶卵囊也具有一定的傳播意義。
(3)易感人羣 人對弓形蟲普遍易感。胎兒和嬰幼兒的易感性較成人高,腫瘤和免疫功能缺陷或受損患者比正常人更易感。人的易感性隨接觸機會增多而上升,但無性別上的差異。