1 拼音
chāo shēng duō pǔ lè tāi ér jiān hù yí chǎn pǐn zhù cè jì shù shěn chá zhǐ dǎo yuán zé
《超聲多普勒胎兒監護儀產品註冊技術審查指導原則》由國家食品藥品監督管理局於2012年5月10日食藥監辦械函[2012]210號印發。
本指導原則旨在指導和規範超聲多普勒胎兒監護儀產品的技術審評工作,幫助審評人員增進對該類產品原理、結構、主要性能、預期用途等方面的理解,把握技術審評工作的基本要求和尺度,以便對產品安全性、有效性作出系統評價。
本指導原則是對超聲多普勒胎兒監護儀的一般要求,申請人/生產企業應依據具體產品的特性對註冊申報材料的內容進行充實細化。
本指導原則是對產品的技術審查人員和申請人/生產企業的指導性文件,但不包括註冊審批所涉及的行政事項,亦不作爲法規強制執行。
本指導原則是在當前認知水平下制訂的,隨着科學技術的不斷髮展,本指導原則的相關內容也將進行適時的調整和更新。審查人員仍需密切關注相關適用的標準以及註冊法規的變化,以確認申報的產品是否符合法規的要求。
2 一、 適用範圍
本指導原則適用於《醫療器械分類目錄》中6823-3中“超聲母嬰監護設備”中的超聲多普勒胎兒監護儀。如果超聲多普勒胎兒監護儀作爲一個系統中的一部分,則本指導原則也適用於該部分。
本指導原則不適用於超聲多普勒胎兒心率儀,超聲多普勒胎兒心率儀指根據多普勒原理從孕婦腹部獲取胎兒心臟運動信息,不用作連續監護,僅獲取胎兒心臟運動信息。該類儀器採用的行業標準爲YY O448-2009《超聲多普勒胎兒心率儀》。
本指導原則所涉及的超聲多普勒胎兒監護儀,其定義採用YY O449-2009《超聲多普勒胎兒監護儀》3.1,即“由主機、超聲探頭、宮縮壓力傳感器及與之相連接的儀器組成,採用超聲多普勒原理,具有監測和貯存胎心率、宮縮數據的功能,並可設置報警。”
3 二、 技術審查要點
3.1 (一) 產品名稱的要求
產品名稱應以發佈的國家標準、行業標準以及《醫療器械產品分類目錄》中的產品名稱爲依據。產品名稱應以體現產品的工作原理、技術結構特徵、功能屬性爲基本準則。如“超聲胎兒監護儀”,“超聲母親/胎兒綜合監護儀”等,不宜採用病症命名。
3.2 (二) 產品的結構和組成
一般由主機、超聲探頭、宮縮壓力傳感器及與之相連接的儀器組成。一般的結構示意框圖如下:
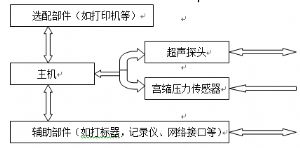
對超聲多普勒胎兒監護儀及其部件進行全面評價所需的基本信息應包含但不限於以下內容:
1.產品設計和說明
應包括對產品工作原理的概述,該部分內容應當包括:
1.1 產品構成說明
1.1.1 整機總體構造的詳細描述,應包括所有組成部分,應給出有標記的圖示(如圖表、照片和圖紙等),清楚的標識關鍵部件/組件,其中包括充分的解釋來方便理解這些圖示。
1.1.2對使用者可接觸的所有控制裝置的說明,包括但不限於:
1.1.2.1控制設置範圍;
1.1.2.2缺省值(如果有)。
1.1.3 產品工作框圖(應包括所有應用部分,以及信號輸入和輸出部分)。
1.1.4 對所有組件的全面描述,至少包括:
1.1.4.1傳感器的規格、參數、工作方式、超聲換能器的輸出功率和聲強等;
1.1.4.2所有附件、配件的列表;
1.1.4.3擬配合使用的設備或部件,並應對接口進行描述。
1.2 接觸患者(孕婦)的材料
應有直接接觸或間接接觸患者(孕婦)的材料的組成清單,應提供所有材料的商品名稱和基本成分名稱(如聚乙烯、聚碳酸酯等)。應根據GB/T 16886等標準給出所用材料的生物相容性評價。
3.3 (三) 產品工作原理
超聲多普勒胎兒監護儀採用超聲多普勒原理對孕婦及胎兒進行連續監護,並在出現異常時及時提供報警信息。一般系附在孕婦腹部,通常採用多元扁平超聲多普勒換能器。
超聲多普勒胎兒監護儀可實時監護胎兒心跳等變化情況,爲臨牀提供準確的診斷及處理資料,它既可單獨使用,也可通過網絡接口與產科中央監護系統連接,形成一套有中央站的網絡監護系統,也可以同時提供多種移動應用解決方案。
檢測胎兒心率信號經處理後將胎兒心率變化趨勢用軌跡描記出來,並能同時插記母體的宮縮曲線。
醫生根據這二條曲線的變化趨勢可以初步判斷胎兒的健康情況,以便及時採取措施、保障胎兒健康,提高新生兒質量。
超聲多普勒胎兒監護儀所使用的超聲波生物物理特性主要有機械效應、熱效應和空化效應。具體產品可能涉及以上全部或部分效應。但其強度一般很低。
3.4 (四) 產品作用機理
超聲多普勒胎兒監護儀作爲非治療設備,其設備向人體傳送能量和從人體取得能量以獲取所需信息。該產品用於診斷、監護,不以治療爲目的,所以超聲聲輸出的強度應儘可能的低。
3.5 (五) 產品適用的相關標準
下列文件對於本指導原則的應用是必不可少的。凡是注日期的引用文件,僅注日期的版本適用於本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
GB/T 191-2008《包裝儲運圖示標誌》
GB 9706.1-2007《醫用電氣設備 第1部分:安全通用要求》(IEC 60601-1:1988,IDT)
GB 9706.9—2O08《醫用電氣設備 第2-37部分:醫用超聲診斷和監護設備安全專用要求》(IEC 60601-2-37:2004,IDT)
GB 9706.15-2008《醫用電氣設備 第1-1部分:安全通用要求 並列標準:醫用電氣系統安全要求》(IEC 60601-1-1:2000,IDT)
GB/T 14710-2009《醫用電器環境要求及試驗方法》
GB/T 16886.1-2011《醫療器械生物學評價 第1部分:評價與試驗》
YY 0505-2005《醫用電氣設備 第1-2部分:安全通用要求 並列標準:電磁兼容要求和試驗》
YY0709-2009《醫用電氣設備 第1-8部分:並列標準 安全通用要求 醫用電氣設備和醫用電氣系統中報警系統的測試和指南》
YY/T 1142—2003《超聲診斷和監護儀器頻率特性的測試方法》
3.6 (六) 產品的預期用途
主要用於監測胎兒的心率和胎動以及宮縮壓力,對孕婦及胎兒進行連續監護,並在出現異常時及時提供報警信息。
3.7 (七) 產品的主要風險
1.超聲多普勒胎兒監護儀的風險管理報告應符合YY/T 0316-2008《醫療器械 風險管理對醫療器械的應用》中的相關要求,判斷與產品有關的危害估計和評價相關的風險,控制這些風險並監視風險控制的有效性。申請人提供註冊產品的風險管理報告應扼要說明:
(1)在產品的研製階段,已對其有關可能的危害及產生的風險進行了估計和評價,並有針對性地實施了降低風險的技術和管理方面的措施;
(2)在產品性能測試中部分驗證了這些措施的有效性,達到了通用和相應專用標準的要求;
(3)對所有剩餘風險進行了評價;
(4)全部達到可接受的水平;
2.風險管理報告的內容至少包括:
(3)產品應符合的安全標準;
申報方應按照YY/T0316-2008《醫療器械 風險管理對醫療器械的應用》附錄C的34條提示,對照產品的實際情況作出針對性的簡明描述。
注意:產品如存在34條提示以外的可能影響安全性的特徵,也應作出說明。
申報方應根據自身產品特點,根據YY/T 0316-2008附錄E的提示,對危害、可預見事件序列、危害處境及可導致的損害作出判定。表1所列爲超聲多普勒胎兒監護儀的常見危害:
編號 | 可預見的事件序列 | 危害處境 | 損害 | |
1 | ||||
1.1 | 電能 | |||
1.1.1 | 電源輸入插頭剩餘電壓 | 導致對孕婦電擊傷害 | ||
1.1.2 | 過量的漏電流 | 絕緣/隔離效果不符合要求 | ||
1.1.3 | 通過應用部分(探頭、宮縮傳感器)引起孕婦觸電 | 1. 隔離措施不足; 2. 電介質強度達不到要求; | ||
1.1.4 | 誤接觸高壓部分 | 1. 安全地線沒有或失效; 2. 高壓絕緣介質年久老化,絕緣性能下降,導致高壓擊穿 | ||
1.2 | 熱能 | |||
1.2.1 | 非預期的或過量的傳感器表面溫升 | 傳感器壓電晶片振動的機械耗損、聲阻抗匹配不佳引起的損耗和高壓開關損耗 | ||
1.2.2 | ||||
1.3 | ||||
1.3.1 | ||||
1.3.2 | ||||
1.4 | 機械力 | |||
1.4.1 | 操作者缺乏相關常識 | 孕婦腹部壓力過大,引起被孕婦不適 | ||
1.4.2 | 銳邊或尖角 | 主機或/和治療頭表面有銳邊或尖角 | 使用者和孕婦被劃傷 | |
2 | ||||
2.1 | 生物不相容性 | 1. 與孕婦接觸的傳感器材料有致敏性; 2. 與孕婦接觸的傳感器材料有刺激性; | ||
3 | ||||
3.1 | 設備受到外界的電磁干擾 | 1. 產品設計時電磁屏蔽及電路抗擾設計不充分; | 不能正常工作 | |
3.2 | 1. 屏蔽、濾波及接地技術不完善; | 引起其他設備不能正常工作 | ||
4 | 器械使用的危害 | |||
4.1 | 誤操作 | 1. 未經培訓的人員使用操作 | 使被孕婦不適 | |
4.2 | 使孕婦皮膚造成不適 | |||
4.3 | 交叉感染 | 可導致感染性疾病 | ||
4.4 | 工作數據的準確性 | 監測數據不準確 | 導致正確狀態誤報或危險狀態不報 | |
(6)明確風險可接受準則。
(7)對所判定的危害確定初始風險控制方案,列出控制措施實施證據清單。
3.8 (八) 產品的主要技術指標
1.安全要求:
至少包括以下要求:
1.1 電氣安全應當符合GB 9706.1,GB 9706.9、GB9706.15和YY 0505的要求。
1.2 生物相容性,直接接觸或間接接觸患者(孕婦)或操作者的材料組成,應當進行生物相容性評價(參見《醫療器械生物學評價和審查指南》),並給出清單,提供所有材料的商品名稱和基本成分名稱(如鋁合金、硅橡膠、聚乙烯、聚碳酸酯等)。
至少包括以下要求:
2.1超聲輸出
胎心率的測量和顯示範圍不窄於65次/min~210次/min。
2.2 報警功能
儀器應裝有發光或發聲的報警裝置,在測量胎心率超過預置值時,應產生報警信號,並可消除警報。從胎心率越限至開始報警的時間不大於30s。
2.3 宮縮壓力測量範圍
宮縮壓力的測量範圍應覆蓋0~100單位,其非線性誤差不大於±10%。
2.4 貯存記錄功能
2.4.1 內置實時記錄器的儀器其走紙速度的誤差不超過±5%。
2.4.2 內置實時記錄器的基線漂移不大於全量程的5%。
2.5 功能要求
3.環境試驗要求
生產企業應在產品標準中按GB/T14710規定氣候環境試驗和機械環境試驗的組別,試驗要求及檢測項目,按YY 0449-2009表1執行。
3.9 (九)產品的檢測要求
性能要求一般至少應包括標準YY0449-2009《超聲多普勒胎兒監護儀》中的5.2胎心率測量和顯示範圍、 5.4報警功能、 5.5宮縮壓力測量範圍和5.10功能要求;
安全要求至少應包括:漏電流、保護接地阻抗(如適用),電介質強度可考慮抽樣檢驗。
3.10 (十) 產品的臨牀要求
1.符合《醫療器械註冊管理辦法》附件12規定,執行國家標準、行業標準的超聲多普勒胎兒監護儀,國內市場上已有同類型產品,可以不提供臨牀試驗資料。
2.生產企業在申報超聲多普勒胎兒監護儀產品註冊時,可以提交已上市同類產品的臨牀試驗資料,同時提交申報產品與已上市同類產品的對比說明。對比說明的內容應當包括:產品結構組成、工作原理、主要技術性能指標、關鍵部件、預期用途等內容。
(4)宮縮壓力測量範圍
(5)貯存記錄功能
3.不符合上述條件的,生產企業在申報超聲多普勒胎兒監護儀產品註冊時,應提交完整的臨牀試驗資料。臨牀試驗機構應爲國家食品藥品監督管理局認定公佈的藥品臨牀試驗基地。臨牀試驗應按照《醫療器械臨牀試驗規定》以及《醫療器械註冊管理辦法》附件12的要求進行。
3.11 (十一)產品的不良事件歷史記錄
暫未見相關報道。
3.12 (十二)產品介紹、標籤、包裝標識
產品使用說明書應當符合《醫療器械介紹、標籤和包裝標識管理規定》(國家食品藥品監督管理局令第10號)的要求以及GB 9706.1-2007、GB 9706.9—2O08和/或GB 9706.15-2008的相關要求。
由於超聲多普勒胎兒監護儀是通過一定量的超聲能量作用於人體達到醫學監測的目的,在以上的規定和標準中,涉及慎重使用的部分應儘可能詳細,清楚,以提示使用者慎重使用。
1.安全預防措施;
2.圖標符號的說明,特別是危險符號,注意事項符號的說明;
3.電磁兼容性的說明,提示用戶,電磁信號有可能對本產品產生干擾;
4.聲輸出資料的公佈說明;
5.產品的安裝,連接。
產品的標籤,外部標記中特別是涉及安全使用的部分也應符合相關的標準(如GB9706系列標準等)。
3.13 (十三)註冊單元劃分的原則
超聲多普勒胎兒監護儀的註冊單元劃分應以《醫療器械註冊管理辦法》爲依據,一般以基本工作原理、主要技術結構、性能指標、預期用途爲劃分條件。
1.不同的工作原理、技術結構產品應作爲不同的註冊單元進行註冊。
2.主要性能指標差異較大的、或不能覆蓋兩種或兩種以上的超聲多普勒胎兒監護儀應考慮劃分爲不同的註冊單元。
3.14 (十四)同一註冊單元中典型產品的確定原則和實例
同一註冊單元應按產品風險與技術指標的覆蓋性確定典型產品。一般來說,典型產品應是同一註冊單元內能夠代表本單元內其他產品安全性和有效性的產品,即功能最全、結構最複雜和風險最高的產品。在同一註冊單元中,若僅輔助功能不同,則可以作爲同一產品的多個型號加以區分。
如某企業生產的具有不同輔助功能的超聲多普勒胎兒監護儀,其主要性能指標一致[見本指導原則(八)2.1—2.5],可作爲同一註冊單元,在同一註冊單元的兩個型號中,A型號具有一種輔助功能,B型號具有兩種以上輔助功能幷包括前者,或A型號的性能和功能是B型號的子集,應選取B型號作爲典型產品。
4 三、 審查關注點
(一)產品的性能要求和安全要求是否執行了規定國家和行業的強制性標準。
1.技術指標[見本指導原則(八)2.1—2.5)];
2.預期用途;
3.關鍵零部件(探頭或傳感器)。
(五)介紹必須告知用戶的信息是否完整以及外部標記是否符合相關的要求。
(六)註冊單元的劃分。
(七)關注聲輸出資料的公佈。
5 編寫說明
5.1 一、指導原則編寫的目的
本指導原則用於指導和規範超聲多普勒胎兒監護儀在註冊申報過程中審評人員對註冊材料的技術審評。
超聲多普勒胎兒監護儀是藉助超聲能量作用對患者(孕婦)予以監測,其臨牀適用較爲廣泛。本指導原則旨在讓初次接觸該類產品的註冊審評人員對產品的原理、結構、主要性能、預期用途等各個方面有一個基本的瞭解,同時讓技術審評人員在產品註冊技術審評時把握基本的尺度,以確保產品的安全、有效。
5.2 二、指導原則編寫的依據
(一)《醫療器械監督管理條例》
(二)《醫療器械註冊管理辦法》(16號令)
(三)《醫療器械臨牀試驗規定》(5號令)
(四)《醫療器械介紹、標籤和包裝標識管理規定》(10號令)
(五)《醫療器械標準管理辦法》(31號令)
(六)關於印發《境內第一類醫療器械註冊審批操作規範(試行)》和《境內第二類醫療器械註冊審批操作規範(試行)》的通知(國食藥監械[2005]73號)
(七)國家食品藥品監督管理局發佈的其他規範性文件
(八)相關標準
GB/T 191-2008《包裝儲運圖示標誌》
GB 9706.1-2007《醫用電氣設備 第1部分:安全通用要求》(IEC 60601-1:1988,IDT)
GB 9706.9—2O08《醫用電氣設備 第2-37部分:醫用超聲診斷和監護設備安全專用要求》(IEC 60601-2-37:2004,IDT)
GB 9706.15-2008《醫用電氣設備 第1-1部分:安全通用要求 並列標準:醫用電氣系統安全要求》(IEC 60601-1-1:2000,IDT)
GB/T 14710-2009《醫用電器環境要求及試驗方法》
GB/T 16886.1-2001《醫療器械生物學評價 第1部分:評價與試驗》
YY 0505-2005《醫用電氣設備 第1-2部分:安全通用要求 並列標準:電磁兼容要求和試驗》
YY 0709-2009《醫用電氣設備 第1-8部分:並列標準 安全通用要求 醫用電氣設備和醫用電氣系統中報警系統的測試和指南》
YY/T 1142—2003《超聲診斷和監護儀器頻率特性的測試方法》
5.3 三、指導原則中部分具體內容編寫的考慮
(一)性能指標以超聲多普勒胎兒監護儀的產品標準YY 0449-2009 《超聲多普勒胎兒監護儀》爲依據。產品的主要技術指標及工作原理的制定徵求了全國醫用電器標準化技術委員會超聲設備分技術委員會的意見,並在一定範圍內召開了專家諮詢會和多次集體討論,本內容主要依據現行有效的行業標準YY 0449-2009超聲多普勒胎兒監護儀,今後如有修訂,應按照新標準的要求執行。
(二)安全要求以GB 9706.1-2007《醫用電氣設備 第1部分:安全通用要求》(IEC 60601-1:1988,IDT)爲依據。
(三)風險管理的要求主要以YY/T0316-2008《醫療器械 風險管理對醫療器械的應用》爲依據。
(四)“產品介紹、標籤、包裝標識”部分以國家相關的法規和相關標準爲依據,沒有具體地在指導原則中闡述,僅對“慎重使用”部分作了提示。
5.4 四、指導原則的編寫人員
本指導原則的編寫人員由湖北省食品藥品監督管理局醫療器械行政審批人員、技術審批人員、國家食品藥品監督管理局湖北醫療器械質量監督檢驗中心的有關專家共同組成。在編寫過程中,徵求了有關檢測機構、臨牀醫療機構及國內部分生產企業的意見,以充分利用各方面的信息和資源,儘量確保指導原則的正確、全面、實用。