5 關於前縱隔腫物
前縱隔腫物多爲實性,可以經胸腔鏡進行腫物活檢以明確診斷,也能完成某些腫瘤切除手術。與經前胸入路接近後縱隔腫物的胸腔鏡手術一樣,可經後胸入路接近前縱隔腫物,便於觀察腫物和周圍組織的關係,有利於操作。通常胸腔鏡套管切口選擇在腋後線第5肋間,其餘兩個套管切口選擇在腋中線第3和腋前線第4肋間,實際位置可根據病變部位進行調整(圖5.10.2.3.1-0-1~5.10.2.3.1-0-3)。

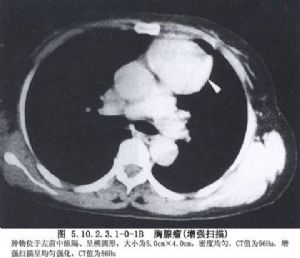

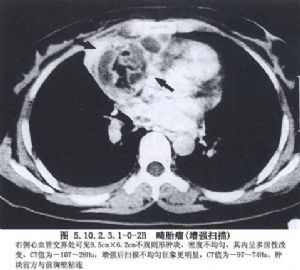

首先探查縱隔結構,包括心包、主動脈、鎖骨下動脈、神經等,結合術前胸部CT檢查確定病變部位。如果行腫物活檢,最好先針吸以免損傷血管,然後使用內鏡活檢鉗夾取病變,電凝止血;如考慮爲惡性病變,應將活檢組織裝在內鏡袋內取出。
6 關於重症肌無力
重症肌無力是以橫紋肌神經肌肉傳導障礙爲特點的自身免疫性疾病。由於突觸處傳導的安全係數降低而致骨骼肌易疲勞和無力,臨牀表現爲活動後橫紋肌無力、容易疲勞、休息後可以緩解。這種疾病並不多見,其發病率爲0.5~5/10萬人,可發生於任何年齡,但女性多見於20~30歲,男性多見於50歲以上,女性與男性之比爲3∶2。
6.1 1.病理生理
在大多數重症肌無力患者血清中,可測出lgG類乙酰膽鹼受體抗體(AchRab),重症肌無力患者有功能的乙酰膽鹼受體減少,其原因可能是抗AchR抗體與神經肌肉接頭處的AchR結合,阻止乙酰膽鹼與其受體的結合,導致肌無力。
重症肌無力除累及橫紋肌外,還有胸腺的病理改變,早期的屍體解剖和近年來胸腺切除標本的大量觀察發現:80%~90%的MG患者胸腺有病理學異常,其中65%~75%的患者伴有胸腺濾泡增生,接近10%的患者伴有胸腺瘤,其他10%~20%的MG患者表現爲胸腺萎縮。胸腺瘤一般由上皮細胞或淋巴細胞組成,良性多見,惡性主要根據腫瘤累及周圍組織、胸膜及心包。胸腺瘤多發現在>30歲的重症肌無力患者,男性居多。兒童和青少年重症肌無力患者多爲胸腺增生。在光鏡下觀察到有癌特徵的胸腺癌甚爲少見。近年的研究發現正常胸腺內有多種細胞,包括肌樣上皮細胞(myoid cell)、胸腺細胞和上皮細胞等,這些細胞均能表達AchR,結構完全與突觸後膜上的AchR相同,但在蛋白水平AchR表達則僅見於胸腺肌樣上皮細胞,這種細胞主要位於胸腺髓質和皮髓質交界區,其形態學和生物化學特點是細胞內含有橫紋肌肌管。生理情況下AchR與免疫系統形成免疫耐受,不能誘導機體產生特異性的AchRab,目前尚不知道MG時如何破壞已經形成的自身耐受,激發自身免疫反應。
6.2 2.發病機制
目前認爲AchRab在重症肌無力發病中具有重要作用,其可能機制有:①加速突觸後膜上乙酰膽鹼受體的退化;②調整或加速受體和抗體複合物細胞內的退化;③減少合成乙酰膽鹼;④與受體結合後,佔領空間,妨礙受體與乙酰膽鹼結合,加速受體的降解和破壞。但也有研究發現:胸腺切除後的患者,血清中抗體的滴度從未轉爲陰性;血漿置換後,血清中抗體滴度的下降是短暫的,而臨牀症狀的緩解可持續數週或數月。因此認爲,血清中抗體滴度與臨牀症狀並無直接關係。
有研究發現補體C3、C9也可能在重症肌無力發病機制中起作用,這可能是抗體與受體結合後激活補體,破壞突觸後膜,進一步發展到突觸後膜由補體介導的融解。實驗性研究發現後期患者,其周圍循環血中的T細胞減少,主要減少T細胞的亞類3AI和OKT4。切除胸腺後,這些變化恢復正常。在動物實驗性重症肌無力急性期,神經肌肉接頭處有嚴重的淋巴細胞浸潤;重症肌無力患者胸腺和周圍血的淋巴細胞對體外培養的肌細胞有細胞毒性作用,直接破壞突觸後膜,上述說明細胞免疫在發病機制中有可能起一定作用。
重症肌無力與遺傳的關係尚無定論,目前認爲自身免疫性疾病多發生在遺傳的基礎上,具有HLA-A1、A8、B8、B12、DW3的重症肌無力患者多爲女性,青年起病,胸腺增生,無腫瘤,乙酰膽鹼受體抗體檢出率低,用抗膽鹼酯酶藥無效,早期切除胸腺療效好。具有HLA-A2、A3的重症肌無力患者多爲男性,40歲以後起病,多合併胸腺瘤,乙酰膽鹼受體抗體檢出率高。提示遺傳在發病中有着重要作用。
胸腺切除術後重症肌無力症狀緩解的原因,可能是①去除啓動自身免疫的胸腺肌樣細胞表面新的抗原決定簇;②去除乙酰膽鹼受體致敏的T細胞;③去除分泌乙酰膽鹼受體抗體的B細胞;④去除與免疫功能障礙有關的其他胸腺因素。有些重症肌無力病例胸腺切除效果不顯著,其可能原因是:①胸腺切除不完全;②神經肌肉接頭處的損傷已不可逆;③在胸腺外,位於脾臟和周圍淋巴結中的淋巴細胞羣仍有類似胸腺的影響。
6.3 3.臨牀表現
主要是變化不定的肌肉無力,一般清晨較輕,活動後加重,可選擇性的累及眼外肌及全身的骨骼肌。眼外肌受累者表現爲複視及眼瞼下垂,可爲單側或雙側,甚至交替出現。咬肌受累可出現咀嚼無力、吞嚥困難、食物從鼻腔反流,部分患者可有語言含糊及鼻音重等。呼吸肌受累,可引起呼吸困難。Osserman根據臨牀表現分爲以下四型:Ⅰ型,即單純眼肌型,症狀侷限於眼部;Ⅱa型,即輕度全身型,有全身症狀但呼吸肌未受累及;Ⅱb型,即中度全身型,除全身症狀更爲明顯外,呼吸肌有輕度受累;Ⅲ型,即急性暴發型,患者迅速出現全身肌無力,並有明顯的呼吸系統症狀;Ⅳ型,即晚期嚴重型,患者從單純眼肌型或輕度全身型發展至嚴重型最少要2年以上。最近美國重症肌無力基金會(MGFA)公佈了新的臨牀分型(表5.8.3.1-0-1),可在臨牀中試用。上述分型對治療的選擇及療效的評價有幫助。值得注意是,40%的重症肌無力起病後1個月的臨牀表現僅侷限於眼部,而真正的單純眼肌型僅佔整個重症肌無力的16%。

6.4 4.診斷
重症肌無力的診斷除根據上述臨牀表現外,尚應作乙酰膽鹼酯酶抑制試驗。由於我國已不生產依酚氯銨(滕喜龍),故採用新斯的明代替。成人肌內注射新斯的明0.5mg,如爲重症肌無力,於注射後數分鐘就可看到症狀明顯緩解,但亦有延至半小時纔出現效果。肌電圖檢查呈減弱反應,全身型MG患者標準肌電圖的敏感性可達76%,單纖維肌電圖可以提高肌電圖的敏感性和特異性,中度至重度MG患者100%呈現異常,甚至單純眼肌型患者、單纖維肌電圖的陽性率也可達60%~75%。大多數MG患者乙酰膽鹼抗體水平特異性增高,但抗體水平高低與疾病的嚴重程度相關不密切。
10%~25%的MG患者合併胸腺瘤,而30%~60%的胸腺瘤患者伴有MG。由於MG患者胸腺瘤的發生率很高,因而應行影像學檢查。有的胸腺瘤已有明顯增大,而胸部X線平片仍不能發現,所以都應作CT掃描。
MG患者常合併其他自身免疫性疾病,如突眼性甲狀腺腫、慢性淋巴細胞性甲狀腺炎(橋本甲狀腺炎)、類風溼性關節炎、系統性紅斑狼瘡和惡性貧血等。有時須與肌無力綜合徵即Lambert-Eaton綜合徵鑑別,這種綜合徵主要表現爲近端肌肉的波動性無力,可累及面部,肌電圖檢查不像MG患者呈減弱反應。肌無力綜合徵亦可能是自身免疫所致,常與惡性病變相關,特別是小細胞肺癌,大約70%的Lambert-Eaton綜合徵與小細胞肺癌有關,而且抗膽鹼酯酶藥物治療效果不明顯。
6.5 5.治療
MG的治療包括抗乙酰膽鹼酯酶藥物,免疫抑制、血漿交換及胸腺切除術等。抗膽鹼酯酶藥物最常應用的是嗅比斯的明或溴新斯的明。新斯的明作用快而短,肌內或靜脈注射,常用於圍手術期的處理。抗膽鹼酯酶藥物主要是緩解MG的症狀,對疾病本身並無明顯作用。皮質激素治療亦可改善MG的症狀,通常用於抗膽鹼酯酶藥物治療效果不佳或不良反應重而難以耐受的患者,但長期使用激素不良反應較大。抗膽鹼酯酶藥物治療無效或不能耐受的患者,亦可採用硫唑嘌呤行免疫抑制治療,其有效率可達71%~83%,但不良反應較多,限制了長期使用。血漿置換可迅速、明顯緩解症狀,但效果持續時間不長,多用於幫助MG患者脫離呼吸機或嚴重全身型胸腺切除術手術前的準備。
自1941年Blalock等報道胸腺切除以來,胸腺切除術治療MG的療效已得到公認。MG行胸腺切除主要基於80%以上的患者有胸腺增生或胸腺瘤及在MG患者的胸腺中發現有乙酰膽鹼受體抗體和其他橫紋肌抗原抗體,這些自身抗體的抗原存在於胸腺的肌樣細胞,胸腺切除可取得顯著的效果(圖5.8.3.1-0-1)。
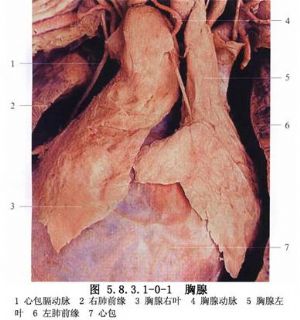
7 適應症
胸腺切除術適用於:
1.所有不伴胸腺瘤的全身型MG患者,採用抗膽鹼酯酶藥物效果不佳或劑量不斷增加者。
2.反覆發生肺部感染,引起一次以上肌無力危象或膽鹼能神經中毒危象者。
4.MG伴胸腺瘤者。
5.單純眼肌型有20%~30%的自然緩解率,手術適應證應從嚴掌握,特別是學齡前兒童。長時間藥物治療反應不佳者,方可考慮手術治療。
9 術前準備
1.掌握抗膽鹼酯酶藥物的應用規律,調整用藥劑量,待病情穩定,能維持一般生活。
2.藥物反應差,症狀嚴重的全身型MG患者,可行血漿置換療法,使血中抗乙酰膽鹼受體抗體迅速降低,減輕抗體對突觸後膜的封閉,經1~2次血漿置換,病情改善後及時手術。
11 手術步驟
11.1 1.手術徑路
雖然胸腺主要位於前上縱隔,但異位胸腺甚多(圖5.8.3.1-1)。由於有不同的看法,因而有不同的手術徑路。
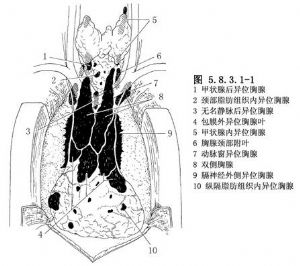
(1)經頸部胸腺切除:於胸骨切跡上方2cm,沿皮紋作弧形長約5~6cm切口(圖5.8.3.1-2),兩側達胸鎖乳突肌,在頸闊肌深面遊離皮瓣,上方至甲狀腺平面,下方至胸骨平面,正中向兩側分開胸骨甲狀肌,即可見到胸腺。胸腺位於胸骨甲狀肌深面,甲狀腺下靜脈的前面,向上常達甲狀腺下極,這一徑路創傷小,但由於顯露較差,目前較少採用。

(2)胸骨劈開徑路:經胸骨劈開有兩種徑路,一爲全胸骨劈開徑路,即上方起於胸骨切跡上1~2cm,下方至劍突,切開皮膚、皮下組織後,按常規從胸骨切跡開始正中劈開胸骨,骨髓腔骨蠟止血後,撐開切口,顯露胸腺。另一徑路爲部分胸骨劈開,即從胸骨切跡劈開胸骨至第3肋間,並在第3肋間向左或右橫斷半側胸骨。
(3)擴大胸腺切除徑路:系前述之頸部切口加全胸骨正中劈口徑路。
全胸骨劈開與擴大胸腺切除徑路,是基於縱隔脂肪內可能含有異位胸腺,強調清除所有縱隔脂肪組織,但併發症的發生率較經頸徑路和部分胸骨劈開徑路高。幾種徑路所行胸腺切除的遠期效果,尚無嚴格的對比研究證明其差異。
(4)電視胸腔鏡下胸腺切除徑路:於右胸腋前線及腋中線之間第6肋間切一小口,進入胸腔,置入胸腔鏡探查,在胸腔鏡指引下分別於腋前線第3或4肋間及鎖骨中線第5肋間切開形成操作孔。
11.2 2.胸腺切除
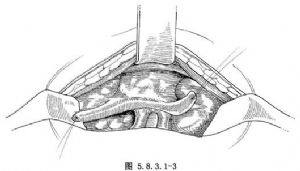
(1)經頸徑路在顯露胸腺後,可從胸腺左上極開始,左上極靠近甲狀腺下靜脈,結紮切斷後,以胸腺上的結紮線作牽引,向下鈍性遊離。然後遊離右上極胸腺。向下遊離至胸骨切跡後,手指插入縱隔,將胸腺與胸骨後、兩側胸膜及後壁無名靜脈細心分開,遇有條索應結紮切斷,將整個胸腺完整切除(圖5.8.3.1-3,5.8.3.1-4)。

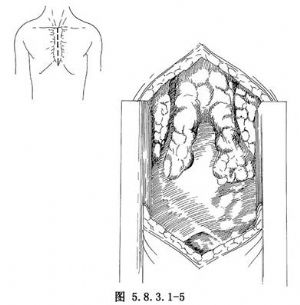
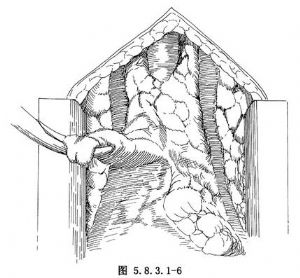
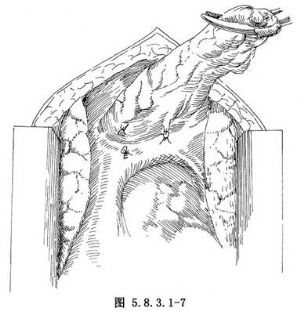
(2)胸骨劈開徑路:全胸骨劈開徑路與擴大胸腺切除徑路的胸腺切除方法大致相同。撐開器撐開劈開的胸骨後,將胸膜往兩側分離,剪開胸腺前之包膜,先分離胸腺的兩下極(圖5.8.3.1-5,5.8.3.1-6),分離後可用粗線貫穿縫合作爲牽引,再遊離後壁及兩側。分離中遇到胸腺靜脈予以結紮切斷。最後遊離胸腺之兩上極,兩上極可有甲狀腺下動脈的分支,予以結紮切斷,即可將胸腺完整切除(圖5.8.3.1-7)。
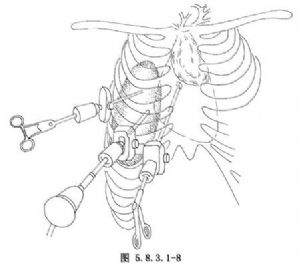
(3)電視胸腔鏡下胸腺切除:於膈神經前沿縱行切開前縱隔胸膜,鈍性推開胸骨後間隙,顯露胸腺右葉,用卵圓鉗提起胸腺下極,沿包膜鈍性和銳性解剖胸腺後方,近無名靜脈處仔細分離出胸腺靜脈,鈦夾鉗閉後切斷。再向上解剖胸腺上極,予以切除。以相同方法分離解剖切除左葉胸腺,並行縱隔脂肪清除(圖5.8.3.1-8)。
11.3 3.縱隔脂肪清除
胸腺切除後,應將膈神經前方的脂肪組織儘可能清除,包括頸部上極周圍,大血管及心包前方。全胸骨劈開徑路及擴大胸腺切除徑路,脂肪組織清除更爲徹底。
11.4 4.放置引流
沖洗切口。胸骨劈開徑路可放置乳膠管或硅膠管引流,縱隔部分剪多個側孔,由劍突處引出。部分胸骨劈開者可在第3肋間平面胸骨右或左另戳一小口引出。電視胸腔鏡手術置胸腔閉式引流。術畢連接閉式引流或負壓引流器吸引。
11.5 5.關閉切口
13 術後處理
1.對症狀較重的全身型或手術結束後體力恢復不佳的患者,可延遲拔出氣管插管,送入監護室後,繼續人工呼吸機輔助治療。
2.嚴密觀察呼吸、血壓、脈搏變化,牀旁備好氣管插管及氣管切開(或環甲膜切開)設備。
4.使用抗生素,但避免用鏈黴素、新黴素、卡那黴素、多粘菌素、慶大黴黴素。
5.對已採用皮質激素治療者,術後應適當增加劑量,以預防腎上腺功能不足。
6.避免使用氯丙嗪、地西泮(安定)、苯妥英鈉、奎尼丁、嗎啡、硫酸鎂、巴比妥鈉等。
7.繼續使用抗膽鹼酯酶藥物,用藥劑量開始時應比術前減少1/2~1/3,然後再根據病情增減。
8.24~48h後拔出引流。
9.MG術後應密切注意危象的發生,可因抗膽鹼酯酶藥物過量而出現膽鹼能危象,表現爲肌無力加劇,瞳孔縮小、出汗、腹痛、肌束震顫,亦可因藥物劑量不足而發生肌無力危象,兩種危象往往難以區別。注射速效、短效的依酚氯銨(氯化騰喜龍)可以改善肌無力危象患者的肌力,而對膽鹼能危象患者無效,是個很好的鑑別方法,但目前已無此種藥物生產。因而對呼吸困難、痰多、已發生危象的患者,應立即行氣管插管或氣管切開,機械通氣治療,同時減少甚至暫時停用抗膽鹼酯酶藥物,以後根據情況逐步調整劑量。氣管內分泌物多者,可用阿托品0.5mg皮下或靜脈注射。