3 頭孢硫脒藥典標準
3.1 品名
3.1.1 中文名
3.1.2 漢語拼音
Toubaoliumi
3.1.3 英文名
Cefathiamidine
3.2 結構式
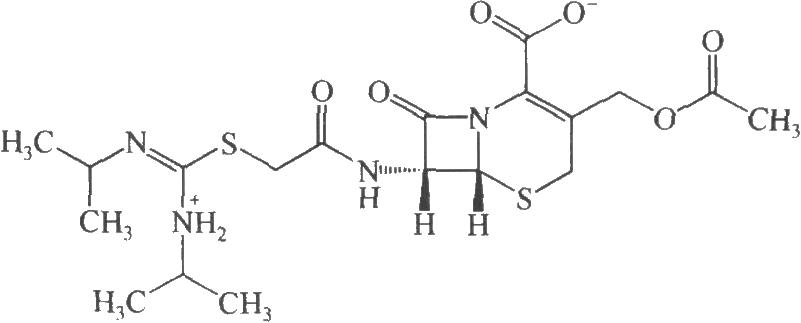
3.3 分子式與分子量
C19H28N4O6S2 472.59
3.4 來源(名稱)、含量(效價)
本品爲(6R,7R)-3-[(乙酰氧基)甲基]-7-[α-(N,N-二異丙基脒硫基)乙酰氨基]-8-氧代-5-硫雜-1-氮雜雙環[4.2.0]辛-2-烯-2-甲酸內銨鹽。按無水物計算,含C19H28N4O6S2不得少於97.0%。
3.5 性狀
本品爲白色或類白色結晶性粉末;幾乎無臭,有引溼性。
本品在水中極易溶解,在乙醇中微溶,在丙酮、三氯甲烷或乙醚中不溶。
3.5.1 比旋度
取本品,精密稱定,加水溶解並定量稀釋製成每1ml中約含10mg的溶液,依法測定(2010年版藥典二部附錄Ⅵ E),比旋度爲+135°至+145°
3.6 鑑別
(1)取本品與頭孢硫脒對照品適量,分別加水溶解並製成每1ml中約含20mg的溶液,作爲供試品溶液與對照品溶液,取對照品溶液和供試品溶液等量混合,作爲混合溶液。照薄層色譜法(2010年版藥典二部附錄Ⅴ B)試驗,吸取上述三種溶液各1μl,分別點於同一硅膠G薄層板(取硅膠G 2.5g,加含1%羧甲基纖維素鈉的磷酸鹽緩衝液(pH 5.8)適量,調漿制板,經105℃活化1小時,放入乾燥器中備用]上,以新鮮製備的甲醇-異丙醇-磷酸鹽緩衝液(pH 5.8)(7:2:1)濾過後爲展開劑,展開,晾乾,100℃加熱30分鐘,置碘蒸氣中顯色。供試品溶液所顯主斑點的位置和顏色應與對照品溶液主斑點的位置和顏色相同,混合溶液應顯單一斑點。
(2)在含量測定項下記錄的色譜圖中,供試品溶液主峯的保留時間應與對照品溶液主峯的保留時間一致。
(3)本品的紅外光吸收圖譜應與對照的圖譜(《藥品紅外光譜集》924圖)一致。
以上(1)、(2)兩項可選做一項。
3.7 檢查
3.7.1 結晶性
取本品少許,依法檢查(2010年版藥典二部附錄Ⅸ D),應符合規定。
3.7.2 酸度
取本品,加水製成每1ml中含0.1g的溶液,依法測定(2010年版藥典二部附錄Ⅵ H),pH值應爲4.0~6.0。
3.7.3 溶液的澄清度與顏色
取本品5份,分別加水製成每1ml中含0.1g的溶液,溶液應澄清無色;如顯渾濁,與1號濁度標準液(2010年版藥典二部附錄Ⅸ B)比較,均不得更濃;如顯色,與黃色或黃綠色6號標準比色液(2010年版藥典二部附錄Ⅸ A第一法)比較,均不得更深。
3.7.4 有關物質
取本品適量,加流動相溶解並稀釋製成每1ml中含0.5mg的溶液,作爲供試品溶液;精密量取適量,用流動相定量稀釋製成每1ml中含5μg的溶液,作爲對照溶液。照含量測定項下的色譜條件,取對照溶液10μl注入液相色譜儀,調節檢測靈敏度,使主成分色譜峯的峯高約爲滿量程的20%,再精密量取供試品溶液與對照溶液各10μl,分別注入液相色譜儀,記錄色譜圖至主成分峯保留時間的4倍。供試品溶液色譜圖中如有雜質峯,單個雜質峯面積不得大於對照溶液主峯面積的0.5倍(0.5%),各雜質峯面積的和不得大於對照溶液主峯面積的1.5倍(1.5%),供試品溶液色譜圖中任何小於對照溶液主峯面積0.05倍的峯可忽略不計。
3.7.5 殘留溶劑
甲醇、乙醇、丙酮與二氯甲烷取本品0.2g,精密稱定,置頂空瓶中,精密加水2ml使溶解,密封,作爲供試品溶液;精密稱取甲醇、乙醇、丙酮、二氯甲烷各適量,加水定量稀釋製成每1ml含甲醇0.3mg、乙醇0.5mg、丙酮0.5mg、二氯甲烷0.06mg的混合溶液,精密量取2ml置頂空瓶中,密封,作爲對照品溶液。照殘留溶劑測定法(2010年版藥典二部附錄Ⅷ P第二法)測定。以6%氰丙基苯基-94%二甲基聚硅氧烷(或極性相近)爲固定液的毛細管柱爲色譜柱,起始溫度40℃,待二氯甲烷出峯後,以每分鐘30℃的速率升溫至150℃,維持5分鐘;進樣口溫度爲200℃;檢測器溫度爲250℃;頂空瓶平衡溫度爲80℃,平衡時間爲30分鐘}取對照品溶液頂空進樣,各峯間的分離度均應符合要求。取供試品溶液與對照品溶液分別頂空進樣,記錄色譜圖,按外標法以峯面積計算,均應符合規定。
3.7.6 水分
取本品,照水分測定法(2010年版藥典二部附錄Ⅷ M第一法 A)測定,含水分不得過1.5%。
3.7.7 可見異物
取本品5份,每份各2g,加微粒檢查用水溶液,依法檢查(2010年版藥典二部附錄Ⅸ H),應符合規定。
3.7.8 不溶性微粒
取本品3份,加微粒檢查用水製成每1ml中含80mg的溶液,依法檢查(2010年版藥典二部附錄Ⅸ C),每1g樣品中含10μm以上的微粒不得過6000粒,含25μm以上的微粒不得過600粒。
3.7.9 細菌內毒素
取本品,依法檢查(2010年版藥典二部附錄Ⅺ E),每1mg頭孢硫脒中含內毒素的量應小於0.075EU。
3.7.10 無菌
取本品,加無菌水適量溶解後,全部轉移至不少於500ml的0.9%無菌氯化鈉溶液中,用薄膜過濾法處理後,依法檢查(2010年版藥典二部附錄Ⅺ H),應符合規定。
3.8 含量測定
照高效液相色譜法(2010年版藥典二部附錄Ⅴ D)測定。
3.8.1 色譜條件與系統適用性試驗
用十八烷基硅烷鍵合硅膠爲填充劑;以磷酸鹽緩衝液(取無水磷酸氫二鈉2.76g,枸櫞酸1.29g,加水溶解並稀釋成1000ml)-乙腈(80:20)爲流動相;檢測波長爲254nm。取頭孢硫脒對照品適量,加水溶解並定量稀釋成每1ml中含頭孢硫脒0.5mg的溶液,在90℃水浴中加熱30分鐘,取10μl注入液相色譜儀,記錄色譜圖,頭孢硫脒峯與相鄰雜質峯的分離度應大於2.0。
3.8.2 測定法
取本品適量,精密稱定,加水溶解並定量稀釋製成每1ml中約含頭孢硫脒0.1mg的溶液,精密量取10μl注入液相色譜儀,記錄色譜圖;另取頭孢硫脒對照品適量,同法測定。按外標法以峯面積計算,即得。
3.9 類別
β-內酰胺類抗生素,頭孢菌素類。
3.10 貯藏
3.11 製劑
3.12 版本
《中華人民共和國藥典》2010年版