1 概述
經頸靜脈肝內門腔靜脈內支架分流術(TIPS)是治療門脈高壓、上消化道出血的介入放射學新療法。它利用外科分流原理,通過一系列介入器具的使用,在肝實質內肝靜脈與門靜脈間建立起人工分流通道,從而降低門脈壓力、減少或消除由於門脈高壓所致的食道靜脈曲張破裂出血、腹水等症狀。
TIPS是在經頸靜脈門脈造影,經皮經頸靜脈肝穿技術日益成熟的基礎上發展起來的。TIPS的突破在於金屬內支架的推廣應用,將金屬支架用於支撐肝內分流道,在較長時間內(19~48周)保持通暢,4周後支架內表面有一層1~1.5mm的菲薄內膜覆蓋。
1980年Eckhauser等研究肝臟病理變化以觀察外科分流術的預後,發現肝穿活檢中存在mallory bodies,又稱櫻桃小體(cherry bodies)。cherry bodies多量和少量時,術後3月、1年、5年生存率分別爲60%、10%、5%及89.85%、74.70%、45.39%,表明cherry bodies有獨特的預示分流術後預後及遠期效果評估的價值。cherry bodies可發生在Child各級病人,以酒精性肝硬化Child C級最爲常見。
1988年,德國學者Richter等首次將TIPS應用於臨牀,並於1991年報道了16例成功的TIPS。其後Zemel(1991),Ring(1992)相繼報道了成功的TIPS結果。1993年TIPS術在各國得以推廣應用。
TIPS器械主要包括TIPS-1000及RUPS-100兩種器械。
3 別名
經頸靜脈肝內門體分流術;TIPS
5 禁忌證
嚴重的心腎功能不全、重型肝炎、難以糾正的凝血障礙,中、重度黃疸爲TIPS禁忌證。Azoulay認爲,TIPS雖相對無創,但可增加肝硬化病人的高動力循環狀態。Feoral認爲,Child-Pugh積分大於11分者不宜行TIPS,但部分學者認爲,Child C級患者雖肝臟血流遭受嚴重障礙,但術後血流動力學狀態相對穩定。因此,在決定是否手術時,一定要全面綜合考慮。
1.絕對禁忌證 ①右心衰竭伴中心靜脈壓升高;②肝臟多囊性病變;③嚴重肝功能損害。④巨大肝癌浸犯肝門,可能妨礙內支撐器置放。
6 準備
1.化驗檢查 血、尿常規、出凝血時間、凝血酶原時原時間,肝、腎功能,電解質及CO2CP,血糖,血氨。
2.內窺鏡或上消化道造影 瞭解食管靜脈曲張程度,排除其他疾患。
7 方法
1.頸內靜脈穿刺 患者取仰臥位,頭向左側15°~20°,暴露出右側頸部,取右耳乳突至右胸鎖乳突肌鎖骨頭連線中上1/3處爲穿刺點,穿刺針與皮膚成20°~30°角,沿胸鎖乳突肌鎖骨頭方向,進針4cm左右。患者可抬高一腿或作Valsava動作促使頸內靜脈充盈。注意進針勿深,以免刺破胸膜,造成氣胸。
2.經導絲送入10F長鞘至下腔靜脈-肝靜脈開口水平。此步應在X線監視下進行,動作應輕柔。應配備心電監測儀,部分患者可出現一過性房性早搏,一旦出現頻發的心律失常時,應暫停操作。
3.經導絲引入5F導管行肝靜脈造影,以瞭解肝靜脈解剖及其毗鄰下腔靜脈位置,確定穿刺點。大部分患者選擇距下腔靜脈一肝靜脈開口水平(肝右或肝中靜脈)右側2~3cm處爲穿刺點。對於門脈血流離肝方向且肝功較差的患者,肝靜脈楔形造影能清晰顯示門脈及其分支情況,協助定位穿刺,此時可將5F導管嵌至肝靜脈遠端造影5ml/25ml(每秒量/總量)。
4.送入外套管保護的穿刺針至穿刺處,調節穿刺針轉向,使穿刺針指向門脈主分支方向(一般爲距門脈分又部2cm之門脈右支),囑患者憋氣,穿刺,回抽有血後,注入造影劑觀察,確認穿刺門脈成功後,換入180cm Amplatz導絲至脾靜脈或腸繫膜上靜脈。
5.導入5F側孔造影導管(或豬尾管)至門脈主幹造影(15ml/45ml),然後測門脈壓及下腔靜脈壓。
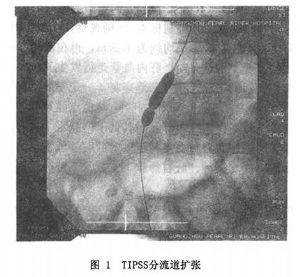
6.送入直徑10mm,長60mm球囊導管擴張肝內穿刺道,此時可見肝、門靜脈壁凹跡,囑患者憋氣,於體外皮膚兩凹跡處作鉛標記,以便釋放支架時定位,反覆擴張至凹跡消失,撤出球囊(圖1)。
7.沿Amplatz導絲引入支架釋放,釋放時肝、門靜脈壁各應多出1cm以保證支撐整個分流道,若未能支撐開肝靜脈壁,可在原支架處相重疊釋放另一支架。一般只要定位準確,一個6cm長的stent足以支撐整個分流道,支架釋放後若開放不全,可用球囊擴張(圖2)。

8.重複門脈造影(15ml/45ml)及測壓。
9.術後處理 TIPS術後處理應注意血氨水平,限制蛋白攝入量(40g/d)以防止肝性腦病,口服潘生丁或阿司匹林120~160mg/d,或長期小劑量(50mg/d)或連續服用進口抵克力得,使血小板最大聚集率由正常降到20%~30%,或INR(凝血酶原時原時間比值)在3~4.5,以防止分流道早閉。此外,應注意肝、腎功能監測並建立定期全面追蹤制度(術後一週、一月、三月、半年)。
10.TIPS術後併發症及處理
(1)狹窄與閉塞 是造成再出血和腹水的原因,亦爲影響TIPS術後長期療效的主要因素。TIPS術後狹窄與閉塞率多在30%以上。Freedman的長期觀察報道,狹窄與閉塞率可達75%。TIPS術後狹窄和閉塞與操作不當,如支架釋放時沒有撐開整個分流道、支架釋放後成角扭曲、頻繁穿刺刺激肝、門靜脈壁或抗凝不當,引起血栓形成及假內膜增生有關。
(2)肝性腦病 發生率5%且絕大部分可被臨牀控制。Conn認爲,保持一定的門脈梯度壓及TIPS術後的向肝性分流特點,減少了腸道對有害物質的吸收,有利於防止肝性腦病發生,而Larberge則認爲,肝性腦病的發生與血流方向無關。
(3)與操作有關的併發症有肝動脈損傷、肝梗死、肝包膜損傷、腹內出血、膽道損傷、氣胸、心包填塞等,其他併發症還有ARDS、腎功衰、肝功衰、敗血症、支架遊走等,但這類併發症的發生率較低。
8 注意事項
操作注意事項。
1.頸內靜脈穿刺在頸內靜脈畸形或開始誤穿頸動脈造成血腫時相當困難,一般穿刺超過10分鐘,考慮從股靜脈引入長導絲定位,以減少併發症,縮短手術時間,Buckley提供了經左頸內靜脈的TIPS,在肝右靜脈與下腔靜脈角度較小,Rups-100不易通過時可考慮。Larberge報道了經股靜脈於肝右下靜脈和右門脈間建立分流道的病例。
2.TIPS難點是肝、門靜脈間穿刺,初期於術前行肝穿門脈造影,置入Dormia籃於門脈中標記,但因其費時且增高腹內出血機率而已廢棄。經腸繫膜上動脈或脾動脈和肝靜脈造影,可較好地確定肝、門靜脈毗鄰關係,因肝硬化時肝內血管循環障礙,間接門脈造影可以靜脈注射罌粟鹼30~60mg或前列腺素E,以擴張血管,提高顯影效果。肝靜脈楔形造影在門脈血流向肝方向時顯影不準,且存在一定損傷。Chet報道了利用CO2作造影劑用於TIPS,使造影劑用量大爲減少,尤其在肝靜脈楔形造影中,氣體的低粘滯性使之能大量快速地通過肝微血管牀,使5F導管在嵌插不完全的狀態下也能獲得良好的顯像。三維CT、MRI能清晰顯示肝、門靜脈解剖與毗鄰臟器的關係,排除佔位性病變,是一種無創性檢查。Jesus報道了41例B超引導下穿刺TIPS,其成功的穿刺均少於7分鐘,手術總時間45~105分,造影劑用量均少於100ml,其成功經驗值得借鑑。穿刺一般在肝右靜脈上支(肝中靜脈)與門脈右支間,但有時需選用其它位置,如肝右(中)至門脈分叉部,至門脈左支,肝左靜脈至門脈左支,肝右靜脈下支至門脈右支(左股靜脈入路)。穿刺方向一般爲後上到前下走行。杜湘珂等通過對人肝臟肝靜脈與門靜脈的標本和剝製標本70例觀察,認爲TIPS較好的穿刺點是在肝右葉內下腔靜脈肝後段至肝右靜脈平均約爲4.9cm,再在後方穿刺約0.55cm,進入門靜脈右後葉上段,建立通道。肝硬化時,肝內血管走行發生了較大變化,最佳穿刺點及途徑的選擇需根據具體病例確定。選擇分叉部穿刺,一定要確認其是否在肝實質內。Scott對31例尸解報道,48.4%的門脈分叉部在肝外。其他點的穿刺方向同樣需要確認是否在肝內。肝右靜脈下支一般不作爲穿刺部,因其低於門脈水平入肝造成經門脈下壁的穿刺。Eduard報道了在細小的肝右靜脈上支和粗大的肝右靜脈下支的變異情況下,置入泊留導絲由肝右靜脈上支、側支循環、肝右靜脈下支、入下腔靜脈固定引導穿刺的病例。
3.分流道大小沿用了外科分流的標準,一般爲直徑10mm或12mm,以門脈壓小於2.45kPa(25cmH2O)爲多,有時單分流道不足以提供足夠的降壓效果需雙分流道來實現。據Larberge報道,約有10%患者建立了雙分流道,部分患者門脈壓小於1.96kPa(20cmH2O)仍有較顯著的靜脈曲張,可同時行曲張靜脈栓塞術,門脈壓小於2.45kPa(25cmH2O)時,將曲張靜脈曠置或再行內鏡硬化(暫不栓塞以觀察)從理論上說應是適宜的。
4.肝門靜脈穿刺和球囊擴張分流道時,患者常有劇痛,給予麻醉劑或穿刺前10分鐘肌注度冷丁50mg,但麻醉劑的應用也降低了機體的反應性,對肝功較差的患者增加了肝臟的負擔。造影劑以非離子造影劑爲好,TIPS術中原則不給予大劑量抗凝,因大部分患者凝血機制較差,結合患者具體情況(凝血酶原時原時間+活動度),可在支架釋放後給予2萬IU肝素抗凝治療,抗生素可在術前給予,亦可術後點滴。