手術名稱
肺結核肺切除術
分類
胸外科/肺手術/肺結核的手術治療
ICD編碼
32.5 01
概述
肺結核是由結核桿菌引起的慢性、傳染性疾病。肺結核的治療方法是休息療養、改善環境衛生、應用抗結核藥物及外科手術等。外科治療肺結核已有近百年的歷史,是肺結核綜合治療的重要組成部分,但外科治療應在休息療養和抗結核藥物治療的基礎上進行,只有各種方法的密切配合應用,才能達到縮短治療日程,擴大治療範圍,提高治癒效果和減少複發率的目的。
目前常用的肺結核外科治療方法有肺切除術和胸廓成形術。肺切除術能直接切除抗結核藥物不能治癒的病肺組織,以消滅傳染病竈,使患者很快恢復健康,易於接受。胸廓成形術因病肺組織仍留在體內,須繼續抗結核治療以促其治癒,術後休息治療的時間較長,部分肺組織萎陷後對肺功能有較大損害,而且體內存在的病竈,有復發或惡化的可能,故目前應用較少,但對個別不適於肺切除的患者,仍是一種可行的方法。
近年來,由於有效抗結核藥物的問世,藥物治療肺結核的效果明顯提高,需要手術切除的病例顯著減少。但對於有些患者,手術仍是必須的、有效的治療方法。
適應症
肺結核肺切除術適用於:
1.空洞型肺結核 有空洞形成的結核患者,常有咳痰、排菌或咯血,經全身抗結核治療及支持療法半年以上,空洞不閉合者,應選擇手術治療。巨大空洞,病變廣泛,肺組織破壞多,周圍纖維化,胸膜粘連固定,自行癒合的機會較少;張力性結核空洞,常因支氣管內膜結核病變而久治不愈;厚壁空洞,其內壁有較厚的肉芽組織,不易癒合;下葉肺結核性空洞,不適於進行肺萎陷手術。這些患者均爲肺切除的適應證(圖5.4.6.1-1,5.4.6.1-2)。



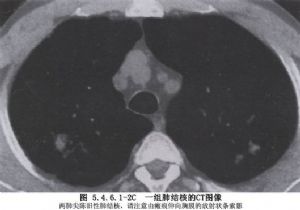
2.肺結核引起的支氣管擴張或狹窄 慢性肺結核常伴隨支氣管內膜結核;肺門腫大淋巴結亦可壓迫或侵蝕支氣管壁,造成支氣管狹窄或擴張,有的形成肺不張、咯血或合併感染,這些患者應施行肺切除術。
3.肺乾酪病竈 肺大塊乾酪病竈,經長期藥物治療不見吸收;直徑大於2cm的結核球,藥物不能穿透纖維組織包裹的病變;或懷疑有癌變不易鑑別者。
4.毀損肺 有廣泛而嚴重的纖維化及陳舊肺結核病變,已基本失去肺功能,而且形成肺動、靜脈短路,藥物治療無效,須進行肺切除術。
5.急性大咯血 肺結核引起的反覆持續咯血或大咯血(大於600ml/24h),常爲開放性結核空洞、支氣管擴張或肺門鈣化的淋巴結侵蝕支氣管壁損傷支氣管動脈所引起,應作急症手術。
禁忌症
1.活動性肺結核,患者全身症狀較重者屬於手術禁忌證。大量排菌,體溫、脈搏、血沉均不正常者,雖局部病變適於手術,但全身情況不宜手術。
2.年齡 兒童和70歲以上的肺結核患者,身體衰弱者,手術治療應慎重考慮。
3.呼吸功能不全的患者,特別有哮喘及重度肺氣腫者、有其他重要臟器嚴重病變(如慢性肝炎肝功損害嚴重,肝硬化,嚴重腎功不全,嚴重心血管疾病,糖尿病等)手術治療應慎重考慮。
術前準備
1.患者應做胸部X線、胸部CT及支氣管鏡檢查,進一步瞭解病變的詳細情況,(病變的範圍、內部結構、與鄰近組織和血管的關係以及支氣管腔內的變化等),以便決定手術方法和切除的範圍。
2.心肺功能檢查 術前肺功能的評估很重要。常用的肺功能臨界參考值:肺活量在1500ml以下,最大通氣量40L/min以下,時間肺活量第1秒在70%以下,通氣儲量在86%以下,選擇肺切除手術時,須慎重考慮切除的範圍。有時,須結合臨牀具體情況綜合評估,如患者活動量的大小,爬樓梯的層數、速度以及活動後的呼吸次數、脈搏、動脈血氧飽和飽和度等。準備作一側全肺切除術的患者,最好能測定分側肺功能。對於有高血壓者,應控制至理想水平。有心肌梗死者,應待其病情穩定半年以上,並無近期心絞痛發生的情況下才考慮手術治療。
3.選擇有效的抗結核藥物和抗生素 長期使用抗結核藥物,痰菌陽性者,應作結核菌耐藥試驗。有耐藥發生時,術前還應加用第二線抗結核藥物或新的抗結核藥,以確保患者術後順利恢復。空洞型肺結核及支氣管擴張者,如痰量較多或合併有繼發感染,術前應作細菌培養和藥敏試驗,並設法使痰量減少。
4.注意其他臟器疾病的治療 判斷肝腎功能不全及損害的程度,對手術成敗影響很大。對於慢性肝炎引起的肝功能不全或有腎功能不全者,應細緻檢查及治療。有糖尿病者,要控制其血糖和尿糖水平接近正常,以免術後發生併發症。
麻醉和體位
靜脈複合麻醉,氣管內雙腔插管或單側支氣管插管,以免氣管內結核播散及術中血液或痰液流入對側肺引起窒息。
體位:一般取側臥位,即患側在上,健側在下。
手術步驟
1.體位、切口
肺切除術的體位和切口需根據病人的具體情況和病變部位選擇使用。常用的有後外側切口和前外側切口,很簡單的外側肺楔形切除術,也可經腋下切口進行,以減輕術後切口疼痛。
2.胸膜粘連的分離
切開胸壁,進入胸腔後,首先應分離粘連,探查清楚肺內病情,才能開始切肺手術。粘連應全部分離,以利操作,也利於部分肺切除術後餘肺擴張。
3.肺裂的分離
肺葉間的裂隙經常是不完全的,或是互相粘連的,除作全肺切除外,必須分離清楚,以便手術操作。疏鬆粘連可用剪刀剪開。如粘連緊密,或爲不全肺裂時,可在肺裂部位安置兩把止血鉗,在鉗間剪開後,用絲線先從肺門向外穿針,繞過止血鉗連續縫合,取下止血鉗,收緊縫線後再繞回作第2層連續縫合[圖1]。這種縫合法既可避免出血,又可防止漏氣。粘連範圍較廣者,可分批鉗夾和切開、縫合。如準備切除的肺葉支氣管和血管可在分開肺裂前分離、切斷,則可用肺段切除術的操作步驟來分離不全肺裂,使術後餘肺最大限度地擴張。
4.肺門血管的處理
肺切除術的關鍵在於對肺門的精確解剖。一般處理肺門的次序是先切斷動脈,再切斷靜脈,最後切斷支氣管。但如某一部位的動脈在靜脈的後面,不能首先顯露時,可先切斷靜脈,再切斷動脈。如果動、靜脈均不能顯露,則可先切斷支氣管。對於肺癌病人則應先切斷靜脈,再切斷動脈,以免在手術操作中造成血運轉移。如痰量很多,有發生窒息或流向對側的危險時,也可先切斷支氣管,再處理血管。肺的動、靜脈比身體其他部位的血管脆薄,因此操作應特別仔細。分離動、靜脈時應先將血管周圍的結締組織分開。緊貼管壁的結締組織尤其緻密,形成一薄膜樣纖維鞘膜,必須將其剪開,顯露血管一側壁[圖2-1]。在這層鞘膜與血管壁之間有一疏鬆間隙,可用細頭止血鉗將這層薄膜提起後,用小紗布球輕輕分開,分離血管。推壓小紗布球的方向應指向血管,與血管垂直,不應沿血管走向分離[圖2-2]。在將血管前壁分離後,可繼續分離兩側緣及部分後側壁[圖2-3]。最後,換用直角血管分離鉗從兩側緣探入後側,仔細分離。分離時鉗端分開的方向應與血管壁垂直,使只有血管分離鉗的一葉側面與血管壁接觸,另一葉推向血管周圍結締組織,將血管與周圍組織分開[圖2-4]。血管分離鉗張開不宜過度,以免撕破血管。張開後的分離鉗不應在原位閉合,更不應反覆開閉,以免夾傷血管後側壁,甚至將管壁撕破。在每一次張開分離鉗後,應保持在張開狀態將鉗退出,然後將鉗閉合,再伸入血管後側,作第二次分離。也可用左手示指經對側緣探入血管後側,引導分離鉗分離,保護血管不被損傷[圖2-5]。待鉗端在血管對側緣隱約顯露後,即可再用小紗布球在鉗端處分離[圖2-6]。最後,將鉗端在對側緣探出,完全分離後側壁。
分離血管的長度應該足夠,一般以超過1.5cm爲宜。作全肺切除時,如原來解剖有變異,或粘連過緊,不能分離足夠長度,或在靠近心包處的血管受損傷或結紮滑脫,或肺癌離肺門太近時,可在膈神經前方(或後方)切開心包,在心包內分離動、靜脈,予以結紮、切斷。必要時,將局部心包與肺一併切除。在作肺葉切除時,則可將部分肺組織分開,顯露遠端分支血管,分別予以分離。
血管分離乾淨後,即可根據血管粗細,用直角分離鉗或止血鉗將4號(或7號)絲線送給安置在血管後側的分離鉗夾住[圖2-7],從後側將線引出,分別結紮近端和遠端。如分離出的血管太短,則應分別結紮遠端各分支。肺血管很脆,結紮時用力要平均,不宜過緊,又不能鬆脫。在將線拉緊時,必須將拉出的肺組織放鬆,使血管處於鬆弛狀態,不易撕裂[圖2-8]。近、遠端結紮線之間應有足夠的長度(至少0.5cm)使切斷後的血管殘端,尤其是近心端,能形成喇叭狀擴大。如遠端不止一條分支,則可在分支上切斷,使近端結紮線不易滑脫。爲了避免結紮線滑脫,在切斷較大血管前,應在近端結紮線的遠側和遠端結紮線的近側,各加一0-1號絲線縫扎。縫扎部位應貼近結紮線,使兩端縫扎線之間保持足夠長度[圖2-9],然後將血管剪斷(或切斷)。剪斷時不能用鉗夾,以免珍碎[圖2-10]。如血管較細或血管分離的長度不夠,不能加作兩道縫扎時,可僅在近端加作縫扎,遠端只用止血鉗夾緊後切斷,再作遠端第2道結紮,或在鄰近肺組織作縫扎,遠端只用止血鉗夾緊後切斷,再作遠端第2道結紮,或在鄰近肺組織作縫扎[圖2-11]。至於很細的血管,尤其是靜脈,則不必作縫扎,僅作兩道結紮即可。如血管較粗,尤其是肺動脈主幹或肺下靜脈,在結紮時應用粗線或雙線,以免線細切斷管壁,發生大出血。近端的縫扎線則不宜太粗,以免滑脫;但遠側端縫扎可用較粗絲線或雙線,較易紮緊。如近端太短或縫扎不牢,可將斷端口作單線連續縫合,以免縫扎滑脫,甚至縮進心包內出血而不被發覺,造成致命性大出血[圖2-12]。
5.支氣管的處理
分離支氣管前可先將支氣管附近的淋巴結摘除,以利顯露;如屬肺癌,則應將肺門淋巴結摘除乾淨。然後在手指觸摸引導下,用紗布球和長彎鉗推開肺組織,分離準備切斷的支氣管1cm以上[圖3-1]。在支氣管後壁膜部常有兩支比較明顯的支氣管動脈,上、下緣也各有一支,均應予以縫扎。縫扎部位應貼近支氣管準備切斷的平面,使支氣管殘端有足夠的血液供應,以利癒合[圖3-2]。如事先不能看清支氣管動脈,則只能在切斷支氣管時發現出血點後立即鉗夾止血,再作結紮或縫扎。
切斷支氣管的平面應貼近鄰肺支氣管的分叉處;如作全肺切除,則應貼近隆凸,使支氣管殘端儘可能縮短,術後不致有分泌物積存於殘端內而引起感染。在分離完畢後,先在近肺側安置一把支氣管鉗,輕夾而不扣緊。在作肺葉或肺段切除時,可予充氣擴肺,如見準備切除的肺臟不再擴張,而其餘部分能夠張開,證明分離的支氣管沒有錯誤,即可夾緊支氣管鉗。在支氣管分叉近側約0.5cm處的上、下緣各縫一針細絲線牽引,由助手拉緊,然後在支氣管鉗與牽引線之間切斷支氣管[圖3-3]。爲了避免從支氣管殘端漏氣過多,影響呼吸,可邊切邊作間斷縫合,拉緊縫線,最後逐條結紮[圖3-4];也可一次切斷,迅速縫事。如支氣管較粗,支氣管軟骨環張力太大,影響縫線紮緊,可在殘端的上、下緣各將軟骨環縱行切斷以減少張力[圖3-5]。縫線可用0~3-0細絲線。每針間距和離斷端邊緣的距離均應保持3mm等距,使張力平均,不致有某一縫線因接受過大的張和而割裂組織,造成脫落和支氣管胸膜瘻的嚴重併發症。如支氣管內積痰很多,或有較多血液流進殘端,可在紮緊縫線前將吸引器頭探進殘端吸引,以防分泌物或血液流入對側,造成播散或繼發感染。
如支氣管可以分離較長,而病肺比較膨脹不能萎縮,影響對支氣管的操作時,可先夾兩把支氣管鉗,在鉗間切斷支氣管,摘除病肺[圖4-1]。然後,在近端支氣管鉗夾部位的近側、支氣管分叉近側0.5~0.8cm處作第二次切斷後縫合[圖4-2]。如支氣管因淋巴結或肺實質阻擋,不能較長地分離,而病肺又不能萎縮,影響視野,甚至兩把支氣管鉗也不能安放,則可先夾一把支氣管鉗,在鉗的遠側邊切邊用組織鉗夾住遠端支氣管,完全切斷後,摘除病肺,再修整近側殘端[圖5]。
縫合支氣管殘端的方法,除作間斷全層縫合外,還有兩種方法:一是粘膜外縫合法,即先用心耳鉗將殘夾住,分離取出1~2個軟骨環,使粘膜遊離,然後將粘膜外的管壁軟組織間斷縫合,使粘膜內翻[圖6]。這種方法可使殘端閉合比較嚴密,且縫線沒有穿透管壁全層,不致使殘端內的分泌物沿縫線流到支氣管外,引起感染,但操作比較複雜。另一方法是將支氣管殘端用粗絲線單純結紮,加作4-0線縫扎[圖7]。這種方法只可在較細的支氣管應用,對較粗的支氣管不宜採用。因粗的支氣管軟骨環彈力較大,結紮線不易收緊,且絲線容易切斷管壁,結紮的遠端血運還會受阻,將影響殘端的癒合。
對支氣管殘端或餘肺粗糙面,應檢查是否尚有漏氣。檢查方法可用溫鹽水灌滿胸腔,同時經氣管內插管加壓充氣,觀察有無氣泡漏出。如支氣管殘端漏氣,應即加作間斷絲線縫合或褥式縫合。餘肺粗糙面細小肺泡的漏氣可在術後24小時內被纖維素包蓋後止漏,不必縫合,以免影響餘肺擴張;如粗糙面有較大漏氣孔,應予褥式縫合。
縫合支氣管殘端以後,應利用周圍肺組織或結締組織覆蓋固定。右側可利用肺門區胸膜或奇靜脈周圍結締組織覆蓋;左側除縱隔胸膜外,尚可利用心包或在主動脈前分離出一片胸膜瓣,翻轉覆蓋固定。覆蓋物應與支氣管殘端緊貼,可以加固殘端閉攏,促進癒合[圖8]。
6.肺切除
參見各部位肺切除步驟。
7.胸壁縫合
縫合胸壁前須仔細檢查有無殘留活動性出血點。在胸膜粘連分離處、胸膜外剝離處、心包、肺門、餘肺粗糙面、膈面、肋骨斷端和切口肌肉斷面,尤其在切口兩端,都是容易忽視的出血或滲血部位,應反覆檢查,分別根據具體情況予以電凝、結紮或縫扎,徹底止血。
(1)安放引流管:全肺切除後,可在第8或第9肋間,腋後線與腋中線之間,安放一條引流管。先將引流管夾緊暫不引流,如胸腔內滲血過多,術側胸內壓升高將縱隔推向健側,以致影響呼吸時,可間斷放出部分積液以調節胸內壓力。上葉切除後,除應在第8或第9肋間安放引流管,將胸內滲出液全部引流外;還可在第2肋間鎖骨中線另外放一較細引流管,以排出胸內積氣,有利餘肺擴張。中、下葉或小塊肺段被楔形切除後,只需在第8肋間引流[圖9]。
(2)沖洗胸腔:根據胸腔污染和積血情況,用溫鹽水沖洗1~3次。
(3)縫合胸壁。
術中注意要點
1.選擇全肺切除術要慎重 全肺切除術的創傷大,術後併發症多,對心肺功能的影響很大,選擇手術對象應嚴格,特別是作右全肺切除更要慎重。要求對側肺功能良好,且肺組織基本無病變,年齡不宜過大,抗結核藥物有一定療效。適應證常是毀損肺、多發慢性纖維空洞型肺結核。對一般情況差,長期應用多種抗結核藥物的患者,若對側肺臟亦有不穩定病變,病側肺雖廣泛破壞,但其下部無主要病變,而且有部分肺功能時,使用胸廓成形術可望治癒。
2.目前常採用的肺段切除爲下葉背段,左上葉尖後前段及左上葉舌段。下葉基底段的病變,即使未累及兩個以上肺段,但因解剖分段困難,一般應作下葉切除或僅留背段而作四個基底段切除。右中葉的結核病變,應作中葉切除,不作肺段切除。
3.肺結核病變累及肺外的範圍較廣泛,胸腔可能有致密的粘連,有的胸膜形成很厚的纖維瘢痕,分離粘連時,注意勿分破病竈,以免污染胸腔。此外,應避免損傷鎖骨下靜脈、奇靜脈、喉返神經、食管、肋間血管。處理支氣管時,最好使用支氣管閉合器,且用肌肉瓣包埋覆蓋支氣管殘端,避免術後發生支氣管瘻。術中注意:對肺切除之斷面滲血、漏氣要妥善處理,以免胸膜瘻的發生。肺切除術後的胸膜殘腔必須消除。否則殘腔積血、積液感染會形成膿胸,感染侵及支氣管殘端,產生支氣管胸膜瘻。因此,手術後胸膜殘腔應儘早處理,術後保持胸腔引流通暢,積氣、積液要徹底排盡,促使餘肺儘早膨脹。
4.肺楔形切除術 僅用於病竈表淺且鄰近肺邊緣的小病竈或結核瘤。
術後處理
1.術後應繼續使用有效抗結核藥物,直到各項檢查指標完全正常。還應定期複查,抗結核藥治療應在半年以上。
2.加強營養。待病情穩定,痰菌轉爲陰性後逐漸增加活動。
併發症
1.支氣管胸膜瘻 爲最嚴重而致命的併發症,其發生率約爲1%~3%;常見於右側較重的肺結核病變,其原因可能爲術前未能控制痰菌陽性或多種細菌感染,有糖尿病或有過胸部放射治療史。
2.膿胸 對肺斷面的滲血、漏氣要處理好,殘存於胸腔內的積液應排除徹底。早期發現胸內感染時,及時處理,應用足量廣譜抗生素。
3.結核播散 多發生在術後早期,主要是大量的結核菌陽性的痰外溢引起。應注意術中操作輕柔,減少擠壓病肺。採用先處理支氣管,後處理肺血管的方法,有助於減少結核的播散。