3 概述
補體結合試驗(complementfixationtest,CFT)是用免疫溶血機制做指示系統,來檢測另一反應系統抗原或抗體的試驗。早在1906年Wasermann就將其應用於梅毒的診斷,即著名的華氏反應。這一傳統的試驗經不斷改進,除了用於傳染病診斷和流行病學調查以外,在一些自身抗體、腫瘤相關以原以及HLA的檢測和分析中也有應用。
補體結合試驗利用抗原抗體複合物同補體結合,把含有已知濃度的補體反應液中的補體消耗掉使濃度減低的現象,以檢出抗原或抗體,是高敏度檢出方法之一,特別是根據抗原物質的特性,抗原抗體反應不能用沉澱反應或凝集反應觀察時也可以利用此法。試驗由兩個階段組成:首先將經過56℃處理30分鐘使補體滅活的抗血清,與抗原及補體(通常將豚鼠血清作適當稀釋後使用)混合使起反應。第二是加入已同抗綿羊紅細胞抗體相結合的綿羊紅細胞(致敏紅細胞)。在最初階段對消耗補體建立起足夠的抗原抗體反應時,沒有發生致敏紅細胞的溶血,但補體剩餘下來則引起溶血反應。用於檢查梅毒的梅毒補體結合反應(瓦氏反應,Wassermann reaction)是最常進行的補體結合試驗。
7 補體結合試驗的原理
抗原抗體複合物可以結合補體,這是補體結合試驗的依據。綿羊紅細胞和其相應抗體(溶血素)的複合物結合補體後出現溶血現象。因此,綿羊紅細胞和溶血素被作爲補體結合試驗中判斷待測系統中有無抗原抗體反應的複合物系統。如待測系統產生抗原抗體複合物,則可結合一定量補體,此時加入溶血系統則不出現溶血。如待測系統中只有抗原或抗體,不能結合補體,加入溶血系統則與遊離補體結合而發生溶血,這就是補體結合試驗的基本原理。
補體結合試驗中有5種成分參與反應,分屬於3個系統:①反應系統,即已知的抗原(或抗體)與待測的抗體(或抗原);②補體系統;③指示系統,即SRBC與相應溶血素,試驗時常將其預先結合在一起,形成致敏紅細胞。反應系統與指示系統爭奪補體系統,先加入反應系統給其以優先結合補體的機會。
如果反應系統中存在待測的抗體(或抗原),則抗原抗體發生反應後可結合補體;再加入指示系統時,由於反應液中已沒有遊離的補體而不出現溶血,是爲補體結合試驗陽性。如果反應系統中不存在的待檢的抗體(或抗原),則在液體中仍有遊離的補體存在,當加入指示系統時會出現溶血,是爲補體結合試驗陰性(圖14-2)。因此補體結合試驗可用已知抗原來檢測相應抗體,或用已知抗體來檢測相應抗原。
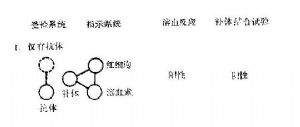
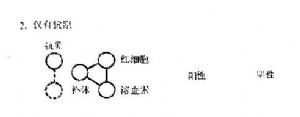
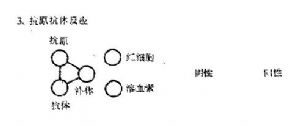
圖14-2補體結合試驗示意圖
8 試驗方法
補體結合試驗的改良方法較多,較常用的有全量法(3ml)、半量法(1.5ml)、小量法(0.6ml)和微量法(塑板法)等。目前以後兩種方法應用較爲廣泛,因爲可以節省抗原,血清標本用量較少,特異性也較好。以下敘述以小量法爲例,即抗原、抗體、溶血素、羊紅細胞各加0.1ml,補體加0.2ml,總量爲0.6ml。
9 試劑
(l)巴比妥緩衝液(BBS):稱取氯化鈉85.0g,氯化鎂六水合物1.68g,氯化鈣0.28g,巴比妥5.75g,巴比妥鈉2.0g,先將巴比妥加入500ml水中加熱溶解後,再加其他成分,補加水至2000ml,此爲保留液,用時稀釋5倍。
(3)2%羊紅細胞:用生理鹽水離心洗滌後,用BBS配成2%懸液。
1.抗原試驗中用於檢測抗體的抗原應適當提純,純度愈高,特異性愈強。如使用粗製抗原時,須經同樣處理的正常組織作抗原對照,以識別待檢血清中可能存在的、對正常組織成分的非特異性反應。
2.抗原和抗本的滴定補體結合試驗中,抗原與抗體按一定比例結合,因而應通過試驗選擇適宜的濃度比例。多采用方陣法進行滴定,選擇抗原與抗體兩者都呈強陽性反應(100%不溶血)的最高稀釋度作爲抗原和抗體的效價(單價)。滴定方法舉例如表14-4。在試管中加入不同稀釋度的抗原,配加不同稀釋度的抗血清,另作不加抗原的抗體對照管和不加抗血清的抗原對照管。按照試驗方法加補體和指示系統,溫育後觀察結果。在表14-4中可見1:64抗原和1:32抗體各作爲1個單位。在正式試驗中,抗原一般採用2~4個單位(1:64~1:32),抗體採用4個單位(1:8)。
| 抗原 | 抗血清稀釋倍數 | 抗原對照 | |||||||
| 1:4 | 1:8 | 1:16 | 1:32 | 1:64 | 1:128 | 1:256 | 1:512 | ||
| 1:4 | 4 | 4 | 4 | 4 | 4 | 4 | 3 | 2 | 0 |
| 1:8 | 4 | 4 | 4 | 4 | 4 | 3 | 2 | 1 | 0 |
| 1:16 | 4 | 4 | 4 | 4 | 3 | 2 | 2 | ± | 0 |
| 1:32 | 4 | 4 | 4 | 4 | 3 | 1 | ± | 0 | 0 |
| 1:64 | 4 | 4 | 4 | ④ | 2 | ± | 0 | 0 | 0 |
| 1:128 | 4 | 2 | 1 | 0 | 0 | 0 | 0 | 0 | 0 |
| 1:256 | 3 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| 1:512 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| 抗體對照 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | |
注:1、2、3、4分別表示溶血反應強度+、++、+++、++++;0爲不溶血。
3.補體滴定按表14-5逐步加入各試劑,溫育後觀察最少量補體能產生完全溶血者,確定爲1個實用單位,正式試驗中使用2個實用單位。如形14-5中的結果爲1:60的補體0.12ml可產生完全溶血,按比例公式0.12×2:60=0.2:X計算,X=50;即實際應用中的2個補體實用單位應爲1:50稀釋的補體0.2ml。
10 血清標本
採集血液標本後及時分離血清,及時檢驗或將血清保存於-20℃。血清在試驗前應先加熱56℃30min(或60℃3min)以破壞補體和除去一些非特異因素。血清標本遇有抗補本現象時可做下列處理之一:①加熱提高12;②-20℃凍融後離心去沉澱;③以3mmol/L鹽酸處理;④加入少量補體後再加熱滅活;⑤以白陶土處理;⑥通入CO2;⑦以小白鼠肝粉處理;⑧用含10%新鮮雞蛋清的生理鹽水稀釋補體。
11 操作方法
血素的滴定:
①取補體1ml,加BBS 9ml,依次稀釋成1∶20,1∶30,1∶40,1∶50,1∶60,1∶80,1∶100,1∶200,1∶400,同時取50%的溶血素0.2ml,加BBS 9.8ml,即爲1∶100的溶血素,然後繼續稀釋成1∶800,1∶1600,1∶3200,1∶6400。
②採取方陣排列試管,縱行各管加不同濃度的補體0.1ml,橫排各管加溶血素0.1ml(皆應從最高稀釋度加起)混勻後,各管加BBS 0.2ml,補體和溶血素對照管各加BBS 0.3ml,最後在各管中加2%羊紅細胞0.1ml。各管總量爲0.5ml,搖勻,放37℃水箱中30min,觀察結果。茲舉一例說明(表1):

以完全溶血的補體和溶血素最高稀釋度爲各自的單位。在實際應用時,溶血素用2U(3200÷2=1600),補體用2.5U(80÷2.5=32)。
(2)正式試驗:
①用V型微量反應板操作,每份標本作一個試驗孔。一個血清對照孔。各孔內先加BBS 0.025ml。②用稀釋棒蘸取血清(0.025ml)加入第一孔,旋轉後移入第二孔,共八孔,如此可得1∶2~1∶256稀釋。③按表2加入各試劑:

以小量法測定抗體的補體結合試驗爲例。按表14-6逐步加入各種試劑,溫育後先觀察各類對照管,應與預期的結果吻合。陰性、陽性對照管中應分別爲明確的溶血與不溶血;抗體或抗原對照管、待檢血清對照管、陽性和陰性對照的對照管都應完全溶血。綿羊紅細胞對照管不應出現自發性溶血。補體對照管應呈現2U爲全溶,1U爲全溶略帶有少許紅細胞,0.5U應不溶。如0.5U補體對照出現全溶表明補體用量過多;如2U對照管不出現溶血,說明補體用量不夠,對結果都有影響,應重複進行試驗。補體結合試驗結果,受檢血清不溶血爲陽性,溶血爲陰性。
12 應用和評價
補體結合試驗是一種傳統的免疫學技術,能夠沿用至今說明它本身有一定的優點:①靈敏度高。補體活化過程有放大作用,比沉澱反應和凝集反應的靈敏度高得多,能測定0.05μg/ml的抗體,可與間接凝集法的靈敏度相當。②特異性強。各種反應成分事先都經過滴定,選擇了最佳比例,出現交叉反應的機率較小,尤其用小量法或微量法時。③應用面廣,可用於檢測多種類型的抗原或抗體。④易於普及,試驗結果顯而易見;試驗條件要求低,不需要特殊儀器或只用光電比色計即可。
補體結合試驗可應用在以下幾方面:①傳染病診斷。病原性抗原及相應抗體的檢測。②其他抗原的檢測。例如腫瘤相關抗原、血跡中的蛋白質鑑定、HLA分型等。③自身抗體檢測。
但是補體結合試驗參與反應的成分多,影響因素複雜,操作步驟繁鎖並且要求十分嚴格,稍有疏忽便會得出不正確的結果,所以在多種測定中已被其他更易被接受的方法所取代。但對於免疫學技術的基本訓練仍是一個很好的試驗。
13 正常值
陰性:0~1∶10