2 英文參考
Quality control for radiation sterilization of medical and hygienical products
ICS 11.080
C 50
中華人民共和國國家標準GB 16383—2014《醫療衛生用品輻射滅菌消毒質量控制》(Quality control for radiation sterilization of medical and hygienical products)由中華人民共和國國家質量監督檢驗檢疫總局、中國國家標準化管理委員會於2014年12月22日發佈,由中華人民共和國國家衛生和計劃生育委員會提出並歸口。本標準自2015年07月01日起實施,同時代替GB 16383—1996。
本標準首次發佈於1996年5月。
3 前言
本標準第6章爲推薦性條款,其餘均爲強制性條款。
本標準按照GB/T 1.1—2009給出的規則起草。
本標準代替GB 16383—1996《醫療衛生用品輻射滅菌消毒質量控制標準》。
本標準與GB 16383—1996比較,主要技術性變化如下:
——標準名稱由《醫療衛生用品輻射滅菌消毒質量控制標準》修改爲《醫療衛生用品輻射滅菌消毒質量控制》;
——對引用標準的版本進行了更新,並增加了GB 18280、GB 18871、《中華人民共和國藥典(二部)》(2010年版);
——依據GB 18280對部分術語和定義滅菌劑量的確定,刪除了對醫療用品生產廠的生產要求;
——增加了可能影響產品質量應採取的糾正措施和預防措施;
——將“微生物監測方法和要求”獨立列爲第6章,“輻射產品的放行要求”列爲第7章。提出適合我國國情的質量要求。
本標準由中華人民共和國國家衛生和計劃生育委員會提出並歸口。
本標準由江蘇省疾病預防控制中心負責起草,蘇州市疾病預防控制中心、中國疾病預防控制中心參加起草。
本標準主要起草人:徐燕、談智、陳學良、張流波、張鈞、李新武、孫俊、吳曉松、陳文森、陳越英。
本標準首次發佈於1996年5月。
5 2 規範性引用文件
下列文件對於本文件的應用是必不可少的。凡是注日期的應用文件,僅注日期的版本適用於本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
GB 18280 醫療保健產品滅菌 確認和常規控制要求 輻射滅菌
GB 18871 電離輻射防護與輻射源安全基本標準
JJG 591 γ射線輻射源(輻射加工用)
中華人民共和國藥典(二部)(2010年版)
6 3 術語和定義
下列術語和定義適用於本文件。
3.1
無菌保證水平 Sterilization assurance level;SAL
3.2
D值 D value
在設定的暴露條件下,殺滅特定試驗微生物總數的90%所需的輻射吸收劑量。
3.3
生物負載 bioburden
3.4
生物指示物 biological indicator
對特定滅菌或消毒程序有確定的抗力,可供消毒滅菌效果監測使用的微生物檢驗器材。
3.5
吸收劑量 absorbed dose
注:吸收劑量單位是戈瑞(Gy),1 Gy=1 J/kg。
3.6
吸收劑量的不均勻度 unevenress
U
輻射產品箱中,不同部位測得的最大吸收劑量(Dmax)除以最小吸收劑量(Dmin)之商,見式(1):
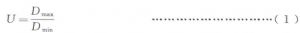
式中:
Dmax——最大吸收劑量;
Dmin——最小吸收劑量。
3.7
劑量計 dosimeter
劑量儀
3.8
工作劑量計 working dosemeter
經標準劑量計校準過的,用來標定輻射場劑量率與測定產品吸收劑量,進行常規劑量監測的劑量計。
3.9
滅菌劑量 sterilization dose
7 4 輻射滅菌和消毒要求
7.1 4.1 在輻射滅菌前醫療衛生用品的要求
4.1.1 醫療衛生用品及包裝材料應是耐輻射滅菌劑量的材料。
4.1.2 醫療衛生用品的初始污染菌應進行檢測,保證使用輻射滅菌的有效性。
4.1.3 對於可能影響產品質量的工藝、生產環境等方面出現的異常情況應有糾正措施。
4.1.4 對於可能影響產品質量的工藝、生產環境等方面潛在的危害應採取相應的預防措施。
7.2 4.2 對輻射滅菌和消毒單位要求
4.2.1 輻射滅菌和消毒單位的輻射設施安裝、鑑定、運行、人員應達到JJG 591、GB 18871及GB 18280要求,同時應取得輻射安全許可證和國家有資質的部門頒發的輻射加工計量許可證;操作人員應經過培訓,持有上崗技術考覈合格證。
4.2.2 輻射滅菌和消毒單位應有足夠的檢測能力,能夠根據待輻射滅菌產品的生物負載及無菌檢測,建立並驗證滅菌劑量,保證輻射加工的有效性。
4.2.3 輻射滅菌和消毒單位對於異常情況應有相應的糾正措施和預防措施。
7.3 4.3 建立滅菌劑量
按照GB 18280的要求進行。
8 5 產品輻射處理要求
8.1 5.1 吸收劑量測量
5.1.2 工作劑量計應放在預先確定的常規劑量點,輻射後,測量劑量,記錄結果並分析。
8.2 5.2 產品的輻射滅菌與消毒
5.2.1 將產品包裝的尺寸、密度以及產品在包裝內的分佈、產品在輻射容器中的裝載模式做詳細說明。
5.2.2 每個待輻射的都應該做劑量分佈圖,確定最大劑量和最小劑量的位置和大小,確定最大劑量與最小劑量和常規劑量點處劑量的關係。
9 6 微生物監測方法和要求
9.1 6.1 初始污染菌檢測
每生產批次產品中至少隨機抽取10個樣品,按照GB 18280的要求進行初始污染菌檢測。
9.2 6.2 消毒滅菌效果檢驗
每批產品應做消毒或滅菌效果監測。於最小劑量處,每次至少布放10片生物指示劑。輻射後取出指示菌片按《中華人民共和國藥典(二部)》(2010年版)的要求進行無菌檢查。
10 7 輻射產品的放行要求
7.1 產品輻射處理後,對包裝完好無損,劑量監測結果符合輻射工藝要求的產品給予放行;對於劑量監測結果合格的符合要求的包裝有破損的產品,僅對被損產品包裝重新輻射處理,其他包裝完好的產品給予放行;對於劑量監測結果不符合輻射工藝要求的產品,應全部報廢或重新進行輻射處理。
11 8 醫療衛生用品輻射後的管理要求
8.1 輻射滅菌(消毒)後的醫療衛生用品包裝箱上應貼輻射化學指示卡、滅菌(消毒)合格證,合格證上應有批號、滅菌消毒日期、有效期、滅菌消毒單位等。
8.2 輻射滅菌(消毒)後的產品應附有輻射滅菌(消毒)工藝的清單,由滅菌(消毒)操作者、審覈者簽名及質量管理人員審覈,其產品的編碼、生產批號和產品數量應和入庫記載一致。
12 附錄A(規範性附錄)初始污染菌檢測
12.1 A.1 試劑、器材
A.1.1 洗脫液:含0.1%吐溫80、1%蛋白腖的生理鹽水。
A.1.3 濾膜(孔徑0.45μm)。
12.2 A.2 採樣方法
A.2.1 對可用破壞性方法取樣的醫療用品,如輸液(血)器、注射器、注射針、透析器及各類管材等,按《中華人民共和國藥典(二部)》(2010年版)規定執行。
A.2.2 對不能用破壞性方法取樣的特殊醫療衛生用品要用無菌生理鹽水的棉拭子塗抹採樣,被採表面小於100 cm2取全部表面,被採表面大於等於100 cm2取100 cm2。
A.2.3 敷料類可用無菌操作取10 g放入100 mL無菌生理鹽水中,充分振盪後取樣。
12.3 A.3 檢測方法
A.3.1 平板傾注法:分別取1 mL處理的洗脫液,接種5個平皿,傾注融化後45℃的營養瓊脂,35℃±2℃培養48 h,同時作平行樣及空白對照。
A.3.2 膜過濾法:對於微生物濃度較低的洗脫液,可用膜過濾法使洗脫液通過0.45μm濾膜,將濾膜貼在營養瓊脂表面培養35℃±2℃培養48 h。

