2 基本信息
《乳腺癌診療指南(2022年版)》由國家衛生健康委辦公廳於2022年4月3日《國家衛生健康委辦公廳關於印發腫瘤和血液病相關病種診療指南(2022年版)的通知》(國衛辦醫函〔2022〕104號)印發,要求各省、自治區、直轄市及新疆生產建設兵團衛生健康委組織做好實施工作。
3 發佈通知
國家衛生健康委辦公廳關於印發腫瘤和血液病相關病種診療指南(2022年版)的通知
國衛辦醫函〔2022〕104號
各省、自治區、直轄市及新疆生產建設兵團衛生健康委:
爲進一步提高腫瘤和血液病診療規範化水平,保障醫療質量安全,維護患者健康權益,我委委託有關單位制修訂了腫瘤和血液病相關病種診療指南。現印發給你們(見附件,可在國家衛生健康委網站醫政醫管欄目下載),請各地衛生健康行政部門組織做好實施工作。
附件:
2.膀胱癌診療指南(2022年版)
5.胰腺癌診治指南(2022年版)
6.腎癌診療指南(2022年版)
7.乳腺癌診療指南(2022年版)
8.子宮內膜癌診療指南(2022年版)
12.甲狀腺癌診療指南(2022版)
13.腦膠質瘤診療指南(2022年版)
16.瀰漫性大B細胞淋巴瘤診療指南(2022年版)
17.骨髓增生異常綜合徵伴原始細胞增多(MDS-EB)診療指南(2022年版)
18.慢性髓性白血病診療指南(2022年版)
19.血友病A診療指南(2022年版)
20.慢性淋巴細胞白血病-小淋巴細胞淋巴瘤診療指南(2022年版)
國家衛生健康委辦公廳
2022年4月3日
4 診療指南全文
乳腺癌診療指南(2022年版)
乳腺癌是女性常見的惡性腫瘤之一,發病率位居女性惡性腫瘤的首位,嚴重危害婦女的身心健康。目前,通過採用綜合治療手段,乳腺癌已成爲療效最佳的實體腫瘤之一。爲進一步規範我國乳腺癌診療行爲,提高醫療機構乳腺癌診療水平,改善乳腺癌患者預後,保障醫療質量和醫療安全,特制定本指南。
4.1 一、乳腺癌篩查
乳腺癌篩查是指通過有效、簡便、經濟的乳腺檢查措施,在無症狀婦女中識別和發現具有進展潛能的癌前病變患者以及早期浸潤性癌患者,以期早期發現、早期診斷及早期治療,其最終目的是降低人羣乳腺癌的死亡率。篩查分爲羣體篩查和機會性篩查。羣體篩查是指在轄區或機構有組織、有計劃地組織適齡婦女進行篩查;機會性篩查是指醫療保健機構結合門診常規工作提供乳腺癌篩查服務。
婦女參加乳腺癌篩查的起始年齡:機會性篩查一般建議40歲開始,但對於乳腺癌高危人羣可將篩查起始年齡提前到40歲以前。羣體篩查國內暫無推薦年齡,國際上推薦40~50歲開始,目前國內開展的羣體篩查採用的年齡均屬於研究或探索性質,缺乏嚴格隨機對照研究的不同年齡成本效益分析數據。
4.1.1 (一)一般風險人羣婦女乳腺癌篩查策略。
4.1.1.1 1.20~39歲
(2)每1~3年1次臨牀檢查。
4.1.1.2 2.40~69歲
(1)適合機會性篩查和羣體性篩查。
(3)對條件不具備的地區或緻密型乳腺(腺體爲C型或D型),可首選乳腺超聲檢查。
(5)每年1次臨牀檢查。
4.1.1.3 3.70歲以上
(3)每年1次臨牀檢查。
4.1.2 (二)高危人羣乳腺癌篩查策略。
建議對乳腺癌高危人羣提前進行篩查(小於40歲),篩查間期推薦每年1次,篩查手段整體原則應聯合乳腺X線檢查和乳腺超聲,必要時還可以應用MRI等影像學手段。乳腺癌高危人羣符合以下3個條件,即:
2.既往有乳腺導管或小葉不典型增生或小葉原位癌(lobular carcinoma insitu,LCIS)的患者;
3.既往行胸部放療。遺傳性乳腺癌-卵巢癌綜合徵基因檢測標準如下[a,b]。
(1)具有血緣關係的親屬中有BRCA1/BRCA2基因突變的攜帶者。
(2)符合以下1個或多個條件的乳腺癌患者[c]:①發病年齡≤45歲;②發病年齡≤50歲並且有1個及以上具有血緣關係的近親[d]也爲發病年齡≤50歲的乳腺癌患者和/或1個及以上的近親爲任何年齡的卵巢上皮癌/輸卵管癌/原發性腹膜癌患者;③單個個體患2個原發性乳腺癌[e],並且首次發病年齡≤50歲;④發病年齡不限,同時2個及以上具有血緣關係的近親患有任何發病年齡的乳腺癌和/或卵巢上皮癌、輸卵管癌、原發性腹膜癌;⑤具有血緣關係的男性近親患有乳腺癌;⑥合併有卵巢上皮癌、輸卵管癌、原發性腹膜癌的既往史。
(5)具有以下家族史:
①具有血緣關係的一級或二級親屬中符合以上任何條件;
②具有血緣關係的三級親屬中有2個及以上乳腺癌患者(至少1個發病年齡≤50歲)和/或卵巢上皮癌/輸卵管癌/原發性腹膜癌患者。
注:a.符合1個或多個條件提示可能爲遺傳性乳腺癌-卵巢癌綜合徵,有必要進行專業性評估。當審查患者的家族史時,父系和母系親屬的患癌情況應該分開考慮。早發性乳腺癌和/或任何年齡的卵巢上皮癌、輸卵管癌、原發性腹膜癌提示可能爲遺傳性乳腺癌-卵巢癌綜合徵。在一些遺傳性乳腺癌-卵巢癌綜合徵的家系中,還包括前列腺癌、胰腺癌、胃癌和黑素瘤。
b.其他考慮因素:家族史有限的個體,例如女性一級或二級親屬<2個,或者女性親屬的年齡>45歲,在這種情況下攜帶突變的可能性往往會被低估。對發病年齡≤40歲的三陰性乳腺癌患者可考慮進行BRCA1/2基因突變的檢測。
d.近親是指一級、二級和三級親屬。e.2個原發性乳腺癌包括雙側乳腺癌或者同側乳腺的2個或多個明確的不同來源的原發性乳腺癌。
4.2 二、診斷
應當結合患者的臨牀表現、體格檢查、影像學檢查、組織病理學等進行乳腺癌的診斷和鑑別診斷。
4.2.1 (一)臨牀表現。
早期乳腺癌不具備典型症狀和體徵,不易引起患者重視,常通過體檢或乳腺癌篩查發現。以下爲乳腺癌的典型體徵,多在癌症中期和晚期出現。
4.2.1.1 1.乳腺腫塊
80%的乳腺癌患者以乳腺腫塊首診。患者常無意中發現腫塊,多爲單發,質硬,邊緣不規則,表面欠光滑。大多數乳腺癌爲無痛性腫塊,僅少數伴有不同程度的隱痛或刺痛。
4.2.1.2 2.乳頭溢液
非妊娠期從乳頭流出血液、漿液、乳汁、膿液,或停止哺乳半年以上仍有乳汁流出者,稱爲乳頭溢液。引起乳頭溢液的原因很多,常見的疾病有導管內乳頭狀瘤、乳腺增生、乳腺導管擴張症和乳腺癌。單側單孔的血性溢液應進一步行乳管鏡檢查,若伴有乳腺腫塊更應重視。
4.2.1.3 3.皮膚改變
乳腺癌引起皮膚改變可出現多種體徵,最常見的是腫瘤侵犯乳房懸韌帶(又稱庫珀韌帶)後與皮膚粘連,出現酒窩徵。若癌細胞阻塞了真皮淋巴管,則會出現橘皮樣改變。乳腺癌晚期,癌細胞沿淋巴管、腺管或纖維組織浸潤到皮內並生長,形成皮膚衛星結節。
4.2.1.4 4.乳頭、乳暈異常
腫瘤位於或接近乳頭深部,可引起乳頭回縮。腫瘤距乳頭較遠,乳腺內的大導管受到侵犯而短縮時,也可引起乳頭回縮或抬高。乳頭乳暈溼疹樣癌即佩吉特病,表現爲乳頭皮膚瘙癢、糜爛、破潰、結痂、脫屑、伴灼痛,甚至乳頭回縮。5.腋窩淋巴結腫大
隱匿性乳腺癌乳腺體檢摸不到腫塊,常以腋窩淋巴結腫大爲首發症狀。醫院收治的乳腺癌患者1/3以上有腋窩淋巴結轉移。初期可出現同側腋窩淋巴結腫大,腫大的淋巴結質硬、散在、可推動。隨着病情發展,淋巴結逐漸融合,並與皮膚和周圍組織粘連、固定。晚期可在鎖骨上和對側腋窩摸到轉移的淋巴結。
4.2.2 (二)乳腺觸診。
進行乳腺觸診前應詳細詢問乳腺病史、月經婚姻史、既往腫瘤家族史(乳腺癌、卵巢癌)。絕經前婦女最好在月經結束後進行乳腺觸診。
受檢者通常採用坐位或立位,對下垂型乳房或乳房較大者,亦可結合仰臥位。乳腺體檢應遵循先視診後觸診,先健側後患側的原則,觸診時應採用手指指腹側,按一定順序,不遺漏乳頭、乳暈區及腋窩部位,可雙手結合。大多數乳腺癌觸診時可以觸到腫塊,此類乳腺癌容易診斷。部分早期乳腺癌觸診陰性,查體時應重視乳腺局部腺體增厚變硬、乳頭糜爛、乳頭溢液,以及乳頭輕度回縮、乳房皮膚輕度凹陷、乳暈輕度水腫、絕經後出現乳房疼痛等,應提高警惕。診斷時要結合影像學和組織病理學檢查結果,必要時可活檢行細胞學診斷。
4.2.3 (三)影像學檢查。
乳腺的影像學檢查主要包括乳腺X線檢查、乳腺超聲以及乳腺MRI等。
4.2.3.1 1.乳腺 X 線攝影
乳腺疾病的最基本檢查方法,在檢出鈣化方面,具有其他影像學方法無可替代的優勢,但對緻密型乳腺、近胸壁腫塊的顯示不佳,且有放射性損害,對年輕女性患者不作爲首選檢查方法。
常規投照體位包括雙側內外側斜位及頭尾位。對常規體位顯示不佳或未包全乳腺實質者,可根據病竈位置選擇補充體位,包括外內側位、內外側位、內側頭足軸位、外側頭足軸位、尾葉位、乳溝位。爲使病竈顯示效果更佳,必要時可開展一些特殊攝影技術,如局部加壓攝影、放大攝影或局部加壓放大攝影等。
4.2.3.1.1 (1)適應證:
適用於篩查性人羣及診斷性患者的乳腺檢查。①無症狀人羣的篩查。②適齡女性篩查或其他相關檢查發現乳腺異常改變。③有乳腺腫塊、局部增厚、異常乳頭溢液、乳腺皮膚異常、局部疼痛或腫脹症狀。④良性病變的短期隨診。⑤乳腺癌保乳術後的隨診。⑥乳房修復重建術後。⑦引導定位及活檢。
對 40 歲以下、無明確乳腺癌高危因素或臨牀查體未見異常的婦女,不建議首先進行乳腺X 線檢查。妊娠期女性通常不進行乳腺 X 線攝影。
4.2.3.1.2 (2)診斷報告基本指南:
見附件1。
4.2.3.2 2.乳腺超聲
超聲檢查因其簡便易行、靈活直觀、無創無輻射等特點,適用於所有疑診乳腺病變的人羣。可同時進行乳腺和腋窩淋巴結的檢查。乳腺超聲掃描體位常規取仰臥位,掃描範圍自腋窩頂部至雙乳下界,包括全乳及腋窩。常規超聲檢查可以早期、敏感的檢出乳腺內可疑病變,通過對病變形態、內部結構及周圍組織改變等特徵的觀察,結合彩色多普勒血流成像觀察病變內血流情況,確定病變性質。超聲造影可以顯示病竈內微血管分佈、走形、血流動力學差異以及病竈與周圍正常組織的關係,對於良惡性病竈的鑑別具有一定的意義。彈性成像可以評價組織硬度,對於部分乳腺病變的良惡性判斷有一定的輔助價值。
4.2.3.2.1 (1)適應證:
①有乳腺相關症狀者:觸診發現乳腺腫物、乳頭溢液、乳頭內陷、局部皮膚改變等。
④乳腺良性病變的隨訪;乳腺癌術後隨訪;絕經後激素替代治療隨訪等。
4.2.3.2.2 (2)診斷報告基本指南:
見附件1。
4.2.3.3 3.乳腺MRI檢查
乳腺MRI檢查的優勢在於敏感性高,能顯示多病竈、多中心或雙側乳腺癌病竈,並能同時顯示腫瘤與胸壁的關係、腋窩淋巴結轉移情況等,爲制訂手術方案提供更可靠的依據。缺點在於特異性中等,假陽性率高,對微小鈣化性病變顯示不滿意,此外檢查時間長、費用昂貴。不作爲首選檢查方法。建議使用高場強(1.5T及以上)MRI設備及乳腺專用相控陣線圈,掃描體位爲俯臥位,掃描序列包括T1加權成像序列(包括不抑脂序列,以及與增強序列相同的抑脂序列)、T2加權成像(加抑脂序列)、彌散加權成像、增強掃描序列(包括橫斷位動態增強掃描及矢狀位掃描)。
(1)適應證:
③評價新輔助化療療效。
④尋找腋窩淋巴結轉移患者的原發竈。⑤乳腺癌術後鑑別治療後瘢痕與腫瘤復發。
⑦乳腺假體植入術後評價。
⑨引導乳腺病竈的定位及活檢。
4.2.3.3.1 (2)禁忌證:
①體內有起搏器、外科金屬夾等鐵磁性物質及其他不得接近強磁場者。
②具有對任何釓螯合物過敏史者。
③幽閉恐懼症者。
④妊娠期婦女。
⑤一般情況很差,不能耐受磁共振檢查者。
4.2.3.3.2 (3)診斷報告基本指南:
見附件1。
4.2.3.4 4. 正電子發射計算機體層成像
根據美國國立綜合癌症網絡(National ComprehensiveCancer Network,NCCN)指南、歐洲腫瘤內科學會(EuropeanSociety for Medical Oncology,ESMO)指南、日本乳腺癌學會(Japanese Breast Cancer Society,JBCS)指南及中國抗癌協會指南。
4.2.3.4.1 (1)正電子發射計算機體層成像(positronemissiontomography-computed tomography,PET-CT)檢查適應證:
①臨牀局部晚期、分子分型預後差、有症狀可疑存在遠處轉移的患者療前分期(尤其是常規影像檢查對是否存在遠處轉移難以判斷或存在爭議時)。
②術後患者隨訪過程中可疑出現局部復發或轉移,包括查體或常規影像檢查出現異常、腫瘤標誌物升高等(對於鑑別復發和放射性纖維化,PET-CT較其他常規影像檢查具有優勢)。
關於PET-CT在乳腺癌骨轉移方面的應用,雖有臨牀研究提示,其具有與骨顯像相似的靈敏度,更高的特異性,對乳腺癌骨轉移治療後病情的跟蹤優於骨顯像,但目前尚未獲得各個指南的常規推薦。
4.2.3.4.2 (2)PET-CT檢查的相對禁忌證:
②嚴重心、肝、腎功能衰竭及對含碘對比劑過敏者不能行增強PET-CT檢查。
③病情危重難以配合、不能平臥15分鐘、尿便失禁或有幽閉恐懼症的患者。
4.2.3.5 5.骨顯像
4.2.3.5.1 (1)浸潤性乳腺癌治療前分期:
①對於臨牀Ⅰ~ⅡB期浸潤性乳腺癌患者,有局部骨痛或鹼性磷酸酶升高時,可行骨顯像檢查評估是否有骨轉移。
②臨牀Ⅲ期浸潤性乳腺癌患者,可行骨顯像檢查或氟化鈉PET-CT檢查,評估是否有骨轉移(2B類)。
③復發或臨牀Ⅳ期乳腺癌患者,可行骨顯像檢查或氟化鈉PET-CT檢查,評估是否有骨轉移。若患者已行的氟代脫氧葡萄糖PET-CT檢查中明確提示有骨骼轉移,且PET及CT的部分均提示有骨骼轉移,那麼骨顯像或氟化鈉PET-CT檢查可能不再需要。
4.2.3.5.2 (2)隨訪:
若患者出現骨痛或鹼性磷酸酶升高時,可行骨顯像檢查評估是否有骨轉移;當缺乏臨牀信號和症狀提示覆發時,不建議影像學的轉移篩查。
4.2.4 (四)實驗室檢查。
4.2.4.1 1.生化檢查
早期無特異性血生化改變,晚期累及其他臟器時,可出現相應的生化指標的變化。如多發骨轉移時,可出現鹼性磷酸酶升高。
4.2.4.2 2.腫瘤標誌物檢測
CA15-3、癌胚抗原是乳腺癌中應用價值較高的腫瘤標誌物,主要用於轉移性乳腺癌患者的病程監測。CA15-3和癌胚抗原聯合應用可顯著提高檢測腫瘤復發和轉移的敏感性。由於其對局部病變的敏感性低,且在某些良性疾病和其他器官的惡性腫瘤中也可升高,因此不適合用於乳腺癌的篩查和診斷。
4.3 三、組織病理學診斷
病理學診斷是乳腺癌確診和治療的依據。規範化的乳腺癌病理診斷報告不僅需要提供準確的病理診斷,還需要提供正確、可靠的與乳腺癌治療方案選擇、療效預測和預後判斷相關的標誌物檢測結果。進行病理學診斷時,臨牀醫師需提供完整、確切的臨牀情況,以及合格、足量、完整的組織標本。
4.3.1 (一)標本類型及固定。
4.3.1.1 1.標本類型
乳腺標本類型主要包括空芯針穿刺活檢標本、真空輔助活檢標本和各種手術切除標本(乳腺微創旋切術、乳腺腫塊局部切除術、乳腺病變保乳切除術、乳腺單純切除術乳腺改良根治術標本、以及乳腺癌新輔助化療後的改良根治標本)。
4.3.1.2 2.標本固定
穿刺或切除後的乳腺組織應立即固定(不得超過1小時爲宜)。應選擇足夠的磷酸緩衝液配製的4%中性甲醛固定液。活檢標本固定時間6~48小時爲宜。對於切除標本,應將其每隔5~10mm切開,宜用紗布或濾紙將相鄰的組織片分隔開,以保障固定液的充分滲透和固定。固定時間12~72小時爲宜。
4.3.2 (二)取材及大體描述指南。
接受標本後,首先必須覈對標本袋信息及病理檢查申請單的信息(包括姓名、性別、年齡、牀位號、住院號、標本類型及部位、臨牀診斷、送檢者等)。
4.3.2.1 1.空芯針穿刺活檢標本
(1)大體檢查及記錄:標明穿刺組織的數目,每塊組織的大小,包括直徑和長度。
(2)取材:送檢組織全部取材。空芯針穿刺活檢標本不宜行術中病理診斷。
4.3.2.2 2.真空輔助(乳腺微創旋切)活檢標本
(2)取材:送檢組織全部取材。如臨牀送檢組織標記鈣化及鈣化旁,需記錄註明,並將其分別置於不同的包埋盒中。真空輔助活檢標本不宜行術中病理診斷。
4.3.2.3 3.乳腺腫塊切除標本
(1)大體檢查及記錄:按外科醫師的標示確定送檢標本的部位。若未標記,應聯繫外科醫師明確切除標本所在的位置。測量標本3個徑線的大小;若帶皮膚,應測量皮膚的大小。測量腫瘤或可疑病變3個徑線的大小。記錄腫瘤或可疑病變的部位和外觀。記錄每塊組織所對應的切片總數及編號。
(2)取材:術中冰凍取材:沿標本長軸每隔5mm做1個切面,如有明確腫塊,在腫塊處取材。如爲鈣化竈,宜對照X線攝片對可疑病變取材或按標記探針位置取材。如無明確腫塊,對可疑病變處取材。
常規標本取材:若腫塊或可疑病變最大徑≤5cm,應至少每1cm取材1塊,必要時[如導管原位癌(ductal carcinomainsitu,DCIS)]宜將病變全部取材後送檢。若腫塊或可疑病變最大徑大於5cm,應每1cm至少取材1塊,如6cm的腫塊至少取材6塊;如已診斷爲DCIS,建議將病竈全部取材。乳腺實質的其他異常和皮膚均需取材。
4.3.2.4 4.乳腺病變保乳切除標本
4.3.2.4.1 (1)大體檢查及記錄。
冰凍另送切緣者需對切緣檢查及記錄。
1)按外科醫師的標示確定送檢標本的部位。若未標記,應聯繫外科醫師明確切除標本所在的位置。
3)根據臨牀標記,正確放置標本,建議將標本各切緣(表面切緣、基底切緣、上切緣、下切緣、內切緣、外切緣)塗上不同顏色的染料。待色標略幹後,吸乾多餘的染料。
4)按從表面到基底的方向,沿標本長軸每隔3~5mm做1個切面,將標本平行切分爲若干塊組織,並保持各塊組織的正確方向和順序。
5)仔細查找病竈,並測量腫瘤3個徑線的大小;若爲化療後標本,則測量瘤牀大小;若爲局切後標本,則描述殘腔大小及有無殘留病竈。
4.3.2.4.2 (2)取材:
1)切緣取材:冰凍另送切緣者除外切緣取材。保乳標本切緣取材主要有2種方法:垂直切緣放射狀取材和切緣離斷取材。2種切緣取材方法各有優缺點。無論採取何種取材方法,建議在取材前將六處標本切緣塗上不同顏色的染料,以便在鏡下觀察時能根據不同顏色對切緣作出準確的定位,並正確測量腫瘤和切緣的距離。保乳標本病理報告中需明確切緣狀態(陽性或陰性)。“陽性切緣”是指墨染切緣處有DCIS或浸潤性癌侵犯。“陰性切緣” 的定義並不一致,但多數指南或共識中將“墨染切緣處無腫瘤”定義爲“陰性切緣”。對於切緣陰性者,建議報告切緣與腫瘤的最近距離,應儘量用客觀的定量描述,而不建議用主觀描述(如距切緣近等)。
垂直切緣放射狀取材:根據手術醫師對保乳標本做出的方位標記,垂直於基底將標本平行切成多個薄片(建議間隔5 mm),觀察每個切面的情況。描述腫瘤大小、所在位置及腫瘤距各切緣的距離,取材時將大體離腫瘤較近處的切緣與腫瘤一起全部取材,大體離腫瘤較遠處的切緣抽樣取材,鏡下觀察時準確測量切緣與腫瘤的距離。垂直切緣放射狀取材的優點是能正確測量病變與切緣的距離,缺點是工作量較大,且對大體離腫瘤較遠的切緣只能抽樣取材。切緣離斷取材: 將六處切緣組織離斷,離斷的切緣組織充分取材,鏡下觀察切緣的累犯情況。切緣離斷取材的優點是取材量相對較少,能通過較少的切片對所有的切緣情況進行鏡下觀察,缺點是不能準確測量病變與各切緣的距離。
①若腫塊或可疑病變最大徑≤5cm,應沿腫瘤或可疑病變的最大切面至少每1cm取材1塊,必要時(如DCIS)宜全部取材後送檢。若腫塊或可疑病變最大徑大於5cm,則每1cm至少取材1塊;如已診斷爲DCIS,建議將病竈全部取材。若爲新輔助化療後標本,則參照乳腺癌新輔助治療後病理診斷規範(2020版)進行取材。若爲手術殘腔:送檢代表性的切面,包括可疑的殘留病竈。
②乳腺實質的其他異常。
③皮膚。
3)補充切緣取材:若首次切除時爲陽性切緣,需再次送檢切緣。補充切緣亦可作爲單獨的標本同切除組織一同送檢。若外科醫師已對補充切緣中真正的切緣做了標記,可用染料對真正切緣處進行塗色,並垂直於標記處切緣將標本連續切開並送檢。如果標本較小,所有組織應全部送檢。
4.3.2.5 5.乳腺切除術(包括單純切除術和改良根治術)
4.3.2.5.1 (1)大體檢查及記錄:
①按正確的方向擺放標本以便識別腫瘤所在的象限:改良根治術標本可通過識別腋窩組織來正確定位(腋窩組織朝向外上方)。單純切除術標本,需根據外科醫師的標記來定位,若未標記方向,則與外科醫師聯繫以確定標本的正確方向。建議標本的基底切緣塗上染料以便鏡下觀察切緣情況。
②測量整個標本及附帶皮膚、腋窩組織的大小。描述皮膚的外觀,如有無手術切口、穿刺點、瘢痕、紅斑或水腫等。
③從基底部水平切開乳頭,取乳頭水平切面組織一塊以觀察輸乳管的橫斷面,而後垂直於乳腺表面切開乳頭其他組織。描述乳頭、乳暈的外觀,如有無破潰及溼疹樣改變等。
⑤仔細查找病竈,記錄病竈所在象限位置,描述腫瘤(質地、顏色、邊界、與皮膚及深部結構的關係)的特徵。若有明確腫塊,則測量腫瘤3個徑線的大小;若爲化療後標本,則測量瘤牀大小;若爲局切後標本,則描述手術殘腔大小及有無殘留病竈。測量腫瘤、殘腔、瘤牀距最近表面切緣及基底切緣的距離。
⑦將腋窩脂肪組織同標本離斷後,仔細尋找淋巴結,對規範的腋窩清掃標本宜至少找及15枚淋巴結。描述淋巴結的總數目及最大徑範圍、有無融合、有無與周圍組織粘連。
4.3.2.5.2 (2)取材:
1)原發腫瘤和手術殘腔的取材:若爲腫瘤:送檢腫瘤的最大切面;若腫塊或可疑病變最大徑≤5cm,應至少每1cm取材1塊,必要時(如DCIS)宜全部取材後送檢。若標本腫塊或可疑病變最大徑>5cm,則每1cm至少取材1塊,如已診斷爲DCIS,應將病竈全部取材。若爲化療後瘤牀:參照乳腺癌新輔助治療後病理診斷規範(2020年版)取材。
若爲手術殘腔:送檢代表性的切面,包括可疑的殘留病竈。
2)其餘組織的異常病竈:乳頭:距腫瘤最近處表面被覆皮膚;距腫瘤最近處基底切緣,儘可能取切緣的垂直切面;周圍象限乳腺組織每個象限代表性取材1塊。腋窩淋巴結:若淋巴結肉眼觀察爲陰性,則送檢整個淋巴結行組織學檢查;若淋巴結肉眼陽性,則沿淋巴結最大徑剖開後取組織送檢,注意需附帶淋巴結周圍的結締組織,以識別淋巴結被膜外的腫瘤轉移竈。
4.3.2.6 6.前哨淋巴結活檢
乳腺癌前哨淋巴結活檢(Sentinel lymph node biopsy,SLNB)已逐漸取代傳統的腋窩淋巴結清掃來評估早期乳腺癌患者的區域淋巴結情況,SLNB陰性者可避免腋窩淋巴結清掃。
4.3.2.6.1 (1)前哨淋巴結轉移竈的定義:
1)孤立腫瘤細胞(isolated tumor cells,ITC):淋巴結中的腫瘤病竈直徑≤0.2mm:淋巴結中,或單張切片上的腫瘤細胞<200個。AJCC定義其爲pN0(i+)。目前大部分臨牀乳腺癌診療指南認爲ITC無臨牀意義,推薦按腋窩淋巴結陰性處理。
2)微轉移:腫瘤轉移竈最大徑>0.2mm,但不超過2mm。AJCC定義其爲pN1mi。ITC與微轉移有着本質的不同,前者爲pN0,後者爲pN1,兩者的鑑別非常重要。本標準中推薦將前哨淋巴結間隔2mm切成若干片組織,主要目的是爲了最大程度檢測出微轉移病竈。
4.3.2.6.2 (2)術中病理評估:
前哨淋巴結中術中病理評估的主要目的是檢測出淋巴結中的轉移病竈,從而進行腋窩淋巴結清掃,以避免二次手術。但目前對前哨淋巴結術中病理評估是否必要存在爭議。術中病理評估的方法主要包括術中細胞印片和術中冷凍切片。
1)術中細胞印片:將淋巴結每間隔2mm切成若干片組織,仔細檢查每片組織上是否存在肉眼可見的轉移竈,對每個切面行細胞印片。推薦巴氏染色和HE染色。術中細胞印片的優點是可保全整個淋巴結組織,對組織無損耗,可對淋巴結的不同切面取材,價廉,所需時間短,製作流程簡單;缺點是在印片的高細胞背景下辨認出分散的癌細胞(如小葉癌)有一定難度。術中細胞印片有很好的診斷特異性,但其診斷敏感性受多種因素的影響。
2)術中冷凍切片:將淋巴結每間隔2mm切成若干片組織,仔細檢查每片組織上是否存在肉眼可見的轉移竈,每片組織製成冷凍切片行病理評估。術中冷凍切片的優點是診斷特異性好,能夠避免因假陽性而造成不必要的腋窩淋巴結清掃;缺點是組織損耗,用時長,費用較高,且難以評估脂肪化的淋巴結等。
4.3.2.6.3 (3)術後常規石蠟病理評估:
術後石蠟切片是前哨淋巴結診斷的金標準,可明顯減少微小轉移的漏診。但是關於如何切分淋巴結、是否需要連續切片、切多少張連續切片、連續切片之間間隔多少尚無統一意見。推薦石蠟切片方案:
③每個蠟塊至少切一張切片;有條件的單位推薦連續切片,間隔150~200m,切6個切面。
4.3.3 (三)病理診斷分類、分級和分期方案。
4.3.3.1 1.組織學分型
參見附件2,組織學分型主要依據2012和2019版WHO乳腺腫瘤分類,某些組織學類型的準確區分需行免疫組化後確定。
對乳腺浸潤性癌進行準確的組織學分型對患者的個體化治療具有非常重要的臨牀意義。在NCCN乳腺癌臨牀實踐指南有關乳腺浸潤性癌的術後輔助治療方案中,針對小管癌、黏液癌這兩類預後較好的乳腺癌,制定了與其他類型的浸潤性癌不同的內分泌治療及放化療方案,因此要嚴格掌握這些特殊類型乳腺癌的診斷標準。對於炎性乳腺癌這類預後較差的乳腺癌,NCCN乳腺癌臨牀實踐指南也制定了有別於其他浸潤性癌的手術及術前術後輔助治療方案。過去認爲髓樣癌預後較好,但目前的研究表明其轉移風險與其他高度惡性的浸潤性癌相當,其診斷重複性在不同觀察者之間的差異也很明顯。因此NCCN指南建議,對伴有髓樣特徵的浸潤性癌患者應根據其臨牀和病理分期接受與浸潤性導管癌(invasiveductal carcinoma,IDC)一樣的治療。某些特殊類型的乳腺癌具有較特殊的臨牀特徵,如浸潤性微乳頭狀癌較易出現淋巴結轉移,即使出現較少比例的浸潤性微乳頭狀癌,也應在病理報告中注明百分比。對於混合性癌,建議報告不同腫瘤類型所佔的比例,並分別報告2種或以上成分的腫瘤分子生物標記的表達情況。
4.3.3.2 2.組織學分級
4.3.3.2.1 (1)浸潤性乳腺癌(參見附件3):
組織學分級是重要的預後因素,多項研究顯示在浸潤性乳腺癌中,組織學分級與預後明確相關。目前應用最廣泛的浸潤性癌病理分級系統是改良的Scarff-Bloom-Richardson(Nottingham)組織計分系統,根據腺管形成的比例、細胞的異型性和核分裂象計數三項重要指標,每項指標分別獨立評估,各給予1~3分,相加後根據總分將浸潤性癌劃分爲1、2、3共三個級別。腺管分化程度的評估針對整個腫瘤,需要在低倍鏡下評估。只計數有明確中央腺腔且由有極向腫瘤細胞包繞的結構,以腺管/腫瘤區域的百分比表示。細胞核多形性的評估要選取多形性最顯著的區域。該項評估參考周圍正常乳腺上皮細胞的核大小、形狀和核仁大小。當週邊缺乏正常細胞時,可用淋巴細胞作爲參照。當細胞核與周圍正常上皮細胞的大小和形狀相似、染色質均勻分佈時,視爲1分;當細胞核比正常細胞大,形狀和大小有中等程度差異,可見單個核仁時,視爲2分;當細胞核的大小有顯著差異,核仁顯著,可見多個核仁時應視爲3分。只計數明確的核分裂象,不計數核濃染和核碎屑。核分裂象計數區域必須要根據顯微鏡高倍視野的直徑進行校正。核分裂象計數要選取增殖最活躍的區域,一般常見於腫瘤邊緣,如果存在腫瘤中的異質性,要選擇核分裂象多的區域。
4.3.3.2.2 (2)乳腺DCIS的分級:
對於DCIS,病理報告中應該包括分級,並建議報告是否存在壞死,組織學結構、病變大小或範圍、切緣狀況。目前乳腺原位癌的分級主要是細胞核分級,診斷標準如下。
低核級DCIS:由小而一致的癌細胞組成,呈僵直搭橋狀、微乳頭狀、篩狀或實體狀結構。細胞核大小一致,染色質均勻,核仁不明顯,核分裂象少見。中核級DCIS:形態介於低級別和高級別DCIS之間,細胞的大小、形狀、極性有輕-中等差異。染色質粗細不等,可見核仁,核分裂象可見,可出現點狀壞死或粉刺樣壞死。
高核級DCIS:由高度不典型的細胞組成,形成微乳頭狀、篩狀或實體狀。細胞核多形性明顯,缺乏極性排列,染色質粗凝塊狀,核仁明顯,核分裂象較多。管腔內常出現伴有大量壞死碎屑的粉刺樣壞死。但腔內壞死不是診斷高級別DCIS的必要條件,有時導管壁襯覆單層細胞,但細胞高度異型,也可以診斷爲高級別DCIS。
4.3.3.3 3.乳腺癌的分期方案
參見附件4。腫瘤分期包括了腫瘤的大小、累及範圍(皮膚和胸壁受累情況)、淋巴結轉移和遠處轉移情況。正確的腫瘤分期是指導患者個體化治療決策的基礎。乳腺癌患者要進行臨牀分期和病理分期。
第8版AJCC乳腺癌分期對腫瘤大小的測量做出了詳盡的規定。腫瘤大小的測量有多種方法,包括臨牀觸診、影像學評估、病理大體測量和顯微鏡下測量。乳腺癌分期中涉及到的腫瘤大小是指浸潤性癌的大小。由於體檢、影像學及大體檢查均無法區分浸潤性癌和導管內癌,因此顯微鏡下測量應該是最準確的測量方式。如果浸潤性癌範圍較大,無法用1個蠟塊全部包埋,則以巨檢時的腫瘤大小爲準。若浸潤性癌病竈侷限,可以用1個蠟塊全部包埋,則腫瘤大小以顯微鏡下測量的大小爲準。
(1)如果腫瘤組織中有浸潤性癌和原位癌2種成分,腫瘤的大小應該以浸潤性成分的測量值爲準,可註明原位癌的範圍和比例等。
(2)原位癌伴微浸潤:出現微浸潤時,應在報告中注明,並測量微浸潤竈最大徑;如爲多竈微浸潤,浸潤竈大小不能累加,需在報告中注明多竈微浸潤,並測量最大浸潤竈的大小。
(3)對於肉眼能確定的發生於同一象限的2個以上多個腫瘤病竈,應在病理報告中注明爲多竈性腫瘤,並分別測量大小。
(4)對於肉眼能確定的發生於不同象限的2個以上多個腫瘤病竈,應在病理報告中注明爲多中心性腫瘤,並分別測量大小。
(5)如果腫瘤組織完全由DCIS組成,應儘量測量其範圍。淋巴結狀態是決定乳腺癌患者治療和預後的重要因素,對於淋巴結轉移數位於分期臨界值(如1、3和10個轉移)附近時,要特別仔細觀察淋巴結的轉移數目,從而做出準確的pN分期。新輔助治療後標本的分期需結合臨牀檢查、影像學檢查和病理檢查信息,根據手術切除標本的情況對治療後的yT和yN進行判定。
4.3.3.4 4.免疫組化和腫瘤分子病理檢測及其質量控制
應對所有乳腺浸潤性癌病例進行雌激素受體(estrogenreceptor,ER)、孕激素受體(progesterone receptor,PR)、HER2免疫組化染色,HER2(2+)病例應進一步行原位雜交檢測。評估ER、PR狀態的意義在於確認內分泌治療獲益的患者羣體以及預測預後,ER和/或PR陽性患者可採用他莫昔芬和芳香化酶抑制劑等內分泌治療。ER、PR的規範化病理報告需要報告陽性細胞強度和百分比。ER及PR陽性定義:≥1%的陽性染色腫瘤細胞。評估HER2狀態的意義在於確認適合HER2靶向治療的患者羣體以及預測預後。HER2陽性定義:經免疫組織化學檢測,超過10%的細胞出現完整胞膜強着色(3+)和/或原位雜交檢測到HER2基因擴增(單拷貝HER2基因>6或HER2/CEP17比值>2.0)。ER、PR檢測參考《中國乳腺癌ER、PR檢測指南》(參見附件5)。HER2檢測參考《中國乳腺癌HER2檢測指南》(參見附件6)。Ki-67增殖指數在乳腺癌治療方案選擇和預後評估上起着越來越重要的作用,應對所有乳腺浸潤性癌病例進行Ki-67檢測,並對癌細胞中陽性染色細胞所佔的百分比進行報告。對於Ki-67計數,目前尚缺乏相關共識。建議在低倍鏡下評估整張切片,觀察陽性細胞分佈是否均勻:若腫瘤細胞中陽性細胞分佈較均勻,可隨機選取3個或以上浸潤性癌高倍視野計數,得出一個平均的Ki-67增殖指數。若腫瘤細胞中陽性細胞分佈不均勻,出現明顯的Ki-67增殖指數高表達區域(熱點區)。主要有2種情況:①在腫瘤組織邊緣與正常組織交界處出現熱點區,而腫瘤組織內Ki-67增殖指數相對較低,推薦選取腫瘤邊緣區域熱點區≥3個浸潤性癌高倍視野進行Ki-67增殖指數評估;②在腫瘤組織內出現熱點區,可對整張切片的Ki-67增殖指數進行平均評估,選取視野時應包括熱點區域在內的≥3個浸潤性癌高倍視野。當Ki-67增殖指數介於10%~30%的臨界值範圍時,建議儘量評估500個以上的浸潤性癌細胞,以提高結果的準確度。開展乳腺癌免疫組化和分子病理檢測的實驗室應建立完整有效的內部質量控制,不具備檢測條件的單位應妥善地保存好標本,以供具有相關資質的病理實驗室進行檢測。具有合格資質的病理實驗室應滿足以下條件:
(1)應建立完善的標準操作程序,並嚴格遵照執行,做好每次檢測情況的記錄和存檔工作。應開展同一組織不同批次染色結果的重複性分析。檢測相關的儀器和設備應定期維護、校驗。任何操作程序和試劑變化均應重新進行嚴格的驗證。
(2)從事乳腺癌免疫組化和分子病理檢測的實驗技術人員和病理醫師應定期進行必要的培訓、資格考覈和能力評估。
(3)實驗室外部質控可通過參加有關外部質控活動來實現。外部質控的陽性和陰性符合率應達到90%以上。外部質控活動推薦每年參加1~2次。
4.3.3.5 5.病理報告內容及指南
乳腺浸潤性癌的病理報告(參見附件5)應包括與患者治療和預後相關的所有內容,如腫瘤大小、組織學類型、組織學分級、有無並存的DCIS、有無脈管侵犯、神經侵犯、乳頭、切緣和淋巴結情況等。還應包括ER、PR、HER2、Ki-67等指標的檢測情況。若爲治療後乳腺癌標本,則應對治療後反應進行病理評估。DCIS的病理診斷報告應報告核級別(低、中或高級別)和有無壞死(粉刺或點狀壞死)、手術切緣情況以及ER和PR表達情況。對癌旁良性病變,宜明確報告病變名稱或類型。對保乳標本的評價宜包括大體檢查及顯微鏡觀察中腫瘤距切緣最近處的距離、若切緣陽性,應註明切緣處腫瘤的類型(原位癌或浸潤性癌)。淋巴管/血管侵犯需要與乳腺癌標本中經常出現的組織收縮引起的腔隙鑑別。相對而言,收縮腔隙在腫瘤組織內更常見,而在腫瘤主體周圍尋找脈管侵犯更可靠。
4.4 四、鑑別診斷
乳腺癌需與乳腺增生、纖維腺瘤、囊腫、導管內乳頭狀瘤、乳腺導管擴張症(漿細胞性乳腺炎)、乳腺結核等良性疾病,與乳房惡性淋巴瘤、間葉源性肉瘤以及其他部位原發腫瘤轉移到乳腺的繼發性乳腺惡性腫瘤進行鑑別診斷。鑑別診斷時需要詳細地詢問病史和仔細地體格檢查,並結合影像學檢查(乳腺超聲、乳腺X線攝影及乳腺磁共振等),最後還需要細胞學和/或病理組織學檢查明確診斷。臨牀查體可觸及腫塊的乳腺癌約佔80%,可以進行外科手術活檢行病理組織學診斷,在有條件的醫院可藉助穿刺活檢儘快明確診斷。但臨牀觸診陰性的乳腺癌增加了診斷的困難,需藉助影像學定位進行病竈穿刺,或在乳腺X線技術引導下放置金屬定位線,再經外科切除活檢明確診斷。少數乳腺癌患者伴有乳頭溢液,需與乳腺增生、導管擴張、乳汁瀦留、導管內乳頭狀瘤及乳頭狀瘤病等鑑別。有條件的醫院可藉助乳頭溢液細胞學塗片查找癌細胞,通過乳管內鏡檢查,瞭解乳管內有無佔位性病變,需要時再經活檢明確診斷。
4.5 五、治療
4.5.1 (一)治療原則。
乳腺癌應採用綜合治療的原則,根據腫瘤的生物學行爲和患者的身體狀況,聯合運用多種治療手段,兼顧局部治療和全身治療,以期提高療效和改善患者的生活質量。
4.5.1.1 1.非浸潤性乳腺癌的治療
4.5.1.1.1 (1)LCIS:
經典型LCIS中的小葉內終末導管或腺泡呈實性膨大,其中充滿均勻一致的腫瘤細胞。腫瘤細胞體積小而一致,黏附性差。細胞核呈圓形或卵圓形,染色質均勻,核仁不明顯。細胞質淡染或淡嗜酸性,可含黏液空泡致細胞核偏位呈印戒細胞樣,細胞質也可透亮。LCIS包括多種亞型:多形性型、旺熾型、透明型、肌樣細胞型等。其中較爲重要的是多形性亞型。多形性LCIS中的腫瘤細胞黏附性差,細胞核顯著增大,有明顯的多形性,可有顯著的核仁和核分裂象,有時可見粉刺樣壞死或鈣化,需與高級別DCIS相鑑別。非典型性小葉增生(atypical lobular hyperplasia,ALH)和LCIS在形態學上具 有相似之處,但累犯終末導管小葉單位(terminal ductal lobular unit,TDLU)的程度不同。當TDLU單位中≥50%的腺泡被診斷性細胞所充滿並擴張時可診斷爲LCIS,小於50%時則診斷爲ALH。根據AJCC(第8版),將LCIS當做乳腺良性病變,然而專家團認爲仍需謹慎適用,推薦對非經典型LCIS需積極處理。LCIS發展爲浸潤性癌的風險相對較小,具有癌變間期長、雙側乳房和多個象限發病的特點。一些研究發現,在診斷爲ALH和LCIS的婦女中,終生發生癌變的概率爲5%~32%,平均癌變率爲8%。LCIS癌變發生於雙側乳房的機會均等,而不僅僅侷限於原發LCIS部位。多數觀點認爲,LCIS是癌變的危險因素,有些研究則認爲LCIS是癌前病變。有研究顯示,LCIS多數進展爲浸潤性小葉癌,但是也可進展爲IDC。這是一個值得重視的癌前病變,對其治療需要更有效而確切的方法。
LCIS可無任何臨牀症狀,亦可沒有乳房腫塊、乳頭溢液、乳頭腫脹及皮膚改變等體徵,有時僅有類似增生樣改變。依據中國女性乳腺特點,應完善乳腺X線、乳腺超聲檢查,必要時可行乳腺MRI;擬行保乳手術患者,術前必須行乳腺X線檢查檢查。在乳腺X線檢查發現有鈣化、腫塊、結構紊亂後,其通過穿刺活檢(包括空芯針穿刺以及真空輔助穿刺活檢)或開放活檢均可被診斷。如穿刺活檢提示爲經典型LCIS患者,則可以進行常規的影像學隨訪而不行開放活檢。若穿刺活檢提示爲多形性LCIS或穿刺結果與影像學檢查不符,需行開放活檢以除外DCIS及浸潤癌。LCIS亦有因其他乳房病變進行手術活檢時發現。典型的LCIS與低級別的DCIS很相似,可採用E-鈣黏蛋白及P120免疫組織化學染色來鑑別。
LCIS如果行廣泛切除後,絕經前可予他莫昔芬(三苯氧胺)治療5年;絕經後口服他莫昔芬或雷洛昔芬降低風險;
若不能排除多形性LCIS可行全乳切除術,視情況進行乳房重建。
4.5.1.1.2 (2)DCIS:
又稱導管內癌,爲非浸潤性癌,多數發生於TDLU,也可發生於大導管,是侷限於乳腺導管內的原位癌。典型的DCIS在乳腺X線檢查上多表現爲不伴腫塊的簇狀微小鈣化竈,惡性鈣化還可表現爲細小點樣、線狀、分支狀鈣化等。在實際工作中,多采用以核分級爲基礎,兼顧壞死、核分裂象及組織結構的分級模式,將DCIS分爲3級,即低級別、中級別和高級別。高級別DCIS往往由較大的多形性細胞構成,核仁明顯、核分裂象常見。管腔內常出現伴有大量壞死碎屑的粉刺樣壞死,但腔內壞死不是診斷高級別DCIS的必要條件。低級別DCIS由小的單形性細胞組成,細胞核圓形,大小一致,染色質均勻,核仁不明顯,核分裂象少見。腫瘤細胞排列成僵直搭橋狀、微乳頭狀、篩狀或實體狀。中級別DCIS結構表現多樣,細胞異型性介於高級別和低級別DCIS之間。DCIS可能是IDC的前驅病變,DCIS不經治療最終可能會發展爲IDC。對最初誤診爲良性病變而導致未能獲得治 療 的 DCIS 研 究 顯 示 , 從DCIS 進展爲IDC的比例爲14%~53%。
依據中國女性乳腺特點,應完善乳腺X線檢查、乳腺超聲檢查,必要時可行乳腺MRI。擬行保乳手術的患者,術前必須行乳腺X線檢查診斷。至少有90%的DCIS是在乳腺X線檢查篩查中被發現,多數表現爲微小鈣化竈,部分表現爲微小鈣化竈伴腫塊影或緻密影,約10%患者有可觸及的腫塊,約6%患者乳腺X線檢查表現爲假陰性。DCIS的典型MRI表現爲沿導管分佈的導管樣或段樣成簇小環狀強化,也可表現爲局竈性、區域性或瀰漫性強化,孤立性或多發性腫塊。超聲下DCIS多表現爲邊界不清的腫塊,內部呈低迴聲,腫塊內多具有瀰漫、成堆或簇狀分佈的針尖樣、顆粒狀鈣化,腫塊內血流多較豐富。空芯針穿刺活檢及開放活檢都是獲取DCIS組織學診斷的手段,但穿刺活檢提示爲DCIS患者,可選擇開放活檢以明確有無浸潤癌。在穿刺結果爲DCIS患者中,25%有IDC成分;在穿刺結果爲LCIS患者中,開放活檢後有17%~27%病理升級爲DCIS或浸潤性癌。因此建議穿刺活檢後行開放活檢。DCIS的病理診斷,推薦完整取材、規範取材。
1)局部擴大切除並全乳放射治療。2)全乳切除,視情況進行SLNB和乳房重建。對於單純原位癌患者,在未獲得浸潤性乳腺癌證據或者未證實存在腫瘤轉移時,不建議行全腋窩淋巴結清掃。然而,仍有一小部分臨牀診斷爲單純原位癌的患者在進行手術時被發現爲浸潤性癌,應按浸潤癌處理。單純LCIS的確診必須依據手術活檢結果。
3)以下情形考慮採用他莫昔芬治療5年以降低保乳手術後同側乳腺癌復發風險:
①接受保乳手術(腫塊切除術)加放療的患者,尤其是ER陽性的DCIS患者;ER陰性的DCIS患者他莫昔芬治療效果尚不確定。
②對於接受全乳切除術的DCIS患者術後可通過口服他莫昔芬或雷洛昔芬來降低對側乳腺癌風險,但需權衡化學預防的臨牀獲益與不良反應。
4.5.1.2 2.浸潤性乳腺癌的治療
(1)保乳手術加放射治療。
(2)乳腺癌全乳切除聯合腋窩淋巴結清掃手術(改良根治術),視情況進行乳房重建。
(4)老年人乳腺癌:局部擴大切除或全乳切除(根據手術及麻醉風險),受體陽性患者需進行內分泌治療,視情況做SLNB。
4.5.2 (二)手術治療。
4.5.2.1 1.手術治療原則
乳腺癌手術範圍包括乳腺和腋窩淋巴結兩部分。乳腺手術有腫瘤擴大切除和全乳切除。腋窩淋巴結可行SLNB和腋窩淋巴結清掃,除原位癌外均需瞭解腋窩淋巴結狀況。選擇手術術式應綜合考慮腫瘤的臨牀分期和患者的身體狀況。
4.5.2.2 2.乳腺手術
4.5.2.2.1 (1)乳房切除手術:
適應證爲TNM分期中0、Ⅰ、Ⅱ期及部分Ⅲ期且無手術禁忌,患者不具備實施保乳手術條件或不同意接受保留乳房手術;局部進展期或伴有遠處轉移的患者,經全身治療後降期,亦可選擇全乳切除術。Halsted傳統根治術中採用的乳房切除術需同時切除胸大小肌,創傷大,併發症發生率高,目前已被改良根治術所取代。其切除範圍包括上至鎖骨下、下至腹直肌前鞘、內至胸骨旁、外至背闊肌的解剖邊界內,連同胸大肌筋膜完整切除乳腺組織及乳頭乳暈複合體,只有當胸肌受累時才需切除部分或全部胸肌。部分學者認爲可保留胸大肌筋膜,尤其是需要進行術中即刻假體/擴張器重建時。目前的乳房切除術已由改良根治術發展爲保留皮膚的乳房切除+乳腺重建手術,兩者治療效果類似,但後者美容效果更好。此外,保留乳頭乳暈的乳房切除術在臨牀上的應用也日趨廣泛,但還缺乏長期研究數據,需進一步完善患者選擇問題。
4.5.2.2.2 (2)保留乳房手術:
嚴格掌握保乳手術適應證。實施保乳手術的醫療單位應具備保乳手術切緣的組織學檢查設備與技術,保證切緣陰性;保乳術後放射治療的設備與技術。保留乳房手術後美容效果評價標準見附件7。保乳手術適用於患者有保乳意願,乳腺腫瘤可以完整切除,達到陰性切緣,並可獲得良好的美容效果、同時可接受術後輔助放療的患者。年輕不作爲保乳手術的禁忌,≤35歲的患者有相對高的復發和再髮乳腺癌的風險,在選擇保乳時,應向患者充分交待可能存在的風險。保乳手術的絕對禁忌證包括病變廣泛或瀰漫分佈的惡性特徵鈣化竈,且難以達到切緣陰性或理想外形;T4期乳腺癌,包括侵犯皮膚、胸壁及炎性乳腺癌;腫瘤經局部廣泛切除後切緣陽性,再次切除後仍不能保證病理切緣陰性者;妊娠期乳腺癌,預估術後放療無法等到分娩後者;患者拒絕行保留乳房手術。相對禁忌證包括腫瘤直徑大於3cm和累及皮膚的活動性結締組織病,尤其是硬皮病和紅斑狼瘡等。
4.5.2.3 3.腋窩淋巴結的外科手術處理
腋窩淋巴結是浸潤性乳腺癌標準手術中的一部分。其主要目的是爲了了解腋窩淋巴結的狀況,以確定分期,選擇最佳治療方案。
4.5.2.3.1 (1)乳腺癌SLNB:
SLNB具有創傷小且相關併發症少等優點,是指對最早接受乳腺癌區域淋巴引流和發生腫瘤轉移的1個(或幾個)淋巴結進行切除活檢,以評估腋窩淋巴結狀態,NCCN乳腺癌臨牀實踐指南推薦臨牀腋窩淋巴結陰性的早期乳腺癌患者選擇SLNB作爲腋窩淋巴結處理的優選手術方式。在SLNB手術前,需進行前哨淋巴結示蹤,目前SLNB常用的示蹤方法有染料法(專利藍、異硫藍、亞甲藍和納米炭)、核素法、染料聯合核素法及熒光示蹤法,運用最廣泛的示蹤方法爲藍染法聯合核素法。SLNB技術能夠準確的進行乳腺癌腋窩淋巴結分期,對於臨牀檢查腋窩淋巴結無明確轉移的患者,進行SLNB後,淋巴結陰性的患者可以免除腋窩淋巴結清掃,以減少上肢水腫等併發症的發生;若SLNB陽性,可進行腋窩淋巴結清掃。
4.5.2.3.2 (2)腋窩淋巴結清掃:
腋窩淋巴結清掃的指徵包括:①臨牀腋窩淋巴結陽性且經穿刺/手術活檢證實有轉移的患者;②前哨淋巴結陽性,且不符合ACOSOGZ0011入組標準的患者如T3、超過2枚前哨淋巴結陽性以及需全部乳腺切除者;③近期不充分的腋窩淋巴結清掃;④前哨淋巴結驗證試驗;⑤SLNB失敗;⑥SLNB發現臨牀可疑的淋巴結;⑦T4;⑧不能施行SLNB;⑨SLNB後腋窩復發。通常情況下,腋窩淋巴結清掃範圍應包括背闊肌前緣至胸小肌外側緣(Level Ⅰ)、胸小肌外側緣至胸小肌內側緣(Level Ⅱ)的所有淋巴結。清掃腋窩淋巴結要求在10個以上,以保證能真實地反映腋窩淋巴結的狀況。只有當LevelⅠ~Ⅱ明顯轉移或者Level Ⅲ(胸小肌內側緣至腋靜脈入口處)探及增大轉移的淋巴結時才需進行Ⅰ~Ⅲ水平的全腋窩淋巴結清掃。
4.5.2.4 4.乳房修復與重建
乳腺癌改良根治手術後的乳房缺損與保乳術後的乳房畸形均需要整形外科進行再造和修復,且已成爲乳腺癌完整治療方案中不可或缺的一個重要組成部分。乳房再造提高術後患者的生活質量及心理滿意度。我國乳房再造的數量逐年增加,方法越來越完善,乳房再造的理念和意識被越來越多的腫瘤外科醫師所認識和接受。乳房再造的腫瘤學安全性是肯定的。是否行乳房再造、再造的時機及再造方式不影響乳腺癌患者術後的生存率和生存時間。乳房再造對外科手術或腫瘤復發、轉移的檢出沒有影響。
正常情況下,乳房再造不影響術後化療的進行。除非即刻再造術後出現較嚴重併發症(如感染、切口裂開等),否則不會對化療的臨牀應用及治療效果造成顯著影響。即刻乳房再造術後輔助化療不會增加再造術後併發症發生率,不會降低即刻乳房再造成功率,不會影響傷口癒合,也不會影響再造效果。但新輔助化療會增加即刻乳房再造術後皮瓣感染及壞死的發生率。化療可造成人體免疫功能下降、抗感染能力降低,化療期間不適合做任何乳房再造手術。無論自體組織再造,還是假體再造,均不是放射治療的禁忌證,也不會對放療效果產生明顯影響。即刻乳房再造增加了術後放療野設計的技術難度,但周密設計的放療方案不影響放療效果。放療會影響再造的遠期美學滿意度及總體滿意度。
(1)必須將腫瘤治療放在首位。乳房再造的任何整形外科治療都不應推遲乳腺癌輔助治療的時間,不應影響乳腺癌輔助治療的進行。
(2)必須將乳房再造納入乳腺癌的整個治療方案,醫師有義務告知患者有選擇進行乳房再造的權利。
(3)在乳腺切除過程中,應在不違反腫瘤學原則的前提下,儘可能保留乳房的皮膚、皮下組織以及重要的美學結構(如乳房下皺襞等),最大限度地爲乳房再造保留條件,提高再造乳房美學效果和患者滿意度。
(4)乳腺癌的治療應當在多學科團隊合作框架下進行,包括放射科、乳腺外科、整形外科、影像科、病理科、心理科、核醫學科、免疫科等。
乳房再造的術前檢查、評估和教育:術前應對患者的條件進行檢測與評估,分析腫瘤學情況、內科情況、組織條件、對側乳房情況等,綜合這些條件選擇創傷小、手術簡化、費用少、併發症發生率低且效果良好的手術方案。禁忌行乳房再造的乳腺癌類型與分期:Ⅳ期浸潤性乳腺癌、復發轉移性乳腺癌。通常認爲放化療期間、放療後半年內禁行乳房再造,對於接受過放療或準備進行放療的患者,應謹慎選擇乳房再造的時機和手術方式。嚴重肥胖和吸菸、嚴重內科疾病、外周血管疾病都是術後出現併發症的重要風險因素,是乳房再造術的相對禁忌證。治療週期及費用:①乳房再造是一個序列化的治療,通常需要多次手術才能達到理想的效果。採用組織擴張法進行乳房再造。②即刻乳房再造在總體治療時間和費用上較二期乳房再造具有優勢。
乳房再造的基本方法:包括皮膚覆蓋的再造和乳房體積的再造。皮膚覆蓋的再造方法包括組織擴張和自體皮瓣移植等,乳房體積的再造方法包括:應用假體、皮瓣組織瓣移植、遊離自體脂肪移植等。自體組織乳房再造常用的皮瓣包括:背闊肌肌皮瓣、腹直肌肌皮瓣、腹壁下動脈穿支皮瓣等。隨訪時間:乳房再造的隨訪時間應從術後開始,至術後5年以上,根據乳房再造方式不同,定期進行隨訪。觀察指標:包括乳腺癌的腫瘤學隨訪、乳房外形與對稱性、切口瘢痕、供區功能、假體完整性、包膜攣縮、其他併發症。必要時還應包括心理變化、生活質量變化等。檢查項目:腫瘤學檢查、乳房體表測量值、照相、供區運動功能測定、乳房假體包膜攣縮分級,必要時行超聲、磁共振等特殊檢查。建議指導:乳房再造術後,應給患者進行詳細的術後指導,包括日常注意事項、運動、腫瘤學檢查、複查時間等。
4.5.3 (三)放射治療。
4.5.3.1 1.早期乳腺癌保乳術後放射治療
4.5.3.1.1 (1)適應證:
原則上,所有接受保乳手術的患者均需接受放射治療。對年齡>70歲、乳腺腫瘤≤2cm、無淋巴結轉移、ER陽性、能接受規範內分泌治療的女性患者,可以考慮省略保乳術後放療。
4.5.3.1.2 (2)照射範圍:
1)在有條件的單位,對經嚴格選擇的低危患者,可以考慮行部分乳腺照射,具體的患者選擇標準及治療方式參見“(三)1.(5)部分乳腺照射”章節。
2)腋窩淋巴結清掃或SLNB未發現淋巴結轉移的患者,照射範圍爲患側乳腺。
3)前哨淋巴結陽性且未行腋窩淋巴結清掃的患者,對於 T 1~2 期、1~2 個前哨淋巴結陽性的浸潤性乳腺癌,可考慮予以全乳高位切線野放療(即切線野上界位於肱骨頭下2cm 以 內 ), 如 採 用 調 強放療(intensity-modulatedradiotherapy,IMRT)技術則需注意將低、中位腋窩與患側全乳設爲一體化靶區進行勾畫與照射;但對於不符合該標準的保乳術後患者,照射範圍建議包括患側乳房,鎖骨上及腋窩淋巴結引流區。
4)接受腋窩淋巴結清掃,陽性淋巴結數爲1~3個的患者,爲了儘可能降低復發風險,原則上建議行淋巴引流區照射,可選擇復發風險低危患者予以免除淋巴引流區照射。照射範圍包括患側鎖骨上、下區,內乳照射應根據個體情況決定。年輕、激素受體(Hormone Receptor, HR)陰性、廣泛脈管癌栓、原發竈位於內側/中央象限、組織學分級高級別等危險因素的重疊可能會增加淋巴引流區照射的重要性。
5)接受腋窩淋巴結清掃且淋巴結轉移≥4個的患者,照射靶區需包括患側乳腺、鎖骨上/下及內乳淋巴引流區(保證心肺安全前提下)。
6)內乳照射目前存在爭議,推薦具備下列條件患者考慮行內乳照射:
④初診時影像學診斷內乳淋巴結轉移或經病理證實內乳淋巴結轉移但未行內乳淋巴結清掃。
內乳照射建議應用現代精準放療技術,以便準確評估心臟等正常組織照射劑量,同時把握全身治療及放療對心臟相關損傷與內乳預防照射的獲益與風險,必要時多學科充分溝通,或鼓勵患者參加臨牀試驗。
7)腋窩清掃徹底的患者,不需要預防照射。腋窩放療可用於具有以下腋窩復發高危因素的患者,但需要權衡腫瘤復發風險和放療增加淋巴水腫的風險。高危因素包括:
①腋窩清掃不徹底,根據患者術前腋窩轉移淋巴結負荷、術中淋巴結與周圍血管粘連情況及手術清掃的徹底程度、放療前腋窩查體及影像學綜合評估判斷淋巴結是否殘留;
②淋巴結包膜外侵犯;
但需要區分腋窩淋巴結總數少是因爲手術清掃不足還是病理科取材不充分,必要時與外科醫師和病理科醫師進行溝通。
8)對接受全乳放療的患者,對符合以下標準的患者,建議瘤牀補量:
①浸潤性乳腺癌:年齡≤50 歲、任意級別,或 51 歲至 70 歲、高級別,或切緣陽性;
②DCIS:年齡≤50 歲,或高級別,或切緣邊距<2 mm,或陽性切緣。
①浸潤性乳腺癌:年齡>70 歲、激素受體陽性、低中級別並有足夠的陰性切緣(邊距≥2 mm);
②DCIS:年齡>50歲、經篩查發現、腫瘤大小≤2. 5cm、低中級別、並有足夠的陰性切緣(邊距≥3 mm)。
對於不符合上述標準的患者,醫師可以根據患者情況權衡利弊(腫瘤控制和美容效果),做出個體化決策。
4.5.3.1.3 (3)照射技術:
保乳術後放療可以通過三維適形放療、固定野或旋轉調強等照射技術進行。無論採取何種技術,推薦採用CT定位並勾畫靶區,將CT圖像導入三維計劃治療系統上進行計劃評估,以準確評估靶區及危及器官的劑量分佈。CT定位時,應採用鉛絲標記患側乳腺外輪廓及乳腺原發竈手術瘢痕,以利於確定全乳腺及瘤牀補量照射範圍。呼吸控制技術,如深吸氣屏氣、俯臥定位等,可能進一步降低正常器官,主要是心肺的照射劑量,推薦在有條件的單位中開展。與二維放療相比,三維適形及調強照射有助於改善靶區內的劑量均勻性,降低正常組織的受照劑量,更好的處理乳腺與區域淋巴結照射野的銜接,在乳腺體積大、需要進行區域淋巴結照射的情況下更有優勢,但增加了計劃設計的複雜程度。推薦根據患者的病情、照射範圍及合併症情況等個體化的選擇照射技術。
乳腺瘤牀補量可採用術中放療、組織間插植、電子線或X線外照射等方式實現。推薦外科醫師在腫瘤切緣放置鈦夾,爲瘤牀補量提供參照。
4.5.3.1.4 (4)照射劑量及分割模式:
推薦全乳±區域淋巴結的照射劑量爲50Gy/2Gy/25f。外照射瘤牀補量可序貫於全乳放療後,序貫照射劑量爲10~16Gy/2Gy/5~8f;在有經驗的單位,可以考慮瘤牀同步加量照射,如瘤牀同步照射劑量60Gy/2.4Gy/25f。對僅行全乳照射的患者,推薦可給予大分割放療40Gy/15f或42.5Gy/16f;在有經驗的單位,也可採用43.5Gy/15f/3w的分割模式。外照射瘤牀補量序貫於全乳大分割放療後,可採用常規分割模式10~16Gy/2Gy/5~8f或大分割模式10~12.5Gy/4~5f;在有經驗的單位,也可採用大分割序貫補量模式8.7Gy/3f。推薦開展針對瘤牀同步大分割加量模式的臨牀研究,如瘤牀同步照射劑量49.5Gy/15f。在有經驗的單位,對於行全乳+區域淋巴結照射的患者,可考慮採用大分割照射模式,照射劑量與全乳大分割照射相同。
4.5.3.1.5 (5)部分乳腺照射:
數項研究提示,在低危乳腺癌保乳術後患者中,部分乳腺照射可能獲得與全乳照射相同的療效。目前鼓勵患者參加部分乳腺照射相關的臨牀試驗;除臨牀試驗外,接受部分乳腺照射的患者需要嚴格選擇,在有經驗的醫療中心結合自身的技術條件和患者意願有序開展,推薦適應證如下:
①年齡≥50 歲;
②浸潤性癌腫瘤大小≤3cm(T1、小T2),陰性切緣≥2 mm;
③單純低-中級別DCIS、篩查發現、腫瘤大小≤2. 5 cm、陰性切緣≥3mm;
⑤單中心病竈;
⑦無廣泛導管內癌成分;
⑧未接受新輔助化療;
部分乳腺照射可以通過術中放療、近距離插植或外照射進行。照射範圍爲乳腺瘤牀。推薦的照射劑量包括:術中放療20Gy,單次完成;近距離插植34Gy/3.4Gy/10f,每天2次,間隔至少6小時,總治療時間5天,或者其他等效生物分割劑量模式;外照射38.5Gy/10f,每天2次,5天完成。RAPID研究的隨訪結果提示,外照射這種分割方式進行部分乳腺放療的晚期美容效果相對較差,考慮到國內加速器相對不足的實際情況,也可採用38.5Gy/10f每天1次或40Gy/10f每天1次的照射模式。
4.5.3.2 2.改良根治術後放射治療
4.5.3.2.1 (1)適應證:
符合以下任一條件的改良根治術後患者,應考慮給予術後輔助放療:①原發腫瘤最大直徑>5cm,或腫瘤侵及乳腺皮膚、胸壁。②腋窩淋巴結轉移≥4個,或存在鎖骨上或內乳淋巴結轉移。③原發腫瘤分期T1~2且腋窩淋巴結轉移1~3個的患者,推薦在改良根治術後接受放射治療。但對其中的無明顯高危復發因素,即年齡≥50歲、腫瘤分級Ⅰ~Ⅱ級、無脈管瘤栓、腋窩淋巴結轉移數1個、激素受體陽性的患者,可考慮省略放療。④對改良根治術前接受新輔助化療的患者,術後放療指證參見“三、1. 新輔助化療後術後放射治療”章節。
4.5.3.2.2 (2)照射範圍:
1)需要接受改良根治術後放療的患者,照射範圍應包括胸壁及鎖骨上下區。
2)內乳照射目前存在爭議,推薦具備下列條件患者考慮行內乳照射:
①腋窩淋巴結清掃術後淋巴結轉移≥4個;②原發腫瘤位於內象限或中央區且伴有腋窩淋巴結轉移;
④初診時影像學診斷內乳淋巴結轉移或經病理證實內乳淋巴結轉移但未行內乳淋巴結清掃。
內乳照射建議應用現代精準放療技術,以便準確評估心臟等正常組織照射劑量,同時把握全身治療及放療對心臟相關損傷與內乳預防照射的獲益與風險,必要時多學科充分溝通,或鼓勵患者參加臨牀試驗。
3)對腋窩淋巴結清掃徹底的患者,放療靶區不推薦包括患側腋窩;對SLNB後發現淋巴結轉移,但未行腋窩清掃或腋窩清掃不徹底的患者,放療靶區應考慮包括腋窩。
4.5.3.2.3 (3)照射技術:
改良根治術後放療可以通過二維照射、三維適形放療、固定野或旋轉調強等照射技術進行。無論採取何種技術,均推薦採用CT定位並勾畫靶區及危及器官,將CT圖像導入三維計劃治療系統上進行個體化計劃評估,以準確評估靶區及危及器官的劑量分佈。同時,無論採取何種照射技術,應注意在胸壁表面增加組織補償物(40%~60%照射劑量),以確保足夠的皮膚劑量。可參照傳統二維照射方式設計照射野,如:鎖骨上照射可採用單前野或前後對穿野照射,內乳淋巴引流區可採用電子線野照射,但要求鎖骨上、內乳區90%的靶體積應達到90%的照射劑量。胸壁可採用切線野或電子線野照射,採用電子線照射時,照射範圍可參照傳統二維布野方式,包全手術疤痕和遊離皮瓣範圍。
與二維放療相比,三維適形及調強放療有助於保證靶區達到處方劑量、改善靶區內的劑量均勻性,降低正常組織的受照劑量,更好的處理胸壁與區域淋巴結照射野的銜接,個體化地治療患者,但增加了計劃設計的複雜程度。推薦根據患者的病情、照射範圍及合併症情況等個體化的選擇照射技術。採用適形調強放療時,應準確勾畫靶區,確保心肺安全,不顯著增加其他正常器官,如甲狀腺、健側乳腺、患側肩關節等的受照劑量。
4.5.3.2.4 (4)照射劑量及分割模式:
推薦的改良根治術後的射劑量爲50Gy/2Gy/25f。在有經驗的單位,可考慮給予大分割放療40~43.5Gy/15f/3w。
4.5.3.2.5 (5)放射治療與全身治療的時序安排:
對於有輔助化療指徵的患者,術後放射治療應該在完成輔助化療後開展;如果無輔助化療指徵,在切口癒合良好的前提下,術後8周內開始放射治療。輔助赫塞汀治療可以和術後放射治療同期開展。放射治療開始前,要確認左心室射血分數(left
ventricular ejection fraction,LVEF)大於50%,同時儘可能降低心臟的照射劑量,尤其是患側爲左側。輔助內分泌治療可以與術後放射治療同期開展。
4.5.3.3 3.特殊情況下的放射治療
4.5.3.3.1 (1)新輔助化療後術後放射治療:
1)新輔助化療後保乳術後放療:對於接受新輔助化療降期後行保乳手術的患者,無論治療反應如何,均應行術後全乳+瘤牀補量放療。瘤牀靶區一般根據新輔助化療後保乳手術的實際切除範圍來確定,必要時也應參考化療前臨牀分期及術後病理分期確定(關鍵是手術前對原發腫瘤退縮情況和方式的準確評估,以及陰性切緣的保障)。新輔助化療術後病理淋巴結陽性的所有患者或新輔助化療前初始臨牀分期爲Ⅲ期的患者,術後常規行全乳聯合淋巴引流區照射。對於初始分期Ⅱ期區域淋巴結陽性的cN 1 期患者,在新輔助化療後達 ypN 0 期者,原則上仍需行術後全乳聯合淋巴引流區照射;臨牀實踐中也可以選取一些低危患者予以謹慎地個體化免除 淋巴引流區照射,如原發竈和腋窩淋巴結新輔助化療後均達 pCR,年齡>40 歲,不合並相關病理危險因素(如組織學 3 級、脈管癌栓、激素受體陰性等)。新輔助化療後保乳術後的預防放療劑量,參照前述無新輔助化療情況。
2)新輔助化療後改良根治術後放療:新輔助化療後的輔助放療決策尚無Ⅲ期隨機對照臨牀試驗結果可以參考,目前推薦爲結合患者新輔助治療前的臨牀分期和新輔助化療後的病理分期,結合患者、腫瘤特徵,進行放療決策。放療指徵如下:
①新輔助化療前初始分期爲Ⅲ期及新輔助後腋窩淋巴結陽性的患者,推薦術後放療;
②初始臨牀分期爲Ⅱ期(cN 1 期),新輔助化療後術後病理腋窩淋巴結陰性,是否行術後放療存在爭議,鼓勵患者參加臨牀研究。
臨牀上可選擇有高危因素患者行術後放療:年齡≤40 歲、ypT>2cm、脈管瘤栓陽性、預後不良的分子亞型(激素受體陰性、HER2陽性且未行靶向治療)等。
新輔助化療後放療的照射範圍、劑量及分割模式和未接受新輔助治療的改良根治術後放療基本相同。初診局部晚期乳腺癌(Locally Advanced Breast Cancer, LABC)新輔助化療後術後放療時需要注意,明顯皮膚受侵或診斷爲炎性乳癌的LABC,可以考慮在全胸壁照射50 Gy分25次後,對遊離皮瓣範圍的胸壁給予補量照射10~16 Gy;放療時可增加皮膚表面填充物的使用次數,保證皮膚劑量充分。初診時有鎖骨上或內乳淋巴結轉移的患者,在局部區域預防照射後應對原鎖骨上或內乳淋巴結轉移部位加量照射。如果化療後鎖骨上或內乳淋巴結達到完全緩解,加量10Gy分5次;如果化療後鎖骨上或內乳淋巴結仍有殘存,加量16~20Gy分8~10次。要求患者初診基線評估時行 CT 檢查明確最初的淋巴結轉移部位,並穿刺明確病理學診斷,爲後續放療確定補量照射範圍提供參考。
4.5.3.3.2 (2)乳腺重建術後放射治療:
全乳切除術後乳房重建患者的放療指徵與相同分期、未做重建的患者一樣,但在決策時需要額外權衡重建植入物的放療併發症風險以及重建對放療技術的挑戰。自體重建組織可以很好地耐受放療,放療未增加自體重建患者的併發症風險。由於放療後可能會導致自體植入物組織萎縮,可以在手術時將重建乳房體積設計略大於對側乳腺。假體重建的使用逐年上升,放療增加假體包膜攣縮風險,降低美容效果。分階段重建時,放療介入時機可以在永久假體植入之前或之後。在永久假體植入之前放療,直接照射組織擴張器,對後續的假體包膜攣縮影響小,但重建失敗率增高。在永久假體植入之後放療,重建失敗率低,但包膜攣縮併發症增加。此外,放療介入時機的選擇還需要考量因植入永久假體手術而導致的放療延遲對腫瘤療效影響,對復發高危患者最好不要過長延遲放療。在永久假體植入之前放療的患者,爲提高重建成功率,放療定位前需要完成擴張器注水程序保證充分的組織擴張,直到放療結束都不允許往擴張器內注入或者抽出鹽水,以保證靶區的體積和位置始終一致。放療需要照射同側胸壁+區域淋巴引流區,淋巴引流區照射原則同未做重建的患者。放療劑量採用常規分割50 Gy分25次,5周完成。傳統的根治術將會有5%~10%的腺體殘留,皮下組織內豐富的淋巴管網是腫瘤轉移至腋窩或內乳淋巴結的重要途徑,這些均是重建術後胸壁放療的重要靶區。因爲位置表淺,部分靶區位於劑量建成區,放療計劃設計時特別注意,在有擺位誤差的情況下,照射野包全靶區。根據所使用放療技術的建成區範圍,推薦在胸壁皮膚表面墊組織填充物照射 10~15 次,以保證靶區劑量充分。
4.5.3.3.3 (3)局部區域復發後的放射治療:
胸壁和鎖骨上淋巴引流區是乳腺癌根治術或改良根治術後復發最常見的部位。胸壁單個復發原則上手術切除腫瘤後進行放射治療;若手術無法切除,應先進行放射治療。既往未做過放射治療的患者,放射治療範圍應包括全部胸壁和鎖骨上/下區域。鎖骨上覆發的患者如既往未進行術後放射治療,照射靶區需包括患側全胸壁及鎖骨上淋巴引流區。如腋窩或內乳淋巴結無復發,無需預防性照射腋窩和內乳區。預防部位的放射治療劑量爲DT45~50 Gy/25f/5w,復發部位縮野補量至DT 60~66Gy/30~33f/6~6.5w。既往做過放射治療的復發患者,需要參考腫瘤復發間隔時間、首程放療的劑量範圍和不良反應程度,以及再程放療的可能療效和不良反應,來決定是否進行再程放療。再程放療時,僅照射覆發腫瘤部位,不推薦大範圍預防照射。局部區域復發患者在治療前需取得復發竈的細胞學或組織學診斷。
4.5.4 (四)化療。
4.5.4.1 1.乳腺癌輔助化療
對患者基本情況(年齡、月經狀況、血常規、重要器官功能、有無其他疾病等)、腫瘤特點(病理類型、分化程度、淋巴結狀態、HER2及激素受體狀況、有無脈管瘤栓等)、治療手段(如化療、內分泌治療、靶向藥物治療等)進行綜合分析,醫師根據治療的耐受性、術後復發風險、腫瘤分子分型和治療敏感性選擇相應治療,並權衡治療給患者帶來的風險-受益,若接受化療的患者受益有可能大於風險,可進行術後輔助化療。乳腺癌術後復發風險的分層見附件8;乳腺癌分子分型的判定見附件9。
4.5.4.1.1 (1)適應證:
②對淋巴結轉移數目較少(1~3個)的絕經後患者,如果具有受體陽性、HER2陰性、腫瘤較小、腫瘤分級Ⅰ級等其他多項預後較好的因素,或者患者無法耐受或不適合化療,也可考慮單用內分泌治療。
③對淋巴結陰性乳腺癌,術後輔助化療只適用於那些具有高危復發風險因素的患者(患者年齡<35歲、腫瘤直徑>2cm、腫瘤分級Ⅱ~Ⅲ級、脈管瘤栓、HER2陽性、ER/PR陰性等)。
4.5.4.1.2 (2)相對禁忌證:
①妊娠期:妊娠早期患者通常禁用化療,妊娠中期患者應慎重選擇化療。
②明顯衰竭或惡病質。
③患者拒絕術後輔助化療。
⑥骨髓儲備功能低下,治療前白細胞≤3.5×109/L,血小板≤80×109/L者。
4.5.4.1.3 (3)輔助化療方案的選擇:
常用的輔助化療方案見附件10)。
1)常用方案:①以蒽環類爲主的方案,如AC(多柔比星/環磷酰胺),EC(表柔比星/環磷酰胺)。雖然吡柔比星(THP)循證醫學證據有限,但在我國臨牀實踐中,用吡柔比星代替多柔比星也是可行的,THP推薦劑量爲40~50mg/m2。
②蒽環類與紫杉類聯合方案,例如TAC(T:多西他賽)。
③蒽環類與紫杉類序貫方案,例如AC→紫杉醇(每週1次),AC→多西他賽(每3周1次),劑量密集型AC續貫紫杉醇(每2周1次),劑量密集型AC續貫紫杉醇(每週1次)。
④不含蒽環類的聯合化療方案:TC方案(多西他賽/環磷酰胺4或6個療程),適用於有一定復發風險的患者。
2)HER2陽性乳腺癌:常用方案參見乳腺癌術後輔助抗HER2靶向治療部分中的相應內容。
4.5.4.1.4 (4)注意事項:
①早期乳腺癌輔助化療的目的是爭取治癒,所以強調標準、規範的化療。
②化療時應注意化療藥物的給藥順序、輸注時間和劑量強度,嚴格按照藥品說明和配伍禁忌使用。
③根據患者的復發風險、耐受程度、患者意願及循證醫學證據選擇化療方案,並制定預防嘔吐、骨髓抑制的支持方案。
④不同化療方案的週期數不同,一般爲4~8個週期。若無特殊情況,不建議減少週期數和劑量。70歲以上患者需個體化考慮輔助化療。
⑤輔助化療一般不與內分泌治療或放療同時進行,化療結束後再開始內分泌治療,放療與內分泌治療可先後或同時進行。
⑥一般推薦首次給藥劑量應按推薦劑量使用,若有特殊情況需調整時,通常不低於推薦劑量的85%,後續給藥劑量應根據患者的具體情況和初始治療後的不良反應,可以1次下調20%~25%。每個輔助化療方案一般僅允許劑量下調2次。
⑦激素受體陰性的絕經前患者,在輔助化療期間可考慮使用卵巢功能抑制藥物保護患者的卵巢功能。推薦化療前1~2周給藥,化療結束後2周給予最後一劑藥物。
⑧蒽環類藥物有心臟毒性,使用時須評估LVEF,一般每3個月1次。
4.5.4.2 2.新輔助化療
新輔助化療是指爲降低腫瘤臨牀分期,提高切除率和保乳率,在手術或手術加局部放射治療前,首先進行全身化療。
4.5.4.2.1 (1)適應證:
①不可手術降期爲可手術,臨牀分期爲ⅢA(不含T3、N1、M0)、ⅢB、ⅢC。
②期望降期保乳患者,臨牀分期爲ⅡA、ⅡB、ⅢA(僅T3、N1、M0)期,除了腫瘤大小以外,符合保乳手術的其他適應證。對希望縮小腫塊、降期保乳的患者,也可考慮新輔助治療。
③對不可手術的隱匿性乳腺癌行新輔助治療是可行的(其中隱匿性乳腺癌定義爲腋窩淋巴結轉移爲首發症狀,而乳房內未能找到原發竈的乳腺癌)。
4.5.4.2.2 (2)禁忌證:
①未經組織病理學確診的乳腺癌:推薦進行組織病理學診斷,並獲得ER、PR、HER2及Ki-67等免疫組化指標,不推薦將細胞學作爲病理診斷標準。
②妊娠早期女性爲絕對禁忌:而妊娠中、晚期女性患者應慎重選擇新輔助化療,爲相對禁忌,國外有成功應用的個案報道。
④原發腫瘤爲廣泛原位癌成分,未能明確浸潤癌存在者需謹慎使用。
⑥患者拒絕術前新輔助治療。
⑧骨髓儲備不足,治療前中性粒細胞≤1.5×109/L,血小板≤75×109/L者。
4.5.4.2.3 (3)新輔助化療方案的選擇:
①對於HR陽性/HER2陰性的乳腺癌患者,有降期或保乳等需求的,優先推薦輔助化療提前到新輔助階段。
②對於HER2陽性和三陰性乳腺癌患者,可適當放寬新輔助治療適應證,通過新輔助治療早期評價治療療效,並通過術後是否病理完全緩解制定升/降階梯輔助治療。
③對於HER2陽性的乳腺癌患者,符合新輔助適應證的,應採用含蒽環聯合紫杉方案或非蒽環方案聯合曲妥珠單抗±帕妥珠單抗進行新輔助治療。加用帕妥珠單抗會進一步提高pCR率,在HR陰性、淋巴結陽性的患者獲益更多。
④對於三陰性乳腺癌患者,新輔助推薦含蒽環類和紫杉類的常規方案。鉑類可作爲三陰性患者新輔助治療方案的一部分,以增加腫瘤退縮的概率和pCR的可能性,但決策加鉑類應該權衡潛在的獲益與傷害,因爲未必轉化爲DFS的遠期獲益。
單純BRCA1/2致病或疑似致病性突變,不足以成爲選擇含鉑治療的理由。對於有心臟基礎疾患的患者,可以考慮單純紫杉類+鉑類的新輔助治療。PD-1/PD-L1抗體在國內尚未獲得相關適應證,遠期毒性和獲益未明,不常規推薦在該類患者新輔助治療中添加免疫檢查點抑制劑。
4.5.4.2.4 (4)注意事項:
①化療前必須對乳腺原發竈行空芯針活檢明確組織學診斷及免疫組化檢查,區域淋巴結轉移可以採用細胞學診斷。②明確病理組織學診斷後實施新輔助化療。
③不建議Ⅰ期患者選擇新輔助化療。
④在治療有反應或疾病穩定的患者中,推薦手術前用完所有的既定週期數。
⑤應從體檢和影像學2個方面評價乳腺原發竈和腋窩淋巴結轉移竈療效,按照實體腫瘤療效評估標準RECIST或WHO標準評價療效。
⑥無效時暫停該化療方案,改用手術、放射治療或者其他全身治療措施(更換化療方案或改行新輔助內分泌治療)。
⑦新輔助化療後,即便臨牀上腫瘤完全消失,也必須接受既定的後續手術治療,根據個體情況選擇乳腺癌根治術、乳腺癌改良根治術或保留乳房手術。
⑧術後輔助化療應根據術前新輔助化療的週期、療效及術後病理檢查結果確定治療方案。
⑨推薦根據化療前的腫瘤臨牀分期來決定是否需要輔助放療及放療範圍。
4.5.4.2.5 (5)全身處理:
對於新輔助化療未達到pCR的患者(已完成足療程的新輔助治療),尤其是三陰性乳腺癌患者,可考慮術後追加6~8個療程卡培他濱治療;HER2陽性患者,優先考慮採用T-DM1強化輔助治療的方式,也可採用繼續完成曲妥珠單抗聯合帕妥珠單抗共1年的方式。無論是否達到pCR,部分研究顯示特定人羣奈拉替尼延長治療1年可進一步降低復發風險。對於HR陽性的患者,需要給予內分泌治療,內分泌治療是否需要強化,以及強化的方式可主要依據患者新輔助前的狀態進行評估。
4.5.4.3 3.晚期乳腺癌化療
晚期乳腺癌的主要治療目的不是治癒患者,而是提高患者生活質量、延長患者生存時間。治療手段以化療和內分泌治療爲主,必要時考慮手術或放射治療等其他治療方式。根據原發腫瘤特點、既往治療、無病生存期、轉移部位、進展速度、患者狀態等多方面因素,因時制宜、因人制宜,選擇合適的綜合治療手段,個體化用藥。有轉移或復發表現的乳腺癌患者的分期評估檢查包括病史、體格檢查、實驗室檢查、胸部X線或CT、腹部超聲、骨顯像等。對疼痛或骨顯像異常患者行骨的放射學檢查,還可考慮腹部診斷性CT或MRI、頭顱CT或MRI。通常不建議使用PET-CT對患者進行評估,在其他檢查結果不確定或可疑時PET-CT是可選擇的。腫瘤轉移竈或第一復發竈的活檢應作爲晚期乳腺癌患者病情評估的一部分,同時檢測ER、PR、HER2、Ki-67等分子標誌物,以制訂針對性治療方案。
4.5.4.3.1 (1)符合下列某一條件的患者可考慮化療:
①ER/PR陰性或低表達。②內臟危象或有症狀的內臟轉移。③ER/PR陽性內分泌治療耐藥者(特別是原發性耐藥)。
4.5.4.3.2 (2)化療藥物與方案:
晚期乳腺癌常用化療方案見附件11。
晚期乳腺癌常用的化療藥物包括蒽環類、紫杉類、長春瑞濱、卡培他濱、吉西他濱、鉑類等。應根據疾病的範圍、腫瘤的分子特徵、既往治療及患者的特點來制訂個體化的化療方案。制訂方案時應充分考慮患者的意願,疾病的不可治癒性,平衡生活質量和生存期。在疾病發展的不同階段合理選擇單藥或聯合化療。
1)單藥化療:對腫瘤發展相對較慢,腫瘤負荷不大,無明顯症狀,特別是老年耐受性較差的患者優選單藥化療。蒽環類(紫杉類)治療失敗的常用定義爲使用蒽環類(紫杉類)解救化療過程中發生疾病進展,或輔助治療結束後12個月內發生復發轉移。對於既往蒽環類治療失敗的患者,通常首選以紫杉類(如紫杉醇、多西他賽及白蛋白結合紫杉醇)爲基礎的單藥或聯合方案;對於既往蒽環類和紫杉類治療均失敗的患者,目前尚無標準化療方案,可考慮其他單藥或聯合方案。
常用的單藥包括:蒽環類,如多柔比星、表柔比星、吡柔比星及聚乙二醇化脂質體多柔比星;紫杉類,如紫杉醇、多西他賽、白蛋白結合型紫杉醇;抗代謝藥如卡培他濱、吉西他濱等;非紫杉類微管形成抑制劑,如長春瑞濱、艾立布林、優替德隆等;依託泊苷膠囊、環磷酰胺片等口服方便,可以作爲後線治療的選擇。
2)聯合化療:適合病情進展較快,腫瘤負荷較大或症狀明顯的患者。聯合化療方案的選擇多種多樣,主要基於既往循證醫學的證據、聯合藥物之間的相互作用、聯合藥物的毒性譜、患者的個體狀態來綜合制定,不推薦聯合三種或三種以上的化療藥物。
①對於三陰性乳腺癌,可選擇GP方案(吉西他濱聯合順鉑)、GC方案(吉西他濱聯合卡鉑)、AP方案(白蛋白紫杉醇聯合順鉑/卡鉑)、PC方案(其他紫杉類藥物聯合卡鉑/順鉑)。
②單藥或聯合化療均可在循證證據支持下聯合靶向治療。
③聯合化療時,是採用持續方式還是4~8個療程後停藥或維持治療需權衡療效、藥物不良反應和患者生活質量。
④對多程化療失敗的患者無標準治療,鼓勵患者參加新藥臨牀試驗或對症支持治療。對於三陰性乳腺癌,sacituzumab govitecan是一種重要的靶向治療選擇,已獲得美國FDA批准,但尚在中國開展臨牀研究。
3)維持化療:對完成了4~6週期化療,治療有效、耐受性較好的患者,可以持續治療至病情進展或出現不能耐受的毒性。聯合化療有效但不能耐受或無意願繼續聯合化療者可考慮維持治療,可選擇原先聯合方案中的一個單藥化療維持,激素受體陽性者還可考慮內分泌±靶向治療維持。維持治療中應該加強患者管理,定期評估療效和不良反應。
4.5.5 (五)內分泌治療。
4.5.5.1 1.輔助內分泌治療
4.5.5.1.1 (1)適應證:
1)激素受體ER和/或PR陽性的浸潤性乳腺癌患者,皆應接受術後輔助內分泌治療。依據最新ASCO/CAP指南,儘管ER免疫組織化學染色爲1%~100%的腫瘤皆被視爲ER陽性,但ER免疫組織化學染色爲1%~10%爲ER低表達。ER低表達的生物學行爲通常與ER陰性乳腺癌相似,在術後輔助內分泌中的獲益較少,在做治療決策時也應當考慮到這一點。
2)原位癌患者如出現以下情況可考慮行5年內分泌治療:①保乳手術後需要放療患者,特別是其中激素受體陽性的DCIS;②僅行局部切除DCIS患者;③行乳腺全切患者,用於預防對側乳腺癌發生。
4.5.5.1.2 (2)禁忌證:
(3)藥物選擇:
②對於中高復發風險的絕經前患者(具體需綜合考量年齡、腫塊大小、淋巴結狀態、組織學分級、Ki-67增殖指數等,具體可參見《中國早期乳腺癌卵巢功能抑制臨牀應用專家共識(2018年版)》)推薦在輔助內分泌治療中應用卵巢抑制劑。對於年輕的(<35歲)的乳腺癌患者,更推薦卵巢功能抑制加芳香化酶抑制劑。他莫昔芬或芳香化酶抑制劑加卵巢切除或卵巢抑制治療5年。
③他莫昔芬治療期間,如果患者已經絕經,可以換用芳香化酶抑制劑。
4.5.5.1.3 (4)注意事項:
1)患者應在化療之前進行激素水平的測定,判斷月經狀態,絕經定義見附件12。
2)術後輔助內分泌治療的治療期限爲5年,延長內分泌治療需要根據患者的具體情況個體化處理,需要結合腫瘤復發的高危因素和患者的意願綜合決策;對於高危絕經前患者,若在他莫昔芬治療滿5年後患者仍未絕經,可以根據情況增加至10年,如果患者在治療過程中絕經,可考慮延長芳香化酶抑制劑治療,直至完成10年的內分泌治療。
3)輔助內分泌治療(促黃體素釋放激素激動劑除外)不建議與輔助化療同時使用,一般在化療之後使用,可以和放療及曲妥珠單抗治療同時使用
①在應用他莫昔芬過程中應注意避孕,需要對子宮內膜進行超聲監測,每6~12個月進行1次婦科檢查。
②對於應用芳香化酶抑制劑患者應監測骨密度和補充鈣劑及維生素D。對於嚴重骨質疏鬆患者可進行正規抗骨質疏鬆治療。
③患者在接受芳香化酶抑制劑治療期間應監測血脂,必要時應給予血脂異常患者相應的治療。對於在內分泌治療中嚴重的不良反應需要考慮停藥或者更換治療方案。
4.5.5.2 2.晚期乳腺癌的內分泌治療
4.5.5.2.1 (1)首選內分泌治療的適應證:
①患者年齡大於35歲。
②無病生存期大於2年(聯合部分靶向藥物時可適當突破該界限)。
⑤ER和/或PR陽性。
⑥受體不明或受體爲陰性的患者,如臨牀病程發展緩慢,也可以試用內分泌治療。
4.5.5.2.2 (2)藥物選擇:
1)絕經後患者的內分泌治療推薦:芳香化酶抑制劑包括非甾體類(阿那曲唑和來曲唑)、甾體類(依西美坦)、ER調變劑(他莫昔芬和託瑞米芬)、ER下調劑(氟維司羣)、孕酮類藥物(甲地孕酮)、雄激素(氟甲睾酮)及大劑量雌激素(乙炔基雌二醇)。
2)絕經前患者內分泌治療推薦:在卵巢功能抑制基礎上(主要是使用促黃體素釋放激素激動劑和手術去勢),可參照絕經後乳腺癌處理。未行卵巢功能抑制的,可考慮ER調變劑(他莫昔芬和託瑞米芬)、孕酮類藥物(甲地孕酮)、雄激素(氟甲睾酮)及大劑量雌激素(乙炔基雌二醇)。
3)絕經前和絕經後患者均可考慮在內分泌治療的基礎上聯合靶向治療(CDK4/6抑制劑、HDAC抑制劑等)。
4.5.5.2.3 (3)晚期乳腺癌一線內分泌治療的選擇:
1)芳香化酶抑制劑聯合CDK4/6抑制劑(哌柏西利、阿貝西利)是HR陽性/HER2陰性絕經後(自然絕經或手術去勢)或絕經前但經藥物去勢後乳腺癌患者一線內分泌治療的優先選擇。
2)當CDK4/6抑制劑不可及時,單藥內分泌治療也是可行的;絕經後(自然絕經或手術去勢)患者可使用氟維司羣、芳香化酶抑制劑(Aromatase Inhibitor, AI)、雌激素受體(Estrogen Receptor, ER)調變劑(他莫昔芬和託瑞米芬);絕經前患者可使用卵巢功能抑制(Ovarian FunctionSuppression, OFS)聯合氟維司羣、OFS聯合AI、OFS聯合ER調變劑、單純ER調變劑。
3)絕經前患者在使用卵巢功能抑制劑後,可按照絕經後模式處理。
4.5.5.2.4 (4)晚期乳腺癌二線內分泌治療的選擇:
一線內分泌治療失敗後,非內臟危象的患者仍然可以選擇二線內分泌治療±靶向治療。不推薦重複使用輔助治療或一線治療已被證明耐藥的內分泌藥物。
1)對於尚未使用過CDK4/6抑制劑的患者:①氟維司羣聯合CDK4/6抑制劑(哌柏西利、阿貝西利)是HR陽性/HER2陰性絕經後(自然絕經或手術去勢)或絕經前但經藥物去勢後乳腺癌患者二線內分泌治療的優先選擇。②甾體/非甾體芳香化酶抑制劑(±OFS)或他莫昔芬(±OFS)聯合CDK4/6抑制劑亦可選用。對於已經使用過CDK4/6抑制劑的患者,目前並無充分證據支持CDK4/6抑制劑的跨線治療。2)當以上聯合的小分子靶向藥物不可及時,單藥內分泌治療也是可行的;絕經後(自然絕經或手術去勢)患者可使用氟維司羣、AI、ER調變劑(他莫昔芬和託瑞米芬);絕經前患者可使用OFS聯合氟維司羣、OFS聯合AI、OFS聯合ER調變劑、單純ER調變劑。
(3)注意事項:
①連續兩線內分泌治療後腫瘤進展,通常提示內分泌治療耐藥,應該換用細胞毒藥物治療或進入臨牀試驗研究。
②在內分泌治療期間,應每2~3個月評估1次療效,對達到治療有效或疾病穩定患者應繼續給予原內分泌藥物維持治療,如腫瘤出現進展,應根據病情決定更換其他機制的內分泌治療藥物或改用化療等其他治療手段。
4.5.6 (六)靶向治療。
目前,針對HER2陽性的乳腺癌患者可進行靶向治療,國內主要藥物是曲妥珠單抗、帕妥珠單抗、吡咯替尼、T-DM1、拉帕替尼等。
4.5.6.1 1. HER2陽性的定義
(1)HER2基因擴增:免疫組化染色3+、FISH陽性或者色素原位雜交法(CISH)陽性。
(2)HER2免疫組化染色(2+)的患者,需進一步行FISH或CISH檢測HER2基因是否擴增。
4.5.6.2 ⒉ 注意事項
(1)治療前必須獲得HER2陽性的病理學證據。
(2)曲妥珠單克隆抗體6mg/kg(首劑8mg/kg)每3周方案,或2mg/kg(首劑4mg/kg)每週方案。
(3)首次治療後觀察4~8個小時。
(4)一般不與阿黴素化療同期使用,但可以序貫使用。
(5)與非蒽環類化療、內分泌治療及放射治療可同期應用。
(6)曲妥珠單克隆抗體開始治療前應檢測LVEF,使用期間每3個月監測1次LVEF。治療中若出現LVEF<45%或低於治療前16%以上,應暫停治療,並跟蹤監測LVEF動態變化,直至恢復到45%以上方可繼續用藥。若不恢復,或繼續惡化或出現心力衰竭症狀則應當終止曲妥珠單抗治療。
4.5.6.3 3.術後輔助靶向治療
4.5.6.3.1 (1)適應證:
①原發浸潤竈>1cm(T1c及以上)的HER2陽性乳腺癌患者推薦使用曲妥珠單抗。
②原發浸潤竈在0.6-1cm的HER2陽性淋巴結陰性乳腺癌患者(T1bN0)及腫瘤更小、但腋窩淋巴結有微轉移的患者(pN1mi)可推薦使用曲妥珠單抗。
③原發浸潤竈<0.5cm(T1a)的HER2陽性淋巴結陰性乳腺癌患者一般不推薦使用曲妥珠單抗,但伴有高危因素的患者,例如激素受體陰性、分級較高、Ki-67高等可以考慮使用。
4.5.6.3.2 (2)相對禁忌證:
①治療前LVEF<40%。
②患者拒絕術後輔助靶向治療。
4.5.6.3.3 (3)治療方案選擇:
常用治療方案見附件13。
①可選擇TCH(P)、AC-TH(P)方案,對於心臟安全要求較高的患者可選擇TCH、TC4H(此處C爲CTX)和wPH治療方案;對於高危復發風險患者(如淋巴結陽性)的患者,推薦曲妥珠單抗與帕妥珠單抗雙靶向治療聯合輔助化療,其中帕妥珠單抗,3周1次,劑量爲420 mg(首次劑量爲840mg),共1年;如ER+,亦可考慮在曲妥珠單抗治療結束後,給予1年的奈拉替尼強化。
②小腫瘤患者(腫瘤直徑≤1cm)患者可以選擇紫杉醇周療加曲妥珠單抗(wPH)方案治療。
4.5.6.3.4 (4)注意事項:
①與蒽環類藥物同期應用必須慎重,但可以在前、後階段序貫應用。與非蒽環類藥物化療、內分泌治療或放療都可同期應用。
②目前曲妥珠單克隆抗體輔助治療期限仍爲1年。
4.5.6.4 4.術前新輔助靶向治療
HER2陽性乳腺癌對抗HER2靶向治療敏感性高,在這部分患者的新輔助治療方案中應包含抗HER2靶向治療。
4.5.6.4.1 (1)新輔助靶向治療藥物的選擇與原則:
①曲妥珠單抗、帕妥珠單抗雙靶向是目前新輔助靶向治療的首選治療策略。②對於HER2陽性的乳腺癌患者,符合新輔助適應證的,應採用含蒽環聯合紫杉方案或非蒽環方案聯合曲妥珠單抗±帕妥珠單抗進行新輔助治療。③在新輔助靶向治療中加入帕妥珠單抗可以進一步提高病理完全緩解率,在HR陰性、淋巴結陽性的患者獲益更多。④有蒽環類藥物使用禁忌、高齡或其他心臟疾病隱患的患者可以使用不含蒽環方案如TCH(P)方案。
4.5.6.4.2 (2)注意事項:
①新輔助治療期間應嚴密監測療效,按照RECIST或WHO標準評價原發竈和/或淋巴結的療效,應用曲妥珠單抗治療期間進展的患者在後續新輔助治療中可考慮保留曲妥珠單抗。②接受新輔助靶向治療的患者輔助階段應補足輔助曲妥珠單抗±帕妥珠單抗治療至1年。③對未達到pCR的HER2陽性患者,優先考慮採用T-DM1強化輔助治療的方式,也可採用繼續完成曲妥珠單抗聯合帕妥珠單抗共1年的方式。無論是否達到pCR,部分研究顯示特定人羣奈拉替尼延長治療1年可進一步降低復發風險。④單獨新輔助靶向治療或與內分泌治療聯用尚缺乏足夠的證據,應用應限制於臨牀研究。
4.5.6.5 5.晚期HER2陽性乳腺癌的靶向治療選擇(常用治療方案見附件14)
持續的抗HER2治療是HER2陽性晚期乳腺癌重要的治療原則。
4.5.6.5.1 (1)HER2陽性晚期腫瘤的一線治療選擇:
1)首選曲妥珠單抗、帕妥珠單抗雙靶向治療聯合紫杉類藥物。其他可選方案包括曲妥珠單抗單靶聯合紫杉類藥物,曲妥珠單抗也可聯合長春瑞濱、卡培他濱等其他化療藥物。
2)對於未使用過曲妥珠單抗或符合曲妥珠單抗再使用條件(曲妥珠單抗輔助治療結束後超過1年以上覆發轉移的)的患者,應首選以曲妥珠單抗±帕妥珠單抗爲基礎的一線治療。而停用曲妥珠單抗至復發間隔時間≤6-12個月患者則建議選用二線抗HER2方案治療。
3)對於HER2陽性/HR陽性的患者,如不適合化療或病情進展緩慢者可以考慮抗HER2治療聯合內分泌藥物作爲一線治療選擇。
4.5.6.5.2 (2)經曲妥珠單抗±帕妥珠單抗治療後疾病進展的治療選擇:
1)曲妥珠單抗治療病情進展後,仍應持續使用抗HER2靶向治療。
2)當一線治療後病情進展時可選擇以下治療策略:
①對於曲妥珠單抗±帕妥珠單抗治療失敗患者,單藥恩美曲妥珠單抗(trastuzumab emtansine,T-DM1)可延長無進展生存時間和總生存時間。
②吡咯替尼聯合卡培他濱較拉帕替尼聯合卡培他濱可延長無進展生存時間。
③其他抗HER2靶向藥物:伊尼妥單抗聯合長春瑞濱等化療也可作爲曲妥珠單抗非耐藥患者的抗HER2治療選擇之一。單純兩種靶向藥物的聯合(如拉帕替尼聯合曲妥珠單抗)也有證據改善OS。
④曲妥珠單抗允許進行跨線治療。
⑤多線抗HER2治療失敗,無法獲得進一步治療的,建議參加臨牀研究。
4.5.6.5.3 (3)注意事項:
①曲妥珠單抗、帕妥珠單抗:治療前LVEF<50%。應用前應進行心功能基線評估,對於心血管事件高危人羣應儘量避免使用。
②同時進行蒽環類藥物化療。應儘量避免同時使用蒽環類等具有協同損害效應的藥物。
③治療過程中應定期進行心功能評估,若LVEF較基線下降≥15%或低於正常範圍且下降≥10%,應暫停抗HER2治療,於3~4周內複查LVEF,再次評估是否能繼續抗HER2治療。
④T-DM1:基線及用藥期間應行血小板規範監測,若出現血小板減少應及時減量或停藥。出現2級及以上血小板減少時應警惕發展爲持續性血小板減少症的可能,若常規升血小板治療效果不佳,應及時請專科醫師會診並處理。
⑤吡咯替尼:用藥前應針對腹瀉等不良反應及管理方案進行患者教育,用藥期間應對腹瀉進行監測和管理。
4.5.7 (七)中醫治療。
中醫藥有助於減輕放療、化療、內分泌治療的副作用和不良反應,調節患者免疫功能和體質狀況,改善癌症相關症狀和生活質量,可能延長生存期,可以作爲乳腺癌治療的重要輔助手段。
內傷情志、痰瘀互結、正氣虧虛是乳腺癌的主要病因、病機,疏肝解鬱、化痰散瘀、調補氣血、滋補肝腎是相應主要治法。在辯證論治法則基礎上,採用中藥湯劑治療是中醫治療的主要方式。此外,秉承中醫外科治療思想,以“陰證”“陽證”論治乳腺癌是臨牀常用方法。小金丸和西黃丸是治療乳腺癌“陰證”“陽證”的代表性中成藥,臨牀中得到廣泛應用。在中醫師指導下正確使用中成藥,患者的安全性和耐受性均較好。
4.6 六、診療流程
4.6.1 (一)診斷流程。
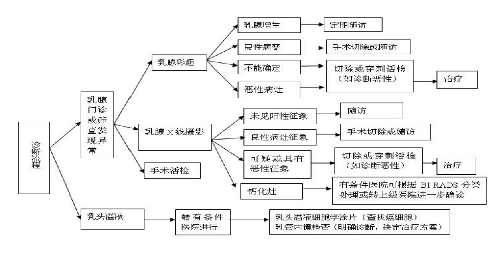
4.6.2 (二)治療流程。
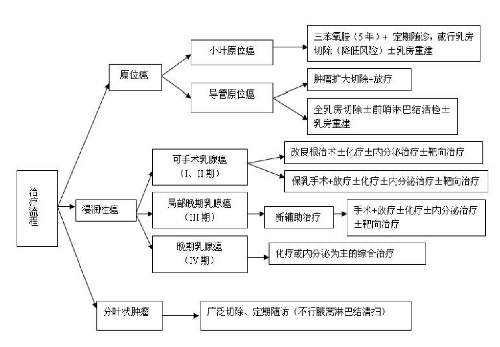
4.7 七、隨訪
(一)臨牀體檢:最初 2 年每4~6 個月1 次,其後3年每 6 個月 1 次,5 年後每年1 次。
(二)乳腺超聲:每6個月1次。
(三)乳腺X線攝影:每年1次。
(四)X線胸片或胸部CT:每年1次。
(五)腹部超聲:每6個月1次,3年後改爲每年1次。
(六)存在腋窩淋巴結轉移4個以上等高危因素的患者,行基線骨顯像檢查,全身骨顯像每年1次,5年後可改爲每2年1次。
5 附件
1.乳腺影像學診斷報告基本指南
4.乳腺癌的pTNM分期(AJCC 第8版)
5.乳腺癌病理報告內容及基本格式
6.乳腺癌HER2/neu FISH檢測報告基本格式
10.常用的輔助化療方案
11.晚期乳腺癌常用化療方案
12.絕經的定義
13.術後輔助靶向治療常用治療方案
14.晚期HER2陽性乳腺癌的靶向治療常用治療方案
15.乳腺癌診療指南(2022年版)編寫審定專家組
5.1 附件1乳腺影像學診斷報告基本指南
5.1.1 一、X線部分
報告內容包括以下5方面:檢查適應證;攝影技術指南;乳腺腺體構成成分的簡要描述;重要徵象的清晰描述;與既往片比較;評估類別及處理。
5.1.1.1 (一)檢查適應證。
無症狀篩查;乳腺疾病X線診斷;乳腺癌家族史;乳腺疾病病史;臨牀發現乳腺腫塊、異常乳頭溢液、皮膚異常、局部增厚、腫脹、疼痛;其他相關檢查發現乳腺異常;40歲以上女性(尤其是高齡生育或未生育女性)每2年至少進行一次乳腺X線攝影;月經初潮年齡在12歲前、絕經年齡超過55歲及其他乳腺癌高危人羣篩查起始年齡可適當提前。
5.1.1.2 (二)攝影技術。
常規投照體位包括雙側內外側斜位及頭尾位。對常規體位顯示不佳或未包全乳腺實質者,可根據病竈位置選擇補充體位,包括外內側位、內外側位、內側頭足軸位、外側頭足軸位、尾葉位、乳溝位。爲使病竈顯示效果更佳,必要時可開展一些特殊攝影技術,如局部加壓攝影、放大攝影或局部加壓放大攝影等。
5.1.1.3 (三)乳腺腺體構成成分簡要描述。
主要根據乳腺構成的纖維腺體組織密度高低和分佈範圍分爲4種類型:A型,脂肪型;B型,散在纖維腺體型;C型,不均勻緻密型;D型,極度緻密型。
5.1.1.4 (四)病變定位。
1.定側:左側、右側或雙側。2.部位:包括象限定位或鐘面定位。象限定位:外上象限、外下象限、內上象限、內下象限。乳暈後區、中央區、腋尾區不要求鐘面定位和深度定位。3.深度:根據與胸壁平行分成3等份,前1/3(前部)、中1/3(中部)、後1/3區(後部)。4.距離乳頭的距離。
5.1.1.5 (五)重要徵象的清晰描述。
採用乳腺X線專業詞彙對病竈進行描述。
5.1.1.5.1 1.腫塊
大小、形狀(圓形、卵圓形、不規則形)、邊緣(清楚、遮蔽、小分葉、模糊、星芒狀)、密度(高密度、等密度、低密度不含脂肪、含脂肪密度)、伴隨鈣化、其他伴隨徵象
5.1.1.5.2 2.鈣化
類型和分佈。
(1)類型包括:
①良性鈣化:皮膚鈣化、血管鈣化、粗糙或爆米花樣鈣化、粗棒狀鈣化、圓形鈣化、點狀鈣化、環形鈣化、鈣乳鈣化、縫線鈣化、營養不良性鈣化。
②可疑鈣化:不定形鈣化(BI-RADS 4B)、粗糙不均質鈣化(BI-RADS4B)、細小多形性鈣化(BI-RADS 4B)、細線樣或細線分支狀鈣化(BI-RADS 4C)。
(2)分佈:散在分佈(多爲良性)、區域分佈、集羣分佈、線樣分佈(可疑)、段樣分佈(可疑)。
5.1.1.5.3 3.結構扭曲
5.1.1.5.4 4.不對稱緻密
球形不對稱(多爲正常變異)、局竈性不對稱、進展性不對稱(可疑)
5.1.1.5.5 5.其他重要徵象
皮膚凹陷,乳頭回縮凹陷,皮膚增厚,小梁結構增粗,腋窩淋巴結增大,結構扭曲,鈣化等。
5.1.1.6 (六)與既往片比較。
5.1.1.6.1 (七)評估分類及處理建議:
1.評估不完全BI-RADS 0:現有影像未能完成評估,需要結合既往片或補充其他影像檢查,推薦其他的影像學檢查包括:局部加壓攝影、放大攝影、加壓放大攝影、特殊投照體位,或行超聲等檢查。
2.評估完全BI-RADS 1:陰性,乳腺X線攝片無異常發現,惡性可能性0,建議常規隨診。
BI-RADS 2:良性發現,存在明確的良性改變,無惡性徵象,惡性可能性0,建議常規隨診。包括鈣化的纖維腺瘤、皮膚鈣化、多發的分泌性鈣化、含脂肪的病變(脂性囊腫、脂肪瘤及混合密度的錯構瘤)、乳腺內淋巴結、血管鈣化、植入體、有手術史的結構扭曲等。
BI-RADS 3:良性可能大,惡性可能性0~2%,建議短期隨訪。期望此病變在短期(小於1年,一般爲6個月)隨訪中穩定或縮小來證實判斷。觸診陰性的無鈣化邊界清楚的腫塊、局竈性不對稱、孤立集羣分佈的點狀鈣化這三種徵象被歸於此類。常規處理意見:對病側乳腺進行X線攝影複查(一般爲6個月),第12個月與24個月時對雙側乳腺進行X線攝影複查,如果病竈保持穩定2~3年,則將原先的3類判讀爲2類。如果隨訪後病竈消失或縮小,則改判斷爲2類或1類;若病竈有進展,應考慮活檢。
BI-RADS 4:可疑異常,但不具備典型的惡性徵象,惡性可能性2%~95%,應考慮活檢。這一類包括了一大類需臨牀干預的病變,缺乏特徵性的乳腺癌形態學改變,但有惡性的可能性。再繼分成4A、4B、4C,臨牀醫師和患者可根據其不同的惡性可能性對病變的處理做出最後決定。
BI-RADS 4A:惡性可能性2%~10%。對活檢或細胞學檢查爲良性的結果比較可以信賴,可以常規隨訪或6個月後隨訪。可捫及的部分邊緣清晰的實性腫塊,如超聲提示的纖維腺瘤、可捫及的複雜囊腫或可捫及的膿腫均歸於此類。
BI-RADS 4B:惡性可能性10%~50%。需要對病理結果和影像表現嚴格對照,良性病理結果的決策取決於影像和病理的一致性。對邊界部分清晰、部分浸潤的腫塊穿刺爲纖維腺瘤或脂肪壞死的可以接受,並予隨訪。而對穿刺結果爲乳頭狀瘤或不典型增生的則需要進一步切取活檢。
BI-RADS 4C:惡性可能性50%~95%。形態不規則、邊緣浸潤的實性腫塊或新出現的簇狀分佈的細小多形性鈣化可歸於此類。此類病變往往爲惡性,對於病理結果爲良性的病例,需要與病理科協商,進一步分析。
BI-RADS 5:高度懷疑惡性,惡性可能性≥95%。有典型乳腺癌的影像學特徵,臨牀應採取適當措施。形態不規則、星芒狀邊緣的高密度腫塊、段樣或線樣分佈的細線狀和分支狀鈣化、不規則星芒狀腫塊伴多形性鈣化均歸於此類。
BI-RADS 6:已活檢證實爲惡性,臨牀應採取積極的治療措施。這一分類用於活檢已證實爲惡性但還未進行治療的影像評價。主要是評價活檢後的影像改變,或監測術前治療的影像學改變。
注意BI-RADS 6不適合用來對惡性病竈完全切除後的隨訪。手術後沒有腫瘤殘餘不需要再切除的病例,其最終的評估應該是BI-RAD 3或2類。與活檢不在同一區域的可疑惡性病變應單獨定側、定位、評估分類及處理建議,其最終的評估應該是BI-RADS 4或5,建議活檢。
5.1.2 二、超聲部分
5.1.2.1 (一)超聲的報告。
內容包括:
1.臨牀病史、檢查指徵
2.是否有相關的既往超聲進行比較3.超聲掃查範圍及檢查技術4.病變描述:
(1)簡要描述掃描範圍乳腺組織類型。
(2)病竈大小測量(至少測量2個徑線),小的單純性囊腫不必全部測量。
(3)病竈位置(採用鐘面描述,還需描述病竈距離乳頭的深度)。
(4)採用超聲專業詞彙對病竈進行簡要描述。5.結合相關的臨牀體檢、X線攝影、MRI或其他影像檢查6.總體評估及處理建議
5.1.2.2 (二)乳腺病竈的超聲評估分類。
參照NCCN篩查及診斷指南提出的BI-RADS(Breast imaging reporting and data system)分類標準。
5.1.2.2.1 1.評估不完全
0類:現有影像未能完成評估,需要其他影像檢查進一步評估或與既往檢查比較。
5.1.2.2.2 2.評估完全
1類:陰性,無異常所見(如有發現乳內、腋前正常形態淋巴結,亦屬於1類)。建議常規體檢(每年1次)。
2類:良性病變,包括單純性囊腫、積乳囊腫;乳房內移植物;穩定的術後改變;隨訪後無變化的纖維腺瘤。建議定期隨訪(每6個月至1年1次)。
3類:良性可能大。包括邊緣光整、呈圓形或橢圓形、橫徑大於高徑的實性腫塊,很可能是纖維腺瘤;還包括觸診陰性的複雜囊腫和簇狀微囊腫。建議短期隨訪(每3~6個月1次),2年隨訪無變化者可降爲2類。
4類:可疑惡性。
4A:低度可疑惡性(≥3%-≤10%)。病理報告結果一般爲非惡性,在獲得良性的活檢或細胞學檢查結果後應進行6個月或常規的隨訪。例如可捫及的、局部界限清楚的實質性腫塊,超聲特徵提示爲纖維腺瘤;可捫及的複雜囊腫或可能的膿腫。
4B:中度可能惡性的病竈(>10%至≤50%)。需綜合影像學檢查與病理學結果。部分界限清楚部分界限不清的纖維腺瘤或脂肪壞死可進行隨訪,但乳頭狀瘤則可能需要切除活檢。
4C:惡性可能較大(>50%至≤94%),但不象5級那樣典型的惡性。例如邊界不清的不規則實質性腫塊或新出現的簇狀細小多形性鈣化。該級病竈很可能會是惡性的結果。建議行病理學檢查(如細針抽吸細胞學檢查、空芯針穿刺活檢、手術活檢)以明確診斷。
5類:高度可疑惡性,臨牀應採取適當措施(幾乎肯定的惡性)。超聲有特徵性的異常徵象,惡性的危險性大於95%。應開始進行確定性治療。考慮前哨淋巴結顯像和新輔助化療時,宜進行影像導引下空芯針穿刺活檢,以取得組織學診斷。
6類:已行活檢證實爲惡性,臨牀應採取適當措施。這一分類用於活檢已證實爲惡性但還未進行治療的影像評價上。主要是評價活檢後的影像改變,或監測手術前新輔助化療的影像改變。
5.1.3 三、乳腺MRI部分
報告內容包括以下6方面:檢查適應證;掃描技術;乳腺腺體構成成分的簡要描述;重要徵象的描述;與既往檢查片對比;評估分類和處理。
5.1.3.1 (一)檢查適應證。
1.檢查指徵
乳腺癌的診斷、乳腺癌分期、新輔助治療療效評估、腋窩淋巴結轉移原發竈不明者、保乳術患者的術前評估及術後隨訪、乳腺成形術後隨訪、高危人羣篩查、MRI引導下的穿刺活檢。
2.臨牀病史
患者的症狀、體徵、家族史、高危因素、月經狀態及月經週期,有無激素替代治療或抗激素治療史,有無胸部放療史,乳腺手術史及病理結果、有無前片及相關檢查(乳腺X線攝影、超聲等)。
3.檢查前的準備
絕經前女性MRI檢查儘量安排在月經週期第2周進行。確診乳腺癌患者則不作此要求。
5.1.3.2 (二)掃描序列及參數。
除了只進行假體植入物的評價外,乳腺MRI檢查均需進行增強掃描。1.掃描序列至少包括:T1加權成像非脂肪抑制序列、T2加權成像脂肪抑制序列、動態增強T1加權成像脂肪抑制序列、彌散加權成像序列。2.增強掃描序列:對比劑選用二乙烯三胺五乙酸釓,注射劑量0.1~0.2mmol/kg,採用壓力注射器以以 2 ~3 ml/s的速率經肘靜脈注入,10秒內快速團注,注射完對比劑後以相同速率注入15 ml生理鹽水衝管。注意增強前後的T1加權成像序列最好有脂肪抑制且雙側乳腺同時成像,建議進行減影處理並繪製動態增強曲線。對比劑注射後共採集5~9次,掃描延遲時間以8~10分鐘爲宜。3. 彌散加權成像:一般行抑脂的單次激發平面回波序列橫軸位掃描,抑制常規使用頻率飽和或水激發方式。使用並行採集技術有利於減低磁敏感僞影而提高圖像質量,常規並行採集因子爲2~3。掃描一般採用2個b值,常規使用0或50s/mm2和800 s/mm2或者1000 s/mm2。
成像參數:掃描層厚≤3mm,層面內的分辨率<1.5mm,掃描時間<2分鐘。
圖像後處理:動態增強掃描序列需要圖像後處理並生成時間-信號曲線(TIC)。注意尋找病竈最大、強化顯著的區域放置感興趣區,應避開出血、液化、壞死及囊變區,感興趣區光標應不小於5個體素。
5.1.3.3 (三)乳腺MRI診斷報告指南。參照BI-RADS標準。
1.乳腺腺體構成成分的簡要描述:需要在非脂肪抑制平掃T1加權成像進行評估。分4種類型:A型,脂肪型;B型,散在纖維腺體型;C型,不均勻緻密型;D型,極度緻密型。
2.乳腺背景實質強化分四種類型:幾乎無強化、輕度強化、中度強化和明顯強化。
3.徵象的描述:採用乳腺MRI專業詞彙對病竈進行描述。
(1)點狀強化。
(2)腫塊:形態(圓形、卵圓形、不規則形)、邊緣(清晰、不規則、毛刺)、內部強化特徵(均勻強化、不均勻強化、環形強化、內部低信號分隔)、動態增強特性(早期強化率:緩慢強化、中等強化、快速強化;時間-信號曲線:緩升持續型、速昇平臺型和速升廓清型)。
(3)非腫塊樣強化:分佈(局竈、線樣、段樣、區域、多區域、瀰漫分佈)、內部強化特徵(均勻、不均勻、集羣卵石樣、簇樣環形強化)。
(4)其他徵象和伴隨徵象:乳腺內淋巴結、皮膚病變、無強化病變(增強前高信號導管、囊腫、術後血腫積液)、皮膚增厚、皮膚水腫、無強化腫塊、結構扭曲、乳頭回縮、皮膚回縮,胸肌侵犯、胸壁侵犯、腋窩淋巴結增大。⑤植入物:假體類型、位置、是否完整。
4.病竈定位:左側/右側;象限和鐘面定位;病變深度;距乳頭的距離。
5.與既往片比較。
(1)評估不完全:0類:現有影像未能完成評估,需要結合既往片或其他影像檢查。一般MR檢查後較少用這個分類。
(2)評估完全:
BI-RADS 1:陰性,惡性可能性0,建議常規隨診。
BI-RADS 2:良性發現,惡性可能性0,建議常規隨診。包括無強化的纖維腺瘤,囊腫、無強化的陳舊瘢痕、乳腺假體、含脂肪的病變(脂性囊腫、脂肪瘤及錯構瘤)等。
BI-RADS 3:可能是良性的病變,惡性可能性小於2%,建議短期隨訪。需通過隨訪確定其穩定性。較可疑者可3個月後隨訪,一般6個月後複查。
BI-RADS 4:可疑惡性,但不具備典型的惡性徵象,惡性可能性2%-95%,應考慮活檢。此類病變無特徵性的乳腺癌形態學改變,但有惡性的可能性。也可參照X線分類將病竈細分爲4A、4B、4C。
BI-RADS 5:高度懷疑惡性,惡性可能性≥95%,臨牀應採取適當措施。
BI-RADS 6:已活檢證實爲惡性,臨牀應採取積極的治療措施。
5.2 附件2 乳腺上皮性腫瘤的組織學分型
浸潤性癌,非特殊類型
伴髓樣特徵的癌
伴神經內分泌分化的癌伴多形性特徵的癌
微浸潤性癌
浸潤性小葉癌(經典型、多形性)小管癌
篩狀癌
黏液癌
黏液性囊腺癌
伴大汗腺分化的癌
化生性癌
低級別腺鱗癌
梭形細胞癌
伴間葉分化的化生性癌(軟骨分化、骨分化、其他間葉分化)
混合性化生性癌
罕見的及涎腺類型的腫瘤
分泌型癌
多形性腺癌
伴極性翻轉高細胞癌
上皮-肌上皮腫瘤
腺肌上皮瘤
惡性腺肌上皮瘤
非典型小葉增生
小葉原位癌(經典型、多形性、旺熾性)
導管原位癌(派傑氏病、伴大汗腺分化、伴神經內分泌分化、印戒樣、透明細胞樣)
乳頭狀病變
導管內乳頭狀瘤
導管內乳頭狀瘤伴ADH/DCIS
乳頭狀DCIS
包裹性乳頭狀癌
良性上皮增生及前驅性病變
普通型導管上皮增生
柱狀細胞病變,包括非典型扁平上皮
非典型導管上皮增生
微腺性腺病
導管腺瘤
5.3 附件3 乳腺浸潤性癌組織學分級
根據是否有腺管形成、細胞核多形性及核分裂象計數3項指標進行分級,建議採用改良的Scarff-Bloom-Richardson分級系統。

注:對腺管結構、細胞核多形性及核分裂計數三個指標分別進行評分:
總分爲3~5分,組織學分級爲Ⅰ級;
6~7分,組織學分級爲Ⅱ級;
8~9分,組織學分級爲Ⅲ級。
核分裂計數(每10HPF的核分裂數目)0~5 0~9 0~1116~11 10~19 12~222≥11 ≥19 ≥223
5.4 附件4 乳腺癌的pTNM分期
___ pTX: 原發腫瘤不能被估量
___ pT0: 無原發腫瘤證據#
___ pTis(導管原位癌):導管原位癌#(小葉原位癌已從此分類中去除)
___ pTis(佩吉特病): 乳頭佩吉特病,不伴隨乳腺實質中的浸潤性癌和/或原位癌(導管原位癌和/或小葉原位癌)成分#
___ pT1: 腫瘤最大徑 ≤20 mm(根據5mm、10mm可細分爲T1a、T1b、T1c)
___ pT1mi: 腫瘤最大徑≤1mm(微小浸潤性癌)pT1a:1mm<腫瘤最大徑≤5mm(1.0-1.9mm之間的腫瘤均計爲2mm)。
pT1b:5mm<腫瘤最大徑≤10mm。pT1c:10mm<腫瘤最大徑≤20mm。___ pT2: 20mm<腫瘤最大徑≤50 mm___ pT3: 腫瘤最大徑>50 mm
___ pT4: 任何大小腫瘤直接侵犯胸壁和/或皮膚(形成潰瘍或肉眼腫塊);僅有腫瘤侵及真皮不診斷T4
___ pT4a: 侵犯胸壁(不包括單純胸大、小肌受累)
___ pT4b:皮膚潰瘍,和/或同側肉眼可見的衛星結節,和/或皮膚水腫(包括橘皮徵)但不到炎性乳癌的診斷標準(僅有鏡下可見的皮膚衛星結節,且無皮膚潰瘍或水腫,不診斷T4b)
___ pT4c: T4a和T4b
___ pT4d: 炎性乳癌##
(注:新輔助化療後ypT應根據殘餘的最大腫瘤竈計算,浸潤癌旁治療相關的纖維化區域不計入腫瘤最大徑;多竈殘留應標註m)
#爲了列表的目的,這些項目應當只用於先前確診爲浸潤性癌,經術前(新輔助)治療後無殘留浸潤癌的情況
##炎性乳癌是一個臨牀-病理學名詞,特徵是瀰漫紅腫和水腫(橘皮),累及乳腺皮膚1/3或更多。皮膚的改變歸因於淋巴水腫,是由皮膚淋巴管內瘤栓引起的,這在小塊皮膚活檢中可以不明顯。然而,對於確定乳腺組織中或至少是皮膚淋巴管內浸潤性癌以及其生物學指標如ER、PR、HER2狀態,組織學診斷仍是必須的。具有皮膚淋巴管內瘤栓而無皮膚的上述臨牀改變不能定義爲炎性乳癌。局部乳腺癌直接侵犯真皮或潰破皮膚而無上述皮膚的臨牀改變以及真皮淋巴管瘤栓也不能定義爲炎性乳癌。因此,炎性乳癌這個詞不應該誤用於局部晚期乳腺癌。罕見病例表現炎性乳癌的所有特徵,但其皮膚病損累及範圍小於1/3,應該根據潛在癌的大小和尺寸來分類。
同時性同側多發癌(多中心):按最大的癌竈進行T分期,並記錄其他癌竈的大小;注意除外癌竈伴衛星結節和複雜形狀癌竈(病理取材結合臨牀影像)區域淋巴結(pN)
___ pN0(i+): 僅有ITCs:腫瘤細胞簇≤0.2mm(單個淋巴結中可有多竈ITC,最大者必須≤0.2mm;若ITCs細胞總數大於200,則應診斷爲微轉移)
___ pN0(mol-): 組織學無轉移,RT-PCR陰性
___ pN0(mol+): 未檢測到ITCs,但RT-PCR陽性
___ pN1mi: 微轉移(約200個細胞,>0.2 mm,≤2.0mm)
___ pN1a: 1~3個淋巴結有轉移,至少1個腫瘤竈>2.0mm
___ pN1b: 轉移至同側內乳前哨淋巴結(胸骨旁,轉移竈>0.2 mm),腋窩淋巴結陰性。
___ pN1c: N1a和N1b
___ pN2a: 4~9個腋窩淋巴結轉移(至少1個腫瘤竈>2.0 mm)
___ pN2b: 臨牀檢測到內乳(胸骨旁)淋巴結轉移(有或無病理證實),不伴腋窩轉移
___ pN3a: ≥10個腋窩淋巴結有轉移(至少1個腫瘤竈>2.0mm)或鎖骨下淋巴結(腋頂部)轉移
___ pN3b: pN1a或pN2a伴有cN2b(影像學證實的內乳淋巴結轉移);或pN2a伴有pN1b。
___ pN3c: 轉移至同側鎖骨上淋巴結分期:T1包括T1mi,而N1mi對分期有意義;如果淋巴結只有前哨,則標記Nx(sn)遠處轉移(M)
___ 不適用
___ cM0(i+): 無臨牀或影像學證據證實遠處轉移;但在沒有轉移症狀和體徵的患者中,分子生物學或顯微鏡下檢測到循環血中、骨髓中或其他非區域淋巴結組織中有≤0.2mm的腫瘤細胞羣
___ pM1:臨牀和影像學手段檢查到遠處轉移和/或組織學證實轉移竈 >0.2 mm
分期

5.5 附件5 乳腺癌病理報告內容及基本格式
病理號
住院號
患者姓名: 性別: 年齡: 科室:
_____________________________________________________________________________ 肉眼所見
左乳癌改良根治標本,大小25cm×16cm×5.4cm,附梭皮,面積 12.5 cm×4cm,乳頭皮膚未見異常。切面於外上現象距乳頭 3.5cm 見一腫物,大小3.4 cm×2.5 cm×1.2cm,切面灰白質硬,界欠清,距胸肌筋膜0.5cm,未累及乳頭皮膚。周圍乳腺部分區灰白質韌。腋窩找到結節數枚,直徑0.2~1.8cm。
病理診斷
乳腺癌新輔助治療後
(1)(左乳癌改良根治標本)乳腺浸潤性癌,非特殊類型,Ⅲ級(3+3+2=8 分),伴少許高級別導管原位癌(約 5%),可見脈管瘤栓及神經侵犯,部分腫瘤細胞退變,伴間質纖維化及局竈淋巴細胞、組織細胞浸潤,符合輕度治療後改變(Miller&Payne 分級,2級)。腫瘤大小 3.4 cm×2.5 cm×1.2cm(浸潤癌成分),未累及乳頭、皮膚及胸肌筋膜。周圍乳腺呈腺病改變,伴部分導管上皮普通型增生。
前哨淋巴結 2/3
ypTNM 分期:ypT2N2Mx
免疫組化檢測結果:ER(+,30%強陽),PR(-,<1%),HER2(2+,需申請進一步 FISH 檢測)CK5/6(-),EGFR(-),Ki-67(30%)。
報告醫師簽名: 診斷日期
_____________________________________________________________________________
5.6 附件6 乳腺癌HER2/neu FISH檢測報告基本格式
病理號
病案號
FISH檢測編號
姓名 性別 年齡 民族 病房 送檢醫師 送檢材料1: 接收日期
病理診斷
檢測結果附圖(可選)
HE染色 免疫組化染色(2+)
FISH
HER2 基因拷貝數目總計(),每個細胞平均HER2拷貝數()。
CEP17 拷貝數目總計(),每個細胞平均CEP17拷貝數()。
HER2 / CEP17 比值=( )
FISH檢測結果:在以下相應()內畫“√”
平均HER2拷貝數/細胞<4.0,比值<2.0(無擴增)陰性 ( )
平均HER2拷貝數/細胞4.0但<6.0,比值<2.0(無擴增)陰性 ( )
平均HER2拷貝數/細胞4.0,比值2.0或平均HER2拷貝數/細胞6.0,比值<2.0(擴增)陽性( )
無法判定( )
HER2 基因有無異質性:無□ 有□( %)HER2基因擴增信號分佈方式:點狀□ 點簇狀或片狀□
注
1.如檢測樣本爲針吸組織標本,建議行手術標本的FISH檢測或複檢。
2.如爲片狀擴增,應註明該區域HER2/CEP17 的比值。
5.7 附件7 保留乳房手術後美容效果評價標準
Ⅰ很好:病側乳腺外形與對側相同。
Ⅱ.好:病側乳腺與對側稍有不同,差異不明顯。
Ⅲ.一般:與對側有明顯不同,但無嚴重畸形。
Ⅳ.差:病側乳腺有嚴重畸形。
5.8 附件8 乳腺癌術後復發風險的評估
| 評估要點 | ||
| 轉移淋巴結 | 其他 | |
| 低度 | 陰性 | 同時具備以下6條:標本中病竈大小(pT)2cm;分級1級a;無脈管瘤栓b;ER和/或PR陽性;HER2基因無過度表達或擴增c;年齡35歲 |
| 中度 | 陰性 | 以下6條至少具備1條:標本中病竈大小(pT)>2cm;分級2~3級;有脈管瘤栓;ER和PR陰性;HER2基因過度表達或擴增;年齡<35歲 |
| 1~3枚陽性 | 無HER2基因過度表達和擴增且ER和/或PR陽性 | |
| 高度 | 1~3枚陽性 | HER2基因過度表達或擴增或ER和PR陰性 |
| ≥4 枚陽性 |
5.9 附件9 乳腺癌分子分型
| 分子分型 | 病理特點義 | 備註 |
| LuminalA型 | ER陽性 PR陽性且PR高表達(>20%)a HER2陰性 Ki-67低表達(<14%) | Ki-67高低表達的判定值在不同病理實驗中心可能不同,一般採用20%~30%作爲判斷Ki-67高低的界值 |
| Luminal B型 | ER和/或PR陽性 HER2陰性 且Ki-67高表達(≥14%) 或PR低表達(≤20%) | |
ER和/或PR陽性 HER2陽性(蛋白過表達或基因擴增) 任何狀態的Ki-67 | ||
| HER2過表達型 | HER2陽性(蛋白過表達或基因擴增) ER和PR陰性 | |
| 基底樣型 | ER陰性,PR陰性,HER2陰性 | 三陰性乳腺癌和Basal-like型乳腺癌之間的吻合度約80%。但是三陰性乳腺癌也包含一些特殊類型乳腺癌如髓樣癌(典型性)和腺樣囊性癌,這類癌的復發轉移風險較低 |
5.10 附件10 常用的輔助化療方案
5.10.1 TAC方案
多西他賽75 mg/m2
iv第1天多柔比星50 mg/m2
iv第1天環磷酰胺500 mg/m2
iv第1天21天爲1個週期,共6個週期(所有週期均用G-CSF支持)。
5.10.2 劑量密集AC→P方案
多柔比星60 mg/m2
iv第1天環磷酰胺600 mg/m2
iv第1天14天爲1個週期,共4個週期序貫以紫杉醇175 mg/m2
iv 3小時第1天14天爲1個週期,共4個週期(所有週期均用G-CSF支持)。
5.10.3 AC→P/T方案
多柔比星60 mg/m2
iv第1天環磷酰胺600 mg/m2
iv第1天21天爲1個週期,共4個週期序貫紫杉醇80 mg/m2
iv 1小時第1天,每週1次,共12周
或紫杉醇175 mg/m2
iv 1小時第1天,每3周1次,共12周
或多西他賽100 mg/m2
iv第1天,每3周1次,共12周。
5.10.4 TC方案
多西他賽75 mg/m2
iv第1天環磷酰胺600 mg/m2
5.10.5 AC方案
多柔比星60 mg/m2
iv第1天環磷酰胺600 mg/m2
5.10.6 FAC方案
氟尿嘧啶500 mg/m2
iv第1、8天多柔比星50 mg/m2
iv第1天環磷酰胺500 mg/m2
5.10.7 EC方案
表柔比星90~100 mg/m2
iv第1天環磷酰胺600~830 mg/m2
5.10.8 FEC→T方案
氟尿嘧啶500 mg/m2
iv第l天表柔比星100 mg/m2
iv第1天環磷酰胺500 mg/m2
iv第1天21 天爲1個週期,共3個週期序貫以多西他賽100 mg/m2
5.10.9 FEC→P方案
氟尿嘧啶600 mg/m2
iv第1天表柔比星90 mg/m2
iv第1天環磷酰胺600 mg/m2
iv第1天21 天爲1個週期,共4個週期序貫以紫杉醇100 mg/m2
iv第1天每週1次,共8周。
5.11 附件11 晚期乳腺癌常用化療方案
5.11.1 優選單藥
紫杉醇80mg/m2,靜滴,第1、8、15天,28天爲一週期
或175mg/m2,靜滴,第1天,21天爲一週期。
卡培他濱 1000-1250mg/m2,口服,每日2次,第1-14天,21天爲一週期。
吉西他濱 800-1200mg/m2,靜滴,第1、8、15天,28天爲一週期。
長春瑞濱 25mg/m2靜滴;或60mg/m2口服,第1、8、15天,28天爲一週期。
多柔比星脂質體 50mg/m2,靜滴,第1天,28天爲一週期。
5.11.2 其他單藥方案
多西他賽60-100mg/m2,靜滴,第1天,21天爲一週期。
白蛋白結合型紫杉醇 100 mg/m2或125mg/m2,靜滴,第1、8、15天,28天爲一週期 。
或260mg/m2,靜滴,第1天,21天爲一週期。
表柔比星60-90mg/m2,靜滴,第1天,21天爲一週期。
或 20mg/m2,靜滴,第1天,每週一次。
環磷酰胺 50~100mg,口服,每日1次,第1-21天,28天爲一週期。
依託泊苷膠囊 75-100mg 口服,第1-10天,21天爲一週期。
5.11.3 聯合化療方案
5.11.3.1 常用化療方案
5.11.3.1.1 TX
多西他賽 75mg/m2,靜滴,第1天
卡培他濱 950~1000mg/m2,口服,每日2次,第1-14天
21天爲一週期。
5.11.3.1.2 GT
吉西他濱 1000-1250mg/m2,靜滴,第1、8天
紫杉醇 175mg/m2,靜滴,第1天。
或多西他賽 75mg/m2,靜滴,第1天
21天爲一週期。
5.11.3.1.3 GC
吉西他濱 1000mg/m2,靜滴,第1、8天
卡鉑 AUC 2,靜滴,第1、8天
21天爲一週期
5.11.3.1.4 ET
表柔比星 60-75mg/m2,靜滴,第1天
多西他賽 75mg/m2,靜滴,第2天
21天爲一週期
5.11.3.2 其他方案
5.11.3.2.1 CAF
環磷酰胺500mg/m2,靜滴,第1天
多柔比星50mg/m2,靜滴,第1天
5-氟尿嘧啶500mg/m2,靜滴,第1、8天
21天爲一週期
5.11.3.2.2 FEC
5-氟尿嘧啶500mg/m2,靜滴,第1、8天
表柔比星50mg/m2,靜滴,第1、8天
環磷酰胺400mg/m2,靜滴,第1、8天
28天爲一週期
5.11.3.2.3 AC
多柔比星60mg/m2,靜滴,第1天環磷酰胺600mg/m2,靜滴,第1天21天爲一週期
5.11.3.2.4 EC
表柔比星75mg/m2,靜滴,第1天環磷酰胺600mg/m2,靜滴,第1天21天爲一週期
5.11.3.2.5 CMF
環磷酰胺100mg/m2,口服,第1-14天甲氨蝶呤40mg/m2,靜滴,第1、8天
5-氟尿嘧啶600mg/m2,靜滴,第1、8天
28天爲一週期
5.12 附件12 絕經的定義
絕經通常是生理性月經永久性終止,或是乳腺癌治療引起的卵巢合成雌激素的功能永久性喪失。絕經標準如下雙側卵巢切除術後。
年齡≥60歲。
年齡<60歲,且在沒有化療和服用他莫昔芬、託瑞米芬和卵巢功能抑制治療的情況下停經1年以上,同時血FSH及雌二醇水平符合絕經後的範圍;而正在服用他莫昔芬、託瑞米芬,年齡<60歲的停經患者,必須連續檢測血FSH及雌二醇水平符合絕經後的範圍。
正在接受LH-RH激動劑或拮抗劑治療的婦女無法判斷是否絕經。
輔助化療前沒有絕經的婦女,停經不能作爲判斷絕經的依據,因爲患者在化療後雖然會停止排卵或無月經,但卵巢功能仍可能正常或有恢復可能。對於化療引起停經的婦女,如果考慮採用芳香化酶抑制劑作爲內分泌治療,則需要考慮有效地卵巢抑制(雙側卵巢完整切除或藥物抑制),或者連續多次監測FSH/或雌二醇水平已確認患者處於絕經後狀態。
5.13 附件13 術後輔助靶向治療常用治療方案
5.13.1 AC→PH(P)方案
多柔比星60 mg/m2
iv 第1天環磷酰胺600 mg/m2
紫杉醇80mg/m2iv 1小時周療,共12周
曲妥珠單抗首劑4mg/kg iv,第一週,以後每次曲妥珠單抗2mg/kg,iv每週,共完成1年。也可在紫杉醇化療後,改變曲妥珠單抗給藥方式爲6mg/kg iv,每3周,共完成1年。
帕妥珠單抗840mg iv(首劑)至420mg iv,第1天,每3周,完成1年。
5.13.2 ddAC→PH(P)方案
多柔比星60 mg/m2
iv 第1天環磷酰胺600 mg/m2
紫杉醇175mg/m2
曲妥珠單抗首劑4mg/kg iv,第一週,以後每次曲妥珠單抗2mg/kg,iv每週,共完成1年。也可在紫杉醇化療後,改變曲妥珠單抗給藥方式爲6mg/kg iv,每3周,共完成1年。(所有週期均用G-CSF支持)。
帕妥珠單抗840mg iv(首劑)至420mg iv,第1天,每3周,完成1年。
5.13.3 TCH(P)方案
多西他賽75 mg/m2iv 第1天
卡鉑 AUC=6 iv 第1天
曲妥珠單抗首劑4mg/kg iv,第一週,序貫曲妥珠單抗2mg/kg iv,每週,或曲妥珠單抗首劑8mg/kg iv,第一週,序貫曲妥珠單抗6mg/kg iv,每3周,完成1年。
帕妥珠單抗840mg iv(首劑)至420mg iv,第1天,每3周,完成1年。
5.13.4 AC→TH(P)方案
多柔比星60 mg/m2
iv 第1天環磷酰胺600 mg/m2
序貫
多西他賽100mg/m2iv 第1天21天爲1個週期,共4個週期
曲妥珠單抗首劑4mg/kg iv,第1周,以後每次曲妥珠單抗2mg/kg,iv每週,共11周序貫曲妥珠單抗6mg/kgiv,每3周,完成1年。
帕妥珠單抗840mg iv(首劑)至420mg iv,第1天,每3周,完成1年。
5.13.5 TC4H
多西他賽75 mg/m2iv 第1天
環磷酰胺600 mg/m2iv 第1天
聯合
曲妥珠單抗首劑4mg/kg iv,第1周,以後每次曲妥珠單抗2mg/kg,iv每週,共11周序貫曲妥珠單抗6mg/kgiv,每3周,完成1年。
5.13.6 PH
紫杉醇80mg/m2
iv 1小時周療,共12周
聯合
曲妥珠單抗首劑4mg/kg iv,第1周,序貫以後每次曲妥珠單抗2mg/kg,iv 每週,共完成1年。也可在紫杉醇化療後,改變曲妥珠單抗給藥方式爲6mg/kg iv,每3周,共完成1年。
5.14 附件14 晚期HER2 陽性乳腺癌的靶向治療常用治療方案
5.14.1 1)HER2陽性晚期乳腺癌一線治療方案
5.14.1.1 曲妥珠單抗+多西他賽
多西他賽 75~100mg/m2,iv,第1天
曲妥珠單抗8mg/kg(首劑)~6mg/kg,iv 第1天21天爲1個週期。
曲妥珠單抗+多西他賽+卡培他濱多西他賽 75mg/m2,iv,第1天
卡培他濱1000mg/m2PO,每天2次,第1~14天
曲妥珠單抗8mg/kg(首劑)~6mg/kg,iv,第1天21天爲1個週期。
5.14.1.2 曲妥珠單抗+紫杉醇:
紫杉醇80mg/m2,iv,每週1次
或175mg/m2,iv,第1天,每3周1次
曲妥珠單抗4mg/kg(首劑)~2mg/kg,iv,每週1次,或曲妥珠單抗8mg/kg(首劑)~6mg/kg,iv,第1天,每3周1次。
5.14.1.3 曲妥珠單抗+紫杉醇+卡鉑周療
紫杉醇80mg/m2,iv,第1、8、15天
卡鉑AUC=2 iv,第1、8、15天
曲妥珠單抗4mg/kg(首劑)~2mg/kg,iv,每週1次28天爲1個週期。
5.14.1.4 曲妥珠單抗+長春瑞濱
長春瑞濱25mg/m2,iv,第1、8、15天曲妥珠單抗4mg/kg(首劑)~2mg/kg,iv,每週1次每28天爲1個週期。
5.14.1.5 曲妥珠單抗+帕妥珠單抗+多西他賽
多西他賽 75~100mg/m2,iv,第1天
曲妥珠單抗8mg/kg(首劑)至6mg/kg,iv,第1天
帕妥珠單抗840mg iv(首劑)至420mg,iv,第1天
21天爲1個週期。
5.14.2 2) 使用過曲妥珠單抗的其他治療方案
5.14.2.1 拉帕替尼+卡培他濱
拉帕替尼 1250mg,PO,每天1次,第1~21天
卡培他濱 1000mg/m2,PO,每天2次,第1~14天
每21天爲1個週期。
5.14.2.2 曲妥珠單抗+拉帕替尼
拉帕替尼 1000mg,PO,每天1次
曲妥珠單抗4mg/kg(首劑)至2mg/kg,iv,每週1次,
或曲妥珠單抗8mg/kg(首劑)至6mg/kg,iv,第1天,每3周1次。
5.15 附件15 乳腺癌診療指南(2022年版)編寫審定專家組
(按姓氏筆畫排序)
組長:徐兵河
副組長:馬飛、王翔
成員:於韜、王永勝、王樹森、王勇、王淑蓮、王靖、付麗、孫強、李國輝、李靜、吳炅、應建明、張清媛、張瑾、陳佳藝、金鋒、胡夕春、魏文強祕書:李俏