3 概述
乳糜微粒(CM)是飲食高脂肪食物後,由腸壁細胞合成的富含TG的巨大脂蛋白,80-100nm。乳糜微粒是人血漿中最大的脂蛋白顆粒。血中半壽期爲10~15分鐘,食後12小時,正常人血中幾乎無CM。脂蛋白電泳時CM位於原點,需注意的是做血清脂蛋白電泳時樣品應新鮮,不可凍存。乳糜微粒在腸上皮細胞合成,並分泌入淋巴管。淋巴CM(初級顆粒)進入血漿時丟失APOA而獲得APOC和E形成次級CM,APOCⅡ是LPL激活劑。CM在LPL作用下脫去TG形成表面殘基和核心殘基。核心殘基轉入肝細胞,其脂類用於VLDL合成,表面殘基中的APOC、FC和磷脂則轉入盤狀HDL。CM含有ApoAⅠ,AⅡ,AⅣ和B48。ApoB48含量多少與攝取食物的TG含量有關。ApoB48是合成CM所必須的蛋白質,CM從胸導管移行入血液過程中,其載脂蛋白的組份迅速改變。CM獲得ApoC和E後,將ApoAⅠ移行到HDl,脫去ApoAⅣ,使進入血中的CM被末梢血管內皮細胞表面的LPL經ApoAⅡ激活,並作用於其內的TG,分解變成脂肪酸和單甘油脂肪酸,再進入肌肉、脂肪組織及心肌組織貯存或利用。CM表面的磷脂和Apo往HDL3移行,顆粒變小,結果轉變成CM殘粒,分別被肝臟LDL受體和清道夫受體識別並攝取。
CM生理功能是轉運外源性脂類,主要是甘油三酯。其中TG在毛細血管中被水解成遊離脂肪酸後進入各組織貯存或利用,而外源性膽固醇則全部進入肝。
4 乳糜微粒醫學檢查
乳糜微粒是人血漿中最大的脂蛋白顆粒,CM是多數膳食TG從小腸吸收部位輸送至體循環。淋巴CM(初級顆粒)進入血漿時丟失APOA而獲得APOC和E形成次級CM,APOCⅡ是LPL激活劑。CM在LPL作用下脫去TG形成表面殘基和核心殘基。核心殘基轉入肝細胞,其脂類用於VLDL合成,表面殘基中的APOC、FC和磷脂則轉入盤狀HDL。CM清除速度快,半衰期爲10min,正常人空腹12h後不能檢出,脂蛋白電泳時CM位於原點。需注意的是做血清脂蛋白電泳時樣品應新鮮,不可凍存。
4.1 分類
4.2 化驗取材
4.3 原理
(1)免疫透射比濁法:血清CM與試劑中的特異性抗人CM抗體相結合,形成不溶性免疫複合物,使反應液產生混濁,以光度計在波長340nm測出吸光度,代表混濁程度,濁度高低反映血清標本中CM的含量,後者可由校準血清所作校準曲線讀出。
試劑中聚乙二醇(PEG)有促進抗原抗體反應的作用。CM主要存在於HDL顆粒表面,血清稀釋及表面活性劑有助於HDL CM抗原位點的暴露,使之能充分地與特異性抗體起反應,表面活性劑還可減輕血清空白濁度。
(2)火箭電泳法:火箭免疫電泳法是單向免疫擴散法的一種改進,通過應用直流電(穩壓穩流)使抗原(CM和B)在含有特異性抗體的瓊脂糖凝膠中擴散,pH 8.6時抗原向陽極移動,在泳動途中與凝膠中的抗體反應,逐漸形成類似火箭的沉澱峯。其峯高(或峯面積)與抗原濃度成正比,故可作抗原定量。
4.4 試劑
①樣品稀釋劑:pH 7.4的磷酸鹽緩衝液(0.01mol/L磷酸鹽中含0.15mol/L氯化鈉),內含PEG-6000 40g/L及表面活性劑適量(選用聚氧乙烯月桂醚類,如Thesit或Tween-20),用GS玻芯漏斗抽濾後用。本試劑的吸光度A340nm<0.05,在2~6℃冰箱中可存放半年。如半年後A值仍<0.05,可繼續應用,如>0.05可按上述條件抽濾後再用。
②羊或兔抗人apoAⅠ抗血清:原血清效價以1∶32~1∶64爲宜。抗血清可用含PEG-6000的磷酸鹽緩衝液(不含表面活性劑)或用硫酸銨沉澱法純化。抗血清應用液濃度因各批抗血清的效價及免疫親和力而異(應按試劑盒介紹,臨用前稀釋)。抗血清中含防腐劑,在2~6℃冰箱中可存放半年。原血清(凍幹)在低溫冰箱中(-20℃以下)可貯存數年。
③參考血清:現在已有國際標準,即WHO CM參考物質SPI-01(凍幹血清)。符合國際標準的校準血清由衛生部北京老年醫學研究所提供。
校準血清保存在-20℃以下,至少穩定半年,化凍後必須徹底混勻後才能應用。最好備有高、中、低濃度(例如apoAⅠ 2.0,1.3與0.6g/L左右)的校準血清各1份。便於作校準曲線。
附註:
①關於抗血清:比濁測定與其他方法相比對抗血清的要求更高。比濁法以用多克隆抗體爲宜。抗血清中必須不含雜抗體。必須十分重視從人血清中提取的apoA-Ⅰ達到免疫純、色譜純與電泳純,這不是一般實驗室都能做到的。抗血清效價(滴度)不可低於16。目前國內某些商品試劑中,apoA-Ⅰ抗血清效價極低,選購試劑盒時必須注意。如果沒有在選購前鑑定抗血清質量的經驗,應請有條件的單位鑑定之。
②上法中標本(血清)稀釋200倍是爲了便於手工操作(加樣100μl),如有精密加樣器,可作20倍稀釋(用10μl)。爲了適合不同實驗室的條件(如不同類型的自動化儀器),作適當修改時應注意抗原抗體的比例,必須十分注意反應體系中不可有抗原過量,線性上限不可低於2.5g/L。換言之,抗血清用量必須充裕,否則標本中apoA-Ⅰ高水平時測出結果偏低。目前國內某些商品試劑盒不但抗血清效價過低,操作中所定標本用量又過大(如3~5μl),抗體明顯不足,測出結果必然不準確。
③爲了達到準確測定的目的,apoA-Ⅰ與B比濁測定(終點法)中必須作校準曲線計算結果。一定範圍(低標本用量)濃度(X)與濁度(Y)基本上成直線關係,直線迴歸計算出在Y軸上有一定截距(A值<0.1),所以用單點校準計算結果偏差較大,使測出結果不能準確反映濃度的高低(高的偏低,低的偏高)。千萬不要因爲單點法簡便而忽略了測定的準確性。無論用何種自動化儀器,必須先試作校準曲線。如果在所用儀器及特定條件下反覆測試,迴歸線的截距不明顯時,才能採用單點校準法。標本用量在3~5μl時,即使加大抗血清用量,濃度與濁度也不成直線關係,只能用曲線直線化轉換後計算。
④主要干擾因素是血清本身的混濁(如高脂血清),用超離心或脂肪酶水解等標本預處理方法都不實用。用表面活性劑消濁的作用也有限,所以在測定中必須作標本空白管。除了自動分析中可採用兩點法外,手工法用單一試劑而不扣除標本空白的做法是錯誤的。爲了減少基質效應對濁度反應的影響,必須用定值血清作校準物。此外,塵埃粒子、比濁皿劃痕等干擾也必須排除。
⑤有的商品試劑盒(包括某些進口產品)所附校準血清定值不準確,是誤差的重要來源。
(2)火箭電泳法:
②10g/L瓊脂糖(標準電內滲)用巴比妥緩衝液配製,加熱溶化,混合後,分裝10ml/管,冷後4℃貯存。
③0.15mol/L NaCl溶液。
④兔(或羊)抗人apoAⅠ抗血清(效價不低於1∶16)及apoB抗血清(效價不低於1∶32)。
⑥染色液:考馬斯亮藍R-250 0.25g溶於甲醇45ml中,加入冰醋酸10ml及水45ml,混合,溶後備用。
4.5 操作方法
①標本應是及時分離的空腹血清,可密封存放在2~6℃冰箱中,1周內測定,-20℃可存放半年。
②用全自動分析儀時,應根據不同儀器設計參數,合理選擇抗原抗體比例及反應時間。也可作速率法散射比濁測定CM如用Beckman比濁儀ICS或protein array system)。
③手工法所用儀器:精密光度計,具有340nm濾光片(或分光器),樣品池體積以0.5ml爲宜(爲節省抗血清),最好用流動杯,樣品稀釋最好用稀釋器、經校正的加樣器。
④標本處理:將血清標本及質控血清各用樣品稀釋劑作1∶200稀釋,即先作1∶20稀釋(5.Oμl血清+95μl稀釋劑)後,再作1∶10稀釋(多餘的1∶20血清作測定apoB用)。然後按表1操作。
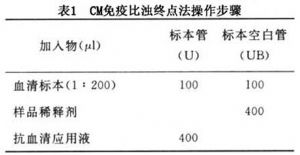
質控同上處理。
混勻後,25~37℃放置30min,在波長340nm比濁,根據U-UB的A值,在標準曲線上讀出結果。
本法批間CV<5%。
⑤校準曲線:在手工與半自動操作中每批測定均需作校準曲線,可將校準血清稀釋成1∶100、1∶200、1∶300和1∶400等4種濃度,與標本同樣操作,根據定值計算出每個標準管CM濃度,以濃度(X)與其相應的A值(Y)作圖(用直線迴歸計算),基本上成直線,但在Y軸上有一定截距,所以不能用單點標準。操作準確時濃度與A值的相關係數應在0.985以上。
如有高、中、低濃度的三份校準血清時,可與標本同樣操作,做三點定標,也可作五點定標(即高、中濃度的血清等量混合,及中、低濃度的血清等量混合,成爲另兩份校準血清)。
本法線性範圍:0.4~2.5g/L。
(2)火箭電泳法:
①澆板:每板用10g/L瓊脂糖10ml,沸水浴中融化,混勻,冷至50~55℃時加入CM抗血清50μl,apoB抗血清8μl(用量視抗血清效價而定),迅速混勻後倒在預置在水平臺上的玻璃板上,冷後放在4℃,20min後打孔,孔在板的陰極端,孔徑3mm,孔間距至少5mm,孔容量5μl。把板放入電泳槽,用濾紙搭橋。
②稀釋抗原:用0.15mol/L NaCl液將校準血清稀釋成1∶100,1∶150,1∶200,1∶300,及1∶400(作校準曲線之用),血清標本按1∶200稀釋,放4℃冰箱不得超過3天。
③加樣:在低電流狀態(10mA/板)將稀釋好的定值血清及標本分別吸取5μl(準確),加入瓊脂糖凝膠加樣孔內。每板都要做一系列標準。
④通電:穩流24mA/板,端電壓6~8V/cm,以流水冷卻使瓊脂糖保持15℃,電泳3~4h。
⑤脫雜蛋白及制幹膠膜:電泳後的瓊脂糖板浸泡在0.15mol/L NaCl中30min,將膠膜託置於聚酯薄膜上,用多層濾紙在輕輕加壓下吸乾膠內水分,然後將濾紙、膠膜與聚酯膜三者一起自然乾燥,或用熱吹風器吹乾,幹後膠膜會自然與濾紙及聚酯膜分開。
⑦脫色:用脫色液浸泡已染色的膠膜至火箭峯清晰,背景基本無色。可在水中用兩片玻璃紙將膠膜夾住,晾乾後可長期保存。也可以用流水浸泡脫色至背景乾淨。
附註:
①抗原稀釋倍數與抗血清用量的選擇,應以火箭峯清晰、校準曲線斜率適中併成直線爲宜。本法同時測定apoA-Ⅰ與apoB,應調整兩種抗血清用量,使二者峯高有區別,apoB峯高不小於1cm。
②不同種類來源的抗血清(如兔與羊),在等效價的情況下進行試驗,結果會有差異。apoA-Ⅰ測定以兔抗血清爲好。用兔血清時峯形尖細,而羊血清所產生的峯粗,峯尖圓鈍,有時在峯頂前出現虛影。校準血清所作校準曲線斜率也不同。但不論用何種抗血清,定量結果差別不大。
③在一定條件下電泳,不同稀釋度校準血清的峯高不會有明顯變動,校準曲線斜率基本一致。如標本峯高超出校準曲線範圍時,應調整標本稀釋倍數後重測。板間CV通常小於5%。
④火箭電泳結果可以用染色法或直接肉眼觀察可見的火箭峯。前者用標本少,節省抗血清,但如適當增加標本及抗血清用量,不染色更爲方便。所用瓊脂糖應爲標準電滲或低電滲的,凝膠中加入適量葡聚糖或聚乙二醇可使火箭峯更清晰。
⑤火箭峯的測量可以計算面積或峯高,面積是峯高乘以峯寬(峯半高處的寬度)。測量精度最好能達0.1mm。須用機械或電子放大設備。標準曲線範圍內峯高以1~4cm爲宜。
⑥本法適用於少量標本分析。也適用於apoAⅡ、CⅠ、CⅡ、CⅢ、D、E及Lp(a)測定。
4.6 正常值
陰性。