3 概述
巨幼細胞性貧血(megaloblastic anemia)是因葉酸和(或)維生素B12缺乏或藥物影響所致的細胞核DNA合成障礙引起血細胞生成異常的貧血[1]。由於細胞核和細胞漿的發育不平衡,紅細胞、粒細胞及巨核細胞的體積增大,呈現形態與功能均不正常的巨幼改變,常導致全血細胞減少[1]。更新較快的胃腸道上皮細胞也會發生類似改變,引發胃腸道症狀[1]。維生素B12缺乏時也常因神經系統的細胞和髓質發生改變,出現神經系統症狀[1]。
巨幼細胞性貧血系脫氧核糖核酸(DNA)合成的生物化學障礙及DNA複製速度減緩所致的疾病。影響到骨髓造血細胞——紅細胞系、粒細胞系及巨核細胞系而形成貧血,甚至全血細胞減少。骨髓造血細胞的特點是胞核與胞質的發育及成熟不同步,前者較後者遲緩,其結果形成了形態、質和量以及功能均異常的細胞,即細胞的巨幼變(megaloblastic change)。體內其他增生速度快的細胞,如消化道上皮細胞等也可受到侵犯。巨幼細胞性貧血絕大多數是由於葉酸或維生素B12或者兩者均缺乏所致。
追溯簡史如下:19世紀Combe(1822)及Addison(1855)先後描述了一種進行性致死的嚴重貧血疾患的臨牀表現,其後名爲惡性貧血(現已知此病經注射維生素B12即可治癒,但仍沿用此歷史性名稱)。1926年Minot及Murphy用口服肝製劑治療惡性貧血獲得成功。Castle於1929年認爲正常人的胃液中存在的“內因子”與動物蛋白質中的“外因子”結合使“抗惡性貧血要素”得以吸收,以治療惡性貧血。1948年美國及英國分別分離出維生素B12,及其結晶,始知維生素B12即爲“外因子”及“抗惡性貧血要素”。1964年Hodgkin明確了維生素B12的化學結構。
在19世紀,Channing(1842)及Barclay(1851)以及於20世紀初Osier(1919)描述了葉酸缺乏的巨幼細胞貧血。1937年Wills報道了孕婦合併巨幼細胞貧血者用“Wills因子”——酵母或肝粗製劑,治療有效。於194l~1946年,蝶酰穀氨酸被提純及結晶化,其結構及合成過程也得以明確,並被命名爲葉酸。
治療巨幼細胞性貧血,需治療基礎疾病,去除病因,糾正偏食及不良的烹調習慣,補充葉酸或維生素B12。巨幼細胞貧血的預後與原發疾病有關。一般患者在進行適當的治療後可得到很快的反應,臨牀症狀迅速改善,神經系統症狀恢復較慢或不恢復。如果血液學指標不能完全被糾正,應尋找是否同時存在缺鐵或其他基礎疾病。
9 巨幼細胞性貧血的流行病學資料
在我國由於葉酸缺乏所致的巨幼細胞貧血散在各地,以晉、秦、豫、魯等省較多見。多與膳食質量不佳,偏食或烹調時間過長有關。維生素B12的缺乏可見於素食者。惡性貧血亦非罕見。在西方國家惡性貧血爲維生素B12缺乏的主要疾患。據估計,美國約有1%的人可能患惡性貧血,而70歲以上者約10%可有維生素B12缺乏的表現。葉酸缺乏多見於酗酒、膳食質量差以及藥物所致。
10 巨幼細胞性貧血的病因
巨幼細胞貧血的發病原因主要是由於葉酸或(及)維生素B12缺乏。
10.1 葉酸缺乏的病因
10.1.1 葉酸攝入不足
葉酸每天的需要量爲200~400µg。人體內葉酸的儲存量僅夠4個月之需。食物中缺少新鮮蔬菜、過度烹煮或醃製均可使葉酸丟失。乙醇可干擾葉酸的代謝,酗酒者常會有葉酸缺缺乏。小腸(特別是空腸段)炎症、腫瘤、手術切除及熱帶性口炎性腹性腹瀉均可導致葉酸的吸收不足。
10.1.2 葉酸需要增加
妊娠期婦女每天葉酸的需要量爲400~600µg。生長發育的兒童及青少年以及慢性反覆溶血、白血病、腫瘤、甲狀腺功能亢進及長期慢性腎功能衰竭用血液透析治療的患者,葉酸的需要都會增加,如補充不足就可發生葉酸缺乏。
10.1.3 藥物的影響
如甲氨蝶呤、氨苯蝶啶、乙胺嘧啶能抑制二氫葉酸還原酶的作用,影響四氫葉酸的生成。苯妥英鈉、苯巴比妥對葉酸的影響機制不明,可能是增加葉酸的分解或抑制DNA合成。約67%口服柳氮磺胺吡啶的患者葉酸在腸內的吸收受抑制。
10.1.4 其他
先天性缺乏5,10-甲酰基四氫葉酸還原酶患者,常在10歲左右才被診斷。有些加強護理病房(ICU)的患者常可出現急性葉酸缺乏。
10.2 維生素B12缺乏的病因
10.2.1 攝入減少
人體內維生素B12的儲存量約爲2~5mg。每天的需要量僅爲0.5~1µg。正常時,每天有5~10µg的維生素B12隨膽汁進入腸腔,胃壁分泌的內因子可足夠地幫助重吸收膽汁中的維生素B12。故素食者一般約需10~15年纔會發展爲維生素B12缺乏。老年人和胃切除患者胃酸分泌減少,常會有維生素B12缺乏。由於有膽汁中的維生素B12的再吸收(腸肝循環),這類患者也和素食者一樣,需經過10~15年纔出現維生素B12缺乏的臨牀表現。故一般由於膳食中維生素B12攝入不足而致巨幼細胞貧血者較爲少見。
10.2.2 內因子缺乏
內因子缺乏主要見於萎縮性胃炎、全胃切除術後和惡性貧血患者。發生惡性貧血的機制目前還不清楚。患者常有特發的胃黏膜完全萎縮和內因子的抗體存在,故有人認爲惡性貧血屬免疫性疾患。這類患者由於缺乏內因子,食物中維生素B12的吸收和膽汁中維生素B12的重吸收均有障礙。
10.2.3 嚴重的胰腺外分泌不足的患者容易導致維生素B12的吸收不良
這是因爲在空腸內維生素B12-R蛋白複合體需經胰蛋白酶降解,維生素B12才能釋放出來,與內因子相結合。這類患者一般在3~5年後會出現維生素B12缺乏的臨牀表現。由於慢性胰腺炎患者通常會及時補充胰蛋白酶,故在臨牀上合併維生素B12缺乏的並不多見。
10.2.4 小腸內存在異常高濃度的細菌和寄生蟲也可影響維生素B12的吸收
因爲這些有機物可大量攝取和截留維生素B12。小腸憩室或手術後的盲端襻中常會有細菌滋生以及腸內產生的魚絛蟲,都會與人體競爭維生素B12,從而引起維生素B12缺乏。
10.2.5 先天性轉鈷蛋白Ⅱ(TCⅡ)缺乏及接觸氧化亞氮(麻醉劑)等
先天性轉鈷蛋白Ⅱ(TCⅡ)缺乏及接觸氧化亞氮(麻醉劑)等也可影響維生素B12的血漿轉運和細胞內的利用,亦可造成維生素B12缺乏。
11 巨幼細胞性貧血的發病機制
巨幼細胞貧血的發病機制主要是細胞內DNA合成障礙。葉酸缺乏時,細胞內脫氧尿嘧啶核苷(dUMP)轉爲脫氧胸腺嘧啶核苷(dTMt)的生化反應受阻。參加正常DNA合成的dTTP被dUTP代替。機體爲了修復這些異常的DNA企圖合成新的DNA,但由於體內缺乏葉酸,仍由dUTP代替dTTP進入新的DNA。如此反覆不已,造成DNA複製的起點多,新合成的小片段不能接成長的子鏈,存在多處單鏈,在重新螺旋化時,易受機械損傷及破壞。促使染色體斷裂、細胞染色質出現疏鬆、斷裂等改變。細胞核的發育停滯,而胞質仍在繼續發育成熟。細胞呈現核漿發育不平衡、細胞體積較正常爲大的巨幼型改變,稱爲巨幼細胞。這些巨幼細胞均有成熟障礙,表現出無效應生成。骨髓內粒系及巨核系細胞亦有類似的DNA合成障礙和成熟障礙。維生素B12缺乏在發病機制中的作用,以及維生素B12缺乏如何阻礙葉酸在細胞DNA合成的作用,有多種解釋。比較成熟的是1964年V.Herbert等提出的“甲基四氫葉酸陷阱學說”。他們認爲在維生素B12缺乏時,同型(高)半胱氨酸轉變爲蛋氨酸的過程受到阻礙,使甲基四氫葉酸不能形成四氫葉酸。亞甲基四氫葉酸的形成亦減少,間接地影響了DNA的合成,故維生素B12缺乏是間接地阻礙了DNA的合成(圖1,2,3)。
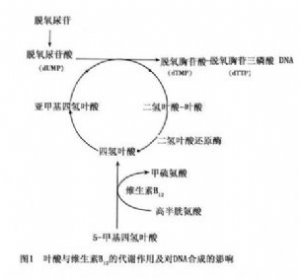
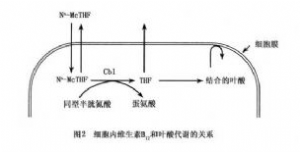
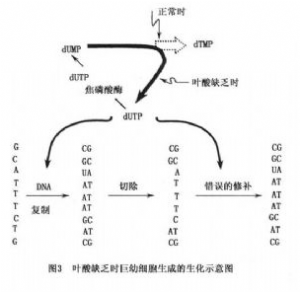
腺苷鈷鈷胺(AdaCbl)是維生素B12的一種形式。AdoCbl作爲輔酶參與琥珀酸輔酶A合成的反應,如果AdoCbl缺乏,此反應不能進行,大量丙酰輔酶A堆積,形成的單鏈脂肪酸影響神經髓鞘磷脂的形成,造成神經的脫髓鞘改變,臨牀上會出現各種神經系統的症狀。
巨幼細胞貧血時,骨髓內雖有各階段的巨幼紅細胞增多,仍不能對貧血起到代償作用。這是因爲巨幼細胞貧血時,細胞的DNA合成減慢,細胞停留在有絲分裂前期的細胞增多,很多巨型的幼紅細胞在骨髓內未到成熟階段即遭到破壞。鐵代謝動態的研究顯示爲紅細胞的無效應生成。紅細胞的壽命約爲正常的1/2~1/3。血漿鐵運轉率比正常人高3~5倍,而幼稚紅細胞對鐵的攝取率不高。血清鐵及轉鐵蛋白飽和度增高,骨髓及肝內均有鐵沉積。
近年的研究提示葉酸缺乏性巨幼細胞貧血時,骨髓紅系造血祖細胞形成BFU-E、CFU-E及CFU-MK的數量較正常明顯增多,而這些造血祖細胞分化發育至晚期成熟階段的過程中大部分遭到了破壞,出現嚴重的無效造血現象。許多實驗證實是葉酸缺乏時發生了細胞增殖受抑制和過度凋亡。葉酸缺乏時巨型變細胞染色質的改變,使細胞增殖受抑,可能觸發凋亡機制,導致細胞過度凋亡,也與巨幼細胞貧血的發生有一定的關係。
巨幼細胞貧血時粒細胞和血小板亦有減少,可能與骨髓內粒系及巨核系細胞亦有類似的DNA合成障礙和成熟障礙有關。
葉酸及維生素B12缺乏時,非造血組織的細胞DNA合成亦會受到影響。對更新代謝較快的各種上皮細胞(如胃腸黏膜、口腔和陰道的黏膜細胞)影響較明顯,臨牀上會出現相應的一些症狀。
12 巨幼細胞性貧血的臨牀表現
12.1 巨幼細胞貧血的一般臨牀表現
12.1.1 貧血
貧血起病隱伏,特別是維生素B12缺乏者,常需數月。而葉酸由於體內儲存量少,可較快出現缺乏。某些接觸氧化亞氮者、ICU病房或血液透析的患者,以及妊娠婦女可在短期內出現缺乏,臨牀上一般表現爲中度至重度貧血,除貧血的症狀如乏力、頭暈、活動後氣短、心悸外,嚴重貧血者可有輕度黃疸。可同時有白細胞和血小板減少,患者偶有感染及出血傾向。
12.1.2 胃腸道症狀
胃腸道症狀表現爲反覆發作的舌炎,舌面光滑、乳突及味覺消失,食慾不振。腹脹、腹瀉及便祕偶見。
12.1.3 神經系統症狀
維生素B12缺乏特別是惡性貧血的患者常有神經系統症狀,主要是由於脊髓後、側索和周圍神經受損所致。表現爲乏力、手足對稱性麻木、感覺障礙、下肢步態不穩、行走困難。小兒及老年人常表現腦神經受損的精神異常、無慾、抑鬱、嗜睡或精神錯亂。部分巨幼細胞貧血患者的神經系統症狀可發生於貧血之前。
上述三組症狀在巨幼細胞貧血患者中可同時存在,也可單獨發生。同時存在時其嚴重程度也可不一致。
12.2 幾種巨幼細胞貧血特殊類型的臨牀表現
12.2.1 麥膠腸病及乳糜瀉(非熱帶性口炎性腹性腹瀉或特發性脂肪下痢)
麥膠腸病在兒童患者中稱爲乳糜瀉。常見於溫帶地區。特點爲小腸黏膜的絨毛萎縮,上皮細胞由柱狀變成骰狀,黏膜層有淋巴細胞浸潤。發病與進食某些穀類物質中的麥膠有關。患者同時對多種營養物質,如脂肪、蛋白質、糖類、維生素以及礦物質的吸收均有障礙。
臨牀表現爲乏力、間斷腹瀉、體重減輕、消化不良、腹脹、舌炎和貧血。大便呈水樣或糊狀,量多、泡沫多、很臭、有多量脂肪。血象及骨髓象爲典型的巨幼細胞貧血。血清和紅細胞葉酸水平降低。治療主要是對症及用葉酸治療,可以取得較好的效果,貧血糾正後宜用小劑量葉酸維持治療。不進含麥膠的食物亦很重要。
12.2.2 熱帶口炎性腹瀉(熱帶營養性巨幼細胞貧血)
熱帶口炎性腹瀉的病因不清楚。多見於印度、東南亞、中美洲以及中東等熱帶地區的居民和旅遊者。臨牀症狀與麥膠腸病相似。血清葉酸及紅細胞葉酸水平降低、用葉酸治療加廣譜抗生素能使症狀緩解及貧血糾正。緩解後應用小劑量葉酸維持治療以防止復發。
12.2.3 乳清酸尿症
乳清酸尿症是一種遺傳性嘧啶代謝異常的疾病。除有巨幼細胞貧血外,尚有智力低下及尿中出現乳清酸結晶。患者的血清葉酸或維生素B12的濃度並不低,用葉酸或維生素B12治療無效,用尿嘧啶治療可糾正貧血。
12.2.4 惡性貧血
惡性貧血是由於胃黏膜萎縮、胃液中缺乏內因子,因而不能吸收維生素B12而發生的巨幼細胞貧血。發病機制尚不清楚。似與種族和遺傳有關。多見於北歐斯堪的那維亞人、英格蘭人和愛爾蘭人。南歐、亞洲及非洲人中均很少見。我國亦罕見。多數患者的血清、胃液和唾液中可檢查出抗自身胃壁細胞的抗體、在血清中還可檢查出兩種內因子(阻斷及結合)抗體,故有人認爲惡性貧血是一種自身免疫性疾病。惡性貧血的發生是遺傳和自身免疫等因素間複雜的相互作用的結果。也有人認爲這些抗胃壁細胞的抗體是不明原因引起胃黏膜破壞後釋放出抗原所引起。
12.2.5 幼年惡性貧血
幼年惡性貧血指嬰兒先天性缺少內因子的純合子狀態,不能吸收維生素B12而發生的惡性貧血。患兒胃黏膜的組織學發現和胃酸的分泌均正常。血清中也不存在抗壁細胞和抗內因子的抗體。其父母和兄弟姊妹中可發現內因子分泌的缺陷。本病需與兒童惡性貧血相鑑別。後者年齡在10歲以上,有胃黏膜萎縮、胃酸缺乏、血清中有抗體。
13 巨幼細胞性貧血的併發症
13.1 心力衰竭
心力衰竭爲惡性貧血患者死亡的主要原因之一。嚴重的貧血可使心肌缺氧而發生心力衰竭。另一方面,心肌能量來源的激活需要藉助維生素B12的作用,如果維生素B12缺乏,則能影響ATP的激活,而加重心肌的障礙,促使心力衰竭的發生。因此,對嚴重的巨幼細胞貧血患者在治療開始時,應注意有無心血管疾病,以便採取必要的措施,防止意外事故的發生。
13.2 出血
部分巨幼細胞性貧血患者由於血小板減少以及其他的凝血因子的缺乏致使本病具有出血的傾向。以前腦出血也是惡性貧血死亡的原因之一。有時可發生眼底出血。
13.3 痛風
嚴重的巨幼細胞貧血可見骨髓內無效造血所致的血細胞破壞亢進,致使血清內尿酸值異常升高,而引起痛風的發作,但極爲罕見。
13.4 精神異常
嚴重的巨幼細胞貧血不僅可發生周圍神經炎,出可發生精神異常,如興奮不安,憂鬱寡言以及夢遊等。這可能與維生素B12缺乏所引起的腦神經組織異常有關。
14 巨幼細胞性貧血的診斷
2.外周血呈大細胞性貧血(MCV>100fl)、大多紅細胞呈大卵圓形,中性粒細胞核分葉過多,5葉者>5%或有6葉者出現。
3.骨髓呈現典型的巨型改變 巨幼紅細胞>10%,粒細胞系統及巨核細胞系統亦有巨型改變。無其他病態造血表現。
4.血清葉酸,水平降低,<6.81nmol/L、紅細胞葉酸水平<227nmol/L、維生素B12水平降低<75pmol/L。
14.1 臨牀表現
14.1.1 貧血表現
起病隱伏,多有明顯貧血症狀,如頭暈、乏力、活動後氣短等[1]。嚴重者因紅細胞未發育到成熟就在骨髓內遭破壞即原位溶血,可出現輕度黃疸[1]。
14.1.2 消化系統症狀
口腔黏膜、舌乳頭萎縮,常有反覆發作的舌炎、舌面光滑呈“牛肉樣舌”、食慾不振,偶有腹脹、腹瀉或便祕等[1]。
14.1.3 神經系統症狀
維生素B12缺乏者可出現神經系統症狀,包括手足對稱性麻木、感覺障礙、步態不穩、行走困難,肌張力增加、腱反射亢進,有些小兒及老年維生素B12缺乏者及少數葉酸缺乏者可出現抑鬱、嗜睡或精神錯亂等精神異常[1]。
14.2 有葉酸和維生素B12缺乏的原因
14.2.1 葉酸缺乏
①攝入不足:食物中缺少新鮮蔬菜或過度烹煮,酗酒,空腸的炎症、腫瘤、手術切除等[1];
②需要增加:妊娠期婦女、生長發育的兒童及青少年、慢性反覆溶血、腫瘤、長期血液透析等[1];
14.2.2 維生素B12缺乏
①攝入減少:常年素食,胃酸缺乏和胃蛋白酶的分泌減少等[1];
②吸收減少:內因子缺乏,胰腺外分泌不足,小腸內細菌和寄生蟲競爭維生素B12等[1]。
14.3 檢查
14.3.1 血象
爲大細胞(MCV>100fl)正色素性貧血,中性粒細胞及血小板也常減少[1]。血塗片中可見大卵圓形的紅細胞和中性粒細胞核分葉過多[1]。
爲大細胞正色素性貧血(MCV>100fl),血象往往呈現全血細胞減少。中性粒細胞及血小板均可減少,但比貧血的程度爲輕。血塗片中可見多數大卵圓形的紅細胞,中性粒細胞分葉過多,可有5葉或6葉以上的分葉。偶可見到巨大血小板。網織紅細胞計數正常或輕度增高。
14.3.2 骨髓象
增生活躍,各系細胞均可出現巨幼變,以紅系細胞最爲顯著[1]。
骨髓呈增生活躍,紅系細胞增生明顯增多,各系細胞均有巨幼變,以紅系細胞最爲顯著。紅系各階段細胞均較正常大,胞質比胞核發育成熟(核質發育不平衡),核染色質呈分散的顆粒狀濃縮。類似的形態改變亦可見於粒細胞及巨核細胞系,以晚幼和桿狀核粒細胞更爲明顯。
14.3.3 血清葉酸和維生素B12水平
血清葉酸和維生素B12水平相應降低。紅細胞葉酸不受短期內葉酸攝入的影響,與血清葉酸相比,其水平降低能更準確地反映體內葉酸的缺乏[1]。
目前二者均可用微生物法或放射免疫法測定。血清葉酸的正常範圍約爲5.7~45.4nmol/L(2.5~20ng/ml),血清維生素B12的正常範圍爲150~666pmol/L(200~900pg/ml)。由於部分正常人中可有血清維生素B12低於150pmol/L(200pg/ml);又因爲這兩類維生素的作用均在細胞內,而不是在血漿中,故此項測定僅可作爲初篩試驗。單純的血清葉酸或維生素B12測定不能確定葉酸或維生素B12缺乏的診斷。
14.3.4 內因子阻斷抗體
在惡性貧血患者的血清中內因子阻斷抗體(Ⅰ型抗體)的檢出率在50%以上,故內因子阻斷抗體測定爲惡性貧血的篩選方法之一。如陽性,應做維生素B12吸收試驗。
14.3.5 紅細胞葉酸測定
可用微生物法或放射免疫法測定。正常範圍是317.8~567.5nmol/L(140~250ng/ml)。紅細胞葉酸不受短期內葉酸攝入的影響,能較準確地反映體內葉酸的儲備量。小於227nmol/L(100ng/ml)時表示有葉酸缺乏。
14.3.6 血清高半胱氨酸和甲基丙二酸水平測定
用以診斷及鑑別葉酸缺乏或維生素B12缺乏。血清高半胱氨酸(正常值爲5~16μmol/L)水平在葉酸缺乏及維生素B12缺乏時均升高,可達50~70μmol/L。而血清甲基丙二酸水平升高(正常值爲70~270nmol/L)僅見於維生素B12缺乏時,可達3500nmol/L。
14.3.7 脫氧尿嘧啶核苷抑制試驗(deoxyuridine suppression test)
方法是取患者的骨髓細胞(或PHA激活的淋巴細胞)加入脫氧尿嘧啶核苷(du)孵育後,再加入3H標記的胸腺嘧啶核苷(3H-TdR)。一定時間後,測定摻入細胞核中DNA的3H-TdR量。當葉酸或(及)維生素B12缺乏時,du利用減少,3H-TdR的摻入量較正常人(<10%)明顯增多(>20%)。還可加入葉酸或維生素B12以糾正。3H-TdR的摻入來判斷患者是缺乏葉酸抑或維生素B12。此試驗較爲敏感,可在血清甲基丙二酸及高半胱氨酸水平升高之前的早期階段出現異常。
14.3.8 維生素B12吸收試驗(schilling test)
主要用來判斷維生素B12缺乏的病因。方法是:給患者肌內注射維生素B121000μg,同時或1h後口服57C0標記的維生素B120.5μC。收集24h尿,測定尿中57C0維生素B12的含量。正常人應>8%,巨幼細胞貧血患者及維生素B12吸收不良者<7%。惡性貧血患者<5%。如在5天後重復此項試驗,同時口服內因子60mg,尿中57C0維生素B12的排出量恢復正常,表示患者的維生素B12缺乏是由於內因子缺乏,否則是其他原因所致。如果給患者服用抗生素7~10天后試驗得到糾正,表示維生素B12的吸收障礙是由於腸道細菌過量繁殖所致。此試驗結果與尿量有關,準確收集24h的尿量及事先了解試驗者的腎功能是否正常,非常重要。
14.3.9 遊離胃酸消失
14.4 試驗性治療
在無條件進行葉酸和維生素B12水平和內因子抗體檢測時,根據病史、臨牀表現、血象和骨髓象疑似診斷的患者可給予生理劑量的葉酸(0.2mg/d)或維生素B12(1μg/d)試驗性治療10天[1]。生理劑量的葉酸(或維生素B12)只對相應元素缺乏的患者有效,有助於診斷與兩者的鑑別[1]。
15 需要與巨幼細胞性貧血鑑別的疾病
15.1 骨髓增生異常綜合徵(MDS)
可以有血象全貧及大細胞貧血的表現,骨髓中可見到紅繫有巨幼型改變。鑑別主要靠MDS有典型病態造血,可波及巨核系及粒系細胞。患者細胞遺傳學的改變亦可幫助鑑別。
15.2 再生障礙性貧血
可有血象全貧,但骨髓增生低下。由骨髓塗片和活檢病理檢查可鑑別。
15.3 溶血性貧血
某些溶血性貧血會有相對的葉酸缺乏,當葉酸缺乏性巨幼細胞貧血臨牀上出現黃疸及網織紅細胞增高時,兩者需加以鑑別。溶血性貧血的骨髓中不會出現典型的巨幼改變,黃疸及網織紅細胞增高的程度較顯著。此外,溶血性貧血的特殊試驗常可幫助證實。
16 巨幼細胞性貧血的治療
16.1 病因治療
治療基礎疾病,去除病因。
去除導致葉酸或維生素B12缺乏的病因,糾正偏食及不良的烹調習慣[1]。
16.2 營養知識教育
16.3 補充葉酸或維生素B12
16.3.1 葉酸缺乏
口服葉酸5~10mg,一天3次[1]。直至血紅蛋白恢復正常[1]。一般不需維持治療[1]。
胃腸道不能吸收葉酸者可肌內注射亞葉酸鈣25mg,每天1次[1]。直至血紅蛋白恢復正常[1]。一般不需維持治療[1]。
16.3.2 維生素B12缺乏
肌內注射維生素B12100μg,一天1次(或200μg,隔日1次),直至血紅蛋白恢復正常[1]。
惡性貧血或胃全部切除者需終身採用維持治療,100μg,一月注射1次[1]。
維生素B12缺乏伴有神經症狀者時,每日用量可增加至500μg,以後每週肌內注射2次,每次50~100μg,直到血象恢復正常;維持量每月肌內注射100μg,或根據血清維生素B12的監測水平調整劑量和給藥間隔[1]。腺苷鈷胺片口服制劑有腺苷鈷胺片,成人一次0.5~1.5mg,一天3次[1]。
單純維生素B12缺乏者不宜單用葉酸治療,否則會加重維生素B12的缺乏,引發或加重神經系統症狀[1]。
16.4 注意事項
嚴重巨幼細胞性貧血的患者在補充治療中因貧血恢復時大量血鉀進入新生紅細胞,會突發低血鉀,需適時補鉀[1]。
嚴重的巨幼細胞貧血患者在補充治療後要警惕低血鉀症的發生。因爲在貧血恢復的過程中,大量血鉀進入新生成的細胞內,會突然出現低鉀血癥,對老年患者和有心血管疾患、納差者應特別注意及時補充鉀鹽。
如治療3~4周後血象恢復不明顯,應尋找是否同時存在缺鐵、感染或其他基礎疾病,予以糾正[1]。
16.5 轉診
17 巨幼細胞性貧血的預後
巨幼細胞貧血的預後與原發疾病有關。一般患者在進行適當的治療後可得到很快的反應,臨牀症狀迅速改善,神經系統症狀恢復較慢或不恢復。網織紅細胞一般於治療後5~7天開始升高,以後血細胞比容和血紅蛋白逐漸增高,血紅蛋白可在1~2月內恢復正常。粒細胞和血小板計數及其他實驗室異常一般在7~10天內恢復正常。如果血液學指標不能完全被糾正,應尋找是否同時存在缺鐵或其他基礎疾病。
19 相關藥品
氧、核糖核酸、葉酸、維生素B12、穀氨酸、甲氨蝶呤、氨苯蝶啶、乙胺嘧啶、苯妥英鈉、苯巴比妥、巴比妥、磺胺、磺胺吡啶、胰蛋白酶、氧化亞氮、半胱氨酸、胱氨酸、蛋氨酸、腺苷、輔酶A、磷脂、組胺
21 參考資料
- ^ [1] 國家基本藥物臨牀應用指南和處方集編委會主編.國家基本藥物臨牀應用指南:2012年版[M].北京:人民衛生出版社,2013:147-149.