3 國家基本藥物
| 序號 | 基本藥物目錄序號 | 藥品名稱 | 劑型 | 規格 | 單位 | 零售指導價格 | 類別 | 備註 |
| 302 | 31 | 阿昔洛韋 | 片劑 | 100mg*24 | 盒(瓶) | 6.3元 | 化學藥品和生物製品部分 | * |
| 303 | 31 | 阿昔洛韋 | 片劑 | 100mg*20 | 盒(瓶) | 5.3元 | 化學藥品和生物製品部分 | |
| 304 | 31 | 阿昔洛韋 | 片劑 | 100mg*30 | 盒(瓶) | 7.8元 | 化學藥品和生物製品部分 | |
| 305 | 31 | 阿昔洛韋 | 片劑 | 200mg*10 | 盒(瓶) | 4.6元 | 化學藥品和生物製品部分 | |
| 306 | 31 | 阿昔洛韋 | 片劑 | 200mg*20 | 盒(瓶) | 9.0元 | 化學藥品和生物製品部分 | |
| 307 | 31 | 阿昔洛韋 | 片劑 | 200mg*24 | 盒(瓶) | 10.7元 | 化學藥品和生物製品部分 | |
| 308 | 31 | 阿昔洛韋 | 片劑 | 200mg*25 | 盒(瓶) | 11.1元 | 化學藥品和生物製品部分 | |
| 309 | 31 | 阿昔洛韋 | 片劑 | 200mg*30 | 盒(瓶) | 13.3元 | 化學藥品和生物製品部分 | |
| 310 | 31 | 阿昔洛韋 | 膠囊 | 200mg*10 | 盒(瓶) | 5.0元 | 化學藥品和生物製品部分 | |
| 311 | 31 | 阿昔洛韋 | 膠囊 | 200mg*24 | 盒(瓶) | 11.5元 | 化學藥品和生物製品部分 | |
| 312 | 31 | 阿昔洛韋 | 分散片 | 100mg*20 | 盒(瓶) | 6.9元 | 化學藥品和生物製品部分 | |
| 313 | 31 | 阿昔洛韋 | 分散片 | 100mg*24 | 盒(瓶) | 8.2元 | 化學藥品和生物製品部分 | |
| 314 | 31 | 阿昔洛韋 | 分散片 | 200mg*20 | 盒(瓶) | 11.7元 | 化學藥品和生物製品部分 | |
| 315 | 31 | 阿昔洛韋 | 乳膏劑 | 300mg:10g | 支 | 2.8元 | 化學藥品和生物製品部分 | * |
| 316 | 31 | 阿昔洛韋 | 滴眼劑 | 8mg:8ml | 支 | 4.0元 | 化學藥品和生物製品部分 | * |
| 317 | 31 | 阿昔洛韋 | 滴眼劑 | 5mg:5ml | 支 | 2.6元 | 化學藥品和生物製品部分 |
注(化學藥品和生物製品部分):
1、表中備註欄標註“*”的爲代表品。
2、表中代表劑型規格在備註欄中加註“△”的,該代表劑型規格及與其有明確差比價關係的相關規格的價格爲臨時價格。
注(中成藥部分):
2、表中備註欄加註“△”的劑型規格,及同劑型的其他規格爲臨時價格。
4 阿昔洛韋藥典標準
4.1 品名
4.1.1 中文名
4.1.2 漢語拼音
Axiluowei
4.1.3 英文名
Aciclovir
4.2 結構式
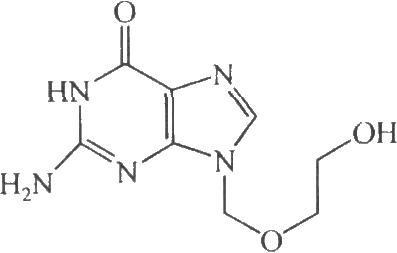
4.3 分子式與分子量
C8H11N5O3 225.21
4.4 來源(名稱)、含量(效價)
本品爲9-(2-羥乙氧甲基)鳥嘌呤。按乾燥品計算,含C8H11N5O3不得少於98.0%。
4.5 性狀
本品爲白色結晶性粉末;無臭,無味。
本品在冰醋酸或熱水中略溶,在乙醚或二氯甲烷中幾乎不溶;在氫氧化鈉試液中易溶。
4.6 鑑別
(1)在含量測定項下記錄的色譜圖中,供試品溶液主峯的保留時間應與對照品溶液主峯的保留時間一致。
(2)本品的紅外光吸收圖譜應與對照的圖譜(《藥品紅外光譜集》213圖)一致。
4.7 檢查
4.7.1 溶液的澄清度與顏色
取本品0.50g,加1%氫氧化鈉溶液10ml使溶解,溶液應澄清無色;如顯渾濁,與1號濁度標準液(2010年版藥典二部附錄Ⅸ B)比較,不得更濃(供注射用)或與2號濁度標準液(2010年版藥典二部附錄Ⅸ B)比較,不得更濃(供口服、外用);如顯色,與黃色1號標準比色液(2010年版藥典二部附錄Ⅸ A第一法)比較,不得更深(供注射用)或與黃色2號標準比色液(2010年版藥典二部附錄Ⅸ A第一法)比較,不得更深(供口服、外用)。[1]
4.7.2 有關物質
取本品,加二甲基亞碸溶解並稀釋製成每1ml中含10mg的溶液,照薄層色譜法(2010年版藥典二部附錄Ⅴ B)試驗,吸取上述溶液5μl,點於硅膠GF254薄層板上,以三氯甲烷-甲醇-濃氨溶液(80:20:2)爲展開劑,展開,晾乾,置紫外光燈(254nm)下檢視,除主斑點外,不得顯其他雜質斑點。
4.7.3 鳥嘌呤與其他有關物質
精密稱取本品約40mg,置200ml量瓶中,加0.4%氫氧化鈉溶液2ml使溶解,加0.1%(V/V)磷酸溶液25ml後用水稀釋至刻度,搖勻,作爲供試品溶液;精密量取1ml,置100ml量瓶中,加0.1%磷酸溶液5ml,用水稀釋至刻度,搖勻,作爲對照溶液;另精密稱取鳥嘌呤對照品10mg,置50ml量瓶中,加0.4%氫氧化鈉溶液5ml使溶解,加0.1%磷酸溶液5ml,用水稀釋至刻度,搖勻,作爲鳥嘌呤對照品貯備液;精密量取1ml,置100ml量瓶中,用水稀釋至刻度,搖勻,作爲鳥嘌呤雜質對照品溶液。照高效液相色譜法(2010年版藥典二部附錄Ⅴ D)測定,用十八烷基硅烷鍵合硅膠爲填充劑;以水爲流動相A,甲醇爲流動相B,按下表進行梯度洗脫;柱溫35℃;檢測波長爲254nm。取鳥嘌呤對照品溶液與對照溶液各適量,等體積混合,搖勻,取20μl注入液相色譜儀,調節色譜系統及檢測靈敏度,阿昔洛韋峯與鳥嘌呤峯之間的分離度應大於3.0;阿昔洛韋峯的峯高約爲滿量程的10%。再精密量取供試品溶液、鳥嘌呤對照品溶液與對照溶液各20μl,分別注入液相色譜儀,記錄色譜圖。供試品溶液色譜圖中如有雜質峯,鳥嘌呤的量按外標法以峯面積計算,不得過0.7%;其他各雜質峯面積之和不得大於對照溶液的主峯面積(1.0%)。
| 時間(分鐘) | 流動相A(%) | 流動相B(%) |
| 0 | 94 | 6 |
| 15 | 94 | 6 |
| 40 | 65 | 35 |
| 41 | 94 | 6 |
| 51 | 94 | 6 |
4.7.4 乾燥失重
取本品,在105℃乾燥至恆重,減失重量不得過6.0%(2010年版藥典二部附錄Ⅷ L)。
4.7.5 熾灼殘渣
取本品1.0g,依法檢查(2010年版藥典二部附錄Ⅷ N),遺留殘渣不得過0.1%。
4.7.6 重金屬
取熾灼殘渣項下遺留的殘渣,依法檢查(2010年版藥典二部附錄Ⅷ H第二法),含重金屬不得過百萬分之十。
4.8 含量測定
照高效液相色譜法(2010年版藥典二部附錄Ⅴ D)測定。
4.8.1 色譜條件與系統適用性試驗
用十八烷基硅烷鍵合硅膠爲填充劑;甲醇-水(10:90)爲流動相;檢測波長爲254nm。取阿昔洛韋對照品溶液5ml,加入鳥嘌呤與其他有關物質項下的鳥嘌呤對照品貯備液1ml,搖勻,取20μl注入液相色譜儀,記錄色譜圖,阿昔洛韋峯與鳥嘌呤峯的分離度應符合要求。
4.8.2 測定法
取本品約50mg,精密稱定,置50ml量瓶中,加0.4%氫氧化鈉溶液5ml使溶解,用水稀釋至刻度,搖勻,精密量取2ml,置100ml量瓶中,用水稀釋至刻度,搖勻,精密量取20μl,注入液相色譜儀,記錄色譜圖;另取阿昔洛韋對照品適量,同法測定。按外標法以峯面積計算,即得。
4.9 類別
抗病毒藥。
4.10 貯藏
4.11 製劑
(1)阿昔洛韋片 (2)阿昔洛韋咀嚼片 (3)阿昔洛韋乳膏 (4)阿昔洛韋膠囊 (5)阿昔洛韋滴眼液 (6)阿昔洛韋顆粒 (7)注射用阿昔洛韋
4.12 版本
《中華人民共和國藥典》2010年版
5 阿昔洛韋介紹
5.1 別名
阿昔洛韋;開鏈鳥嘌呤核苷;開糖環鳥苷;舒維療;無環鳥嘌呤;無環鳥嘌呤核甘 、無環鳥苷、永信克皰、甘泰、建適療、9-(2-羥乙氧甲基)鳥嘌呤
5.2 外文名
Aciclovir, Aciclor, ACV, Acycloguanosine, BW 248U, Poviral, ZOVIRAX
5.3 阿昔洛韋的適應症
臨牀應用於防治單純皰疹病毒HSC1和HSC2的皮膚或粘膜感染,還可用於帶狀皰疹病毒感染。尚用於治療乙型肝炎。
5.4 阿昔洛韋的用量用法
1.口服:1次200mg,每4小時1次或1日1g,分次給予。療程根據病情不同,短則幾日,長者可達6個月。腎功能不足者酌減量。
2.靜滴:1次每千克體重用量5mg,加入輸液中,滴注時間爲1小時,每8小時1次,連續7日。12歲以下兒童1次按每平方米體表面積250mg用量給予。對腎功能不足者應減量:肌酐清除率每平方米體表面積每分鐘25~50ml者按上量每12小時1次;清除率每平方米體表面積每分鐘10~25ml者減爲每24小時1次;清除率每平方米體表面積每分鐘0~10ml者減爲每千克體重2.5mg,每24小時給藥1次。國內治療乙型肝炎的用法爲1次滴注每千克體重7.5mg,1日2次,溶於適量輸液,維持滴注時間約2小時,連續應用10~30日。
3.治療生殖器皰疹:1次0.2g,1日4次,連用5~10日。
5.5 注意事項
1.注射給藥,只能緩慢滴注(持續1~2小時),不可快速推注,不可用於肌注和皮下注射。
3.不良反應有一時性血清肌酐升高、皮疹、蕁麻疹,尚有出汗、血尿、低血壓、頭痛、噁心等。靜脈給藥者可有靜脈炎。
4.並用丙磺舒,可使本品的排泄減慢,半衰期延長,體內藥物易蓄積。
5.6 規格
膠囊劑:每膠囊200mg。注射用阿昔洛維(凍乾製劑):每瓶500mg(標示量)
滴眼液:0.1%,8ml/支. 眼膏:3%,3g/支. 霜劑:3%-5%,10g/支. 注射劑:250mg/瓶.
5.7 阿昔洛韋的不良反應
除偶有頭暈、嘔吐、頭痛外,口服阿昔洛韋幾乎無毒,靜注耐受較好,只1%病人會發生腦病,高劑量靜注可引發神經系統障礙。大劑量突擊性注射,可發生急性腎小管壞死。其不良反應報告以泌尿系統、神經系統、神經系統和過敏反應等不良反應最多見。
5.8 阿昔洛韋與急性腎功能衰竭
1988年至2006年5月,國家藥品不良反應監測中心病例報告數據庫中有關阿昔洛韋的病例報告928份。阿昔洛韋不良反應主要表現爲噁心、嘔吐、腹痛、腹瀉、頭暈、頭痛、泌尿系統損害、肝功能損害、皮疹、過敏樣反應等。其中有關泌尿系統損害的病例報告34份:急性腎功能衰竭22例,腎功能異常9例,腎小管損害1例,腎絞痛1例,血尿1例。在泌尿系統損害病例報告中,急性腎功能衰竭佔64.71%。
5.9 阿昔洛韋引起急性腎功能衰竭的特點
1、大多數患者既往無藥物過敏史,原發疾病基本爲面部皰疹,生殖器皰疹等,既往體健,肝、腎功能正常;
2、各年齡均有發病,但老年人、血容量不足、有基礎腎臟疾病者更易發生;
3、用藥至發生血尿的時間短,可數小時或數天,最長不超過2周,以速髮型爲主;
4、靜脈給藥導致急性腎功能衰竭的可能性更大,且與藥物劑量、濃度、給藥速度有關;
5、發生血尿的同時,部分病例伴有腎外表現,如:腰痛、腰痠、噁心、嘔吐等;
6、阿昔洛韋致急性腎功能衰竭的病理特徵可表現爲急性腎小管壞死或急性間質性腎炎;
7、停藥,經積極治療後大多預後良好,一般不遺留腎功能損害,僅有部分患者留有不同程度的腎功能損害,甚至危及生命。
5.10 建議
鑑於阿昔洛韋引發的急性腎功能衰竭與超出規定的適應症用藥、藥物劑量過大、濃度過高、給藥速度過快、藥物配伍不當等因素有關。故提醒臨牀醫生要合理、規範用藥,嚴格掌握用藥,特別是靜脈用藥指徵。老年人、孕婦、兒童等高危特殊人羣應慎用或在監測下使用。用藥時注意給藥濃度、速度、分次給藥及用藥後水化治療等問題,避免與其它腎毒性藥物配伍使用,用藥期間應監測尿常規和腎功能。一旦發現異常應立即停藥,並儘快明確診斷,及時給予對症治療。同時建議加強臨牀合理使用抗病毒藥物的教育與宣傳,避免此類嚴重不良反應和藥源性疾病的重複發生。
6 化藥部頒標準
6.1 拼音名
Axiluowei
6.2 英文名
Aciclovir
6.3 來源
本品爲9-(2-羥乙氧甲基)鳥嘌呤。按乾燥品計算,含C8H11N5O3不得少於98.0%。
6.4 性狀
本品爲白色結晶性粉末;無臭,無味。 本品在冰醋酸或熱水中略溶,在水中極微溶解,在乙醚或氯仿中幾乎不溶,在稀氫 氧化鈉溶液中溶解。 吸收係數 取本品,精密稱定,加水溶解並稀釋成每1ml中約含10μg的溶液,照分 光光度法(中國藥典1995年版二部附錄Ⅳ A),在252nm的波長處測定吸收度,吸收系 數(E1% 1cm)爲603~641。
6.5 鑑別
(1)取本品20mg,置蒸發皿中,加鹽酸2ml,置水浴上蒸乾,再加鹽酸1ml 與氯酸鉀約30mg,置水浴上蒸乾,冷卻,於殘渣中滴加氨試液2~3滴,殘渣顯紫紅色。 再加氫氧化鈉試液數滴,紫紅色消失。
(2)取本品加水溶解並製成每1ml中含10μg的溶液,照分光光度法(中國藥典1995年 版二部附錄Ⅳ A)測定,在252nm的波長處有最大吸收;220nm的波長處有最小吸收。
(3)本品的紅外光吸收圖譜與對照的圖譜(藥品紅外光譜集1995年版213圖)一致。
6.6 檢查
溶液的澄清度與顏色 取本品0. 5g,研細,加0.4%氫氧化鈉溶液10ml, 溶解後,溶液應澄清無色;如顯渾濁,與2號濁度標準液(中國藥典1995年版二部附錄Ⅸ B)比較,不得更濃;如顯色,與黃色2號標準比色液(中國藥典1995年版二部附錄Ⅸ A 第一法)比較,不得更深。 有關物質 取本品,加二甲基亞碸製成每1ml中含10mg的溶液,照薄層色譜法(中國 藥典1995年版二部附錄Ⅴ B)試驗,吸取上述溶液5μl,點於硅膠GF254薄層板上,以 氯仿-甲醇-氨水(80:20:2)爲展開劑,展開後,晾乾,置紫外光燈(254nm)下檢視,除 主斑點外,不得顯其他斑點。 鳥嘌呤 取本品約50mg,精密稱定,置50ml量瓶中,加0.4%氫氧化鈉溶液5ml使溶 解,用水稀釋至刻度,搖勻,精密量取10ml,置50ml量瓶中,用水稀釋至刻度,搖勻, 作爲供試品溶液;另取鳥嘌呤對照品10mg,置100ml量瓶中,加0.4%氫氧化鈉溶液適量 使溶解,並稀釋至刻度,搖勻,精密量取2ml,置100ml量瓶中,用水稀釋至刻度,搖勻, 作爲對照品溶液。用含量測定項下的方法和溶液,取20μl注入液相色譜儀,調節檢測靈 敏度,使主成分色譜峯達記錄儀的滿標度,再分別取供試品溶液和對照品溶液各20μl, 分別注入液相色譜儀,記錄色譜圖,供試品溶液中鳥嘌呤色譜峯的峯面積不得大於鳥嘌 呤對照品溶液峯面積。 乾燥失重 取本品,在105℃乾燥至恆重,減失重量不得過6.0%(中國藥典1995年版 二部附錄Ⅷ L)。 熾灼殘渣 取本品1. 0g,依法檢查,遺留殘渣不得過0.1%(中國藥典1995年版二部 附錄Ⅷ N)。 重金屬 取熾灼殘渣項下遺留的殘渣,依法檢查(中國藥典1995年版二部附錄ⅧH 第二法),含重金屬不得過百萬分之十。
6.7 含量測定
照高效液相色譜法(中國藥典1995年版二部附錄Ⅴ D)測定。 色譜條件與系統適用性試驗 用十八烷基硅烷鍵合硅膠爲填充劑;甲醇-水(10:90) 爲流動相;檢測波長爲254nm。理論板數按阿昔洛韋峯計算,應不低於2000。 測定法 取本品約50mg,精密稱定,置50ml量瓶中,加0.4%氫氧化鈉溶液5ml使溶 解,用水稀釋至刻度,搖勻,精密量取2ml,置100ml量瓶中,用水稀釋至刻度,搖勻, 精密量取20μl注入液相色譜儀,記錄色譜圖;另精密稱取阿昔洛韋對照品,同法測定, 按外標法以峯面積計算。
6.8 作用與用途
6.9 用法與用量
口服 一次0.1~0. 2g 一日0.5~ 1g
6.10 貯藏
6.11 製劑
(1)阿昔洛韋片
(2)阿昔洛韋軟膏
(3)阿昔洛韋眼膏
(4)阿昔洛韋滴 眼液
(5)注射用阿昔洛韋
7 參考資料
- ^ [1] 國家藥典委員會.中華人民共和國藥典:2010年版:第二增補本[M].北京:中國醫藥科技出版社,2010.