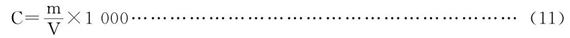2 英文參考
Methods for determination of sulfides in the air of workplace
ICS 13.100
C52
中華人民共和國國家職業衛生標準GBZ/T 160.33—2004《工作場所空氣有毒物質測定 硫化物》(Methods for determination of sulfides in the air of workplace)由中華人民共和國衛生部於2004年05月21日發佈,自2004年12月01日起實施,同時代替GB/T 16024—1995、GB/T 16026—1995、GB/T 16027—1995、GB/T 16028—1995、GB 8777—88 附錄A、GB 16184—1996 附錄A。
本標準首次發佈於1988年,本次是第一次修訂。
3 前言
爲貫徹執行《工業企業設計衛生標準》(GBZ 1)和《工作場所有害因素職業接觸限值》(GBZ 2),特制定本標準。本標準是爲工作場所有害因素職業接觸限值配套的監測方法,用於監測工作場所空氣中硫化物[包括二氧化硫(Sulfur dioxide)、三氧化硫(Sulfur trioxide)、硫酸(Sulfuric acid)、硫化氫(Hydrogen sulfide)、二硫化碳(Carbon disulfide)、硫酰氟(Sulfuryl fluoride)、六氟化硫(Sulfur hexafluoride)和氯化亞碸(Thionyl chloride)等]的濃度。本標準是總結、歸納和改進了原有的標準方法後提出。這次修訂將同類化合物的同種監測方法和不同種監測方法歸併爲一個標準方法,並增加了長時間採樣和個體採樣方法。
本標準從2004年12月1日起實施。同時代替GB/T 16024—1995、GB/T 16026—1995、GB/T 16027—1995、GB/T 16028—1995、GB 8777—88 附錄A、GB 16184—1996 附錄A。
本標準首次發佈於1988年,本次是第一次修訂。
本標準由全國職業衛生標準委員會提出。
本標準由中華人民共和國衛生部批准。
本標準起草單位:中國疾病預防控制中心職業衛生與中毒控制所、江蘇省揚州市疾病預防控制中心、重慶市疾病預防控制中心、四川省疾病預防控制中心、黑龍江省勞動衛生職業病研究所、上海醫科大學公共衛生學院、天津市疾病預防控制中心。
本標準主要起草人:楊秀珍、曾昭慧、顧希陶、楊一超、張學煃、武皋緒、侯樹椿和李建國。
硫化物
5 2 規範性引用文件
下列文件中的條款,通過本標準的引用而成爲本標準的條款。凡是注日期的引用文件,其隨後所有的修改單(不包括勘誤的內容)或修訂版均不適用於本標準,然而,鼓勵根據本標準達成協議的各方研究是否可使用這些文件的最新版本。凡是不注日期的引用文件,其最新版本適用於本標準。
6 3 二氧化硫的四氯汞鉀-鹽酸副玫瑰苯胺分光光度法
6.1 3.1 原理
空氣中二氧化硫用四氯汞鉀溶液採集,與甲醛及鹽酸副玫瑰苯胺反應生成玫瑰紫色絡合物,在548nm波長下測量吸光度,進行定量。
6.2 3.2 儀器
3.2.1 多孔玻板吸收管。
3.2.2 空氣採樣器,流量0~1L/min。
3.2.3 具塞比色管,25ml。
3.2.4 分光光度計。
6.3 3.3 試劑
3.3.1 吸收液:稱取10.86g氯化汞、0.066g乙二胺四乙酸二鈉和5.96g氯化鉀,溶於水中並稀釋至1000ml。
3.3.3 甲醛溶液:吸取1ml甲醛溶液(36%~38%),用水稀釋至200ml。保存於具塞玻璃瓶中,臨用前配製。
3.3.4 鹽酸副玫瑰苯胺溶液:稱取0.200g鹽酸副玫瑰苯胺鹽酸鹽(純度不得低於95%),溶於100ml鹽酸溶液(1mol/L)中,爲貯備液。取20ml此液和25ml磷酸溶液(3mol/L)於250ml容量瓶中,用水稀釋至刻度。在暗處可保存9個月。要求其空白值的吸光度小於0.04μg/ml的SO2吸光度應爲0.030。否則,應提純後配製。
3.3.5 標準溶液:稱取0.15g偏亞硫酸鈉(Na2S2O5)或0.2g亞硫酸鈉,溶於250ml吸收液中。如有沉澱,需過濾。經標定後,計算出二氧化硫的濃度。再用吸收液稀釋成5.0μg/ml二氧化硫標準溶液。置於4℃冰箱內保存可穩定30d。
取6只250ml碘量瓶分成A、B兩組,A組各加10ml吸收液,B組各加10.0ml二氧化硫貯備液;各組加90ml水、5ml冰乙酸和25ml碘液(0.010mol/L)。蓋塞後置暗處放置5min。用硫代硫酸鈉溶液(0.0100mol/L l/2Na2S2O3)滴定,分別記錄硫代硫酸鈉的用量,求出A和B瓶的平均值。用式(1)計算二氧化硫的含量。
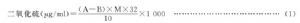
式中:
32——(1/2SO2)摩爾量;
6.4 3.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
3.4.1 短時間採樣:在採樣點,用1只裝有10.0ml吸收液的多孔玻板吸收管,以0.5L/min流量採集15min空氣樣品。
3.4.2 樣品空白:將裝有10.0ml吸收液的多孔玻板吸收管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣時應避免陽光直射吸收液。採樣後,封閉吸收管進出氣口,置清潔的容器內運輸和保存。樣品在4℃冰箱內可保存7d。
6.5 3.5 分析步驟
3.5.1 樣品處理:將採過樣的吸收液洗滌吸收管內壁3次,搖勻,取1.0ml於具塞比色管中,加9.0ml吸收液,搖勻,供測定。若樣品液中待測物的濃度超過測定範圍,可用吸收液稀釋後測定,計算時乘以稀釋倍數。
3.5.2 標準曲線的繪製:取6只具塞比色管,分別加入0.00、0.50、1.00、2.00、3.00、4.00ml二氧化硫標準溶液,各加吸收液至10.0ml,配成0.0、2.50、5.00、10.0、15.0、20.0μg二氧化硫標準系列。向各標準管中加入1.0ml氨基磺酸溶液,搖勻;放置10min。準確加入2.0ml甲醛溶液和5ml鹽酸副玫瑰苯胺溶液,用煮沸放冷的水稀釋至刻度,搖勻。在22℃±1℃水浴中反應30min後,於548nm波長下,以水爲空白測量吸光度,每個濃度重複測定3次,以吸光度均值對二氧化硫含量(μg)繪製標準曲線。
3.5.3 樣品測定:用測定標準系列的操作條件測定樣品和樣品空白溶液。測得吸光度值後,由標準曲線得二氧化硫含量(μg)。
6.6 3.6 計算

式中:
Vo——標準採樣體積,L;
V——採樣體積,L;
t——採樣點的溫度,℃;

式中:
Vo——標準採樣體積,L。
3.6.3 時間加權平均接觸濃度按GBZ 159規定計算。
6.7 3.7 說明
3.7.1 本法的檢出限爲0.075μg/ml;最低檢出濃度爲0.01mg/m3(以採集7.5L空氣樣品計)。測定範圍爲0.075~2.0μg/ml;相對標準偏差爲3.6%~6.8%。
3.7.2 本法的平均採樣效率爲98%。
3.7.3 加入氨基磺酸以消除二氧化氮的干擾。加入EDTA二鈉和磷酸可消除一些金屬元素的干擾。延長放置時間可消除臭氧的干擾。氨、硫化物和醛類不干擾。
3.7.4 在配製吸收液時,應戴防護手套操作。若皮膚接觸此溶液,必須立即用水沖洗。
3.7.5 甲醛如有沉澱不能使用。
7 4 二氧化硫的甲醛緩衝液-鹽酸副玫瑰苯胺分光光度法
7.1 4.1 原理
空氣中二氧化硫用甲醛緩衝液採集,生成穩定的羧甲基磺酸,加氫氧化鈉後釋放出二氧化硫,與鹽酸副玫瑰苯胺反應生成紅色化合物,於575nm波長下測量吸光度,進行定量。
7.2 4.2 儀器
4.2.1 多孔玻板吸收管。
4.2.2 空氣採樣器,流量0~1L/min。
4.2.3 具塞比色管,25ml。
4.2.4 分光光度計,575nm。
7.3 4.3 試劑
4.3.1 磷酸,ρ20=1.68g/ml。
4.3.3 吸收液,甲醛緩衝液:稱取1.82g環己二胺四乙酸,溶於10ml氫氧化鈉溶液,用水稀釋至100ml,置於冰箱內保存。取20ml此液和5.3ml甲醛、2.04g鄰苯二甲酸氫鉀,用水稀釋至100ml,置於冰箱內保存。臨用前,再用水稀釋100倍。
4.3.6 鹽酸副玫瑰苯胺溶液:精確稱取0.2g鹽酸副玫瑰苯胺鹽酸鹽,溶於100ml鹽酸(1mol/L)中。吸取20ml此液於250ml容量瓶中。加入200ml磷酸溶液,用水稀釋至刻度。放置24h後使用。可穩定4個月。
4.3.7 標準溶液:稱取0.15g偏亞硫酸鈉(Na2S2O5)或0.2g亞硫酸鈉,溶於250ml吸收液中。標定其準確濃度後,爲標準貯備液。標定方法見上法。再用吸收液稀釋成4.0μg/ml二氧化硫標準溶液,置於4℃冰箱內可穩定1個月。或用國家認可的標準溶液配製。
7.4 4.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
4.4.1 短時間採樣:在採樣點,用1只裝有10.0ml吸收液的多孔玻板吸收管,以0.5L/min流量採集15min空氣樣品。
4.4.2 樣品空白:將裝有10.0ml吸收液的多孔玻板吸收管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後,置清潔的容器內運輸和保存。樣品在室溫下可穩定15d。
7.5 4.5 分析步驟
4.5.1 樣品處理:用吸收管中的吸收液洗滌進氣管內壁3次。取4.0ml於具塞比色管中,加入6ml吸收液,混勻,供測定。若樣品液中待測物的濃度超過測定範圍,可用吸收液稀釋後測定,計算時乘以稀釋倍數。
4.5.2 標準曲線的繪製:在7只具塞比色管中,分別加入0.0、1.50、2.00、2.50、4.00ml二氧化硫標準溶液,各加吸收液至10.0ml,配成0.0、0.60、0.80、1.00、1.60μg/ml二氧化硫標準系列。向各標準管加入1.0ml氨基磺酸溶液,搖勻,放置10min。加1.0ml氫氧化鈉溶液。迅速將此溶液倒入裝有3ml鹽酸副玫瑰苯胺溶液的具塞比色管中,塞好塞子,混勻。在20℃±2℃水浴中反應15min。取出,於575nm波長下,以水作參比測量吸光度,每個濃度重複測定3次,以測得的吸光度均值對相應的二氧化硫濃度(μg/ml)繪製標準曲線。
4.5.3 樣品測定:用測定標準管的操作條件測定樣品和樣品空白溶液,測得吸光度值後,由標準曲線得二氧化硫的濃度(μg/ml)。
7.6 4.6 計算

式中:
c——測得樣品溶液中二氧化硫的濃度(減去樣品空白),μg/ml;
Vo——標準採樣體積,L。
4.6.3 時間加權平均接觸濃度按GBZ 159規定計算。
7.7 4.7 說明
4.7.1 本法的檢出限爲0.45μg/ml。最低檢出濃度爲0.6mg/m3(以採集7.5L空氣樣品計)。測定範圍爲0.45~1.6μg/ml;平均相對標準偏差<5.0%。
4.7.2 本法的平均採樣效率>99%。
4.7.3 顯色劑加入方式對吸光度影響很大,一定要按本操作步驟進行。
4.7.4 氧化氮的干擾用氨基磺酸消除;15μg以下的Mn2+、Cr3+、Cu2+不干擾測定;0.5μgCr6+即可引起褪色,故應避免用鉻酸洗液洗滌玻璃儀器。
8 5 三氧化硫和硫酸的離子色譜法
8.1 5.1 原理
空氣中三氧化硫和硫酸用裝有鹼性溶液的多孔玻板吸收管採集,經色譜柱分離,電導檢測器檢測,保留時間定性,峯高或峯面積定量。
8.2 5.2 儀器
5.2.1 多孔玻板吸收管。
5.2.2 空氣採樣器,流量0~3L/min。
5.2.3 微孔濾膜,孔徑0.2μm。
5.2.4 過濾裝置。
5.2.5 具塞刻度試管,5ml。
5.2.6 離子色譜儀
儀器操作參考條件
色譜柱:Ionpac AS 4A陰離子色譜柱和Ionpac AG 4A陰離子保護柱;
流動相:吸收液;
流動相流量:1.5ml/min。
8.3 5.3 試劑
5.3.1 吸收液(流動相):稱取1.908g碳酸鈉和1.428g碳酸氫鈉溶於100ml水中,置冰箱內備用。臨用前,取出10ml,用水稀釋至1L。
5.3.2 標準溶液:稱取0.1776g硫酸鉀(於110℃乾燥2h),溶於水,定量轉移入1000ml容量瓶中,稀釋至刻度。貯存在塑料瓶中。此溶液爲100μg/ml標準貯備液。臨用前,用吸收液稀釋成10.0μg/ml硫酸標準溶液。或用國家認可的標準溶液配製。
8.4 5.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
5.4.1 短時間採樣:在採樣點,用一隻裝有5.0ml吸收液的多孔玻板吸收管,以1L/min流量採集15min空氣樣品。
5.4.2 樣品空白:將裝有5.0ml吸收液的多孔玻板吸收管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後,封閉吸收管的進出氣口,在清潔的容器中運輸和保存;在室溫下樣品可保存7d。
8.5 5.5 分析步驟
5.5.1 樣品處理:用吸收管中的吸收液洗滌吸收管進氣管內壁3次,經微孔濾膜過濾後,加入具塞刻度試管中,供測定。若樣品液中待測物的濃度超過測定範圍,可用吸收液稀釋後測定,計算時乘以稀釋倍數。
5.5.2 標準曲線的繪製:取4只具塞刻度試管,分別加入0.0、0.50、1.00、2.00ml硫酸標準溶液,各加吸收液至5.0ml,配成0.0、1.0、2.0、4.0μg/ml硫酸標準系列。參照儀器操作條件,將離子色譜儀調節至最佳測定條件,流動相流量爲1.5ml/min,進樣50μl,分別測定標準系列,每個濃度重複測定3次,以峯高或峯面積對相應的硫酸濃度(μg/ml)繪製標準曲線。
5.5.3 樣品測定:用測定標準系列的操作條件測定樣品和樣品空白溶液,測得樣品峯高或峯面積值後,由標準曲線得硫酸的濃度(μg/ml)。
8.6 5.6 計算
式中:
5——吸收液的體積,ml;
c——測得樣品溶液中硫酸的濃度(減去樣品空白),μg/ml;
Vo——標準採樣體積,L。
5.6.3 時間加權平均接觸濃度按GBZ 159規定計算。
8.7 5.7 說明
5.7.1 本法的檢出限爲0.46μg/ml;最低檢出濃度爲0.15 mg/m3(以採集15L空氣樣品計)。測定範圍爲0.46~4μg/ml;相對標準偏差爲2.6%~5.5%。
5.7.2 本法的採樣效率爲92%~99%。
5.7.3 本法可以同時測定空氣中的HF、HC1和H2SO4。若單獨檢測硫酸霧時,用微孔濾膜採樣,用5.0ml水洗脫,過濾後測定。
5.7.4 色譜柱可用同類型的柱。
9 6 三氧化硫和硫酸的氯化鋇比濁法
9.1 6.1 原理
空氣中三氧化硫和硫酸霧用微孔濾膜採集,用水洗脫後,與氯化鋇反應生成硫酸鋇;在420nm波長下測量吸光度,進行定量。
9.2 6.2 儀器
6.2.1 微孔濾膜,孔徑0.8μm。
6.2.2 採樣夾,濾料直徑爲40mm。
6.2.4 空氣採樣器,流量0~3 L/min和0~10L/min。
6.2.5 具塞比色管,10ml。
6.2.6 分光光度計,420nm。
9.3 6.3 試劑
6.3.1 鹽酸,ρ20=1.18 g/ml。
6.3.2 氯化鋇溶液:稱取5g氯化鋇,溶於水中,加入0.4ml鹽酸,加水至100ml。
6.3.3 混合試劑:混合乙醇(95% v/v):氯化鋇溶液:乙二醇(或丙三醇)=1:2:1。
6.3.4 標準溶液:準確稱取0.1776g硫酸鉀(在105℃乾燥2h),溶於水,並定量轉移入100ml容量瓶中,用水稀釋至刻度。此液爲1.0mg/ml標準儲備液。臨用前,用水稀釋成50.0μg/ml硫酸標準溶液。或用國家認可的標準溶液配製。
9.4 6.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
6.4.1 短時間採樣:在採樣點,將裝好微孔濾膜的採樣夾,以5L/min流量採集15min空氣樣品。
6.4.2 長時間採樣:在採樣點,將裝好微孔濾膜的小型塑料採樣夾,以1L/min流量採集2~8h空氣樣品。
6.4.3 個體採樣:在採樣點,將裝好微孔濾膜的小型塑料採樣夾,佩戴在採樣對象的前胸上部,儘量接近呼吸帶,以1L/min流量採集2~8h空氣樣品。
6.4.4 樣品空白:將裝好微孔濾膜的採樣夾帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後,將濾膜的採樣面朝裏對摺2次後,置於具塞比色管內運輸和保存。樣品在室溫下可保存3d。
9.5 6.5 分析步驟
6.5.1 樣品處理:向裝有采過樣的濾膜的具塞比色管中加入10.0ml水,振搖;放置5min,搖勻。取5.0ml樣品溶液置另一具塞比色管中,供測定。若樣品液中待測物的濃度超過測定範圍,可用水稀釋後測定,計算時乘以稀釋倍數。
6.5.2 標準曲線的繪製:取7只具塞比色管,分別加入0.0、0.10、0.20、0.60、1.00、1.40、2.00ml硫酸標準溶液,各加水至5.0ml,配成0.0、5.0、10.0、30.0、50.0、70.0、100μg硫酸標準系列。向各標準管加入2ml混合試劑,輕輕搖勻後,放置5min。於420nm波長下測量吸光度,每個濃度重複測定3次,以吸光度均值對相應的硫酸含量(μg)繪製標準曲線。
6.5.3 樣品測定:用測定標準系列的操作條件測定樣品和樣品空白溶液,測得吸光度值後,由標準曲線得硫酸含量(μg)。
9.6 6.6 計算

式中:
乘0.82即爲三氧化硫的濃度。
Vo——標準採樣體積,L。
6.6.3 時間加權平均接觸濃度按GBZ 159規定計算。
9.7 6.7 說明
6.7.1 本法的檢出限爲1μg/ml;最低檢出濃度爲0.13mg/m3(以採集75L空氣樣品計)。測定範圍爲1~20μg/ml;相對標準偏差爲2.2%~6.0%。
6.7.2 樣品和標準各管的操作條件要一致;加混合試劑時要慢;測定前應將各管重新搖勻。
10 7 硫化氫的硝酸銀比色法
10.1 7.1 原理
空氣中硫化氫用多孔玻板吸收管採集,與硝酸銀反應生成黃褐色硫化銀膠體溶液,比色定量。
10.2 7.2 儀器
7.2.1 多孔玻板吸收管。
7.2.2 空氣採樣器,流量0~3 L/min。
7.2.3 具塞比色管,10ml。
10.3 7.3 試劑
7.3.1 硫酸,ρ20=1.84 g/ml。
7.3.2 吸收液:溶解2g亞砷酸鈉於100ml碳酸銨溶液(50g/L)中,用水稀釋至1000ml。
7.3.3 澱粉溶液,10g/L:溶解1g可溶性澱粉於10ml冷水中,攪勻後,慢慢倒入90ml沸水中,邊加邊攪拌,煮沸1min;放冷。
7.3.4 硝酸銀溶液,10g/L:溶解1g硝酸銀於90ml水中,加入10ml硫酸。放置過程中如有沉澱產生,需過濾。
7.3.5 硫代硫酸鈉溶液:稱取25g硫代硫酸鈉(Na2S2O3·5H2O),溶於煮沸放冷的水中,轉移入1000ml容量瓶中,加0.4g氫氧化鈉,加水至刻度。
標定:準確稱取0.1500g碘酸鉀(優級純,於105℃乾燥30min)於250ml碘量瓶中,加100ml水,加熱溶解;放冷後,加入3g碘化鉀和10ml冰乙酸,生成碘;迅速用硫代硫酸鈉溶液滴定,直至顏色變成微黃,加入1ml澱粉溶液,繼續滴定至藍色褪去。用式(7)計算硫代硫酸鈉的濃度:
式中:
c——硫代硫酸鈉溶液的濃度,mol/L;
m——碘酸鉀的質量,g;
v——硫代硫酸鈉的用量,ml。
7.3.6 標準溶液:取6.0ml硫代硫酸鈉溶液(0.1mol/L)於100ml容量瓶中,用煮沸放冷的水稀釋至刻度。此溶液相當於0.20mg/ml硫化氫標準貯備液。臨用前,用吸收液稀釋成20.0μg/ml硫化氫標準溶液。
10.4 7.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
7.4.1 短時間採樣:在採樣點,串聯2只各裝有10.0ml吸收液的多孔玻板吸收管,以0.5L/min流量採集15min空氣樣品。
7.4.2 樣品空白:將裝有10.0ml吸收液的多孔玻板吸收管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後,封閉吸收管的進出氣口,置於清潔的容器內運輸和保存。樣品至少可保存5d。
10.5 7.5 分析步驟
7.5.1 樣品處理:用採過樣的吸收液洗滌吸收管進氣管內壁3次。前後管各取5。0ml吸收液於具塞比色管中,搖勻,供測定。若樣品液中待測物的濃度超過測定範圍,可用吸收液稀釋後測定,計算時乘以稀釋倍數。
7.5.2 標準曲線的繪製:取10只具塞比色管,分別加入0.0、0.10、0.20、0.30、0.40、0.50、0.60、0.70、0.80、1。00ml硫化氫標準溶液,各加吸收液至5.0ml,配成0.0、2.0、4.0、6.0、8.0、10.0、12.0、14.0、16.0、20.0μg硫化氫標準系列。向各標準管加入0.2ml澱粉溶液,搖勻;加入1.0ml硝酸銀溶液。搖勻,放置5min,供比色。
7.5.3 樣品測定:用測定標準系列的操作步驟操作樣品溶液和樣品空白溶液,用目視比色法與標準系列比色,得硫化氫含量(μg)。
10.6 7.6 計算

式中:
m1,m2——測得前後管樣品中硫化氫的含量(減去樣品空白),μg;
Vo——標準採樣體積,L。
10.7 7.7 說明
7.7.1 本法的檢出限爲0.4μg/ml;最低檢出濃度爲0.53mg/m3(以採集7.5L空氣樣品計)。測定範圍爲0.4~4μg/ml。平均相對標準偏差爲3.4%。
7.7.2 硫化物對測定有干擾。
11 8 二硫化碳的二乙胺分光光度法
11.1 8.1 原理
空氣中二硫化碳用活性炭管採集,用苯解吸後,二硫化碳與二乙胺和銅離子反應生成黃棕色二乙氨基二硫代甲酸銅;在435nm波長下測量吸光度,進行定量。
11.2 8.2 儀器
8.2.1 活性炭管:溶劑解吸型,內裝100mg/50mg活性炭。
8.2.2 空氣採樣器,流量0~500ml/min。
8.2.4 分光光度計,435nm。
11.3 8.3 試劑
實驗用水爲蒸餾水。
8.3.2 苯,分析純。
8.3.3 硫酸銅乙醇溶液:0.01g硫酸銅溶於20ml水,用95%(v/v)乙醇稀釋至100ml。
8.3.4 顯色劑:稱取0.5g鹽酸二乙胺,加20.0ml硫酸銅乙醇溶液和0.4ml氨水,溶解後,加95%(v/v)乙醇稀釋至100ml。
8.3.5 標準溶液:於25ml容量瓶中加入10ml苯,準確稱量,加數滴二硫化碳,再準確稱量,加苯至刻度,混勻,由2次稱量之差計算溶液中二硫化碳的含量,爲標準貯備液。置4℃冰箱內保存。臨用前,用苯稀釋成50μg/ml二硫化碳標準溶液。或用國家認可的標準溶液配製。
11.4 8.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
8.4.1 短時間採樣:在採樣點,打開活性炭管的兩端,以200ml/min流量採集15min空氣樣品。
8.4.2 長時間採樣:在採樣點,打開活性炭管的兩端,以50ml/min流量採集2~8h空氣樣品。
8.4.3 個體採樣:在採樣點,打開活性炭管的兩端,佩戴在採樣對象的前胸上部,以50ml/min流量採集2~8h空氣樣品。
8.4.4 樣品空白:將活性炭管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後立即封閉兩端,置清潔容器內運輸和保存。樣品在4℃冰箱內可保存7d。解吸後應儘快測定。
11.5 8.5 分析步驟
8.5.1 樣品處理:將採過樣的前後兩段活性炭分別倒人溶劑解吸瓶中,各加5.0ml苯,振搖1min,解吸30min。取0.5ml苯解吸液,加4.5ml顯色液,供測定。若解吸液中待測物的濃度超過測定範圍,可用苯稀釋後測定範圍,計算時乘以稀釋倍數。
8.5.2 標準曲線的繪製:取6只具塞比色管,分別加入0.0、0.1、0.2、0.3、0.4、0.5ml二硫化碳標準溶液,加苯至0.5ml,配成0.0、5.0、10.0、15.0、20.0、25.0μg二硫化碳標準系列。各加4.5ml顯色劑。搖勻,放置15min。於435nm波長下測量吸光度,每個濃度重複測定3次,以吸光度均值對相應的二硫化碳含量(μg)繪製標準曲線。
8.5.3 樣品測定:用測定標準系列的操作條件測定樣品和樣品空白溶液,測得吸光度值後,由標準曲線得二硫化碳含量(μg)。
11.6 8.6 計算

式中:
m1,m2——測得前後段樣品溶液中二硫化碳的含量(減去樣品空白),μg;
Vo——標準採樣體積,L;
D——解吸效率,%。
8.6.3 時間加權平均接觸濃度按GBZ 159規定計算。
11.7 8.7 說明
8.7.1 本法的檢出限爲0.4μg/ml;最低檢出濃度爲1.3mg/m3(以採集3L空氣樣品計)。測定範圍爲0.4~5μg/ml;相對標準偏差爲1.5%~10%。
8.7.2 本法的平均採樣效率爲94.4%。100mg活性炭的穿透容量爲2.6mg。平均解吸效率爲89%。每批活性炭管應做解吸效率。
12 9 二硫化碳的溶劑解吸-氣相色譜法
12.1 9.1 原理
空氣中二硫化碳用活性炭管採集,用苯解吸,經OV-17色譜柱分離後,用火焰光度檢測器檢測,以保留時間定性,峯高或峯面積定量。
12.2 9.2 儀器
9.2.1 活性炭管,溶劑解吸型,100mg/50mg活性炭。
9.2.2 空氣採樣器,流量0~500ml/min。
9.2.4 微量注射器,10μl、1μl。
9.2.5 氣相色譜儀,火焰光度檢測器(394nm濾光片)。
儀器操作參考條件
色譜柱:1.5m×4mm,OV-17:Chromosorb W=2:100;
柱溫:50℃;
汽化室溫度:150℃;
檢測室溫度:150℃;
載氣(氮氣)流量:20ml/min。
12.3 9.3 試劑
9.3.3 OV-17,色譜固定相。
9.3.4 Chromosorb W,色譜擔體,60~80目。
9.3.5 標準溶液:於25ml容量瓶中加入10ml苯,精確稱量後加1滴二硫化碳,再精確稱量,加苯至刻度。由2次稱量之差計算出二硫化碳的濃度,爲標準貯備液。置於4℃冰箱內保存。臨用前,用苯稀釋成10.0μg/ml二硫化碳標準溶液。或用國家認可的標準溶液配製。
12.4 9.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
9.4.1 短時間採樣:在採樣點,打開活性炭管的兩端,以200ml/min流量採集15min空氣樣品。
9.4.2 長時間採樣:在採樣點,打開活性炭管的兩端,以50ml/min流量採集2~8h空氣樣品。
9.4.3 個體採樣:在採樣點,打開活性炭管的兩端,佩戴在採樣對象的前胸上部,以50ml/min流量採集2~8h空氣樣品。
9.4.4 樣品空白:將活性炭管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後立即封閉兩端,置清潔容器內運輸和保存。樣品在4℃冰箱內可保存7d。解吸後應儘快測定。
12.5 9.5 分析步驟
9.5.1 樣品處理:將採過樣的前後兩段活性炭分別倒入溶劑解吸瓶中,各加5.0ml苯,振搖1min,解吸30min。供測定。若解吸液中待測物的濃度超過測定範圍,可用苯稀釋後測定,計算時乘以稀釋倍數。
9.5.2 標準曲線的繪製:取5只溶劑解吸瓶,分別加入0.0、0.50、1.0、2.0、3.0ml二硫化碳標準溶液,各加苯至5.0ml,配成0.0、1.0、2.0、4.0、6.0μg/ml二硫化碳標準系列。參照儀器操作條件,將氣相色譜儀調節至最佳測定狀態,各標準管取1.0μl進樣,測量峯高或峯面積,每個濃度重複測定3次,以峯高或峯面積均值對相應的二硫化碳濃度(μg/ml)繪製標準曲線。
9.5.3 樣品測定:用測定標準系列的操作條件測定樣品和樣品空白溶液。測得峯高或峯面積值後,由標準曲線得二硫化碳濃度(μg/ml)。
12.6 9.6 計算

式中:
5——解吸液的體積,ml;
c1,c2——測得前後段樣品中二硫化碳的濃度(減去樣品空白),μg/ml;
Vo——標準採樣體積,L。
9.6.3 時間加權平均接觸濃度按GBZ 159規定計算。
12.7 9.7 說明
9.7.1 本法的檢出限爲0.01μg/ml;最低檢出濃度爲0.02mg/m3(以採集3L空氣樣品計)。測定範圍爲0.01~6μg/ml;相對標準偏差爲0.8%~4.8%。
9.7.2 本法的平均採樣效率爲94.4%。100mg活性炭的穿透容量>2.6mg。本法的平均解吸效率爲89%。
9.7.3 本法也可以採用相應的毛細管色譜柱。
13 10 六氟化硫和硫酰氟的直接進樣-氣相色譜法
13.1 10.1 原理
空氣中的六氟化硫和硫酰氟用注射器採集,直接進樣,六氟化硫經癸二酸異二辛酯柱分離,熱導檢測器檢測;硫酰氟經聚三氟氯乙烯蠟柱分離,電子捕獲檢測器檢測,以保留時間定性,峯高或峯面積定量。
13.2 10.2 儀器
10.2.1 注射器,100ml,50ml,1ml。10.2.2 氣相色譜儀
儀器操作參考條件
色譜柱1(用於六氟化硫):2m×4mm,癸二酸異二辛酯:Porapak Q=2:100,與柱長1m的6402硅膠柱串聯。
柱溫:64℃。
汽化室溫度:75℃。
檢測室溫度:75℃。
載氣(氫氣)流量:15ml/min。
色譜柱2(用於硫酰氟):3m×4mm,聚三氟氯乙烯蠟:401有機擔體=2:100。
柱溫:60℃。
汽化室溫度:180℃。
檢測室溫度:180℃。
載氣(高純氮)流量:50ml/min。
13.3 10.3 試劑
10.3.2 Porapak Q和401有機擔體,色譜擔體,60~80目。
10.3.3 6402硅膠,80~100目。
10.3.4 標準氣。
10.3.4.1 六氟化硫標準氣:取一定量的六氟化硫(色譜純,在20℃時,1ml六氟化硫氣體爲6.08mg)注入100ml注射器中,用清潔空氣稀釋至100ml,配成100μg/ml標準氣。或用國家認可的標準氣配製。
10.3.4.2 硫酰氟標準氣:取一定量的硫酰氟純氣(在20℃時,1ml硫酰氟爲4.252mg),注入100ml注射器中,用清潔空氣稀釋至100ml,配成0.1μg/ml標準氣。或用國家認可的標準氣配製。
13.4 10.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
10.4.1 樣品採集:在採樣點,用空氣樣品抽洗100ml注射器3次,然後抽100ml空氣樣品,用橡膠帽封閉注射器口,垂直放置,置清潔的容器內運輸和保存。
10.4.2 樣品空白:注射器應在樣品採集前,用氮氣或清潔空氣充滿收集器帶至現場,並隨樣品一起儲存和運輸。
樣品應當天儘快測定。
13.5 10.5 分析步驟
10.5.1 樣品處理:將採過樣的注射器放在測定標準系列的同樣環境中,供測定。若樣品氣中待測物的濃度超過測定範圍,可用清潔空氣稀釋後測定,計算時乘以稀釋倍數。
10.5.2 標準曲線的繪製:用清潔空氣稀釋標準氣成0.0、3.0、6.0、10.0μg/ml六氟化硫的標準系列,0.O、0. 01、0.03、0.05y_g/ml硫酰氟的標準系列,參照儀器操作條件,將氣相色譜儀調節至最佳測定狀態,六氟化硫進樣1.0ml,硫酰氟進樣0.4ml,分別測定各標準管,每個濃度重複測定3次。以測得的峯高或峯面積均值對相應的六氟化硫或硫酰氟含量(μg)繪製標準曲線。
10.5.3 樣品測定:用測定標準管的操作條件測定樣品氣和樣品空白氣,測得峯高或峯面積值後,由標準曲線得六氟化硫或硫酰氟含量(μg)。
13.6 10.6 計算
10.6.1 按式(11)計算空氣中六氟化硫或硫酰氟的濃度。
式中:
V——進樣體積,ml。
10.6.2 時間加權平均接觸濃度按GBZ 159規定計算。
13.7 10.7 說明
本法的最低檢出濃度:六氟化硫爲1630mg/m3(以進樣Iml計),硫酰氟爲0.04mg/m3(以進樣0.4ml計)。測定範圍:六氟化硫爲1630~10000mg/m3,硫酰氟爲0.04~50mg/m3相對標準偏差分別爲2.3%和1.1%。
14 11 氯化亞碸的硫氰酸汞分光光度法
14.1 11.1 原理
空氣中的氯化亞碸被四氯化碳吸收後,經氫氧化鈉溶液提取,遊離出氯離子,與硫氰酸汞作用置換出硫氰酸根,與鐵離子作用生成紅色,於460nm波長處比色定量。
14.2 11.2 儀器
11.2.1 多孔玻板吸收管。
11.2.2 空氣採樣器,流量0~1L/min。
11.2.3 具塞比色管,25ml。
11.2.4 分光光度計,460nm。
14.3 11.3 試劑
11.3.2 硫氰酸汞乙醇溶液:取0.4g硫氰酸汞,溶於100ml無水乙醇中。
11.3.3 硫酸鐵銨溶液,120g/L:溶解12g硫酸鐵銨[(NH4)2SO4·Fe2(SO4)3·24H2O]於適量水中,加40ml硝酸(ρ20=1.42 g/ml),用水稀釋至100ml,如有沉澱應過濾。
11.3.5 標準溶液:於50ml容量瓶中,加入少量四氯化碳,準確稱量後,加入約0.1ml氯化亞碸,再準確稱量,用四氯化碳稀釋至刻度,搖勻。由2次稱量之差計算出氯化亞碸的濃度,爲標準貯備液,置於冰箱中保存。臨用前,用四氯化碳稀釋成20.0μg/ml氯化亞碸標準溶液。或用國家認可的標準溶液配製。
14.4 11.4 樣品的採集、運輸和保存
現場採樣按照GBZ 159執行。
11.4.1 短時間採樣:在採樣點,用1只裝有10.0ml吸收液的多孔玻板吸收管,以0.5L/min流量採集15min空氣樣品。
11.4.2 樣品空白:將裝有10.0ml吸收液的多孔玻板吸收管帶至採樣點,除不連接空氣採樣器採集空氣樣品外,其餘操作同樣品。
採樣後立即封閉進出氣口,置於清潔容器內運輸和保存。應儘快測定。
14.5 11.5 分析步驟
11.5.1 樣品處理:用吸收管中的吸收液洗滌吸收管進氣管內壁3次,將吸收液轉移至具塞比色管中,加10ml氫氧化鈉溶液,振搖200次,靜置分層,取上清液5.0ml放入另一具塞比色管中。供測定。若樣品液中待測物的濃度超過測定範圍,可用吸收液稀釋後測定,計算時乘以稀釋倍數。
11.5.2 標準曲線的繪製:取6只具塞比色管,分別加入0.0、1.0、2.0、3.0、4.0、5.0ml氯化亞碸標準溶液,加吸收液至5.0ml,配成0、20、40、60、80和100μg氯化亞碸的標準系列。向各管加入10ml氫氧化鈉溶液,振搖200次,靜置分層,取上清液5.0ml放入另一具塞比色管中。加入1ml硫酸鐵銨溶液,混勻。再加入1.5ml硫氰酸汞溶液,混勻。用水稀釋至10ml,混勻。放置20min後,於460nm波長下測量吸光度,每個濃度重複測定3次;以吸光度均值對相應的氯化亞碸含量(μg)繪製標準曲線。
11.5.3 樣品測定:用測定標準系列的條件測定樣品和樣品空白吸收液,測得吸光度值後,由標準曲線得氯化亞碸的含量(μg)。
14.6 11.6 計算
式中:
Vo——標準採樣體積,L。
14.7 11.7 說明
11.7.1 本法的檢jLH限爲1.0μg/ml;最低檢出濃度爲1.3mg/m3(按採集7.5L空氣樣品計)。測定範圍爲1~10μg/ml。相對標準偏差爲2.0%~3.8%。
11.7.2 本法的採樣效率爲95.5%~99.0%。