3 基本信息
ICS 11.080
C 50
中華人民共和國國家標準 GB/T 33420—2016《壓力蒸汽滅菌生物指示物檢驗方法》(Evaluation standard of biological for moist heat sterilization processes)由中華人民共和國國家質量監督檢驗檢疫總局、中國國家標準化管理委員會於2016年12月30日發佈,自2017年07月01日起實施。
4 前言
本標準按照GB/T 1.1—2009給出的規則起草。
本標準由中華人民共和國國家衛生和計劃生育委員會提出並歸口。
本標準起草單位:中國疾病預防控制中心環境與健康相關產品安全所、中國人民解放軍疾病預防控制所、山東新華醫療器械股份有限公司、中國醫學科學院協和醫院、山東利爾康消毒科技股份有限公司、3M中國有限公司、杭州魯沃夫貨物進出口有限公司。
本標準主要起草人:張流波、張劍、姚楚水、張青、王妍彥、沈瑾、黃靖雄、朱曉明、朱漢泉、史紹毅、馬玲、班海羣。
5 標準正文
5.1 1 範圍
5.2 2 規範性引用文件
下列文件對於本文件的應用是必不可少的。凡是注日期的引用文件,僅注日期的版本適用於本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
GB 18281.1 醫療保健產品滅菌 生物指示物 第1部分:通則
GB/T 24628 醫療保健產品滅菌 生物與化學指示物 測試設備
消毒技術規範(2002年版)衛生部
5.3 3 術語和定義
下列術語和定義適用於本文件。
3.1
對指定條件下的特定滅菌程序具有一定抗力,並裝在內層包裝中可供使用的染菌載體。
3.2
載體 carrier
試驗微生物的支持物。
3.3
在規定的條件下暴露於殺菌因子,試驗的生物指示物中微生物存活的最長時間。
3.4
測定生物指示物抗力時,受試樣本經殺菌因子作用後,全部無菌生長的最短作用時間。
3.5
D值 D value
在設定的暴露條件下,殺滅特定試驗微生物總數的90%所需的時間。
3.6
存活曲線 survlvor curve
在固定的滅菌因子作用下,微生物的存活情況與暴露變化的關聯曲線。
3.7
生物指示物抗力測試儀 biological indicator evaluator resistometer
產生限定條件下滅菌過程中物理化學變化規定組合,以測量抗力的專用設備。
5.4 4 檢驗指標與方法
5.4.1 4.1 抗力
5.4.1.1 4.1.1 菌種
用於製作壓力蒸汽滅菌生物指示物的菌株爲嗜熱脂肪桿菌芽孢(Geobacillusstearothermophilus
ATCC7953或SSI K31)或被證明具有本標準所要求的同等性能的微生物。
5.4.1.2 4.1.2 菌量
回收菌量大於等於1×105CFU/片或大於等於1×105CFU/支,對於成品的指示物,載體回收的菌量與介紹上的菌量誤差在一50%~+300%之間,懸液回收的菌量與介紹上的菌量誤差在±35%。測定菌量時,應最少測試4個樣本,具體檢測方法參見附錄A。
5.4.1.3 4.1.3 D值
測試抗力時應使用生物指示物抗力測試儀,生物指示物抗力測試儀要求見GB/T 24628。在121℃時,D值的要求:D值大於或等於1.5 min,對於成品的指示物,測試的D值應在介紹上的D值±20%的範圍內。應至少使用下列2種方法進行測試:
c)驗證法測試D值,將a)或者b)測試出的D值和4.1.2的回收菌量的平均數帶入式(1)和式(2),計算出ST值和KT值。參照附錄D進行驗證:
ST≥(logN0-2)×D值 ………(1)
KT≤(logN0+4)×D值 ………(2)
式中:
5.4.1.4 4.1.4 存活時間與殺滅時間
在121℃時,ST值的要求:大於或等於4.5 min;KT值的要求:小於或等於24 min。
5.4.2 4.2 載體的要求
符合GB 18281.1的要求。
5.4.3 4.3 恢復培養基的要求
5.4.3.1 4.3.1 恢復培養基應滿足下列要求:
5.4.3.2 4.3.2 恢復培養基按以下方法檢驗:
每個樣本的恢復培養基中,接種10 CFU~100 CFU的嗜熱脂肪桿菌芽孢(ATCC7953),同時設置陰性對照和陽性對照,培養至規定時間後觀察有無嗜熱脂肪桿菌芽孢生長(一般觀察培養基的顏色變化)。如果恢復培養基有菌生長,並且陰性對照無菌生長和陽性對照有菌生長,判斷恢復培養液合格。
5.4.4 4.4 穩定性試驗
取包裝完好的同批次生物指示物放置於製造商建議的保存條件下,存放至標籤和介紹規定的有效期限,取出再次進行評價,生物指示物應符合4.1、4.2和4.3的要求。
6 附錄
6.1 附錄A(資料性附錄)活菌培養計數方法
A.1 取含有10 mL TPS(0.1%胰蛋白腖的生理鹽水溶液)的無菌試管,加入適量無菌玻璃珠,將計數菌片投入試管,用電動混合器混合,到菌片被完全打碎,製成菌懸液。
A.2 將試管按需要數量分組排列於試管架上,每管加入4.5 mL TPS。各組由左向右,逐管標上10-1、10-2、10-3……等。
A.3 將菌懸液用電動混勻器混合20 s,或在手掌上用力振打80次,隨即吸取0.5 mL加至10-1管內。
A.4 將10-1管依前法用電動混勻器混合20 s,或在手掌上用力振打80次,混勻,再吸取出0.5 mL加入10-2管內。如此類推,直至最後一管。必要時,還可作某稀釋度的1:1或1:4稀釋。
A.5 選擇適宜稀釋度試管(以預計生長菌落數每平板爲15 CFU~300 CFU者爲宜),吸取其中混合均勻的懸液1.0 mL加於無菌平皿內。每一稀釋度接種2個平皿。一般需接種2個~3個不同稀釋度。
A.6 將40℃~45℃熔化的嗜熱脂肪桿菌芽孢恢復培養基參見《消毒技術規範(2002年版)》,傾注於已加入樣液的平皿中,每平皿15 mL~20 mI_。
A.7 將平皿蓋好,即刻輕輕搖動混勻,平放。待瓊脂凝固後,翻轉平皿使底向上,置56℃±2℃恆溫培養箱內培養。
A.8 培養至72 h,計數菌落數。一般以肉眼觀察,必要時用放大鏡檢查。以每平板菌落數在30 CFU~300 CFU的稀釋度爲準記錄結果。
A.9 根據稀釋倍數和接種量計算每毫升菌液巾或每一菌片(染菌載體)上的平均菌落數。 A.10 菌液計數從A.3步驟開始操作。
6.2 附錄B(資料性附錄)存活曲線法測試D值
B.2 根據不同的暴露溫度設置10個暴露時間點,每個時間點測試5個樣本,最短的暴露時間可以設定爲0 s,最長的暴露時間使菌量減少到小於或等於初始菌量的0.01%。
B.3 測試之前,首先對生物指示物抗力測試儀進行預熱。
B.4 按照生物指示物抗力測試儀操作介紹的流程進行操作,分別對10個暴露時間分別處理。
B.5 處理完畢,參照附錄A對各組樣本隨機抽取3個進行活菌計數。
B.6 用所得的全部存活菌數的常用對數值,對時間(min)作圖,用最小二乘法進行迴歸分析,確定最佳線性曲線。迴歸分析時不應包括原先菌落數0.510g範圍內的存活數據點。計算所得直線斜率的負倒數值,即等於以分鐘表示的指定暴露條件下的D值,同時所得線性曲線相關係數應不小於0.8。
6.3 附錄C(資料性附錄)部分陰性法計算D值
C.2 生物指示物抗力測試儀參數設置:
a) 暴露溫度設置121℃;
b) 暴露時間至少爲6個時間點,至少1個時間點全部有菌生長,至少2個時間點部分有菌生長,至少2個時間點全部無菌生長。
C.4 暴露完成後將6組生物指示物在56℃±2℃溫度下,按照介紹要求培養到規定時間,記錄陰性和陽性結果。當最短暴露時間點全部爲陽性,最長暴露時間全部爲陰性,並且中間至少2組有部分樣本陽性,試驗結果有效,帶入式(C.1)和式(C.2)計算D值。
C.5 Limited Spearman-Karber法(LSKP),達到無菌生長平均時間的計算見式(C.1):
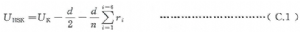
D值的計算見式(C.2):
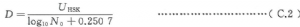
式中:
UK——首次顯示所有樣本無菌生長的暴露時間,單位爲秒(s);
d——暴露時間的固定間隔,單位爲秒(s);
n——每組的樣本量,單位爲個;
N0——回收菌落數,單位爲CFU;
0.2507——計算係數。
6.4 附錄D(資料性附錄)驗證法測試D值
6.4.1 D.1 ST值驗證
將50個試驗樣本放入壓力蒸汽滅菌生物指示物抗力測試儀中,作用濃度爲2.3 mg/L±0.4 mg/L,在50℃±0.5℃時,暴露時間設定爲計算出的ST值,暴露完成後,將50個生物指示物樣本取出,置於56℃±2℃培養至介紹規定時間。若全部有菌生長,則計算的ST值通過驗證;若有樣本無菌生長,則計算的ST值沒有通過驗證。
6.4.2 D.2 KT值驗證
將50個試驗樣本放入壓力蒸汽滅菌生物指示物抗力測試儀中,作用濃度爲2.3 mg/L±0.4 mg/L,在50℃±0.5℃時,暴露時間設定爲計算出的KT值,暴露完成後,將50個生物指示物樣本取出,置於56℃±2℃培養至介紹規定時間。若全部無菌生長,則計算的KT值通過驗證;若有樣本有菌生長,則計算的KT值沒有通過驗證。