2 英文參考
Analytical method and evaluation requirements of antiviral drugs in disinfectant and antibacterial and bacteriostatic agents
3 基本信息
ICS 11.080
C 50
WS
中華人民共和國衛生行業標準WS/T 686—2020《消毒劑與抗抑菌劑中抗病毒藥物檢測方法與評價要求》(Analytical method and evaluation requirements of antiviral drugs in disinfectant and antibacterial and bacteriostatic agents)由中華人民共和國國家衛生健康委員會於2020年07月20日發佈,自2021年02月01日起實施。
4 發佈通告
關於發佈《消毒試驗用微生物要求》等4項推薦性衛生行業標準的通告
國衛通2020年14號
現發佈《消毒試驗用微生物要求》等4項推薦性衛生行業標準,編號和名稱如下:
WS/T 683—2020消毒試驗用微生物要求
WS/T 684—2020消毒劑與抗抑菌劑中抗菌藥物檢測方法與評價要求
WS/T 685—2020消毒劑與抗抑菌劑中抗真菌藥物檢測方法與評價要求
WS/T 686—2020消毒劑與抗抑菌劑中抗病毒藥物檢測方法與評價要求
上述標準自2021年2月1日起施行。
特此通告。
國家衛生健康委
2020年7月20日
5 前言
本標準按照 GB/T1.1—2009 給出的規則起草。
本標準起草單位:北京市疾病預防控制中心、中國計量科學研究院、北京市理化分析測試中心、中國食品藥品檢定研究院、江蘇省疾病預防控制中心、中國疾病預防控制中心、山東省疾病預防控制中心。
本標準主要起草人:丁曉靜、王萍、楊奕、高運華、趙新穎、勾新磊、牛夏夢、李莉、李碩、李潔、趙珊、徐燕、李放、張流波、李炎、崔樹玉、蘇冠民。
6 標準正文
6.1 1 範圍
本標準規定了消毒劑與抗抑菌劑中抗病毒藥物的檢測方法和評價要求。
本標準適用於消毒劑與抗抑菌劑中更昔洛韋、阿昔洛韋、噴昔洛韋和利巴韋林及其它抗病毒藥物的測定和評價。
6.2 2 規範性引用文件
下列文件對於本標準的應用是必不可少的。凡是注日期的引用文件,僅注日期的版本適用於本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
6.3 3 術語和定義
下列術語和定義適用於本文件。
3.1
抗病毒藥物 antiviral drugs
6.4 4 更昔洛韋、阿昔洛韋和噴昔洛韋的檢測方法
6.4.1 4.1 高效液相色譜法
6.4.1.1 4.1.1 原理
以乙酸甲醇混合溶液超聲提取試樣中的更昔洛韋、阿昔洛韋和噴昔洛韋,提取液經離心、過濾,C18色譜柱分離,紫外檢測器或二極管陣列檢測器檢測,外標法定量。
6.4.1.2 4.1.2 試劑和材料
除另有說明,本方法所用試劑均爲分析純,水爲 GB/T 6682 規定的一級水。
4.1.2.1 試劑
4.1.2.1.1 甲醇(CH3OH):色譜純。
4.1.2.1.2 冰乙酸(CH3COOH)。
4.1.2.1.3 乙酸銨(CH3COONH4)。
4.1.2.2 試劑配製
4.1.2.2.1 樣品提取溶液:分別移取甲醇 80 mL 和冰乙酸 10 mL,置於試劑瓶中,加入水 10 mL,混勻。
4.1.2.2.2 乙酸銨乙酸緩衝溶液:稱取乙酸銨 0.77 g,置於試劑瓶中,加入水 400 mL 溶解,再加入冰乙酸 2 mL,加水至 500 mL,混勻。
4.1.2.3 標準品
更昔洛韋、阿昔洛韋和噴昔洛韋純度均大於 97%或經國家認證並授予證書的標準物質,其它相關信息參見附錄 A。
4.1.2.4 標準溶液配製
4.1.2.4.1 標準儲備液:準確稱取更昔洛韋、阿昔洛韋和噴昔洛韋各 25.0 mg,分別置於 50 mL 容量瓶中,加入樣品提取溶液約 40 mL,超聲 10 min,溶解,用樣品提取溶液定容至刻度,配製成質量濃度均爲 500 mg/L 的標準儲備液。冷藏保存,有效期爲 3 個月。
4.1.2.4.2 混合標準中間液:分別移取更昔洛韋、阿昔洛韋和噴昔洛韋標準儲備液,用樣品提取溶液稀釋成質量濃度均爲 50 mg/L 的混合標準中間液。冷藏保存,有效期爲 1 個月。
4.1.2.4.3 混合標準系列溶液:取不同體積的混合標準中間液,用樣品提取溶液稀釋成混合標準系列溶液,如 0.5 mg/L、2.5 mg/L、5.0 mg/L、10.0 mg/L、20.0 mg/L。臨用現配。
4.1.2.5 材料
4.1.2.5.1 有機系濾膜:孔徑爲 0.45 m。
4.1.2.5.2 玻璃珠:Φ<5 mm。
6.4.1.3 4.1.3 儀器和設備
4.1.3.1 高效液相色譜儀:帶二極管陣列檢測器或紫外檢測器。
4.1.3.3 離心機:≥3 000 r/min。
4.1.3.4 渦旋混合器。
4.1.3.5 超聲波清洗器。
6.4.1.4 4.1.4 分析步驟
4.1.4.1 樣品前處理
4.1.4.1.1 液體劑型
稱取0.5 g(精確至1 mg)試樣於10 mL具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL刻度,渦旋混勻1 min,超聲10 min,經濾膜過濾,備用。
4.1.4.1.2 其它劑型
稱取 0.5 g(精確至 1 mg)試樣於 10 mL 具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL 刻度,加入 1 至 2 顆玻璃珠,渦旋混勻至溶液呈均勻狀態,超聲 10 min,離心 5 min,取上清液經濾膜過濾,備用。
4.1.4.2 高效液相色譜參考條件
高效液相色譜參考條件如下:
a) 色譜柱:C18柱(柱長 250 mm,內徑 4.6 mm,粒徑 5 m),或相當者;
c) 流速:1.0 mL/min;
d) 柱溫:30℃;
e) 進樣體積:5 L;
f) 檢測波長:254 nm;
4.1.4.3 標準曲線的製作
將混合標準系列溶液,按濃度由低到高依次注入高效液相色譜儀,以色譜峯的峯面積爲縱座標,與其對應的質量濃度爲橫座標,繪製峯面積—質量濃度(mg/L)標準曲線。更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液的高效液相色譜圖參見附錄 C.1。
4.1.4.4 測定
將處理好的試樣溶液注入高效液相色譜儀,根據標準曲線計算試樣溶液中目標化合物的質量濃度。
4.1.4.5 結果計算和表述

式中:
X——試樣中目標化合物的含量,單位爲毫克每千克(mg/kg);
ρ——標準曲線計算的試樣溶液中目標化合物的質量濃度,單位爲毫克每升(mg/L);
V——定容體積,單位爲毫升(mL);
m——稱樣量,單位爲克(g)。
結果保留三位有效數字。
4.1.4.6 精密度
在重複條件下獲得的兩次獨立測定結果的絕對差值不應超過算術平均值的10%。本方法回收率和精密度見附錄D。
當取樣量爲0.5 g,定容體積爲10 mL,本方法的檢出限和定量限:更昔洛韋、阿昔洛韋和噴昔洛韋的檢出限均爲2.0 mg/kg;定量限均爲7.0 mg/kg。
6.4.2 4.2 膠束電動毛細管色譜法
6.4.2.1 4.2.1 原理
以含有十二烷基硫酸鈉的樣品提取溶液提取試樣中的更昔洛韋、阿昔洛韋和噴昔洛韋,用膠束電動毛細管色譜分離模式進行分離,紫外檢測器或二極管陣列檢測器檢測,外標法定量。
6.4.2.2 4.2.2 試劑和材料
除另有說明,本方法所用試劑均爲分析純,水爲 GB/T 6682 規定的一級水。
4.2.2.1 試劑
4.2.2.1.1 十二烷基硫酸鈉(SDS,C12H25SO4Na)。
4.2.2.1.2 硼砂(Na2B4O7·10H2O)。
4.2.2.1.3 無水磷酸二氫鈉(NaH2PO4)。
4.2.2.1.4 氫氧化鈉(NaOH)。
4.2.2.2 試劑配製
4.2.2.2.1 分離緩衝溶液:稱取 SDS 2.019 g、硼砂 0.191 g 和無水磷酸二氫鈉 0.150 g,置於同一具塞帶刻度塑料離心管中,加水至 50 mL 刻度,超聲溶解、混勻,配製成含有 140 mmol/L SDS、10 mmol/L硼砂和 25 mmol/L 磷酸二氫鈉的分離緩衝溶液。
4.2.2.2.2 樣品提取溶液:將分離緩衝溶液用水稀釋 10 倍,配製成樣品提取溶液。
4.2.2.2.3 氫氧化鈉溶液:稱取氫氧化鈉 2 g,加入預先裝有 40 mL 水的塑料離心管中,振搖溶解,再加水至 50 mL 刻度、混勻,配製成 1 mol/L 氫氧化鈉溶液。
4.2.2.3 標準品
同4.1.2.3。
4.2.2.4 標準溶液配製
4.2.2.4.1 標準儲備液:準確稱取更昔洛韋、阿昔洛韋和噴昔洛韋各 10.0 mg,分別置於 10 mL 容量瓶中,加入樣品提取溶液約 5 mL,振搖(或超聲)溶解,用樣品提取溶液定容至刻度,配製成質量濃度均爲 1000 mg/L 的標準儲備液。臨用現配。
4.2.2.4.2 混合標準中間液:分別移取更昔洛韋、阿昔洛韋和噴昔洛韋標準儲備液,用樣品提取溶液稀釋成質量濃度均爲 100 mg/L 的混合標準中間液。臨用現配。
4.2.2.4.3 混合標準系列溶液:取不同體積的混合標準中間液,用樣品提取溶液稀釋成混合標準系列溶液,如 1.0 mg/L、5.0 mg/L、10.0 mg/L、20.0 mg/L、40.0 mg/L。臨用現配。
4.2.2.5 材料
同4.1.2.5。
6.4.2.3 4.2.3 儀器和設備
4.2.3.1 毛細管電泳儀:帶二極管陣列檢測器或紫外檢測器。
4.2.3.2 未塗層熔融石英毛細管:內徑 50 m,外徑 375 m。
4.2.3.3 同 4.1.3.2。
4.2.3.4 同 4.1.3.4。
4.2.3.5 同 4.1.3.5。
6.4.2.4 4.2.4 分析步驟
4.2.4.1 樣品預處理
4.2.4.1.1 液體劑型
稱取0.5 g(精確至1 mg)試樣於10 mL具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL刻度,渦旋混勻1 min,超聲10 min,備用。
4.2.4.1.2 其它劑型
稱取0.5 g(精確至1 mg)試樣於10 mL具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL刻度,加入1至2顆玻璃珠,渦旋混勻至溶液呈均勻狀態,超聲10 min,備用。
4.2.4.2 毛細管電泳參考條件
毛細管電泳參考條件如下:
a) 分離柱:未塗層熔融石英毛細管,302 mm(有效長度爲 200 mm);
b) 電壓:10 kV;
c) 進樣壓力:3.448 kPa;
d) 進樣時間:4 s(進樣體積約 7.9 nL);
e) 檢測波長:254 nm;
f) 清洗程序:新裝毛細管在使用前分別用 NaOH 溶液沖洗 20 min,水沖洗 5 min,分離緩衝溶液沖洗 5 min。每次進樣前依次用 NaOH 溶液沖洗 1.5 min,水沖洗 1.5 min,分離緩衝溶液沖洗1.5 min。
4.2.4.3 標準曲線的製作
將混合標準系列溶液,按濃度由低到高依次注入毛細管電泳儀,以色譜峯的校正峯面積(峯面積除以遷移時間)爲縱座標,與其對應的質量濃度爲橫座標,繪製校正峯面積—質量濃度(mg/L)標準曲線。更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液的毛細管電泳圖參見附錄 E.1。
4.2.4.4 測定
將處理好的試樣溶液注入毛細管電泳儀,根據標準曲線計算試樣溶液中目標化合物的質量濃度。
4.2.4.5 結果計算和表述
結果保留三位有效數字。
4.2.4.6 精密度
在重複條件下獲得的兩次獨立測定結果的絕對差值不應超過算術平均值的 10%。
當取樣量爲 0.5 g,定容體積爲 10 mL,本方法的檢出限和定量限:更昔洛韋、阿昔洛韋和噴昔洛韋的檢出限均爲 4.0 mg/kg;定量限均爲 14.0 mg/kg。
6.4.3 4.3 超高效液相色譜-串聯質譜確證方法
6.4.3.1 4.3.1 原理
以乙酸甲醇混合溶液超聲提取試樣中的更昔洛韋、阿昔洛韋和噴昔洛韋,經離心、過濾,用超高效液相色譜-串聯質譜儀進行確證。
6.4.3.2 4.3.2 試劑和材料
除另有規定外,所有試劑均爲分析純,水爲符合 GB/T 6682 中規定的一級水。
4.3.2.1 試劑
4.3.2.1.1 甲醇(CH3OH):色譜純。
4.3.2.1.2 甲酸(HCOOH):色譜純。
4.3.2.1.3 冰乙酸(CH3COOH)。
4.3.2.2 試劑配製
4.3.2.2.1 同 4.1.2.2.1。
4.3.2.2.2 0.1 %甲酸甲醇溶液:100 mL 甲醇中加入 0.1 mL 甲酸,混勻。
4.3.2.2.3 0.1 %甲酸水溶液:100 mL 水中加入 0.1 mL 甲酸,混勻。
4.3.2.3 標準品
同 4.1.2.3。
4.3.2.4 標準溶液配製
4.3.2.4.1 同 4.1.2.4.1。
4.3.2.4.2 混合標準中間液:分別移取更昔洛韋、阿昔洛韋和噴昔洛韋標準儲備液,用水釋成質量濃度均爲 5 mg/L 的混合標準中間液。冷藏保存,有效期爲 1 個月。
4.3.2.4.3 混合標準應用液:將混合標準中間液用水稀釋 100 倍,配成質量濃度均爲 50 g/L 的混合標準應用液。臨用現配。
4.3.2.5 材料
4.3.2.5.1 有機系濾膜:孔徑爲 0.22 m。
4.3.2.5.2 同 4.1.2.5.2。
6.4.3.3 4.3.3 儀器和設備
4.3.3.1 超高效液相色譜-串聯質譜儀:帶電噴霧離子源。
4.3.3.2 同 4.1.3.2。
4.3.3.3 同 4.1.3.3。
4.3.3.4 同 4.1.3.4。
4.3.3.5 同 4.1.3.5。
4.3.4 分析步驟
4.3.4.1 樣品前處理
4.3.4.1.1 液體劑型
稱取 0.5 g(精確至 1 mg)試樣於 10 mL 具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL 刻度,渦旋混勻 1 min,超聲 10 min,經濾膜過濾,濾液用水稀釋至少 10 倍,混勻,備用。
4.3.4.1.2 其它劑型
稱取 0.5 g(精確至 1 mg)試樣於 10 mL 具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL 刻度,加入 1 至 2 顆玻璃珠,渦旋混勻至溶液呈均勻狀態,超聲 10 min,離心 5 min,上清液經濾膜過濾,將濾液用水稀釋至少 10 倍,混勻,備用。
4.3.4.2 超高效液相色譜參考條件
超高效液相色譜參考條件如下:
a) 色譜柱:C18(柱長 50 mm,內徑 2.1 mm,粒徑 1.7 m),或相當者;
b) 流動相:A 相爲 0.1 %甲酸甲醇溶液;B 相爲 0.1 %甲酸水溶液;
c) 流速:0.3 mL/min;
d) 柱溫:40℃;
e) 進樣量:5 L;
4.3.4.3 質譜參考條件
質譜參考條件如下:
a) 電離方式:ESI+;
b) 脫溶劑氣溫度:350℃;
c) 乾燥氣流量:550 L/h;
d) 碰撞氣流量:0.15 mL/min;
e) 毛細管電壓:3.5 kV;
g) 其它質譜參數:見附錄 F.1。
4.3.4.4 混合標準應用液測定
將均爲 50 g/L 的混合標準應用液注入超高效液相色譜-串聯質譜儀。質譜色譜圖參見附錄 C.2。
4.3.4.5 確證
將處理好的試樣溶液注入超高效液相色譜-串聯質譜儀。在相同測試條件下,試樣中目標化合物色譜峯的保留時間與相應標準色譜峯的保留時間相比較,變化範圍應在±2.5%之內,且檢測到的離子相對丰度,應與濃度相當的標準溶液中相對離子丰度一致。其相對丰度比偏差應符合表1要求。
表1 相對離子丰度的最大允許偏差
| 相對離子丰度(A,%) | >50 | 20<A≤50 | 10<A≤20 | ≤10 |
| 允許的最大偏差(%) | ±20 | ±25 | ±30 | ±50 |
4.3.4.6 檢出限
當取樣量爲 0.5 g,定容體積爲 10 mL,本方法的檢出限:更昔洛韋、阿昔洛韋和噴昔洛韋均爲 20.0g/kg。
6.5 5 利巴韋林的檢測方法
6.5.1 5.1 電滲流反轉的毛細管電泳法
5.1.1 原理
以含有硼酸和硼砂的樣品提取溶液提取試樣中的利巴韋林,用電滲流反轉的區帶電泳分離模式進行分離,紫外檢測器或二極管陣列檢測器檢測,外標法定量。
5.1.2 試劑和材料
除另有規定外,所有試劑均爲分析純,水爲符合 GB/T 6682 中規定的一級水。
5.1.2.1 試劑
5.1.2.1.1 硼酸(H3BO3)。
5.1.2.1.2 硼砂(Na2B4O7·10H2O)。
5.1.2.1.3 十六烷基三甲基溴化銨(CTAB,C19H42BrN)。
5.1.2.1.4 氫氧化鈉(NaOH)。
5.1.2.2 試劑配製
5.1.2.2.1 分離緩衝溶液:稱取硼酸 0.309 g、硼砂 1.144 g 和 CTAB 0.009 g,置於同一具塞帶刻度塑料離心管中,加水約 40 mL 振搖溶解,再加水至 50 mL 刻度,混勻,配製成含有 100 mmol/L 硼酸、60 mmol/L 硼砂和 0.5 mmol/L CTAB 的分離緩衝溶液。
5.1.2.2.2 樣品提取溶液:將分離緩衝溶液用水稀釋 10 倍,配製成樣品提取溶液。
5.1.2.2.3 同 4.2.2.2.3。
5.1.2.3 標準品
利巴韋林純度大於97%或經過國家認證並授予證書的標準物質,其它相關信息參見附錄A。
5.1.2.4 標準溶液配製
5.1.2.4.1 標準儲備液:準確稱取利巴韋林 10.0 mg,置於 10 mL 容量瓶中,加入水約 5 mL 振搖溶解,再用水定容至刻度,配製成質量濃度爲 1000 mg/L 的標準儲備液。冷藏保存,有效期爲 3 個月。
5.1.2.4.2 標準中間液:將利巴韋林標準儲備液用樣品提取溶液稀釋 10 倍,配製成質量濃度爲 100mg/L 的標準中間液。臨用現配。
5.1.2.4.3 標準系列溶液:取不同體積的利巴韋林標準中間液,用樣品提取溶液稀釋成混合標準系列溶液,如 1.5 mg/L、5.0 mg/L、10.0 mg/L、20.0 mg/L、50.0 mg/L。臨用現配。
5.1.2.5 材料
同4.1.2.5.2。
5.1.3 儀器和設備
5.1.3.1 毛細管電泳儀:帶二極管陣列檢測器或紫外檢測器。
5.1.3.2 未塗層熔融石英毛細管:內徑 50 m,外徑 375 m。
5.1.3.3 同 4.1.3.2。
5.1.3.4 同 4.1.3.4。
5.1.3.5 同 4.1.3.5。
5.1.4 分析步驟
5.1.4.1 樣品前處理
5.1.4.1.1 液體劑型
稱取0.5 g(精確至1 mg)試樣於10 mL具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL刻度,渦旋混勻1 min,超聲10 min,備用。
5.1.4.1.2 膏體劑型
稱取0.2 g(精確至1 mg)試樣於10 mL具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL刻度,加入1至2顆玻璃珠,渦旋混勻至溶液呈均勻狀態,超聲10 min,備用。
5.1.4.1.3 其它劑型
稱取0.5 g(精確至1 mg)試樣於10 mL具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL刻度,加入1至2顆玻璃珠,渦旋混勻至溶液呈均勻狀態,超聲10 min,備用。
5.1.4.2 毛細管電泳參考條件:
a) 未塗層熔融石英毛細管,700 mm(有效長度爲 600 mm);
b) 電壓:29 kV;
c) 進樣壓力:3.448 kPa;
d) 進樣時間:20 s(進樣體積約 17 nL);
e) 檢測波長:214 nm;
f) 清洗程序:新裝毛細管在使用前分別用 NaOH 溶液沖洗 20 min,水沖洗 5 min,分離緩衝溶液沖洗 5 min。每次進樣前依次用 NaOH 沖洗 1.5 min,水沖洗 1.5 min,分離緩衝溶液沖洗 1.5 min。
5.1.4.3 標準曲線的製作
將標準系列溶液,按濃度由低到高依次注入毛細管電泳儀,以色譜峯的校正峯面積(峯面積除以遷移時間)爲縱座標,與其對應的質量濃度爲橫座標,繪製校正峯面積—質量濃度(mg/L)標準曲線。利巴韋林標準溶液的毛細管電泳圖參見附錄 E.2。
5.1.4.4 測定
將處理好的試樣溶液注入毛細管電泳儀,根據標準曲線計算試樣溶液中利巴韋林的質量濃度。
5.1.4.5 結果計算和表述
結果保留三位有效數字。
5.1.4.6 精密度
在重複條件下獲得的兩次獨立測定結果的絕對差值不應超過算術平均值的 10%。
膏體試樣:當取樣量爲 0.20 g,定容體積爲 10 mL,本方法的檢出限爲 20 mg/kg,定量限爲 70 mg/kg;其它試樣:當取樣量爲 0.50 g,定容體積爲 10 mL,本方法的檢出限爲 8 mg/kg,定量限爲 30 mg/kg。
6.5.2 5.2 超高效液相色譜-串聯質譜確證方法
5.2.1 原理
以甲醇水混合溶液超聲提取試樣中的利巴韋林,經 C18-固相萃取柱淨化,用超高效液相色譜-串聯
質譜儀進行確證。
5.2.2 試劑和材料
除另有規定外,所有試劑均爲分析純,水爲符合 GB/T 6682 中規定的一級水。
5.2.2.1 試劑
5.2.2.1.1 甲醇(CH3OH):色譜純。
5.2.2.1.2 甲酸(HCOOH):色譜純。
5.2.2.1.3 乙腈(CH3CN):色譜純。
5.2.2.2 試劑配製
5.2.2.2.1 樣品提取溶液:將甲醇 10 mL 與水 90 mL 混勻。
5.2.2.2.2 0.1%甲酸水溶液:往 100 mL 水中加入甲酸 0.1 mL,混勻。
5.2.2.3 標準品
同 5.1.2.3。
5.2.2.4 標準溶液配製
5.2.2.4.1 標準儲備液:準確稱取利巴韋林 10.0 mg,置於 10 mL 容量瓶中,加入約 5 mL 水振搖溶解,用水定容至刻度,配製成質量濃度爲 1000 mg/L 的標準儲備液,冷藏保存,有效期爲 3 個月。
5.2.2.4.2 標準中間液:將利巴韋林標準儲備液,用樣品提取溶液稀釋成質量濃度爲 5 mg/L 的標準中間液。冷藏保存,有效期爲 1 個月。
5.2.2.4.3 標準應用液:將利巴韋林標準中間液用樣品提取液稀釋 100 倍,配成質量濃度均爲 50 g/L的標準應用液。臨用現配。
5.2.2.5 材料
5.2.2.5.1 C18固相萃取小柱:3 mL,200 mg。
5.2.2.5.2 同 4.3.2.5.1。
5.2.2.5.3 同 4.1.2.5.2。
5.2.3 儀器和設備
5.2.3.1 超高效液相色譜-串聯質譜儀:帶電噴霧離子源(ESI)。
5.2.3.2 同 4.1.3.2。
5.2.3.3 同 4.1.3.3。
5.2.3.4 同 4.1.3.4。
5.2.3.5 同 4.1.3.5。
5.2.4 分析步驟
5.2.4.1 樣品前處理
5.2.4.1.1 液體劑型
稱取 0.5 g(精確至 1 mg)試樣於 10 mL 具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL 刻度,渦旋混勻 1 min,超聲 10 min,經濾膜過濾,濾液用水稀釋至少 10 倍,混勻,過 C18-固相萃取小柱,濾液備用。
5.2.4.1.2 其它劑型
稱取 0.5 g(精確至 1 mg)試樣於 10 mL 具塞帶刻度離心管(比色管)中,加入樣品提取溶液至10 mL 刻度,加入 1 至 2 顆玻璃珠,渦旋混勻至溶液呈均勻狀態,超聲 10 min,離心 5 min,上清液經濾膜過濾,將濾液用水稀釋至少 10 倍,混勻,過 C18-固相萃取小柱,濾液備用。
5.2.4.2 超高效液相色譜參考條件
超高效液相色譜參考條件如下:
a) 色譜柱:C18(柱長 100 mm,內徑 2.1 mm,粒徑 1.8 m),或相當者;
b) 流動相:A 相爲乙腈;B 相爲 0.1 %甲酸水溶液;
c) 流速:0.3 mL/min;
d) 柱溫:40℃;
e) 進樣量:5 L;
5.2.4.3 質譜參考條件:
a) 電離方式:ESI+;
b) 脫溶劑氣溫度:350℃;
c) 乾燥氣流量:550 L/h;
d) 碰撞氣流量:0.15 mL/min;
e) 毛細管電壓:3.5 kV;
g) 其它質譜參數:見附錄 F.2。
5.2.4.4 標準應用液測定
將 50 g/L 混合標準應用液注入超高效液相色譜-串聯質譜儀。質譜色譜圖參見附錄 C.3。
5.2.4.4.1 確證
同4.3.4.5。
5.2.4.5 檢出限
當取樣量爲0.5 g,定容體積爲10 mL,檢出限爲20.0 g/kg。
6.6 6 其它抗病毒藥物的檢測方法
《中華人民共和國藥典》未涵蓋的檢測方法,可參考文獻報道的方法,並通過認證後方可應用。
6.7 7 評價要求
7 附錄
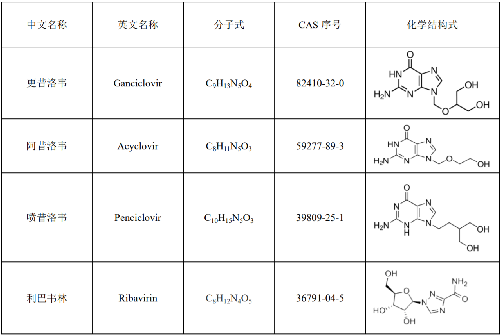
7.1 附錄A(資料性附錄)標準品相關信息
更昔洛韋、阿昔洛韋、噴昔洛韋和利巴韋林標準品的相關信息見表A.1。
表A.1 更昔洛韋、阿昔洛韋、噴昔洛韋和利巴韋林標準品的相關信息
7.2 附錄B(規範性附錄)色譜梯度洗脫程序
B.1 阿昔洛韋、更昔洛韋和噴昔洛韋高效液相色譜法的梯度洗脫程序見表B.1。
表 B.1 阿昔洛韋、更昔洛韋和噴昔洛韋的高效液相色譜法的梯度洗脫程序
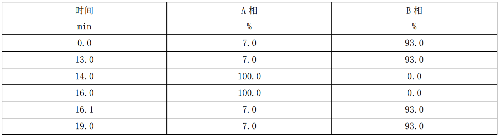
B.2 阿昔洛韋、更昔洛韋和噴昔洛韋的超高效液相色譜-串聯質譜確證法的梯度洗脫程序見表B.2。
表 B.2 阿昔洛韋、更昔洛韋和噴昔洛韋的超高效液相色譜-串聯質譜確證法的梯度洗脫程序
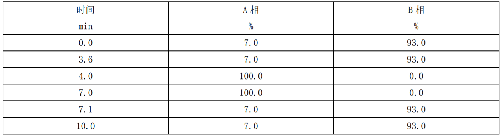
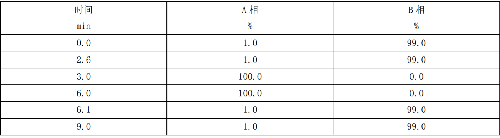
B.3 利巴韋林的超高效液相色譜-串聯質譜確證法的梯度洗脫程序見表B.3。
表 B.3 利巴韋林的超高效液相色譜-串聯質譜確證法的梯度洗脫程序
7.3 附錄C(資料性附錄)色譜圖
C.1 更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液 20 mg/L的高效液相色譜圖見圖 C.1

C.2 更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液 50 μg/L的超高效液相色譜-串聯質譜色譜圖見圖C.2

圖 C.2 更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液的超高效液相色譜-串聯質譜色譜圖
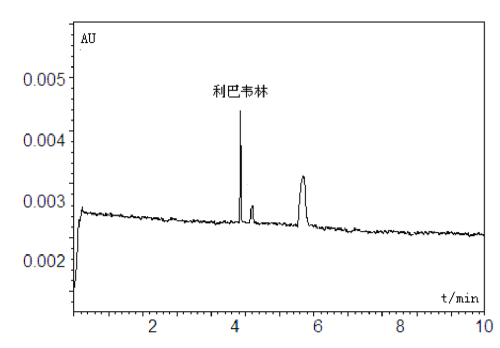
C.3 利巴韋林標準溶液 50 g/L的超高效液相色譜-串聯質譜色譜圖見圖 C.3

圖 C.3 利巴韋林標準溶液的超高效液相色譜-串聯質譜色譜圖
7.4 附錄D(規範性附錄)回收率與精密度
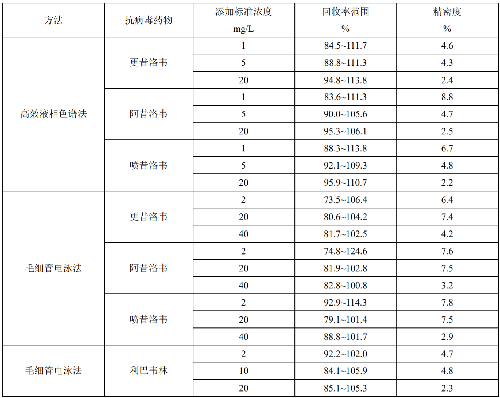
更昔洛韋、阿昔洛韋、噴昔洛韋和利巴韋林的回收率與精密度見表D.1。
表 D.1 更昔洛韋、阿昔洛韋、噴昔洛韋和利巴韋林的回收率與精密度
7.5 附錄E(資料性附錄)電泳圖
E.1 更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液 20 mg/L的電泳圖見圖E.1。

圖 E.1 更昔洛韋、阿昔洛韋和噴昔洛韋混合標準溶液的電泳圖
7.6 附錄F(資料性附錄)其它質譜參數
F.1 更昔洛韋、阿昔洛韋和噴昔洛韋的超高效液相色譜-串聯質譜法的其它質譜參數見表F.1。
表F.1 更昔洛韋、阿昔洛韋和噴昔洛韋的超高效液相色譜-串聯質譜法的其它質譜參數

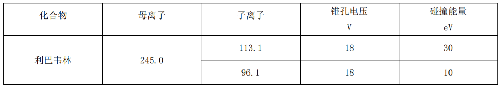
F.2 利巴韋林的超高效液相色譜-串聯質譜法的其它質譜參數見表F.2。
表F.2 更昔洛韋、阿昔洛韋和噴昔洛韋的超高效液相色譜-串聯質譜法的其它質譜參數