2 英文參考
Evaluation requirement of indicators for medical purpose-low temperature steam and formaldehyde sterilization processes
3 基本信息
ICS 11.080
C 59
中華人民共和國衛生行業標準WS/T 651—2019《醫用低溫蒸汽甲醛滅菌指示物評價要求》(Evaluation requirement of indicators for medical purpose-low temperature steam and formaldehyde sterilization processes)由中華人民共和國國家衛生健康委員會於2019年01月30日《關於發佈〈過碳酸鈉消毒劑衛生要求〉等6項推薦性衛生行業標準的通告》(國衛通〔2019〕4號)發佈,自2019年07月01日起實施。
4 發佈通知
關於發佈《過碳酸鈉消毒劑衛生要求》等6項推薦性衛生行業標準的通告
國衛通〔2019〕4號
現發佈《過碳酸鈉消毒劑衛生要求》等6項推薦性衛生行業標準,編號和名稱如下:
WS/T 647—2019 溶葡萄球菌酶和溶菌酶消毒劑衛生要求
WS/T 651—2019 醫用低溫蒸汽甲醛滅菌指示物評價要求
上述標準自2019年7月1日起施行。
特此通告。
國家衛生健康委員會
2019年1月30日
5 前言
本標準按照 GB/T1.1—2009 給出的規則起草。
本標準起草單位:山東省疾病預防控制中心、中國疾病預防控制中心環境與健康相關產品安全所、江蘇省疾病預防控制中心、山東省精神衛生中心、廣東檢驗檢疫技術中心、臨沭縣安全生產監督管理局、濰坊醫學院。
本標準主要起草人:崔樹玉、楊彬、張流波、李子堯、劉雷、蘇冠民、孫文魁、張劍、沈瑾、孫惠惠、陳璐、董非、孟蔚、趙克義、溫憲芹、徐燕、孫啓華、廖如燕、田忠梅、劉曉康、周建芳、鄒以華、楊靜、謝卡羅、王曉雲。
6 標準正文
6.1 1 範圍
本標準規定了醫用低溫蒸汽甲醛滅菌指示物的分類、通用要求、化學指示物要求及生物指示物要求。
本標準適用於通過化學、生物指標的變化反映醫用低溫蒸汽甲醛滅菌過程的指示物。
6.2 2 規範性引用文件
下列文件對於本文件的應用是必不可少的。凡是注日期的引用文件,僅所注日期的版本適用於本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改單)適用於本文件。
GB 18281.1 醫療保健產品滅菌 生物指示物 第1部分:通則
消毒產品標籤介紹管理規範(2005年) 衛生部(衛監督發〔2005〕426號)
6.3 3 術語和定義
下列術語和定義適用於本文件。
3.1
低溫蒸汽甲醛滅菌 low temperature steam and formaldehyde sterilization
在溫度低於85℃時,強制排出空氣後,負壓狀態下注入蒸汽甲醛,待滅菌物品暴露於蒸汽甲醛,在穩定的狀態下維持一定時間,達到滅菌要求。
3.2
化學指示物 chemical indicator
指示劑及其載體按預定形式的組合,暴露於低溫蒸汽甲醛滅菌程序中一個或多個預定過程變量而產生化學或物理變化。
3.3
生物指示物 biological indicator
3.4
D值 D value
3.5
3.6
6.4 4 指示物分類
6.4.1 4.1 化學指示物
6.4.1.1 4.1.1 滅菌過程指示物
指示每個獨立單元的滅菌物品是否經過滅菌程序,包括卡、膠帶、標籤等。
6.4.1.2 4.1.2 滅菌效果指示物
用於證明獨立單元物品經過整個滅菌程序後,是否達到所選參數的設定值。
6.4.2 4.2 生物指示物
4.2.1 按結構可分爲片狀生物指示物和自含式生物指示物,片狀生物指示物需要使用陽性對照和陰性對照,而自含式生物指示物只需要陽性對照即可。
4.2.2 按培養時間可分爲常規型生物指示物和快速型生物指示物。
6.5 5 指示物通用要求
5.1 醫用低溫蒸汽甲醛滅菌過程評價參數應包括作用時間、溫度、甲醛濃度。
5.2 包裝標籤和介紹應符合《消毒產品標籤介紹管理規範》的要求。
5.3 指示物應標明其用途。
5.4 指示物應根據使用用途與不同的過程挑戰裝置相組合,模擬滅菌因子最難達到的部位。
5.5 指示物應標明儲存條件和效期。
5.6 經符合各項預設參數的滅菌週期後,指示物變化應與生產商規定的合格要求一致;若預設的最低限度參數不符合或預設的參數不合理,則指示物變化應與生產商規定的合格要求不一致。
5.7 用於日常監測的生物指示物應與化學指示物同時使用,二者均合格,才能視爲達到滅菌效果。
5.8 指示物包裝材料和載體應避免選擇對甲醛有吸附作用的材質,且應不影響指示物的使用,確保其無害。
5.9 取包裝完好的指示物放置於生產商標明儲存條件下,存放至規定的效期,取出再次進行評價,指示物應滿足本標準規定的技術要求。
6.6 6 化學指示物要求
6.6.1 6.1 滅菌過程化學指示物
滅菌過程化學指示物應按表1設定的條件進行測試並符合要求。測定方法見附錄A。
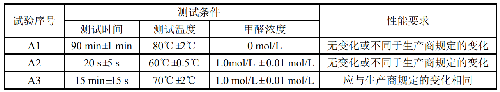
注1:若過程化學指示物僅標明在低於 55℃或高於 65℃的溫度下滅菌週期使用,則表 1 中的測試應在生產商規定的最高溫度和甲醛濃度下進行。
注2:爲了證明對特殊過程的適用性,應增加生產商規定的低溫蒸汽甲醛滅菌程序進行附加的功能測試。
6.6.2 6.2 滅菌效果化學指示物
滅菌效果化學指示物應按表2設定的條件進行測試並符合要求。測定方法見附錄A。
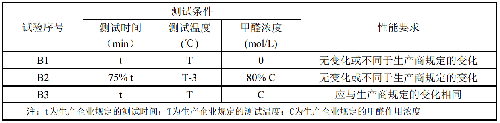
注:t爲生產企業規定的測試時間;T爲生產企業規定的測試溫度;C爲生產企業規定的甲醛作用濃度
6.7 7 生物指示物要求
6.7.1 7.1 指示菌
7.1.1 指示菌株應爲嗜熱脂肪地芽胞桿菌或者是相當性能的其他菌株。推薦嗜熱脂肪地芽胞桿菌有NCIB 8224、 DSM 6790、 ATCC 7953、 ATCC 10149 和 ATCC 12980 用於試驗,製備成芽胞。如果使用其他的菌株,應首先測定其抗力。
7.1.2 由生產企業提供的最終產品應無雜菌。
6.7.2 7.2 指示菌數量和抗力
7.2.1 生產企業應標明指示菌的數量和抗力特性。
7.2.2 指示菌活菌數應≥1.0×105CFU/載體。對於成品的指示物,載體回收的菌量與介紹上的菌量誤差在–50%~+300%之間。測定方法見附錄 B。
7.2.3 在 60℃條件下,以時間(min)爲單位的 D 值表示指示菌的抗力,精確到小數點後一位。每批次/批號的生物指示物或染菌載體都應標註相應的 D 值。
7.2.4 生物指示物中指示微生物的 D 值應≥6.0 min;其它指示微生物應當具有符合使用條件的 D 值。
測定方法見附錄 C。
7.2.5 D 值的驗證,按附錄 C 測定方法。ST 值驗證 D 值,樣本應全部有菌生長;KT 值驗證 D 值,樣本應全部無菌生長。ST 值和 KT 值分別按式(1)和式(2)計算。

式中:
ST——存活時間,單位爲分鐘(min);
KT——殺滅時間,單位爲分鐘(min);
N0——每批生物指示物的回收菌量的平均數,單位爲CFU/載體。
6.7.3 7.3 載體和內層包裝
7.3.1 測試應滿足下列條件:
a) 暴露溫度:同生產商規定載體和內層包裝的最高暴露溫度;如果生產商沒有規定,暴露溫度至少爲 100℃。
b) 暴露時間:至少爲 160 min。
7.3.2 在滅菌處理中及滅菌後,生物指示物系統的任何材料,不應殘留或釋放出任何抑制試驗菌生長的物質。測定方法按照 GB 18281.1 進行。
7 附錄A(規範性附錄)化學指示物檢測方法
7.1 A.1 檢測儀檢測法
A.1.1 檢測儀應能設置、監測與確認溫度、時間、甲醛濃度等參數。
A.1.2 滅菌過程化學指示物置於檢測儀內,按表1要求的測試條件進行測試;滅菌效果化學指示物置於檢測儀內,按表2要求的測試條件進行測試。
A.1.3 同批次化學指示物每次試驗測試不少於10個,試驗不少於3次。
7.2 A.2 甲醛溶液檢測法(僅適用於不具有吸水性能的材質製備的化學指示物檢測)
A.2.1 滅菌過程指示物根據6.1的要求配製甲醛水溶液,滅菌效果指示物根據6.2的要求配製甲醛水溶液。
A.2.3 將化學指示物置於固定的樣品架上,樣品架不應影響化學指示物的性能。
A.2.4 將樣品架置於預熱的甲醛溶液中,確保化學指示物浸泡在甲醛溶液裏,按6.1或6.2規定時間測試。
A.2.5 從甲醛溶液中取出樣品架,去除多餘的甲醛,1.5 min內指示物呈現的顏色維持在一定水平不再變化,檢測指示物的性能,記錄結果。
8 附錄B(規範性附錄)生物指示物活菌數測定
B.2 取含有 10mLTPS(0.1%胰蛋白腖的生理鹽水溶液)的無菌試管,加入適量無菌玻璃珠,將生物指示物染菌載體投入試管,用電動混合器充分混合,製成菌懸液。
B.3 選擇適宜稀釋度菌懸液,吸取其中混合均勻的懸液 1.0mL 加於無菌平皿內。每一稀釋度接種 2個平皿。一般需接種 2 個~3 個稀釋度。
B.4 將 40℃~45℃ 熔化的嗜熱脂肪桿菌芽胞恢復培養基或相應的培養基傾注於已加入菌懸液的平皿中,每平皿 15mL~20mL。
B.5 待瓊脂凝固後,翻轉平板使底向上,置 56℃±2℃恆溫培養箱內培養。
B.6 培養至 72h,計數菌落數。一般以肉眼觀察,必要時用放大鏡檢查。報告菌落數在 15CFU~300CFU 的稀釋度的結果。
9 附錄C(規範性附錄)微生物抗力測定方法
9.1 C.1 接種載體暴露條件
C.1.1 水溶液中甲醛濃度1mol/L±0.01mol/L。
C.1.2 暴露溫度60℃±0.5℃。
C.1.3 暴露時間能維持在1min~150min,精確度在±10s。
9.2 C.2 方法
C.2.1 取10mL甲醛溶液置於試管中,預先加熱至暴露溫度,將生物指示物載體完全浸入其中。
C.2.2 確保載體完全浸泡在甲醛溶液中,並儘量減少試管振動。
C.2.3 嚴格執行無菌操作。
C.2.5 去除載體表面多餘的液體後,將其置於含2%的亞硫酸鈉溶液中和劑中至少10min,用以中和殘留的甲醛溶液。密封試管,並儘量減少振動,以防止載體上的受試微生物脫落。
注:2%的亞硫酸鈉溶液可用過濾除菌的方式進行處理。也可使用其它驗證有效的中和劑。
C.2.6 選擇適合的培養基復甦受試微生物。建議選擇大豆酪蛋白消化培養基。
C.2.8 將試管置於90℃,60min。
C.2.9 活菌數測定,參見附錄B。
9.3 C.3 用微生物存活曲線法測定 D 值
C.3.2 至少有 5 次暴露,包括
b) 有 1 次暴露使活菌總數至少減少到初始接種量的 0.01%,且存活菌量大於 50CFU;
C.3.3 每 2 次相鄰暴露的時間間隔應相等。
C.3.4 每次測定中每次暴露所用的染菌載體應不少於4個,每次暴露必須採用數目相同的同樣的試樣。
C.3.5 每次暴露後,按 C.2.4~C.2.9 對試樣進行處理。
C.3.6 用所得的全部存活菌數的常用對數值,對時間 (min) 作圖,用最小二乘法進行迴歸分析,確定最佳線性曲線。迴歸分析時不應包括原先接種細菌數 0.51og 範圍內的存活數據點。計算所得直線斜率的負倒數值,即等於以分鐘表示的D值,數據舉例見表C.1。
C.3.6.1 最佳線性曲線斜率按式(C.1)計算:

式中:
m ——最佳線性曲線斜率;
n ——數據點之和;
A ——暴露間隔時間之和;
B ——存活菌數的對數值之和;
C ——暴露間隔時間平方之和。

注:迴歸分析時不應包括0.5 log10y1範圍內的存活數據點
C.3.6.2 D值按式(C.2)計算:
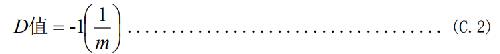
C.3.7 所得存活菌曲線的線性相關係數應不小於0.8。線性相關係數按式(C.3)計算:
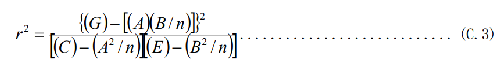
式中:
E ——存活菌數的對數值平方之和。
9.4 C.4 用部分陰性分析法計算D值
C.4.2 至少有5種暴露,包括:
C.4.3 每2次相鄰暴露的時間間隔應相等。
C.4.4 每次測定中每次暴露所用的染菌載體應不少於20個,每次暴露應採用相同數目同樣的試樣。
C.4.5 每次暴露後,試樣接種含中和劑的增菌液,按生產廠商規定的溫度和時間進行培養後觀察結果,數據示例見表C.2。
C.4.6 D值的計算
C.4.6.1 有限Holcomb-Spearman-Karber法(LHSKP),滅菌的平均時間按式(C.4)計算:
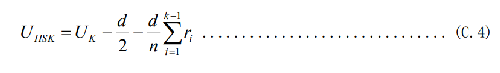
式中:
d —— 暴露的時間間隔,各間隔完全相同;
n —— 每次暴露的測試樣本量,要求每次暴露的樣本量相同,如均爲20個;
N0 —— 通過總活菌計數法(見附錄B)獲得的每個指示劑活菌計數的平均值;

C.4.6.3 方差按式(C.6)計算:

C.4.6.4 標準差按式(C.7)計算:

C.4.6.5 D 值95%的可信區間(p=0.05)Dcalc按式(C.8)計算:
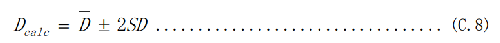
C.4.6.6 D值可信區間上限按式(C.9)計算:

C.4.6.7 D值可信區間下限按式(C.10)計算:

表C.2 LHSKP 測定 D 值數據示例

注:如果經過U1暴露(如沒有陰性樣本,r=0),且經過相繼暴露的UK所有重複試驗均爲陰性(r= n)(如都不生長),則測試爲有效。
9.5 C.5 D 值的驗證
C.5.1 ST 值驗證 D 值
將50個試驗樣本放入C.1 規定的暴露條件下,暴露時間設定爲計算出的ST值,暴露完成後,將樣本取出接種含中和劑的增菌液,按生產商規定的溫度和時間進行培養後觀察結果。
C.5.2 KT 值驗證 D 值
將50個試驗樣本放入C.1規定的暴露條件下,暴露時間設定爲計算出的KT值,暴露完成後,將樣本取出接種含中和劑的增菌液,按生產商規定的溫度和時間進行培養後觀察結果。