1 拼音
W S / T 4 0 4 . 1 0 — 2 0 2 2 lín chuáng cháng yòng shēng huà jiǎn yàn xiàng mù cān kǎo qū jiān dì 1 0 bù fèn : xuè qīng sān diǎn jiǎ zhuàng xiàn yuán ān suān 、 jiǎ zhuàng xiàn sù 、 yóu lí sān diǎn jiǎ zhuàng xiàn yuán ān suān 、 yóu lí jiǎ zhuàng xiàn sù 、 cù jiǎ zhuàng xiàn jī sù
2 英文參考
Reference intervals for common clinical biochemistry tests-Part 10: Serum triiodothyronine, thyroxine, free triiodothyronine, free thyroxine and thyroid stimulating hormone
3 基本信息
ICS 11.020
CCS C 50
中華人民共和國衛生行業標準
WS/T 404.10—2022《臨牀常用生化檢驗項目參考區間第10部分:血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素》(Reference intervals for common clinical biochemistry tests-Part 10: Serum triiodothyronine, thyroxine, free triiodothyronine, free thyroxine and thyroid stimulating hormone)由中華人民共和國國家衛生健康委員會於2022年12月29日發佈,自2023年06月01日起實施。
4 發佈通知
關於發佈推薦性衛生行業標準《臨牀常用生化檢驗項目參考區間第10部分:血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素》的通告
國衛通〔2022〕16號
現發佈推薦性衛生行業標準《臨牀常用生化檢驗項目參考區間第10部分:血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素》,編號和名稱如下:
WS/T 404.10—2022 臨牀常用生化檢驗項目參考區間第10部分:血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素
該標準自2023年6月1日起施行。
特此通告。
國家衛生健康委
2022年12月29日
5 前言
WS/T 404《臨牀常用生化檢驗項目參考區間》分爲10部分:
——第1部分:血清丙氨酸氨基轉移酶、天門冬氨酸氨基轉移酶、鹼性磷酸酶和γ-谷氨酰基轉移酶;
——第3部分:血清鉀、鈉、氯;
——第5部分:血清尿素、肌酐;
——第6部分:血清總鈣、無機磷、鎂、鐵;
——第9部分:血清C-反應蛋白、前白蛋白、轉鐵蛋白、β2-微球蛋白;
——第10部分:血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素。
本標準爲WS/T 404的第10部分。
本標準由國家衛生健康標準委員會臨牀檢驗標準專業委員會負責技術審查和技術諮詢,由國家衛生健康委醫療管理服務指導中心負責協調性和格式審查,由國家衛生健康委醫政司負責業務管理、法規司負責統籌管理。
本標準起草單位:中國醫科大學附屬第一醫院、廣東省中醫院、北京醫院/國家衛生健康委臨牀檢驗中心、復旦大學附屬中山醫院、北京大學第三醫院、中國人民解放軍空軍軍醫大學附屬第一醫院、四川大學華西醫院。
本標準主要起草人:尚紅、黃憲章、陳文祥、潘柏申、張捷、郝曉柯、王蘭蘭、趙敏、穆潤清、張傳寶。
6 標準正文
臨牀常用生化檢驗項目參考區間第10部分:血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素
6.1 1 範圍
本標準適用於醫療衛生機構臨牀實驗室血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素檢驗結果的報告和解釋,有關體外診斷產品生產廠商也可參照使用。
6.2 2 規範性引用文件
下列文件中的內容通過文中的規範性引用而構成本標準必不可少的條款。其中,注日期的引用文件,僅該日期對應的版本適用於本標準;不注日期的引用文件,其最新版本(包括所有的修改單)適用於本標準。
6.3 3 術語和定義
WS/T 402界定的術語和定義適用於本標準。
6.4 4 參考區間
中國成人(≥18 歲)血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素參考區間見表 1。
中國成人(≥18 歲)血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素參考區間建立及驗證過程的相關信息參見附錄 A。
表1 中國成人(≥18 歲)血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素參考區間

表1 中國成人(≥18歲)血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素參考區間(續)
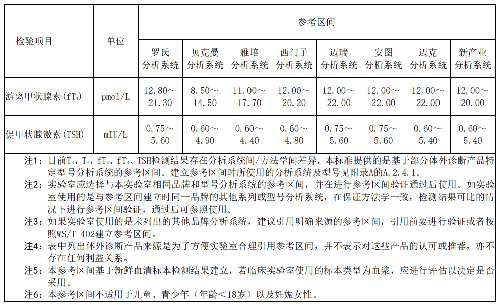
注1:目前T3、T4、fT3、fT4、TSH檢測結果存在分析系統間/方法學間差異,本標準提供的是基於部分體外診斷產品特定型號分析系統的參考區間。建立參考區間時所使用的分析系統及型號見附錄A的A.2.4.1。
注2:實驗室應選擇與本實驗室相同品牌和型號分析系統的參考區間,並在進行參考區間驗證通過後使用。如實驗室使用的是與參考區間建立時同一品牌的其他系列或型號分析系統,在保證方法學一致,檢測結果可比的情況下進行參考區間驗證,通過後可參照使用。
注3:如果實驗室使用的是未列出的其他品牌分析系統,建議引用明確來源的參考區間,引用前要進行驗證或者按照WS/T 402建立參考區間。
注4:表中列出體外診斷產品來源是爲了方便實驗室合理引用參考區間,並不表示對這些產品的認可或推薦,亦不存在任何利益關係。
注5:本參考區間基於新鮮血清標本檢測結果建立,若臨牀實驗室使用的標本類型爲血漿,應進行評估以決定是否採用。
注6:本參考區間不適用於兒童、青少年(年齡<18歲)以及妊娠女性。
6.5 5 參考區間的應用
6.5.1 5.1 一般原則
注1:本標準的參考區間基於中國成年人羣多中心大規模研究建立。
注2:建立參考區間的研究工作量大、成本高,臨牀實驗室引用參考區間比自己建立參考區間更爲現實、可行。
6.5.2 5.2 參考區間評估、驗證和使用
5.2.1 臨牀實驗室應按照 WS/T 402 有關規定進行參考區間的評估和驗證。
5.2.2 實驗室應首先對分析全過程的質量管理以及使用的分析系統和目標應用人羣進行評估,若與參考區間建立時有足夠可比性,可引用本標準的參考區間。
5.2.3 實驗室在引用本標準的參考區間前應進行必要的驗證。
5.2.4 驗證前實驗室應保證分析系統性能符合要求,且室內質控在控,室間質評合格。
a) 篩選合格參考個體不少於 20 例,性別、年齡應分佈均衡。篩選標準參見附錄 A 的 A.2.2;
注:增加驗證的參考個體例數,如≥60例,有利於獲得更可靠的評估結果。
b) 按本實驗室操作程序採集、處理、分析標本,分析前需保證分析系統性能符合要求;
c) 按適當方法檢查並剔除離羣值(若有離羣值,則另選參考個體補足),離羣值檢驗採用 Dixon方法:首先將檢測結果按照大小排序並計算極差(最大值與最小值之差)R,然後分別計算最大值和最小值與其相鄰數值之差 D;若 D/R≥1/3,則將最大值或最小值視爲離羣值予以剔除;將其餘數據重複前述步驟進行離羣值檢驗,直至剔除所有離羣值;
d) 如選擇 20 例合格參考個體,將 20 例檢驗結果與參考區間比較,若在參考區間之外的數據不超過 2 例,則通過驗證;若超過 2 例,則另選 20 例合格參考個體重新按照上述判斷標準進行驗證。如參考個體多於 20 例,在參考區間之外的數據不超過 10%爲通過驗證;若超過 10%的數據在參考區間之外,則另選至少 20 例合格參考個體,重新按照上述判斷標準進行驗證。
5.2.6 參考區間驗證通過,實驗室可使用本標準參考區間。在變更參考區間時需注意事項參見附錄 C。
5.2.7 參考區間驗證未通過時的處理程序:參考區間驗證未通過時,實驗室應從參考個體和分析質量兩方面進行重新評估:
a) 實驗室應首先分析納入驗證的參考個體數據。若經離羣值分析和剔除,仍有參考個體存在多個指標明顯異常時,應進行充分評估以決定是否納入驗證;
b) 實驗室應重新評估分析質量,尤其是正確度,若證實是分析系統導致的檢測質量問題,應改進或更換分析系統。分析質量評價可採用(但不限於)下列方式:
c) 若證明是人羣差異導致的驗證不通過(如特定高海拔地區、特殊生活習慣地區等),應按 WS/T 402 的要求建立或引用適合本地區人羣的參考區間。
5.2.8 實驗室在所使用的體外診斷產品方法學、計量學溯源發生改變,項目校準品或試劑發生換代時,應重新進行參考區間驗證。
7 附錄A(資料性)參考區間建立及驗證過程的相關信息
7.1 A.1 參考區間建立的步驟
本標準參考區間按WS/T 402要求建立,主要包括以下步驟:
a) 選擇參考個體,組成參考樣本組;
7.2 A.2 參考樣本組的建立
7.2.1 A.2.1 參考個體的選擇
參考人羣來自東北、華北、華東、華南、西南、西北六大區農村和城市社區,年齡≥18歲。採用多級整羣抽樣方法在六大區進行人羣抽樣,經過嚴格的健康篩查選擇參考個體。
7.2.2 A.2.2 參考個體的入選條件
抽樣表觀健康個體,徵得知情同意,通過問卷調查、體格檢查、實驗室檢查、超聲檢查篩選參考個體,滿足以下要求:
a) 問卷調查、體格檢查納入標準:
1) 自覺健康;
2) 無急、慢性疾病:無急慢性感染,無甲狀腺系統疾病個人史、家族史以及手術史,無心腦血管疾病、糖尿病、呼吸系統疾病、泌尿系統疾病、消化系統疾病、風溼性疾病、血液系統疾病、腫瘤、垂體功能異常;
3) 6 個月內未進行手術,4 個月內未獻血、輸血或大量失血;
4) 無長期用藥史,2 周內未服用藥物;
6) 無可見或可觸及的甲狀腺腫。
b) 實驗室檢查排除標準:
1) 血清丙氨酸氨基轉移酶:男性>50 U/L,女性>40 U/L;或者血清γ-谷氨酰基轉移酶:男性>60 U/L,女性>45 U/L;或者血清天門冬氨酸氨基轉移酶:男性>40 U/L,女性>35 U/L;
2) 血清白蛋白<40 g/L;
3) 血清肌酐:男性(20 歲~59 歲)>97 μmol/L,男性(60 歲~79 歲)>111 μmol/L;
女性(20 歲~59 歲)>73 μmol/L,女性(60 歲~79 歲)>81 μmol/L;
4) 空腹血糖≥7.0 mmol/L;
5) 白細胞計數:WBC<3.0 ×109/L 或 WBC>10.0 ×109/L;
6) 血紅蛋白:男性<130 g/L;女性<115 g/L;
7) 乙型肝炎病毒表面抗原、丙型肝炎病毒抗體、人免疫缺陷病毒抗體任意一項陽性;
c) 甲狀腺超聲排除標準:甲狀腺腫大、慢性淋巴細胞性甲狀腺炎(橋本氏病)、甲狀腺功能亢進、亞急性甲狀腺炎、甲狀腺癌、甲狀腺缺如。
注:排除標準依據衛生行業標準、美國生化學會指南、內科學、超聲診斷學,結合檢驗及臨牀專家意見制定。
7.2.3 A.2.3 血液標本採集與處理
血液標本採集與處理按照WS/T 225、WS/T 661文件進行。主要要求如下:
a) 參考個體準備:採血前三天保持正常生活習慣,不做劇烈運動和重體力勞動。採血前一天晚餐後至第二天上午採血前禁食,禁食時間 8 h~14 h;
b) 採血:採血時間爲上午 8:00~10:00,受檢者取坐位,採血前靜息 15 min,使用血清分離膠管,採用真空採血方式,自肘前靜脈採血;
c) 血液標本處理:標本在採集後 2 h 內及時分離血清,檢查並剔除溶血、黃疸或乳糜標本,血清分離後 2 h 內進行分析。
7.2.4 A.2.4 血清標本分析
A.2.4.1 分析系統:採用羅氏 E170/Cobas e601 電化學發光免疫分析儀、雅培 ARCHITECT i2000SR 化學發光免疫分析儀、貝克曼-庫爾特 DXI 800 化學發光免疫分析儀、西門子 ADVIA Centaur XP 化學發光免疫分析儀、邁瑞 CL-6000i 全自動化學發光免疫分析儀、安圖 AutoLumo A2000 Plus 全自動化學發光測定儀、邁克 i 3000 全自動化學發光免疫分析儀、新產業 MAGLUMI X8 全自動化學發光免疫分析儀及其配套試劑、校準品。
注:本參考區間建立所使用的分析方法及其檢測結果的計量學溯源參見附錄B。
A.2.4.2 分析系統性能評估:在參考個體血清標本分析前進行分析性能評估。精密度評估:測定正常和異常兩個濃度水平的質控物,每日測定 1 批,重複測定 3 次,連續測定 5 天,以生物學變異導出的允許不精密度的最低標準作爲判定標準;一致性評估:使用人混和血清盤(包括正常和異常水平),評估各實驗室間同一分析系統的一致性以及所有分析系統的可比性,計算均值的偏差,以生物學變異導出的允許偏倚作爲判定標準。
A.2.4.3 血清標本分析:分析系統性能符合要求後進行血清標本分析,每份血清標本分析一次。
A.2.4.4 標本分析的質量控制:使用正常和異常兩個濃度水平的第三方質控物及一個正常濃度水平的人混和血清質控物進行精密度控制,每獨立分析批同步進行質控物分析。
7.2.5 A.2.5 參考值處理與參考區間建立
A.2.5.1 離羣值檢查和處理:數據經 Box-Cox 轉換後,剔除均值±3 倍標準差以外的數據。
A.2.5.2 分組判斷:使用nested ANOVA方法對性別、年齡、地區三個因素進行分組分析。SDR(SD ratio,分組因素的標準差與個體間的標準差的比值)≤0.3 時,不提示分組;>0.3 時提示按該因素分組。
A.2.5.3 參考限和參考區間建立:採用非參數法,計算參考值的下限(2.5%分位數)和上限(97.5%分位數)及其 95%置信區間,結合臨牀意見和置信區間對參考限進行適當取整形成參考區間。
7.2.6 A.2.6 參考區間驗證
參考區間驗證過程中參考個體的納入與排除標準與參考區間建立相一致。驗證數據來源於我國東北、華北、華東、華南、西南、西北六個地區的醫療機構,驗證結果滿足 WS/T 402規定要求。
7.2.7 A.2.7 參考區間的同行評議
8 附錄B(資料性)甲狀腺相關激素分析方法和檢測結果的計量學溯源
B.1 血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素分析方法和檢測結果的計量學溯源見表 B.1。
表B.1 血清三碘甲狀腺原氨酸、甲狀腺素、遊離三碘甲狀腺原氨酸、遊離甲狀腺素、促甲狀腺激素分析方法和檢測結果的計量學溯源

9 附錄C(資料性)變更參考區間注意事項
a) 實驗室變更參考區間前應與相關臨牀科室進行充分溝通、論證;
b) 實驗室應將參考區間變更情況報醫務部門審批、備案;
c) 實驗室在參考區間變更前應將變更信息及時告知臨牀醫護人員和實驗室人員;
e) 參考區間變更後,實驗室應與臨牀科室保持密切聯繫,追蹤參考區間變更後臨牀應用效果,及時發現、解釋和解決參考區間使用過程中遇到的問題。
10 參考文 獻
[1] Clinical and Laboratory Standards Institute (CLSI). Defining, establishing, and verifying reference intervals in the clinical laboratory; Approved Guideline-Third Edition.CLSI document EP28-A3c. CLSI, Wayne, PA, USA, 2010.
[2] Ichihara K, Boyd JC. IFCC Committee on Reference Intervals and Decision Limits (CRIDL).An appraisal of statistical procedures used in derivation of reference intervals.Clin Chem Lab Med.2010.48(11):1537-1551.
[3] Clinical and Laboratory Standards Institute (CLSI). Method comparison and bias estimation using patient samples; Approved Guideline-Third Edition. CLSI document EP9-A3.CLSI, Wayne,PA, USA, 2013.
[4] Baloch Z, Carayon P, Conte-Devolx B, Demers LM, Feldt-Rasmussen U, Henry JF, LiVosli VA, Niccoli-Sire P, John R, Ruf J, Smyth PP, Spencer CA, StockigtJR. Guidelines Committee, National Academy of Clinical Biochemistry. Laboratory medicine practice guidelines. Laboratory support for the diagnosis and monitoring of thyroid disease. Thyroid.2003.13(1):3-126.